一种生物结合化学法制备D-脯氨酸的方法与流程
本发明属于生物技术和化工领域,涉及一种生物结合化学法制备d-脯氨酸的方法,更具体的是一种基因工程重组菌株e.coli bl21/petduet-race-dglucy的构建,以及利用其催化产物结合化学合成d-脯氨酸的方法。
背景技术:
1、d-脯氨酸(d-proline,分子式:c5h9no2,cas号:344-2532)是一类重要的手性试剂和手性中间体。既可用作拆分试剂和手性试剂,也可以作为合成某些手性药物的手性中间体,如可以作为抗偏头痛药物依来曲普坦的关键手性中间体。依来曲普坦(eletriptan)是由辉瑞公司开发的于2001年首次在澳大利亚上市,后续在多个国家上市,市场需求量较大,其作用原理主要是通过激活人体内5-ht1相关受体抑制神经肽释放,收缩颅内血管丙抑制神经性炎症发挥抗偏头痛效应;此外,d-脯氨酸还是合成一叶萩型生物碱(-)-securininea的关键前体,该生物碱用于临床治疗小儿麻痹症、肌萎缩侧索硬化症和慢性再生障碍性贫血等疾病;并且,d-脯氨酸还是合成(r)-harmicine的关键前体,该物质是一种具有多重药理活性的β-咔啉生物碱。而作为不对称的有机催化剂是由于d-脯氨酸具有刚性构象,可以作为不对称有机催化剂催化多个反应如不对称mannich反应、aldol反应、mannich–azamichael反应、morita-bayllis-hillman反应、heck交叉偶联反应、多组分反应,用于合成各种结构的手性分子。综上,d-脯氨酸无论是作为手性试剂还是作为医药中间体都具有重要的价值,具有广阔的市场前景。
2、目前,d-脯氨酸的制备方法可以分为化学法和生物法两种。化学法目前工业上主要是通过采用化学不对称转化技术制备,该技术是以l-脯氨酸为原料,正丁醛为催化剂,在正丁酸溶剂中与l-酒石酸反应制备d-脯氨酸-l-酒石酸盐,然后在甲醇中用氨水处理得到d-脯氨酸,该方法主要存在生产成本偏高、环境污染大等问题;另一种化学方法制备d-脯氨酸是以吡咯烷-2-甲醛为原料,不对称还原为d-脯氨醇,然后氧化为d-脯氨酸,但是该方法需要采用昂贵的原料和手性金属催化剂,d-脯氨酸的对映体过量(enantiomeric excess,ee)值也不高。
3、生物法制d-脯氨酸的方法主要有生物不对称合成法制备、生物拆分法制备、对映选择性降解法制备d-脯氨酸。其中,生物不对称合成法主要是以l-精氨酸为原料,化学合成l-cl-精氨酸,利用微生物菌体将其水解为(s)-5-氨基-2-氯戊酸,然后自动反转、关环为d-脯氨酸,该路线成本非常高,不适合工业化应用;生物拆分法主要是利用一种特异性的酶去作用于dl-脯氨酸衍生物中的l-脯氨酸衍生物,而d-脯氨酸衍生物得到保留。l-脯氨酸衍生物被酶催化后还原为l-脯氨酸,分离出的l-脯氨酸可作为制备dl-脯氨酸的原料;对映体选择降解法制备主要是以dl-脯氨酸为原料,通过特定微生物在培养基中生长的同时降解dl-脯氨酸中的l-脯氨酸,d-脯氨酸得到保留。该法的优点是环境污染较轻,但是制备的产量较低,依赖于底物dl-脯氨酸原材料,所制备d-脯氨酸的成本高,无法工业化应用。
4、由于生物法制备d-脯氨酸的技术和成本问题,市场上现有技术为化学法生产,因此,针对于现有化学法、生物法制备d-脯氨酸的关键问题,开发更为高效、低成本的d-脯氨酸合成工艺技术具有重要的价值和意义。
技术实现思路
0、
技术实现要素:
1、本发明提供了一种生物酶法催化+化学法合成d-脯氨酸的路线,相比单一的化学法和生物催化方法,选用了更为廉价易得的底物l-谷氨酸作为前体物质,不受原材料来源限制,酶法催化步骤反应完全,得率更高,化学法反应完全,产物手性纯度更高,为一条全新的d-脯氨酸合成路线。
2、为实现此目的,本发明采用的技术方案如下:
3、一种生物结合化学法制备d-脯氨酸的方法,包括以下步骤:
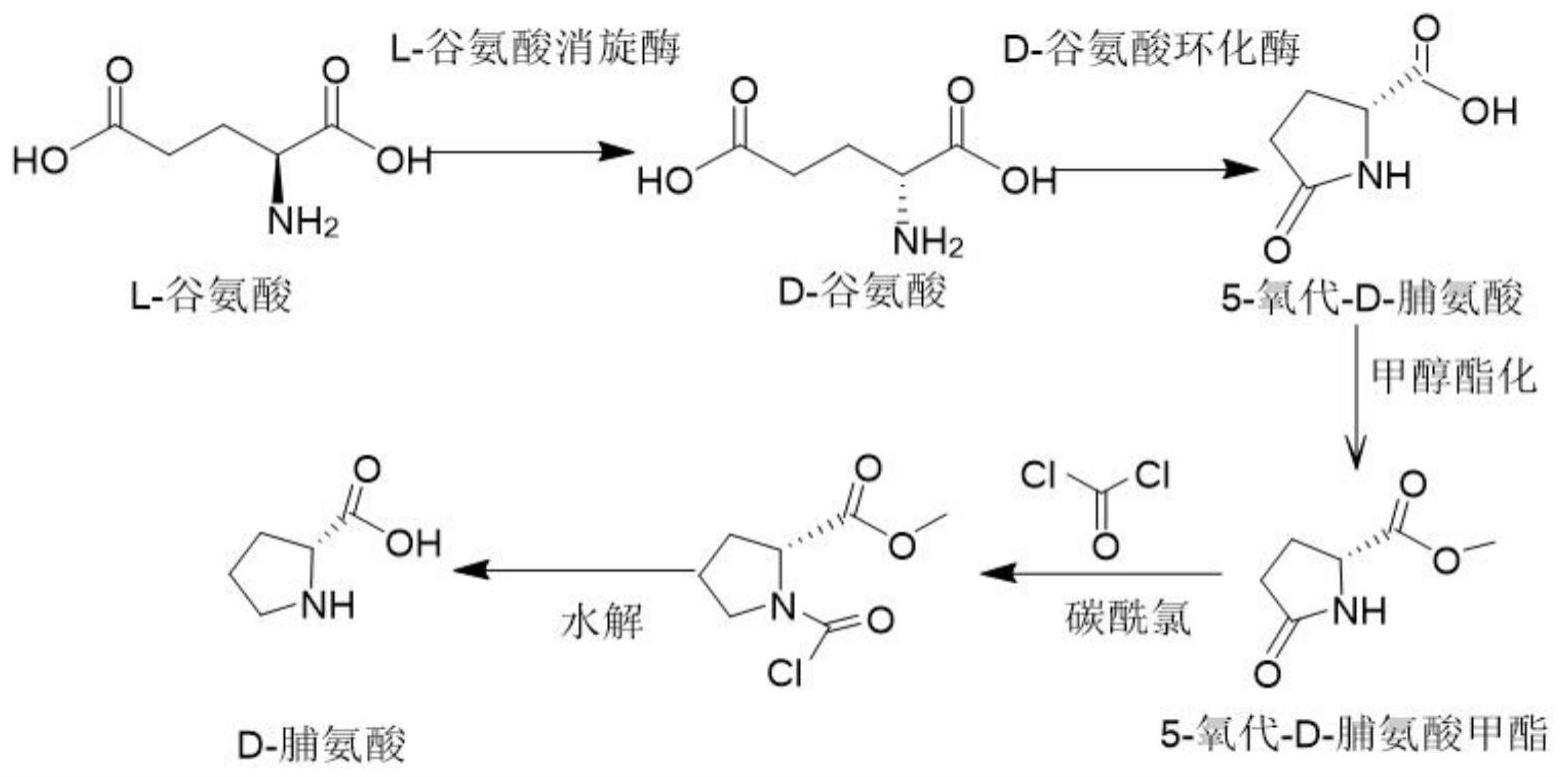
4、1)含有谷氨酸消旋酶基因和d-谷氨酸环化酶基因共表达载体的基因工程菌作为催化剂,用l-谷氨酸为前体,催化合成d-脯氨酸前体5-氧代-d-脯氨酸;
5、2)以5-氧代-d-脯氨酸化学法合成d-脯氨酸。
6、所述的方法,
7、谷氨酸消旋酶基因和d-谷氨酸环化酶基因构建至表达载体;将共表达载体转化至表达菌株中,抗生素筛选后即为含有谷氨酸消旋酶和d谷氨氨酸环化酶基因的工程重组菌株。
8、进一步地,
9、谷氨酸消旋酶基因和d-谷氨酸环化酶基因构建至大肠杆菌原核表达载体petduet-1,其中谷氨酸消旋酶基因构建至petduet-1中的多克隆位点mcs1中,基因5’端带有ncoi酶切位点,基因3’端带有hindiii酶切位点;d-谷氨酸环化酶基因构建至petduet-1的多克隆位点mcs2中,基因5’端带有ndei酶切位点,基因3’端带有xhoi酶切位点;将共表达质粒构建至大肠杆菌表达菌株bl21(de3)中,抗生素筛选后即为含有谷氨酸消旋酶和d谷氨氨酸环化酶基因的工程重组菌株e.coli bl21/petduet-race-dglucy。
10、更进一步地,谷氨酸消旋酶基因race的氨基酸序列如seq id no.1所示;d-谷氨酸环化酶基因dglucy的氨基酸序列如seq id no.2所示。
11、所述的方法,
12、工程菌发酵过程为:从lb的固体培养基上挑取单菌落接种于lb液体培养基中,180-220rpm,30-37℃振荡过夜培养,次日按照0.5-2%接种量接种至tb发酵培养基中,180-220rpm,30-37℃振荡培养4-6h,待od600nm=0.4-0.6时,添加终浓度为0.5-1%的乳糖,180-220rpm,25-30℃诱导培养8-12h,收集菌体,进行后续的全细胞的催化合成反应。
13、所述的方法,催化合成d-脯氨酸前体5-氧代-d-脯氨酸的过程:
14、l-谷氨酸用适量缓冲液溶解后,加入磷酸吡哆醛、mncl2,再加入适量水搅拌溶解后,调ph,加入基因工程重组菌株反应。
15、进一步地,
16、催化合成体系中l-谷氨酸的浓度为3.5-50g/l,反应ph为7.0-8.0,反应温度为30-35℃,180-220r/min,磷酸吡哆醛含量为20-50.0mg/l,mncl2含量为20-50mg/l,湿菌体浓度为200-400g/l;反应时间3-7h。
17、所述的方法,5-氧代-d-脯氨酸经过酯化、酰氯化、水解反应三个步骤最后得到d-脯氨酸。
18、进一步包括:
19、将步骤1)反应液超滤除去酶液后,加入甲醇溶液进行酯化反应,在搅拌下缓慢滴加98%硫酸,保持温度65-70℃反应,至反应液全部变清,低温冷却至5-10℃,调节ph=7.5-8.0,收集沉淀;将沉淀溶解后用光气进行酰氯化反应,待反应完成后,向体系中加入盐酸溶液,后用醇溶结晶后,得到目的产物d-脯氨酸。
20、本发明还提供了工程重组菌株,谷氨酸消旋酶基因和d-谷氨酸环化酶基因构建至表达载体;将共表达载体转化至表达菌株中,抗生素筛选后即为含有谷氨酸消旋酶和d谷氨氨酸环化酶基因的工程重组菌株;
21、进一步地:
22、谷氨酸消旋酶基因和d-谷氨酸环化酶基因构建至大肠杆菌原核表达载体petduet-1,其中谷氨酸消旋酶基因构建至petduet-1中的多克隆位点mcs1中,基因5’端带有ncoi酶切位点,基因3’端带有hindiii酶切位点;d-谷氨酸环化酶基因构建至petduet-1的多克隆位点mcs2中,基因5’端带有ndei酶切位点,基因3’端带有xhoi酶切位点;将共表达质粒构建至大肠杆菌表达菌株bl21(de3)中,抗生素筛选后即为含有谷氨酸消旋酶和d谷氨氨酸环化酶基因的工程重组菌株e.coli bl21/petduet-race-dglucy;
23、更进一步地,谷氨酸消旋酶基因race的氨基酸序列如seq id no.1所示;d-谷氨酸环化酶基因dglucy的氨基酸序列如seq id no.2所示。
24、本发明还提供了所述的工程重组菌株在制备d-脯氨酸中的应用。
25、本发明提供了所述的重组菌株用于d-脯氨酸前体5-氧代-d-脯氨酸的催化制备,其中谷氨酸消旋酶race是以l-谷氨酸为底物催化合成d-谷氨酸,d-谷氨酸环化酶dglucy是以d-谷氨酸为底物催化合成5-氧代-d-脯氨酸。
26、本发明采用酶法+化学法相结合的方法生产脯氨酸,摒弃了化学法不对称转化技术的缺点,利用了酶法高效合成的优点,且选择大宗原材料谷氨酸为起始底物,原料的来源简单易获得,不受原材料来源限制,在谷氨酸消旋酶和d-谷氨酸环化酶的作用生成5-氧代-d-脯氨酸,再结合化学方法生成d-脯氨酸,该技术相比现有的化学合成法和生物法技术具有明显优势:原材料易获得、成本更低、谷氨酸的消旋反应结合环化反应,反应向正向发生,转化效率更高,产物手性纯度更高,为一条全新的d-脯氨酸合成路线。
- 还没有人留言评论。精彩留言会获得点赞!