检测MDV、ALV和REV的组合物、检测方法与应用
本发明属于基因工程,具体涉及一种检测mdv、alv和rev的组合物、检测方法与应用。
背景技术:
1、马立克病病毒(marek's disease virus,mdv)、禽白血病病毒(avian leukosisvirus,alv)和网状内皮组织增生症病毒(reticuloendotheliosis virus,rev)是三种常见的导致家禽免疫抑制的产生肿瘤的病毒。家禽感染这些病毒后,不仅会造成机体免疫功能下降,更易受其他病原的并发或继发感染。临床上这3种免疫抑制病病原有时呈混合感染,不同免疫抑制病病原的混合感染,既可抑制机体正常免疫反应,又可相互作用,增强病毒的致瘤性。在共感染的状态下,会发生协同免疫抑制,导致疫苗的免疫效力降低,促进病毒的复制。近年来,关于家禽免疫抑制病病原共感染的报道越来越多,共感染导致家禽免疫器官受损,肿瘤类型及肿瘤范围变广,死亡率变高。家禽病原多重感染的现象已经非常普遍,疾病的复杂性增加,给广大养殖户带来严重的经济损失,也使我国养禽业疾病预防控制治疗面临更高的风险挑战。
2、临床诊断过程中因mdv、rev和alv均可引起鸡群发生肿瘤,眼观临床症状相似,且临床上这3种免疫抑制病病原有时呈混合感染,仅靠临床诊断很难区分病原,需要进一步进行实验室方法检测。已知的检测方法方法包括病毒分离鉴定、血清学检测、常规pcr检测方法、染料法荧光定量pcr检测方法等,但该类方法各自均存在缺陷。例如,病毒分离鉴定是公认的病毒检测的金标准,但它费时费力,还需进行电镜观察、细胞病变观察、间接免疫荧光等试验来佐证,不适合实际操作中临床样品的快速检测;血清学检测灵敏度较低,假阳性问题易发生;常规pcr检测方法耗时长,且灵敏度、检测效率等方面还需提高;染料法荧光定量pcr检测快速、敏感性较高,但是易受到非特异性扩增和引物二聚体的影响,导致特异性不足。而taqman荧光定量pcr技术具有检测快速、敏感性较高、特异性更强的特点,并且可以利用多种荧光信号进行多重检测分析,近年来被越来越多地应用于临床病原诊断上。
3、有鉴于此,本技术基于mdv、rev、alv序列保守区设计特异性引物,建立操作简易、敏感性高、重复性好、特异性强的三重taqman实时荧光定量pcr检测方法,以期用于临床上mdv、rev、alv的感染检测。
4、现有技术中,公开号为cn106521037a的发明专利公开了一种用于诊断fadv/mdv/alv/rev 4重pcr检测试剂盒,可有效鉴别ⅰ群禽腺病毒、马立克氏病病毒、鸡淋巴细胞白血病病毒与禽网状内皮组织增生症病毒;公开号为cn103981288b的发明专利公开了一种针对禽肿瘤性病毒的非诊疗目的多重pcr检测方法,可以同时检测rev、mdv、alv-j和alv-a病毒;虽然上述发明均能实现实现mdv、alv和rev的有效检测,但是检测限度相对较高,无法实现低于10copies/ul的病原检测。
技术实现思路
1、有鉴于此,本发明的目的之一在于提供一种用于检测alv和/或rev的组合物,利用该组合物可以有效检测混合感染rev和alv两种免疫抑制病病原的家禽的具体病原。
2、为实现上述目的,本发明采用以下技术方案:
3、用于检测alv和/或rev的组合物,所述组合物包括:
4、(1)用于检测alv的探针b和引物对b:所述探针b包含如seq id no.4的核酸序列,所述引物对b包含核酸序列如seq id no.5所示的正向引物b和核酸序列如seq id no.6所示的反向引物b;
5、和/或(2)用于检测rev的探针c和引物对c:所述探针c包含如seq id no.7的核酸序列,所述引物对c包含核酸序列如seq id no.8所示的正向引物c和核酸序列如seq idno.9所示的反向引物c。
6、进一步,所述探针c的5′端标记hex荧光基团,3′端标记eclipse淬灭基团;所述探针b的5′端标记rox荧光基团,3′端标记bhq-2淬灭基团。
7、本发明的目的之二在于提供一种用于同时检测mdv、alv和rev的组合物,利用该组合物可以有效检测混合感染mdv、rev和alv三种免疫抑制病病原的家禽的具体病原,为三重taqman实时荧光定量pcr检测方法的建立以及混合感染免疫抑制病病原的痕量检测提供了技术支持。
8、为实现上述目的,本发明采用以下技术方案:
9、用于同时检测mdv、alv和rev的组合物,所述组合物由前述用于检测alv和/或rev的组合物以及用于检测mdv的探针a和引物对a组成;所述探针a包含如seq id no.1的核酸序列,所述引物对a包含核酸序列如seq id no.2所示的正向引物a和核酸序列如seq idno.3所示的反向引物a。
10、进一步,所述探针a的5′端标记fam荧光基团,3′端标记bhq-1淬灭基团。
11、本发明的目的之三在于提供一种前述用于检测alv和/或rev的组合物和/或前述用于同时检测mdv、alv和rev的组合物在制备用于检测mdv、alv和/或rev的试剂盒中的应用。
12、本发明的目的之四在于提供一种用于检测mdv、alv和/或rev的试剂盒。
13、为实现上述目的,本发明采用以下技术方案:
14、用于检测mdv、alv和/或rev的试剂盒,所述试剂盒含有前述用于检测alv和/或rev的组合物和/或前述用于同时检测mdv、alv和rev的组合物。
15、进一步,所述试剂盒还含有阳性对照和阴性对照;所述阴性对照为双蒸水;所述阳性对照为mdv、alv和/或rev的阳性质粒混合物。
16、本发明的目的之五在于提供一种基于三重taqman实时荧光定量pcr技术的检测mdv、alv和/或rev的方法,该方法可以实现mdv、alv和rev的痕量检测,mdv检测限低至3.22copies/ul;alv检测限低至7.15copies/ul;rev检测限低至5.81copies/ul。
17、为实现上述目的,本发明采用以下技术方案:
18、基于三重taqman实时荧光定量pcr技术的检测mdv、alv和/或rev的方法,所述方法为非诊断和治疗目的的方法,包括以下步骤:
19、(1)提取待测样本的dna/cdna;
20、(2)以步骤(1)所得dna/cdna为模板,利用前述用于检测alv和/或rev的组合物和/或前述用于同时检测mdv、alv和rev的组合物对dna模板进行pcr扩增;
21、(3)根据步骤(2)的扩增结果判断待测样本是否感染mdv、alv和/或rev。
22、进一步,步骤(2)中,所述pcr扩增的反应体系为:qpcr taqman probe master mix10μl,3对上下游引物各0.4μl,探针0.4μl,dna模板2μl,加灭菌超纯水至20μl。
23、进一步,所述3对上下游引物浓度为10μm;探针浓度为10μm。
24、进一步,步骤(2)中,所述pcr扩增程序为:95℃1min;95℃10s,59℃30s,连续45个循环;退火温度为59℃。
25、进一步,根据待测样本在fam通道、rox通道和/或hex通道是否扩增出特异性曲线来判断待测物是否感染mdv、alv和/或rev。
26、更进一步,结果判定方法如下:
27、只有fam通道扩增出特异性曲线时,表示待测样本mdv阳性,alv和rev阴性;只有rox通道扩增出特异性曲线时,表示待测样本alv阳性,mdv和rev阴性;只有hex通道扩增出特异性曲线时,表示待测样本rev阳性,mdv和alv阴性;当fam通道和rox通道同时扩增出特异性曲线,表示待测样本mdv和alv双重阳性,rev阴性;当fam通道和hex通道同时扩增出特异性曲线,表示待测样本mdv和rev双重阳性,alv阴性;当rox通道和hex通道同时扩增出特异性曲线,表示待测样本alv和rev双重阳性,mdv阴性;当fam通道、rox通道和hex通道同时扩增出特异性曲线,表示待测样本mdv、alv和rev三重阳性;当fam通道、rox通道和hex通道均没有扩增出特异性曲线,表示待测样本阴性,未感染mdv、alv和rev。
28、进一步,mdv阳性标准质粒/mdv阳性样本的最低检测下限为3.22copies/ul;alv阳性标准质粒/alv阳性样本的最低检测下限为7.15copies/ul;rev阳性标准质粒/rev阳性样本的最低检测下限为5.81copies/ul。
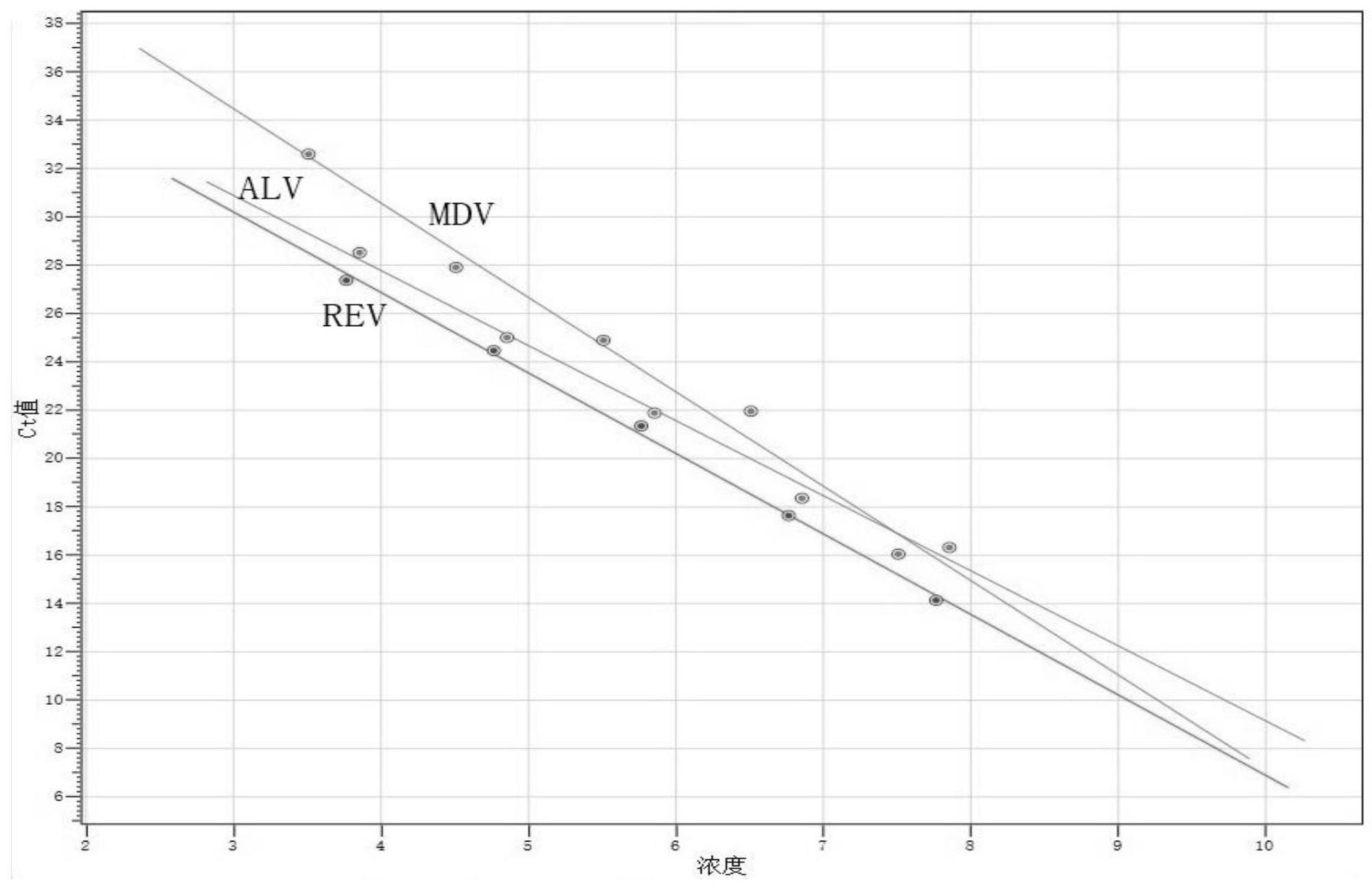
29、进一步,在109copies/ul~100copies/ul的浓度范围内,mdv的标准曲线方程为:y=-3.9x+46.19,r2=0.992;alv的标准曲线方程为:y=-3.33x+40.18,r2=0.999;rev的标准曲线方程为:y=-3.11x+40.2,r2=0.996;其中,y为y轴,表示ct值;x为x轴,表示浓度,r表示相关系数。
30、本发明的有益效果在于:
31、本发明基于mdv、rev、alv序列保守区设计特异性引物,建立了可以实现mdv、rev、alv的感染检测的三重taqman实时荧光定量pcr检测方法,该方法操作简易、敏感性高、重复性好、特异性强,为我国养禽业家禽免疫抑制病病原共感染相关疾病的预防、控制和治疗提供了技术支持。
- 还没有人留言评论。精彩留言会获得点赞!