一种吡唑并杂芳基类衍生物的制备方法与流程
本公开属于医药领域,涉及一种吡唑并杂芳基类衍生物的制备方法,属于制药领域。
背景技术:
1、无论是正常细胞还是肿瘤细胞中,每天都会出现成千上万次dna的损伤。这使得dna损伤修复在维持基因组的稳定性和细胞存活方面起到至关重要的作用。相比较于正常细胞,肿瘤细胞承受了更大的复制压力,携带更多的内源性dna损伤,并且经常出现一个或多个dna损伤修复通路的缺失。这使得肿瘤细胞的存活更加依赖于dna损伤修复的顺利进行。
2、同源重组修复是dna双链断裂的主要修复方式,以未受损的姐妹染色单体的同源序列作为其修复的模板复制受损处的dna序列,精确修复dna。这种修复方式主要发生在细胞的g2期和s期。atr是同源重组修复通路中的关键酶,属于pikk家族。当atr/atrip复合物与覆盖了复制蛋白a(rpa)的受损dna结合后,atr被激活并通过磷酸化下游蛋白chk1和smarcal等,调节细胞周期各个检查点,引起细胞周期阻滞;保证受损dna的稳定性;提高dntp浓度,促使dna损伤得以修复。细胞周期s期中出现的dna损伤修复主要由atr通路完成,说明atr对于保证细胞增殖非常重要。对于临床肿瘤样品的分析结果表明在多种肿瘤组织中,例如胃癌、肝癌、结直肠癌、卵巢癌、胰腺癌等,均观察到atr表达水平升高。并且在卵巢癌、胰腺癌病人中,高水平的atr往往伴随着较低的存活率。由此可见atr是一个重要的肿瘤治疗的靶标。
3、现已公开的atr抑制剂的专利申请包括wo2010071837、wo2011154737、wo2016020320、wo2016130581、wo2017121684、wo2017118734、wo2018049400、wo2019050889、wo2014140644、wo2021098811a等。
技术实现思路
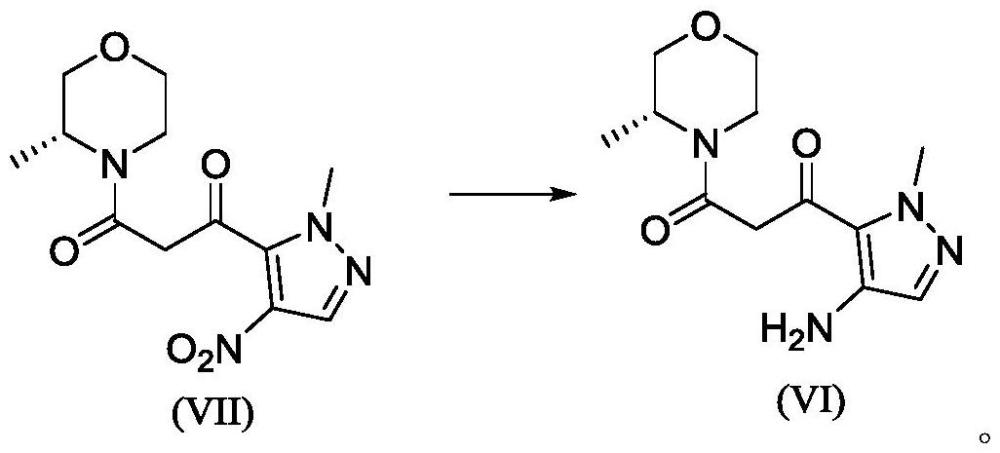
1、本公开提供一种式(vi)所示化合物的制备方法,可选的实施方案中,包含如下步骤:式(vii)所示化合物在催化剂作用下发生还原反应的步骤,
2、
3、在其他的实施方案中,本公开提供的式(vi)所示化合物的制备方法包含如下步骤:式(x)所示化合物与式(viii)所示化合物,在非亲核性碱性试剂作用下发生缩合反应的步骤,
4、
5、在一些实施方案中,方法1中硝基还原的方式为氢化还原,可选地,所述的催化剂为pd/c。
6、本公开中,式(vii)所示化合物可由式(ix)所示化合物与式(viii)所示化合物在非亲核性碱性试剂作用下发生缩合反应制备得到,
7、
8、可选的实施方案中,本公开中所述非亲核性碱性试剂选自双(三甲基硅基)胺基锂(lihmds)、二异丙基氨基锂(ldia)、二乙基氨基锂(ldea)、异丙基环己基氨基锂(lica)、二环己基氨基锂(ldca)或2,2,6,6-四甲基哌啶氨基锂(ltmp)。
9、一些实施方案中,所述非亲核性碱性试剂为双(三甲基硅基)胺基锂(lihmds)。
10、可选的实施方案中,式(x)所示化合物与非亲核性碱性试剂的物质的量比选自1:1-1:10,具体可选1:1、1:1.5、1:2、1:2.5、1:3、1:3.5、1:4、1:4.5、1:5、1:5.5、1:6、1:6.5、1:7、1:7.5、1:8、1:8.5、1:9、1:9.5或1:10,或任意两点之间的数值。
11、可选的实施方案中,式(ix)所示化合物与非亲核性碱性试剂的物质的量比选自1:1-1:10,具体可选1:1、1:1.5、1:2、1:2.5、1:3、1:3.5、1:4、1:4.5、1:5、1:5.5、1:6、1:6.5、1:7、1:7.5、1:8、1:8.5、1:9、1:9.5或1:10,或任意两点之间的数值。
12、可选的实施方案中,式(x)所示化合物与式(viii)所示化合物在非亲核性碱性试剂作用下发生缩合反应的步骤,或式(ix)所示化合物与式(viii)所示化合物在非亲核性碱性试剂作用下发生缩合反应的步骤的反应温度选自0℃至-50℃,具体地,可选0℃、-5℃、-10℃、-15℃、-20℃、-25℃、-30℃、-35℃、-40℃、-45℃或-50℃,或任意两点之间的数值;反应溶剂为非质子溶剂,具体可选自乙腈、四氢呋喃等。
13、可选的实施方案中,式(ix)所示化合物与式(viii)所示化合物反应的步骤在惰性气体保护下发生,惰性气体具体可选氮气或氦气。
14、本公开另一方面提供一种式(v)所示化合物或其可药用盐的制备方法,包括式(vi)所示化合物在脱水剂和碱性试剂作用下环合的步骤,
15、
16、进一步包括前述的式(vi)所示化合物的制备步骤。
17、可选的实施方案中,式(v)所示化合物或其可药用盐的制备方法中,所述脱水剂选自pocl3、pcl5,p2o5或socl2,所述碱性试剂选自二异丙基乙胺,三乙胺或吡啶。
18、可选的实施方案中,式(v)所示化合物或其可药用盐的制备方法中,所述脱水剂为pocl3,所述碱性试剂为二异丙基乙胺。
19、可选的实施方案中,式(vi)所示化合物与脱水剂的物质的量比选自1:1-1:10,具体可选1:1、1:1.5、1:2、1:2.5、1:3、1:3.5、1:4、1:4.5、1:5、1:5.5、1:6、1:6.5、1:7、1:7.5、1:8、1:8.5、1:9、1:9.5或1:10,或任意两点之间的数值。
20、可选的实施方案中,式(vi)所示化合物与碱性试剂的物质的量比选自1:1-1:10,具体可选1:1、1:1.5、1:2、1:2.5、1:3、1:3.5、1:4、1:4.5、1:5、1:5.5、1:6、1:6.5、1:7、1:7.5、1:8、1:8.5、1:9、1:9.5或1:10,或任意两点之间的数值。
21、可选的实施方案中,式(v)所示化合物或其可药用盐的制备方法中,反应的溶剂选自1,2-二氯乙烷、四氢呋喃或乙腈。
22、本公开另一方面提供一种式(i)所示化合物或其可药用盐的制备方法,包括前述的式(vi)所示化合物的制备步骤和/或前述的式(v)所示化合物或其可药用盐的制备步骤,任选进一步包括选自式(iv)所示化合物、式(iii)所示化合物、式(ii)所示化合物的一个或多个化合物的制备步骤,
23、
24、在一些实施方案中,本公开提供的式(i)所示化合物或其可药用盐的制备方法,步骤如下所示:
25、
26、可选的实施方案中,本公开提供的式(vi)所示化合物、式(v)所示化合物或其可药用盐、式(vii)所示化合物的制备方法,为大于500g级别(产物大于500g)的制备方法。
27、本公开另一方面提供一种式(vii)、(vi)所示的化合物,
28、
29、本公开进一步提供一种经由前述方法制备得到的式(i)所示化合物或其可药用盐。
30、本公开进一步提供药物组合物,其包含经由前述方法制备得到的式(i)所示化合物或其可药用盐和一种或多种药学上可接受的赋形剂。
31、本公开中所述的“赋形剂”包括但不限于任何已经被美国食品和药物管理局批准对于人类或家畜动物使用可接受的任何助剂、载体、助流剂、甜味剂、稀释剂、防腐剂、染料/着色剂、增香剂、表面活性剂、润湿剂、分散剂、助悬剂、稳定剂、等渗剂或乳化剂。
- 还没有人留言评论。精彩留言会获得点赞!