一种高生物活性环肽的制备方法及应用与流程
本发明涉及化学合成及生物工程,尤其涉及一种高生物活性环肽的制备方法及应用,具体涉及基于一种胶原小分子环肽的制备方法及其在化妆品、美容护肤领域抗衰功效的应用。
背景技术:
1、环肽(或环状肽),属于多肽类别中的一种,如最简单的环肽为两个末端基团一起反应形成肽键而封闭了肽主链;还有一些环肽,在其末端胺和侧链之间或在末端羧基和侧链之间或两个侧链之间产生共价键,从而使肽分子部分地环状。环肽相对于常规肽具有许多优点如,它们对外肽酶不敏感,比其线性对应物更稳定;环状肽由于其骨架的弯曲和较小的自由度,许多键的旋转被阻断,具有更可用于与外部靶标相互作用的侧链,与它们的靶标相互作用的强度增大,相邻的氨基酸不干扰分子相互作用。与线性肽相比,它们具有强的生物利用度,被广泛应用在医学和生物学领域。近年来,科学家证实环肽具有体内半衰期长、结构较稳定和渗透性强等特点,因此,外用含环肽产品能够起到一定的护理和防御、减缓衰老的效果,开发环肽在美容护肤领域中应用也具有一定的创新性及实用性。
2、环肽的合成和目前多肽合成方法一致,如多肽的合成主要分为化学合成和生物合成。经典多肽化学合成方法包括液相多肽合成法(lpps)和固相多肽合成法(spps),如利用固相或者液相介质,将肽链依照顺序逐个添加到合成中间产物上,即酰胺官能团的构建。在该制备中对不希望参与反应的氨基酸官能团进行保护,然后依次进行化学偶联,最后再脱保护,化学合成方法适用于二肽、三肽等短链的合成,但对于较长的多肽链合成,就会出现反应步骤多,副产物和中间产物多,整体收率低、存在消旋体、纯化成本高等问题;目前,已经发展了许多构建环肽的策略,如利用cu催化的炔基[3+2]环加成、ru催化的烯烃复分解、pd催化的半胱氨酸cys sh和赖氨酸lys nh2的芳基化、无金属催化二硫键的形成、恶二唑的形成和petasis-borono-mannich反应构建环肽。这些策略的弊端在于:需要引入非天然氨基酸;需要过渡金属催化;需要非水溶剂等。
3、生物合成法主要是利用生物系统的蛋白表达或基因重组,将多肽融合蛋白表达在宿主内部,再经过蛋白纯化和多肽释放来获得目标多肽。该方法不受多肽长度和序列的影响,可以简单高效地合成多肽,副产物少,但生物合成的方法需要经过菌株破碎和蛋白纯化的步骤,提高了多肽的生产成本,也制约了合成规模,目前应用上定向性比较强,受限于天然氨基酸的多肽合成。生物技术尤其酶催化构建酰胺键合成多肽是一种较为经济绿色的合成策略。与化学法原理不同,酶促多肽连接法的区域选择性与立体选择性来源于酶活性中心的空间位阻以及基团间的非共价作用,满足多肽拼接在区域选择性及抑制外消旋方面的基本要求,在多肽及蛋白的合成领域发挥着愈加重要的作用。
4、由细菌或真菌通过自身代谢合成的天然多肽化合物,例如青霉素、环孢素、棘白霉素类化合物等,是国内外新药创制的重要源泉。即其生物合成途径分为两类,一类通过核糖体来源的多肽进行缩合、修饰及环合,另一类则通过一种具有高度模块化特征的非核糖体多肽合酶(nrps)将天然或非天然的氨基酸逐一组装起来,这种机制兼具高效性和灵活的特异性,保证了天然多肽产物结构的多样性。(doi:10.12211/2096-8280.2020-064)。如研究人员,发现了天冬酰胺/天冬氨酸(asx)肽连接酶—丁烯酶1。这种高效酶是从产环肽的药用植物clitoria ternatea中分离出来的。butelase 1与legumain蛋白酶具有71%的序列同一性和相同的催化三联体,但不水解legumain的蛋白酶底物。相反,丁烯酶1使植物和动物来源的各种肽环化,产率大于95%。丁烯酶1的催化效率高达542000m-1s-1,是已知最快的肽连接酶。值得注意的是,丁烯酶1对肽底物的n-末端氨基酸也显示出广泛的特异性,从而为c末端特异性分子间肽连接提供了新的工具。(nguyen,giang k t;wang,shujing;qiu,yibo;hemu,xinya;lian,yilong;tam,james p(2014).butelase 1is an asx-specific ligaseenabling peptide macrocyclization and synthesis.nature chemical biology,10(9),732–738.)
5、另外,还有atp-grasp酶(atp依赖性羧酸-胺连接酶)是合成短寡肽的良好候选者。atp-grasp酶广泛分布于自然界中,能够通过激活羧酸作为酰基磷酸中间体并伴随atp的水解来催化酰胺键的形成。在atp-grasp超家族中,l-氨基酸连接酶(lals:ec 6.3.2.28)可以接受两种未受保护的l-氨基酸作为其最佳底物,以atp依赖性方式催化肽键的生物合成。这种反应是单向的;此外,不需要复杂的底物保护或衍生程序。
6、与皮肤衰老紧密相关的是皮肤中胶原蛋白,其中序列pro-x-gly pro的多肽是胶原蛋白的同源序列片段,分子量低,能够有效的渗入角质层、真皮层,因此被广泛用于皮肤保湿、防皱、修复、丰胸等护理品中。然而此胶原小分子易被机体蛋白酶识别及水解,大大降低了其生物利用度,因而通过环化改性可大幅提升其稳定性、生物利用率。同时,提升其空间结构复杂性、增加比表面积,提供更多与靶点接触可能性,达到功效更加多样性、多维度的提升功效的作用。经检索cn 111670027 a的中国发明专利申请,公开了环肽在美容中的用途,证实了环肽可应用在美容护肤领域。针对环肽的合成制备上,中国专利申请号为202210368579.1,申请案公开了一种环六肽的制备方法,采用传统固相合成直链肽长链,后利用化学缩合剂环化得到,最后分离纯化,得到相关环六肽及其衍生物,上述申请案的固相合成方法相对来说,收率有限,亟需发明一种产率更高,制备工艺简单的新的合成方法。而中国专利申请号为cn 115820578 a,申请公开了一种小分子胶原三肽的制备方法,采用氨基酸连接酶将l-甘氨酸、l-脯氨酸以及l-羟脯氨酸依次连接从而高转化率的生成胶原三肽,最后分离纯化,得到相关三肽,上述申请案的生物酶合成方法相对于长链多肽分子没有涉及,因此亟需发明一种长链多肽、环肽及其新的合成方法。
7、因此在本领域仍需要用于使肽环化的、克服现有技术的缺陷并且理想地是简单、快速和通用的改进手段。本发明的一个目的就是针对这类特殊序列提供一种简单可行的环化合成策略,提高多肽分子的合成产率。将化学方法与酶促连接方法联用来建立多样的环肽合成策略。
技术实现思路
1、为解决上述问题,本发明的目的在于提供了一种高生物活性环肽的制备方法及应用。通过创新一种高效而更简洁多肽合成法化学-酶合成法,将l-甘氨酸、l-脯氨酸以及l-谷氨酰胺依次连接从而高转化率的生成胶原三肽,而后通过温和简单的氨基酸连接酶(生物酶)催化合成酰胺反应就能快速生成一系列目标产物—环化多肽。相比于市面上常见的纯化提取、酶切割工艺、及化学合成等方法,本专利规模化生产工艺稳定,同时该方法纯度高副产物少、显著优于纯化学合成方法。此多肽合成方法兼备了原子经济和环境友好的优点,将化合物的有机和生物转化相结合,提升合成效率,可以更加快捷、节约、高效地大规模合成多肽及其衍生物,溶剂用量最小化、绿色化,而且原料易得,降低原材料浪费、减少废弃物污染、利于环保,在有机合成和多肽化学中具有明显的实际应用价值。该系列环肽主要应用于美容护肤领域,并对其进行特性研究发现该组环肽具备优良的稳定性,不易被降解,并具有非常强的皮肤渗透性,促进胶原生成等能力,在美容护肤及医美抗衰领域具有更强的应用潜能。
2、本发明基于l-谷氨酸连接酶(ec 6.3.2.60)肽连接酶/环化酶及其突变体。所述突变体酶能够以非常高的催化活性连接/环化肽,它识别c-末端处的于l-谷氨酸,并且无需经过其它基团的修饰,环化合成效率高,无需后续复杂的纯化等。值得注意的是,所述酶不仅可以有效地环化相应的氨基酸及短肽片段,这使得它在期望环化给定含l-谷氨酸、谷氨酰胺等肽,大环寡肽或蛋白质的各种应用中是高度通用且有用的,丰富了其在医药等领域中的应用。其合成得到的环肽及环肽混合物具有优异的生物活性,可应用在美容护肤等领域中。
3、本发明中提到的l-谷氨酸连接酶(ec 6.3.2.60)肽连接酶/环化酶及其突变体的功能不局限于制备环肽,可用于制备其他的肽。
4、小分子短肽适合有机合成,长链肽有机合成产率会较低,而酶合成对酶及相应的结构具有严格要求,如特异性酶,特异性结构,酶促合成的优点—酶的专一性。并不是任意的肽键都可以合成,而且影响肽键合成产率的各种因素和条件又可能随着反应物的不同而改变;本发明通过大量合成试验研究得到了一种高生物活性环肽的制备方法。
5、制备路线如式(2)所示,环化反应前的步骤均通过有机合成进行,环化反应的酰胺环化酶为l-谷氨酸连接酶ec 6.3.2.60、l-谷氨酸连接酶ec 6.3.2.60的突变体的一种或多种;所述l-谷氨酸连接酶ec 6.3.2.60的突变体的核苷酸序列为seq id no:1、seq id no:2、seq id no:3、seq id no:4中的任一种。式(2)中环(gly-pro-gln-gly-pro-gln)的r基团为(ch2)2conh2。
6、
7、本发明提供了一类环肽,所述环肽的环内含有3-6个酰胺键,分别为序列环(gly-pro-gln)、环(gly-pro-gln-gly)、环(gly-pro-gln-gly-pro)、环(gly-pro-gln-gly-pro-gln)。在三磷酸腺苷(atp)及对应的连接酶作用下高收率的酰胺键环化而制得相应的环肽产物。制得的环状结构上具有酰胺键,几元环就表示环状结构上有几个酰胺键,如六元环表示环状结构上有六个酰胺键。
8、本发明的这些环肽及其衍生物或其盐可以作为立体异构体或立体异构体的混合物存在;例如,包含它们的这些氨基酸可以具有l-、d-的构型、或彼此独立地是外消旋的。因此,有可能获得同分异构混合物以及外消旋混合物或非对映混合物、或纯的非对映异构体或对映异构体,这取决于不对称碳的数量和存在什么同分异构体或同分异构混合物。本发明的这些肽的优选的结构是纯的同分异构体,即,对映异构体或非对映异构体。
9、本发明提供的制备方法还能制备环肽衍生物或其盐;环肽衍生物包括:式(2)中环(gly-pro-gln-gly-pro-gln),其中r基团为选自h、(ch2)nch3、(ch2)mnh2、(ch2)xcooa1、(ch2)m cona2中的任意一种;其中的n、m、x为独立选自0或自然数;a1、a2独立选自h2、oh、nh2、cooh、c1-18烷基、苯基、杂芳基中任一种或多种。
10、所述环肽衍生物的盐包括环肽衍生物的金属盐,所述金属包括:锂、钠、钾、钙、镁、锰、铜、锌或铝。
11、所述环肽衍生物的盐包括环肽衍生物与有机碱形成的盐,所述有机碱包括:乙胺、二乙胺、乙二胺、乙醇胺、二乙醇胺、精氨酸、赖氨酸、组氨酸或哌嗪。
12、所述环肽衍生物的盐包括环肽衍生物与无机酸或有机酸形成的盐,所述有机酸包括:乙酸、柠檬酸、乳酸、丙二酸、马来酸、酒石酸、延胡索酸、苯甲酸、天冬氨酸、谷氨酸、琥珀酸、油酸、三氟乙酸、草酸、扑酸或葡萄糖酸;所述无机酸包括:盐酸、硫酸、硼酸或碳酸。
13、本发明提供的制备方法不局限于gln、gly、pro三种氨基酸,其他天然氨基酸和非天然氨基酸,均可通过本方法制备成环肽,但其制备产率、纯度、生物活性等取决于连接酶的活性与选择性,不排除连接酶突变后能够高产率、高纯度、高生物活性地制备其他环肽的可能性。
14、一方面,本发明提供了一种环肽的制备方法,首先有机合成短肽序列或者其片段,而后经酶催化环化而制得相应的环肽产物;所述酶包括l-谷氨酸连接酶ec 6.3.2.60、l-谷氨酸连接酶ec 6.3.2.60的突变体的一种或多种;所述l-谷氨酸连接酶ec 6.3.2.60的突变体的核苷酸序列为seq id no:1、seq id no:2、seq id no:3、seq id no:4中的任一种。
15、进一步的,所述l-谷氨酸连接酶ec 6.3.2.60的突变体的核苷酸序列如seq idno:1、seq id no:2、seq id no:3、seq id no:4中的任一种所示的序列缺失、取代、插入或添加1至10个氨基酸残基。
16、进一步的,所述l-谷氨酸连接酶ec 6.3.2.60的突变体的核苷酸序列如与seq idno:1、seq id no:2、seq id no:3、seq id no:4中的任一种所示的序列具有85%或更多同一性的序列。
17、上述序列的同一性可通过已知的手段比如fasta检索、blast检索等进行,具有同一性的序列均属于本发明的突变体。
18、优选的,所述l-谷氨酸连接酶ec 6.3.2.60的突变体的核苷酸序列为seq id no:4所示的序列。
19、在序列为seq id no:4的突变酶的催化环化下,环肽的收率最高,纯化后的纯度最高,制备得到的环肽在抗光老化、抗皱的功效上效果最佳,具有最高的抗酶解和皮肤渗透性能。
20、进一步的,所述环肽含有gln,gln在环化反应中位于短肽序列或其片段的首或尾。
21、本发明设计并定向突变得到的突变酶,具有连接gln与其他氨基酸的高特异性;针对性选用突变体,定向突变,筛选后得到现有突变体及其表达得到的酶可以高效合成目标产物。合成目标分子中作为在酰胺键连接酶中,l-谷氨酸连接酶可催化谷氨酸/谷氨酰胺与任意氨基酸偶联形成肽键,进而环化。
22、进一步的,所述环肽的环内含有3-6个酰胺键。
23、进一步的,所述环肽由gln、gly、pro三种氨基酸进行酰胺键合成及酶催化环化而制得。
24、
25、另一方面,本发明提供了上述环肽的制备方法制备而来的环肽。
26、本发明的环肽制备方法制备而来的环肽,具有其他制备方法而来的环肽而不具备的更好的抗光老化、抗皱的功效,以及更高的抗酶解和皮肤渗透性能。
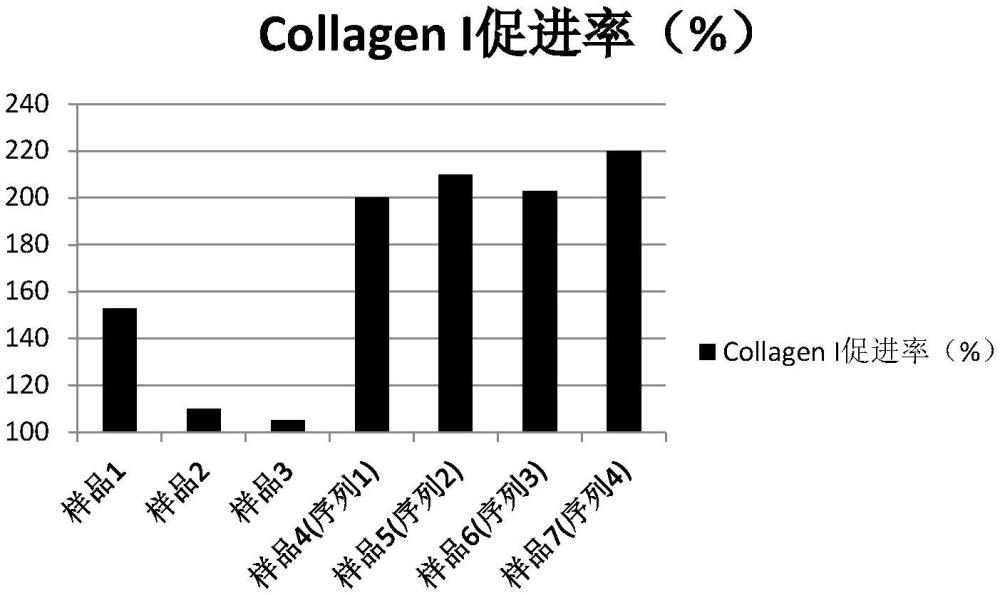
27、本发明还对不同方法制备得到的环肽功效进行了对比测试,发现本发明提供的化学-酶合成法得到的环肽在促进collagen i基因表达、抗蛋白酶酶解、透皮渗透功效方面均显著优与常规方法(全化学合成、全酶合成、化学-天然酶合成)制备得到的环肽,显示本发明提供的制备方法制备得到的环肽具有更高的生物活性。
28、上述现象可能的原因:一方面是产物纯度及含量差异,本发明提供的化学-酶合成法得到的产物收率高、纯化容易,纯化后的环肽纯度高、含量高,能够取得更好的效果;另一方面由于生产工艺不同引入了其他有益因素,例如环肽的构象更稳定、不包含拮抗环肽功效的杂质等,上述有益因素均使得本发明制备得到的环肽具有更高的生物活性。本发明提供的片段合成-酶促环化方法既具有生产制造意义,也能在应用上更加有益。
29、进一步的,所述环肽包含特定的氨基酸和/或特定的序列环(gln-gly-pro-x);至少一个gln、gly、pro;和/或至少两个谷氨酰胺gln、一个gly、一个脯氨酸pro;和/或至少两个gln、一个gly、一个pro;和/或至少两个gln、gly、pro序列;或其对映异构体;
30、另一方面,本发明提供了一种制备环肽的酶,所述酶由l-谷氨酸连接酶ec6.3.2.60定向突变而来;所述酶的核苷酸序列为seq id no:1、seq id no:2、seq id no:3、seq id no:4中的任一种。
31、优选的,所述酶的核苷酸序列为如seq id no:4所示的序列。
32、进一步的,所述l-谷氨酸连接酶ec 6.3.2.60的突变体的核苷酸序列如seq idno:1、seq id no:2、seq id no:3、seq id no:4中的任一种所示的序列缺失、取代、插入或添加1至10个氨基酸残基。
33、进一步的,所述l-谷氨酸连接酶ec 6.3.2.60的突变体的核苷酸序列如与seq idno:1、seq id no:2、seq id no:3、seq id no:4中的任一种所示的序列具有85%或更多同一性的序列。
34、上述序列的同一性可通过已知的手段比如fasta检索、blast检索等进行,具有同一性的序列均属于本发明的突变体。
35、另一方面,本发明提供了上述的酶用于高转化率地制备高纯度环肽的用途,所述环肽的制备首先有机合成短肽序列或者其片段,而后经所述的酶催化环化而制得环肽产物。
36、另一方面,本发明提供了一种由上述制备方法制备的环肽用于制备抗光老化的制剂的用途,所述制备方法制备得到的环肽能够促进collagen i基因表达,抵抗uv照射下collagen i胶原蛋白的减少。
37、另一方面,本发明提供了一种由上述制备方法制备的环肽用于制备抗皱的制剂的用途,所述制备方法制备得到的环肽能够促进collagen i基因表达,促进collagen i含量的增加,达到抵抗皱纹产生的作用。
38、胶原蛋白主要是由存在于皮肤真皮层的成纤维细胞产生的,是支撑皮肤的重要元素,其中collagen i为胶原i约占皮肤真皮层80%的比重,使得皮肤饱满充盈,促进collagen i含量的增加,可以达到一定抵抗皱纹产生的作用。uv照射的离体皮肤很明显的能够看出collagen i的减少,本发明提供的环肽通过促进collagen i基因表达,促进collagen i含量的增加,实现了抗光老化、抗皱功效。
39、另一方面,本发明提供了一种由上述制备方法制备的环肽用于制备不易降解的制剂的用途,其特征在于,所述制备方法制备得到的环肽具有抗蛋白酶酶解性能。
40、另一方面,本发明提供了一种由上述制备方法制备的环肽用于制备提高皮肤渗透的制剂的用途,其特征在于,所述制备方法中的酶能够提高产物环肽的渗透性能。
41、本发明的有益效果包括:
42、1、本发明所述的一系列胶原小分子环肽及其衍生物通过化学合成-生物酶催化连接合成法得到,合成方便,且对人体安全无刺激,可以应用于化妆品领域。
43、2、需要指出的是,此方法采用两段序列分别合成的方式,而后进行一个特异性酶催化环化,该步骤能够大幅提高多肽的合成速度;本发明的进一步的目的是提高粗品纯度,以提供具有更高纯度(>95%)的最终多肽产品。
44、3、另外在多肽固相合成中由于某些二级结构的形成会包埋反应位点,导致合成难度增大,而这种片段酶缩合法能阻止这些二级结构的形成,从而明显降低了合成难度,这也是传统方法所不具备的重要优势。
45、4、本发明所述的环肽及其衍生物或其盐的应用,其能够抵御酶解、更好的稳定性、生物利用度、提高成纤维细胞活性,促进成纤维细胞增殖,促进胶原蛋白生成,修复皮肤屏障(光损伤修复、划痕修复),增加皮肤弹性,提高皮肤紧致度,预防甚至治疗皮肤松弛,治疗、预防或修复皮肤老化或光老化,具有良好的皮肤修复、紧致效果,可以应用于皮肤修复、紧致抗皱等的产品中。
- 还没有人留言评论。精彩留言会获得点赞!