一种线粒体功能损伤评价胁迫条件下斑马鱼幼鱼发育毒性的方法与流程
本发明涉及一种线粒体功能损伤评价胁迫条件下斑马鱼幼鱼发育毒性的方法,属于生物。
背景技术:
1、线粒体最主要功能是供能,线粒体能为细胞的生命活动提供场所,是细胞内氧化磷酸化和形成atp的主要场所,有细胞“动力工厂(powerplant)”之称。线粒体还参与诸如细胞分化、细胞信息传递和细胞凋亡等过程,并拥有调控细胞生长和细胞周期的能力。
2、除了合成atp为细胞提供能量等主要功能外,线粒体还承担了许多其他生理功能。如调节膜电位并控制细胞程序性死亡,当线粒体内膜与外膜接触位点处生成了由己糖激酶(细胞质基质蛋白)、外周苯并二氮受体和电压依赖阴离子通道(线粒体外膜蛋白)、肌酸激酶(线粒体膜间隙蛋白)、adp-atp载体(线粒体内膜蛋白)和亲环蛋白d(线粒体基质蛋白)等多种蛋白质组成的通透性转变孔道(pt孔道)后,会使线粒体内膜通透性提高,引起线粒体跨膜电位的耗散,从而导致细胞凋亡。而在外界各种致病因素作用下线粒体极易出现损伤,造成线粒体功能的障碍,进一步导致细胞功能的损伤,引起细胞的自噬、凋亡。
3、斑马鱼最早作为胚胎发育生物学和遗传学的实验动物模型,具有易饲养、繁殖力强,发育快,受精卵透明易观察等特点,斑马鱼作为低等脊椎动物的代表,与人类基因同源性达87%,现在越来越广泛地应用于疾病模型创制、毒性检测以及环境健康风险评价等不同领域中。当前对生物发育毒性评价的研究只是单一的方面,并不能做一个准确、全面的评价。
4、因此,一种快速、直观、操作简便的利用线粒体功能损伤评价胁迫条件下生物发育毒性的方法亟待研究。
技术实现思路
1、本发明的目的在于提供一种线粒体功能损伤评价胁迫条件下斑马鱼幼鱼发育毒性的方法。
2、为实现上述目的及其他相关目的,本发明提供的技术方案是:一种线粒体功能损伤评价胁迫条件下斑马鱼幼鱼发育毒性的方法,包括下列步骤:
3、步骤1:利用至少8对雌雄野生型斑马鱼交配并产卵,收集受精卵并混匀在一起,均匀分组,包括至少两组对照组、至少一组高糖组和至少一组h2s组,对照组使用的培养液为胚胎培养液,高糖组使用的培养液为葡萄糖溶液,h2s组使用的培养液为h2s溶液,同等条件下进行培养;
4、培养过程中:第一组对照组和高糖组每隔10-14小时更换一次培养液, 第二组对照组和h2s组每隔20-28小时更换一次培养液,第五天开始每天更换培养液时投喂斑马鱼幼鱼饲料,观察斑马鱼生长形态;当斑马鱼表现出脊柱弯曲和卵黄囊水肿时,表明存在线粒体功能损伤;
5、线粒体荧光分析:利用转基因的线粒体自发荧光斑马鱼交配并产卵,收集受精卵并混匀在一起,重复上述操作,观察斑马鱼幼鱼线粒体荧光强弱变化;持续暴露在葡萄糖溶液里7天的和h2s溶液里5天的斑马鱼幼鱼线粒体荧光减弱,荧光越暗;表明存在线粒体功能损伤;
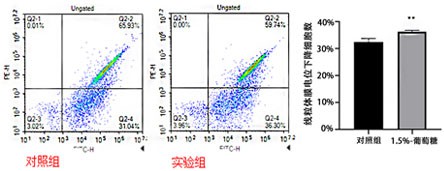
6、线粒体膜电位检测:对照组和高糖组于培养的第七天进行线粒体膜电位检测,各组分别取100条存活的斑马鱼幼鱼,先用细胞悬液制备试剂盒制备细胞悬液,再用线粒体膜电位检测试剂盒进行染色,利用流式细胞仪进行分析;当线粒体膜电位降低的细胞越多,表明线粒体功能损伤程度越严重。
7、优选的技术方案为:所述雌雄野生型斑马鱼为ab型。
8、优选的技术方案为:所述葡萄糖溶液的质量浓度为1.5%。
9、优选的技术方案为:所述h2s溶液的质量浓度为0.03%。
10、优选的技术方案为:培养条件为:28.5℃,光周期为:光照/黑暗14/10 小时。
11、本发明与现有技术相比具有的优点是:本发明既能够提供一种快速、直观、操作简便的评价在胁迫条件下线粒体功能损伤对斑马鱼幼鱼发育毒性的危害,又能够为线粒体功能损伤对斑马鱼幼鱼的发育毒性机制研究提供参考。该方法快速有效、成本低廉,安全无害,适于推广应用。
技术特征:
1.一种线粒体功能损伤评价胁迫条件下斑马鱼幼鱼发育毒性的方法,其特征在于:包括下列步骤:
2.根据权利要求1所述的线粒体功能损伤评价胁迫条件下斑马鱼幼鱼发育毒性的方法,其特征在于:所述雌雄野生型斑马鱼为ab型。
3.根据权利要求1所述的线粒体功能损伤评价胁迫条件下斑马鱼幼鱼发育毒性的方法,其特征在于:所述葡萄糖溶液的质量浓度为1.5%。
4.根据权利要求1所述的线粒体功能损伤评价胁迫条件下斑马鱼幼鱼发育毒性的方法,其特征在于:所述h2s溶液的质量浓度为0.03%。
5.根据权利要求1所述的线粒体功能损伤评价胁迫条件下斑马鱼幼鱼发育毒性的方法,其特征在于:培养条件为:28.5℃,光周期为:光照/黑暗14/10 小时。
技术总结
一种线粒体功能损伤评价胁迫条件下斑马鱼幼鱼发育毒性的方法,该方法利用至少8对雌雄野生型斑马鱼交配并产卵,收集受精卵并混匀在一起,均匀分组,包括对照组、高糖组和H<subgt;2</subgt;S组,对照组使用的培养液为胚胎培养液,高糖组使用的培养液为葡萄糖溶液,H<subgt;2</subgt;S组使用的培养液为H<subgt;2</subgt;S溶液,同等条件下进行培养,通过线粒体荧光分析、线粒体膜电位检测斑马鱼幼鱼发育毒性。该方法是一种快速、直观、操作简便的评价在胁迫条件下线粒体功能损伤对斑马鱼幼鱼发育毒性的危害,又能够为线粒体功能损伤对斑马鱼幼鱼的发育毒性机制研究提供参考。
技术研发人员:彭仁义,王义飞,谭云
受保护的技术使用者:温达生物科技(苏州)有限公司
技术研发日:
技术公布日:2024/1/15
- 还没有人留言评论。精彩留言会获得点赞!