一种无卤素离子液体制备环状碳酸酯的方法
本发明属于有机催化,特别涉及一种无卤素离子液体催化剂催化二氧化碳和环氧化物进行环加成反应制备环状碳酸酯类化合物的方法。
背景技术:
1、上世纪70年代至今,全球碳排放与全球经济发展基本呈现出正相关关系,随着全球经济发展,碳排放和人均排放均有大幅增长。化石能源的使用和人类生产活动导致大气中二氧化碳的浓度急剧增加,引起了全球变暖,海平面上升和频繁的极端天气等诸多世界性难题。因此,固定和利用二氧化碳转化成具有较高附加值的化学成为当下的研究热点。二氧化碳与环氧化物结合生成环状碳酸酯的方法是利用二氧化碳最有前景的路线之一。
2、二氧化碳的化学性质极其稳定(δfh°=-394kj/mol),环加成反应需要能够同时激活二氧化碳和环氧化物的催化剂。通常,这些反应需要苛刻的条件,比如高温、高压以及高纯的二氧化碳。
3、常用的催化剂有金属复合物、碱金属盐、金属氧化物、离子液体和有机催化剂。金属催化剂催化得到的碳酸酯产物容易有金属残留,无法直接应用于生物医学和微电子等领域。cn115364886b提供了一种等离子体光催化材料——cn-ag光催化剂,其合成原料为贵金属,且合成温度较高(达到500℃),成本昂贵,不适于大规模应用。相较之下,有机催化剂具有能耗小、环境友好的特点,同时该反应的原子利用率为100%,符合绿色化学的思想。但是这些催化剂或原料昂贵,或纯化方法复杂,或合成步骤过多使得产率下降,或含卤素造成金属设备腐蚀,从而限制了其广泛生产应用。因此,寻找高效稳定的应用于催化环氧化物固定二氧化碳的有机催化剂仍然是化学工业面临的挑战之一。
技术实现思路
1、本发明的目的在于提供一种无卤素离子液体催化剂催化二氧化碳和环氧化物进行环加成反应制备环状碳酸酯类化合物的方法。
2、本发明的技术方案如下:
3、一种二氧化碳和环氧化物的环加成反应,采用式(ii)或(iii)或(iv)所示的环氧化物和二氧化碳在式(i)所示的无卤素离子液体催化剂的催化下生成环状碳酸酯类化合物:
4、
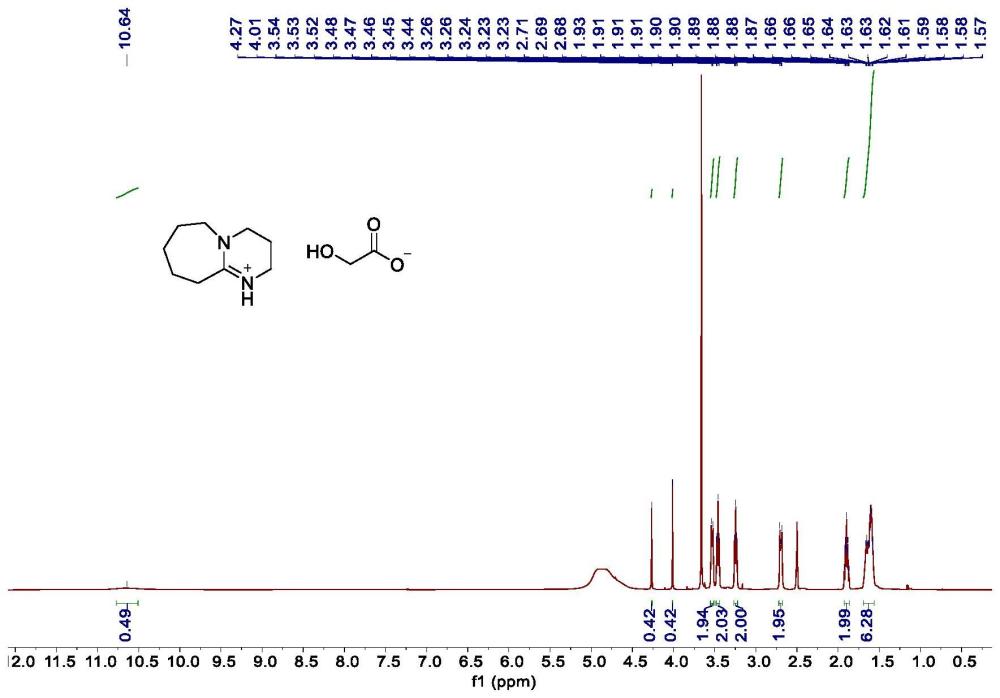
5、其中,式(i)所示的催化剂是由a和α-羟基酸制备得到的无卤素离子液体催化剂,a为具有双杂环结构的脒类有机强碱或胍类有机强碱;
6、优选的,a选自1,8-二氮杂二环[5.4.0]十一碳-7-烯(dbu)、1,5,7-三氮杂双环[4.4.0]癸烯-5-烯(tbd)、7-甲基-1,5,7-三氮杂二环[4.4.0]癸-5-烯(mtbd)、1,5-二氮杂双环[4.3.0]壬-5-烯(dbn);
7、r1选自h,甲基,苯基,苄基;
8、催化剂制备方法:
9、将α-羟基酸(1eq)溶于甲醇溶液中备用,在25ml圆底烧瓶中加入转子,取有机强碱(1eq)置于瓶中,在冰浴条件下(-20~5℃),边搅拌边缓慢滴加α-羟基酸-甲醇溶液,室温下搅拌5h,溶液逐渐变为淡黄色液体,将反应液真空浓缩,乙醚沉淀洗涤三次,柱层析(dcm:meoh=1:1)纯化,真空干燥至恒重即得到催化剂为黄色粘稠液体,即为无卤素离子液体催化剂。
10、优选的,无卤素离子液体催化剂选自如编号1~16所示的结构:
11、
12、式(ii)所示环氧化物中的r2、r3独立地选自氢、具有1~4个碳原子的直链或支链烷基、乙烯基、烯丁基、苯基、卤素或烷基取代的苯基、氯或溴取代的烷基、r4-o-ch2-,所述的r4选自苯基、烯丙基或1~4个碳原子支链或直链的烷基;
13、优选的,所述的r2、r3独立地选自氢、正丁基、烯丁基、乙烯基、卤代甲基、苯基、或r4-o-ch2-,所述的r4选自苯基、烯丙基、叔丁基或甲基。
14、更优选的,所述的环氧化物的结构如下:
15、
16、环状碳酸酯类化合物的制备方法为:
17、步骤一:将式(i)所示的无卤素有机盐催化剂加入反应容器,将式(ii)或(iii)或(iv)所示的环氧化合物加入反应容器,并用二氧化碳置换反应容器中的空气;
18、步骤二:向反应容器中充入二氧化碳至0.05~2mpa,升温至60~150℃;反应进行1~24h后得到含产物的溶液,通过柱层析得到环状碳酸酯类化合物;
19、其中,环氧化合物与无卤素有机盐催化剂的摩尔比为(150~5):1。
20、有益效果
21、(1)本发明所用催化剂能够高效合成具有高附加值的环状碳酸酯,相比于现有技术中利用金属催化剂合成的环状碳酸酯,具有产率高、无金属残留、应用广泛等特点。在生物医药和微电子等对金属残留要求严格的领域具有很大商业应用的潜力。
22、(2)本发明所用催化剂合成方法简单,更加易得且不含卤素、成本低廉。目前报道的有机催化剂或原料昂贵,或纯化方法复杂,或合成步骤过多使得产率下降,或含卤素造成金属设备腐蚀。反应过程不需要使用溶剂,避免有机溶剂的毒性,催化剂溶解性好,均相催化,反应效率大大提高。
23、综上所述,本发明相比于现有的其他催化体系具有温和、高效、易制备、不含金属和卤素等明显优势。
技术特征:
1.一种无卤素离子液体催化剂催化环氧化物和二氧化碳制备环状碳酸酯类化合物的方法,其特征在于,采用式i所示的催化剂催化式ii、式iii或式iv所示的环氧化物和二氧化碳进行环加成反应,得到环状碳酸酯类化合物,
2.如权利要求1所述的制备方法,其特征在于,所述式i所示的催化剂中a独立地选自1,8-二氮杂二环[5.4.0]十一碳-7-烯、1,5,7-三氮杂双环[4.4.0]癸烯-5-烯、7-甲基-1,5,7-三氮杂二环[4.4.0]癸-5-烯、1,5-二氮杂双环[4.3.0]壬-5-烯。
3.如权利要求1所述的制备方法,其特征在于,所述式i所示的催化剂选自如式1~16所示的结构:
4.如权利要求1所述的制备方法,其特征在于,所述式ii所示的环氧化物中的r2为氢,r3独立地选自氢、正丁基、烯丁基、乙烯基、氯代甲基、溴代甲基、苯基、或r4-o-ch2-;
5.如权利要求1所述的制备方法,其特征在于,所述式ii所示的环氧化物选自如式17~28所示的环氧化物:
6.如权利要求1所述的制备方法,其特征在于,所述式i所示的催化剂的制备方法为:
7.如权利要求6所述的制备方法,其特征在于,步骤一所述α-羟基酸独立地选自乙醇酸、dl-扁桃酸、乳酸或d-3-苯基乳酸;步骤二所述的低温条件为-20~10℃;步骤三所述的纯化处理为将待处理溶液真空浓缩,用乙醚沉淀洗涤,然后用柱层析法进行纯化。
8.如权利要求1所述的制备方法,其特征在于,所述的环加成反应为:
9.如权利要求8所述的制备方法,其特征在于,步骤二中二氧化碳的初始压力为0.05~2mpa,反应温度为60~150℃,反应时间为1~24h,环氧化物与无卤素离子液体催化剂的摩尔比为(150~5):1。
10.如权利要求1所述的制备方法,其特征在于,所述的催化剂独立地选自式1~4、6~8、10~12、14~16所示的催化剂;所述的环氧化物选自式17~28所示的环氧化物;反应初始二氧化碳的压力为0.1~1mpa,反应温度为80~140℃,反应时间为6~24h;环氧化物与无卤素离子液体催化剂的摩尔比为(100~10):1。
技术总结
本发明提供了一种无卤素离子液体催化剂催化二氧化碳和环氧化物进行环加成反应制备环状碳酸酯类化合物的方法,本发明属于有机催化技术领域。本发明所用催化剂能够高效合成具有高附加值的环状碳酸酯,相比于现有技术中利用金属催化剂合成的环状碳酸酯,具有产率高、无金属残留、应用广泛等特点。在生物医药和微电子等对金属残留要求严格的领域具有很大商业应用的潜力。本发明所用催化剂合成方法简单,更加易得且不含卤素、成本低廉。
技术研发人员:郭凯,李宁,何军,李振江,胡永铸,黄卫州,常通,吴禧群,王俊晖
受保护的技术使用者:南京工业大学
技术研发日:
技术公布日:2024/2/21
- 还没有人留言评论。精彩留言会获得点赞!