酮还原酶突变体、其组合物、生物材料及应用的制作方法
本发明涉及生物工程,具体涉及酮还原酶突变体、其组合物、生物材料及应用。
背景技术:
1、达芦那韦(darunavir)是fda批准用于抗人类免疫缺陷病毒(hiv)感染的新药,是第二代hiv蛋白酶抑制剂,可以阻断hiv病毒复制的蛋白酶,当与其他抗hiv药物联用时,可以降低病毒载量,提高免疫能力。达芦那韦是由强生公司的子公司爱尔兰的泰博特克药品公司(tibotec)开发,于2006年7月首次在美国上市,其商品名为:prezista,化学名为:[(1r,5s,6r)-2,8-二氧双环[3.3.0]-癸烷-6-基]-n-[(2s,3r)-4-[(4-氨基苯基)磺酰基-(2-甲基丙基)氨基]-3-羟基-1-苯基-丁烷-2-基]氨基甲酸酯。达芦那韦已在美国、欧盟及其他国家和地区上市。
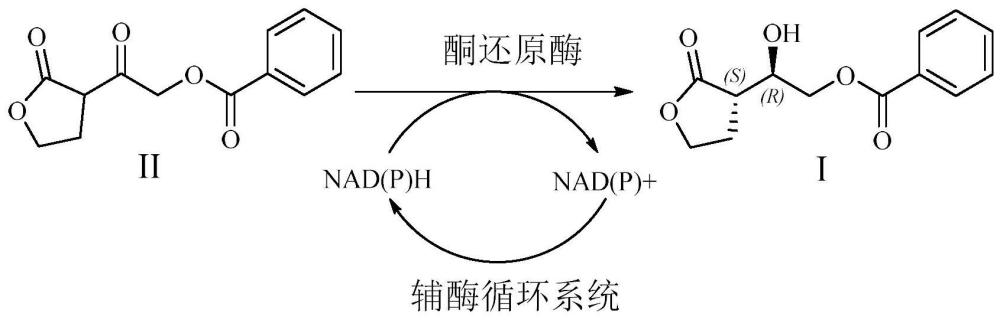
2、手性化合物i是合成达芦那韦的中间体,其具有如图1所示的结构式。该化合物及其异构体的合成包括手性催化和酮还原酶催化合成。
3、文献more,ganesh v.,et al."ru-catalyzed asymmetric transferhydrogenation ofα-acyl butyrolactone via dynamic kinetic resolution:asymmetric synthesis of bis-thf alcohol intermediate of darunavir."tetrahedron letters 66(2021):152831.研究了手性钌配体催化剂(r,r)-ru-fsdpen构建化合物i异构体的方法,因用到昂贵的重金属催化剂不太适合产业化;
4、现有专利中已涉及利用酶催化合成化合物i,欧洲专利ep2634180a1涉及使用不同羰基还原酶来催化制备多种手性达芦那韦中间体,并且提及化合物i及其异构体的合成,其中16种羰基还原酶均为来自codexis inc.的商业酶,其中包括来自saccharomycescerevisiae ynl331c的酮还原酶催化反应合成化合物i,并披露了该酮还原酶相关信息(该专利已被撤销);cn110372641b(同族专利wo2019196263a1),以及cn110272398b(同族专利wo2019174176a1),披露用来自saccharomyces kudriavzevii的醛酮还原酶催化合成多种达芦那韦手性中间体,包括提及化合物i的制备。
5、但是上述专利中存在所用酶的选择性还不够理想、酶活力偏低,投料浓度低,投酶量大,原料转化不完全等问题,导致成本高,反应物需分离产物和剩余原料等。
技术实现思路
1、有鉴于此,本发明要解决的技术问题在于提供酮还原酶突变体、其组合物、生物材料及应用。
2、本发明提供了酮还原酶在达芦那韦中间体合成中的应用,所述酮还原酶具有如seq id no:1所示的氨基酸序列。
3、本发明提供了酮还原酶突变体,所述的酮还原酶突变体包括如seq id no:1所示的氨基酸序列的第235位色氨酸突变为酪氨酸和如下所示突变中的至少一种:
4、第257位谷氨酸突变为天冬氨酸;和/或
5、第259位亮氨酸突变为丙氨酸;和/或
6、第272位谷氨酸突变为丝氨酸。
7、进一步的,本发明所述的酮还原酶突变体包括:
8、如seq id no:1所示的氨基酸序列的第235位色氨酸突变为酪氨酸和第259位亮氨酸突变为丙氨酸;或
9、如seq id no:1所示的氨基酸序列的第235位色氨酸突变为酪氨酸,第259位亮氨酸突变为丙氨酸和第272位谷氨酸突变为丝氨酸;或
10、如seq id no:1所示的氨基酸序列的第235位色氨酸突变为酪氨酸、第257位谷氨酸突变为天冬氨酸和和第259位亮氨酸突变为丙氨酸;或
11、如seq id no:1所示的氨基酸序列的第235位色氨酸突变为酪氨酸,第257位谷氨酸突变为天冬氨酸,第259位亮氨酸突变为丙氨酸和第272位谷氨酸突变为丝氨酸。
12、本发明以筛选得到的源于saccharomyces cerevisiae s288c的野生型酮还原酶进行突变,获得酮还原酶突变体,第一次将其应用于达芦那韦中间体的合成,与野生型酮还原酶相比,本发明所述酮还原酶突变体对底物(酮化合物ii)的反应具有更高的酶活力和立体选择性,酶用量明显减少,反应产物i的异构体纯度大幅度提高,能够更好的满足工业化生产需求。并且本发明中,酮还原酶突变位置的不同,获得的突变体的转化率以及最终产物异构体纯度存在差异;其中,以如seq id no:1所示的氨基酸序列的第235位色氨酸突变为酪氨酸和第259位亮氨酸突变为丙氨酸的酮还原酶突变体的转化率达到99.02%,纯度达到97%;以如seq id no:1所示的氨基酸序列的第235位色氨酸突变为酪氨酸,第259位亮氨酸突变为丙氨酸和第272位谷氨酸突变为丝氨酸的酮还原酶突变体的转化率达到99.48%,纯度达到96.92%;以如seq id no:1所示的氨基酸序列的第235位色氨酸突变为酪氨酸、第257位谷氨酸突变为天冬氨酸和和第259位亮氨酸突变为丙氨酸的酮还原酶突变体的转化率达到99.24%,纯度达到96.21%;以如seq id no:1所示的氨基酸序列的第235位色氨酸突变为酪氨酸,第257位谷氨酸突变为天冬氨酸,第259位亮氨酸突变为丙氨酸和第272位谷氨酸突变为丝氨酸的酮还原酶突变体的转化率达到99.86%,纯度达到96.20%。
13、本发明提供了组合物,其包括组合物1或组合物2中的任意一种,
14、所述组合物1包括:辅酶再生酶和酮还原酶;
15、所述组合物2包括:辅酶再生酶和本发明所述的酮还原酶突变体;
16、所述辅酶再生酶包括葡萄糖脱氢酶、异丙醇脱氢酶或甲酸脱氢酶中的任意一种;
17、所述葡萄糖脱氢酶的氨基酸序列如seq id no:6所示;
18、所述异丙醇脱氢酶的氨基酸序列如seq id no:7所示;
19、所述甲酸脱氢酶的氨基酸序列如seq id no:8所示;
20、所述酮还原酶的氨基酸序列如seq id no:1所示。
21、本发明提供了酮还原酶制剂、酮还原酶突变体酶制剂,或所述组合物制剂,所述制剂可以为固体、液体或半固体,所述制剂中还可以包括稳定剂、表面活性剂、缓冲液等,用于维持或协助所述酶的保存或发挥作用。
22、本发明提供了生物材料,其包括如下a)~d)所示中的至少一种:
23、a)、编码本发明所述的酮还原酶变体或本发明所述的组合物的核酸;
24、b)、含有a)所述核酸的重组载体;
25、c)、转化或转染如b)所述重组载体的宿主细胞;
26、d)、培养如c)所述的宿主细胞获得的混合物。
27、本发明所述的核酸可以是dna、rna、cdna或pna。在本发明实施例中,所述核酸为dna形式。所述dna形式包括cdna、基因组dna或人工合成的dna。所述dna可以是单链的或是双链的。核酸可以包括具有不同功能的核苷酸序列,如编码区和非编码区如调控序列(例如启动子或转录终止子)。核酸在拓扑学上可以是线性或环状的。核酸可以是载体(如表达或克隆载体)的一部分,或一个片段。所述核酸可直接从天然来源获得,或者可由重组、酶法或化学技术辅助制备。
28、在本发明中,所述核酸可以是经优化的也可以是未经优化的,这些优化包括但不限于:密码子使用偏好性,消除不利于表达的二级结构(如发夹结构),改变gc含量,cpg二核苷酸含量,mrna的二级结构,隐蔽剪接位点,早期多聚腺苷化位点,内部核糖体进入位点和结合位点,负cpg岛,rna不稳定区,重复序列(直接重复、反向重复等)和可能影响克隆的限制性位点等。
29、本发明中还提供了包含所述核酸的转录单元,所述转录单元是指启动子开始至终止子结束的dna序列。启动子和终止子两侧或之间还可包括调控片段,所述调控片段可以包括与核酸序列可操作地连接的启动子、增强子、转录终止信号、多腺苷酸化序列、复制起点、核酸限制性位点、和同源重组位点,例如启动子的增强子,poly(a)信号等。
30、本发明所述重组载体,是指重组的核酸载体,是一种重组dna分子,其包含期望的编码序列和对可操作连接的编码基因在具体宿主生物内的表达所必不可少的合适的核酸序列或元件。对原核细胞中的表达必需的核酸序列或元件包括启动子,核糖体结合位点及可能的其它序列。已知原核细胞利用启动子,增强子以及终止子。一经转化进入合适的宿主,载体可以独立于宿主基因组进行复制和发挥作用,或者,在一些情况下,自己整合进入基因组。在本说明书中,“质粒”和“载体”有时可以交换通用,因为质粒是当前最普遍使用的载体形式。然而,本发明意图包括表达载体的这样的其它形式,其发挥等价作用,其在本领域是已知的或将变为已知的,包括但不限于:质粒,噬菌体颗粒,病毒载体和/或仅为潜在的基因组插入物。具体实施例中,所述核酸可构建于各种原核表达载体中,例如,pet系列载体,本发明的具体实施例中为pet28a。
31、本发明的宿主细胞,其转化或转染所述重组载体,使用重组dna技术构建的载体转化或转染宿主细胞,这样转化的宿主细胞有能力复制编码蛋白质的载体或表达期望蛋白质。
32、进一步的,所述转化的方法包括:化学转化和电转化;所述转染的方法包括磷酸钙共沉淀、人工脂质体法、病毒转染。所述的病毒转染包括腺病毒转染、腺相关病毒转染、慢病毒转染等。
33、更进一步的,本发明提供的宿主细胞,其来源包括植物、动物、细菌、真菌、噬菌体或病毒,本发明对此不做限定。本发明的一些具体实施例中,所述宿主为细菌,具体的为大肠杆菌,更具体的为大肠杆菌bl21(de3)。
34、本发明提供了如下i)~iv)所示中的至少一种在达芦那韦中间体合成中的应用:
35、i)、氨基酸序列如seq id no:1所示的酮还原酶;
36、ii)、本发明所述的酮还原酶突变体;
37、iii)、本发明所述的组合物;
38、iv)、本发明所述的生物材料。
39、本发明提供了达芦那韦中间体的制备方法,包括利用如下i)~iv)所示中的至少一种进行达芦那韦中间体合成:
40、i)、氨基酸序列如seq id no:1所示的酮还原酶;
41、ii)、本发明所述的酮还原酶突变体;
42、iii)、本发明所述的组合物;
43、iv)、本发明所述的生物材料。
44、进一步的,本发明所述的制备方法,包括如下步骤:
45、在催化剂、辅酶再生酶、辅底物、辅酶存在的条件下,将如式ii所示的底物反应生成如式i所示的达芦那韦中间体;
46、式i和式ii所示的结构如下:
47、
48、
49、其中,
50、所述催化剂为如seq id no:1所示的酮还原酶或本发明所述的酮还原酶突变体中的任意一种;所述酮还原酶的氨基酸序列如seq id no:1所示;
51、所述辅酶再生酶包括葡萄糖脱氢酶、异丙醇脱氢酶或甲酸脱氢酶中的任意一种;
52、所述葡萄糖脱氢酶的氨基酸序列如seq id no:6所示;
53、所述异丙醇脱氢酶的氨基酸序列如seq id no:7所示;
54、所述甲酸脱氢酶的氨基酸序列如seq id no:8所示;
55、所述辅底物包括异丙醇、葡萄糖或甲酸铵;
56、所述辅酶为nadp。
57、更进一步的,本发明所述的制备方法中,
58、所述辅酶再生酶为异丙醇脱氢酶,则辅底物为异丙醇;
59、所述辅酶再生酶为葡萄糖脱氢酶,则辅底物为葡萄糖;
60、所述辅酶再生酶为甲酸脱氢酶,则辅底物为甲酸铵。
61、具体的,本发明中,
62、所述底物的浓度为0.05g/ml~0.1g/ml;
63、含有所述催化剂的菌体的浓度为0.025g/ml~0.05g/ml;
64、含有所述辅酶再生酶的菌体的浓度为0.005g/ml~0.02g/ml;
65、异丙醇的浓度为50μl/ml;
66、所述葡萄糖的浓度为0.05g/ml~0.1g/ml;
67、所述甲酸铵的浓度为0.05g/ml;
68、所述nadp在反应体系中,使用的是质量分数5%的nadp水溶液,其用量为3μl/ml~5μl/ml;
69、所述反应的缓冲液为0.1m ph 7.5三乙醇胺缓冲液;
70、所述反应的条件为20℃~50℃、ph为4~10,优选反应温度为30℃、反应液ph为7.5;
71、所述底物需要在反应前需要溶解于dmso,底物在dmso中的浓度为0.5g/ml~1g/ml。
72、本发明的具体实施例中,在1ml的反应体系中,酮还原酶突变体酶液加入125μl(酶液中含有的菌体浓度为0.2g/ml),对应体系中的含有酮还原酶或酮还原酶突变体的菌体的浓度为0.025g/ml;异丙醇脱氢酶酶液加入100μl(所述酶液中含有的菌体浓度为200g/l=0.2g/ml),对应的含有所述异丙醇脱氢酶的菌体的浓度为0.02g/ml;加入异丙醇50μl,对应浓度为50μl/ml;5%nadp水溶液加入5μl,对应的浓度为5μl/ml;原料(底物)加入50mg,对应的浓度为0.05g/ml(此时,酮还原酶突变体酶液中菌体与原料的浓度比为0.5:1),且原料利用100μl dmso溶解后加入,原料在dmso中的溶解浓度为0.5g/ml;
73、本发明的具体实施例中,在1ml的反应体系中,酮还原酶或酮还原酶突变体酶液加入250μl(所述酶液中含有的菌体浓度为0.2g/ml),对应的含有酮还原酶或酮还原酶突变体的菌体的浓度为0.05g/ml;异丙醇脱氢酶酶液加入100μl(酶液中含有的菌体浓度为0.2g/ml),对应的含有所述异丙醇脱氢酶的菌体的浓度为0.02g/ml;加入异丙醇50μl,对应浓度为50μl/ml;5%nadp水溶液加入5μl,对应的用量为5μl/ml;原料(底物)加入50mg,对应的浓度为0.05g/ml(此时,含有酮还原酶或酮还原酶突变体酶液中菌体与原料的浓度比为1:1),原料利用100μl dmso溶解后加入,原料在dmso中的溶解浓度为0.5g/ml;
74、本发明的另一些具体的实施例中,在20ml的反应体系中,酮还原酶或酮还原酶突变体酶液加入5ml(所述酶液中含有的菌体浓度为0.2g/ml),对应体系中含有酮还原酶或酮还原酶突变体的菌体的浓度为0.05g/ml;异丙醇脱氢酶酶液加入2ml(酶液中含有的菌体浓度0.2g/ml),对应体系含有所述异丙醇脱氢酶的菌体的浓度为0.02g/ml;加入异丙醇1ml,对应浓度为50μl/ml;5% nadp水溶液加入100μl,对应的用量为5μl/ml;原料(底物)加入2g,对应的浓度为0.1g/ml(此时,含有酮还原酶或酮还原酶突变体酶液中菌体与原料的浓度比为0.5:1),此时,原料利用2ml dmso溶解后加入,原料在dmso中的溶解浓度为1g/ml;
75、本发明的另一些具体的实施例中,在20ml的反应体系中,酮还原酶突变体酶液加入5ml(所述酶液中含有的菌体浓度为0.2g/ml),对应体系含有酮还原酶或酮还原酶突变体的菌体的浓度为0.05g/ml;葡萄糖脱氢酶酶液加入1ml(酶液中含有的菌体浓度0.2g/ml),对应的含有所述葡萄糖脱氢酶的菌体的浓度为0.01g/ml;加入葡萄糖2g,对应浓度为0.1g/ml;5% nadp水溶液加入100μl,对应的用量为5μl/ml;原料(底物)加入2g,对应的浓度为0.1g/ml(此时,酮还原酶突变体酶液中菌体与原料的浓度比为0.5:1),原料利用2ml dmso溶解后加入,原料在dmso中的溶解浓度为1g/ml;
76、本发明的另一些具体的实施例中,在20ml的反应体系中,酮还原酶突变体酶液加入5ml(所述酶液中含有的菌体浓度为0.2g/ml),对应的含有酮还原酶或酮还原酶突变体的菌体的浓度为0.05g/ml;甲酸脱氢酶酶液加入2ml(酶液中含有的菌体浓度0.2g/ml),对应的含有所述甲酸脱氢酶的菌体的浓度为0.02g/ml;加入甲酸铵1g,对应浓度为0.05g/ml;5% nadp水溶液加入100μl,对应的用量为5μl/ml;原料(底物)加入2g,对应的浓度为0.1g/ml(此时,酮还原酶突变体酶液中菌体与原料的浓度比为0.5:1),原料利用2ml dmso溶解后加入,原料在dmso中的溶解浓度为1g/ml;
77、在本发明的另一些实施例中,在2l的反应瓶中,反应体系为1l,酮还原酶突变体酶液加入250ml(所述酶液中含有的菌体浓度为0.2g/ml),对应体系含有酮还原酶突变体的菌体的浓度为0.05g/ml;葡萄糖脱氢酶酶液加入50ml(酶液中含有的菌体浓度0.2g/ml),对应的含有所述葡萄糖脱氢酶的菌体的浓度为0.01g/ml;加入葡萄糖100g,对应浓度为0.1g/ml;5% nadp水溶液加入6ml,对应的用量为6μl/ml;原料(底物)加入100g,对应的浓度为0.1g/ml(此时,酮还原酶突变体酶液中菌体与原料的浓度比为0.5:1),原料利用100mldmso溶解后加入,原料在dmso中的溶解浓度为1g/ml;
78、本发明中,对所述的制备方法进行了优化,辅酶循环系统的筛选,所述辅酶循环系统包括:
79、由辅酶再生酶异丙醇脱氢酶和其辅底物异丙醇组成的辅酶循环系统;
80、由辅酶再生酶葡萄糖脱氢酶和其辅底物葡萄糖组成的辅酶循环系统;
81、由辅酶再生酶甲酸脱氢酶和其辅底物甲酸铵组成的辅酶循环系统;
82、这三种辅酶循环系统进行筛选,结果表明,以由辅酶再生酶葡萄糖脱氢酶和其辅底物葡萄糖组成的辅酶循环系统的底物转化效果最好,转化成本最低。
83、本发明中,对所述的制备方法进行了优化,还包括对反应ph和温度的优化,实验结果表明在反应温度为20℃~50℃、ph为4~10的范围内,温度为30℃、ph为7.5时转化率最好,产物异构体纯度最好。
84、本发明中,所述酮还原酶、酮还原酶突变体、辅酶再生酶均通过将目的基因与载体重组获得重组载体后构建基因工程菌株,所述基因工程菌株经培养和诱导获得上所述酶,将上述酶用于达芦那韦中间体的合成中,与化学合成相比较,合成步骤简单、成本低。
85、进一步的,本发明中,所述培养利用的培养基为任何可使菌体生长并诱导产生前述酶的培养基,优选lb培养基(蛋白胨10g/l,酵母粉5g/l,nacl10g/l,蒸馏水溶解,ph7.0),培养方法和培养条件可以根据宿主类型和培养方法、实验条件等因素的不同按需调整。
86、本发明将以筛选得到的源于saccharomyces cerevisiae s288c的野生型酮还原酶进行突变,获得酮还原酶突变体,第一次将其应用于达芦那韦中间体的合成,与野生型酮还原酶相比,本发明所述酮还原酶突变体对底物(酮化合物ii)的反应具有更高的酶活力和立体选择性,酶用量明显减少,反应产物i的异构体纯度大幅度提高,能够更好的满足工业化生产需求。
- 还没有人留言评论。精彩留言会获得点赞!