一种T细胞的活化方法及其应用与流程
本发明属于生物,涉及一种t细胞的活化方法及其应用。
背景技术:
1、近年来肿瘤的免疫治疗获得突破进展,而t细胞则是主要效应细胞。以pd 1抗体为代表的t细胞免疫调节抗体快速进入临床,广谱用于肿瘤治疗,但有效人群比例较低,在最大适应症肺癌有效率约为18%。联合免疫治疗是提高疗效的发展方向,包括pd-1抗体联合化疗、放疗、抗血管生成药物和联合治疗策略,此对于扩大收益人群,延长病人存活、甚至治愈肿瘤具有现实意义,也是国际公认的研究方向。
2、car-t和tcr-t疗法是目前过继性免疫细胞疗法的研究热点,无论是car-t还是tcr-t细胞的体外培养,t细胞都需要被激活后才能进行后续操作步骤,因此寻找一种t细胞高效的活化激活方法是十分重要的。
技术实现思路
1、为了解决现有技术中存在的技术问题,本发明提供了以下技术方案:
2、本发明第一方面提供了一种t细胞的活化方法,所述活化方法包括如下步骤:
3、1)样本添加淋巴分离液,离心,分离得到pbmc;
4、2)步骤1)中pbmc加生理盐水,离心,收集pbmc;取少量pbmc,测cd3+t细胞比例;
5、3)取磁珠,涡旋,加等体积dpbs混匀,磁力架上1min,弃上清;
6、4)根据步骤2)中测量结果,调节cd3+t细胞浓度,步骤3)磁珠加入细胞悬液,混匀,室温孵育,使用dpbs稀释,将稀释后磁珠和细胞混合物放置于磁力架2min,弃上清;
7、5)用t细胞扩增培养基重悬磁珠和细胞混合物,调整细胞密度,置于37℃的5%浓度的co2培养箱中培养,去除磁珠,继续培养至14天,得到活化的t细胞。
8、如本文所用,术语“t细胞”或“t淋巴细胞”是本领域公认的,并且旨在包括胸腺细胞、初始t淋巴细胞、未成熟t淋巴细胞、成熟t淋巴细胞、静息t淋巴细胞或激活的t淋巴细胞。t细胞可以是t辅助(th)细胞,例如t辅助1(th1)或t辅助2(th2)细胞。t细胞可以是辅助t细胞(htl;cd4+t细胞)、细胞毒性t细胞(ctl;cd8+t细胞)、肿瘤浸润性细胞毒性t细胞(til;cd8+t细胞)、cd4+cd8+t细胞、cd4-cd8-t细胞、表达t细胞受体(tcr)的α和β链的αβt细胞和表达tcrγ和δ链的γδt细胞,或t细胞的任何其他子集。适用于特定实施方案的其他说明性t细胞群包括记忆t细胞,合适地为早期记忆t细胞。术语“t细胞”在其范围内包括天然t细胞(例如,从生物体分离的,所述生物体例如为哺乳动物,例如,人,例如,受试者)、离体生长的t细胞和遗传工程化的t细胞。术语t细胞还包括包含t细胞受体(例如,天然tcr,或重组tcr)的t细胞和包含人工t细胞受体的t细胞(例如,car-t细胞)。
9、进一步,步骤1)中分离pbmc使用离心机升速9降速0分离得pbmc的方法。
10、进一步,所述步骤1)中样本来自哺乳动物。
11、进一步,所述步骤1)中样本来自人或其他非人哺乳动物。
12、进一步,所述样本包括血液样本。
13、术语“样本”来自于任何可携带t细胞的细胞悬液,包括但不限于血液、组织液、淋巴液等。在广义上认为,术语“样本”与“生物样本”同义,是指从如本文所述的感兴趣的生物来源(例如,组织或生物体或细胞培养物)获得或衍生的样本。在一些实施方案中,感兴趣的来源包括生物体,诸如动物或人。在一些实施方案中,生物样本为或包含生物组织或流体。在一些实施方案中,生物样本可为或包含骨髓;血液;血细胞;腹水;组织或细针活检样本;含细胞体液;自由浮动的核酸;痰液;唾液;尿;脑脊液、腹膜液;胸膜液;粪便;淋巴;妇科液体;皮肤拭子;阴道拭子;口腔拭子;鼻拭子;冲洗液或灌洗液,诸如导管灌洗液或支气管肺泡灌洗液;抽吸物;刮擦物;骨髓样本;组织活检样本;手术样本;粪便、其它体液、分泌物和/或排泄物;和/或来自它们的细胞等。在一些实施方案中,生物样本为或包含从个体获得的细胞。在一些实施方案中,获得的细胞为或包括来自获得样本的个体的细胞。在一些实施方案中,样本为通过任何适当的方式直接从感兴趣的来源获得的“初级样本”。例如,在一些实施方案中,初级生物样本通过选自由以下组成的组的方法获得:活检(例如,细针抽吸或组织活检)、手术、体液(例如,血液、淋巴、粪便等)收集等。在一些实施方案中,如从上下文将清楚,术语“样本”是指通过处理初级样本(例如,通过除去初级样本的一种或多种组分和/或通过向初级样本中添加一种或多种剂)获得的制剂。
14、进一步,所述步骤1)所述的离心力为2000rpm,离心时间为25min。
15、进一步,所述步骤2)中所述的离心力为1800rpm,离心时间为8min。
16、进一步,所述步骤3)中涡旋时间为30s。
17、进一步,所述步骤3)中磁珠为cd3分选磁珠。
18、进一步,所述步骤3)中磁珠为cd3/cd28分选磁珠。
19、进一步,所述步骤4)中调节cd3+t细胞浓度为1×107个/ml。
20、进一步,所述步骤4)中磁珠与细胞数量的比例包括1-2:1。
21、在一些实施方案中,所述步骤4)中磁珠与细胞数量的比例包括1:1、1.1:1、1.2:1、1.3:1、1.4:1、1.5:1、1.6:1、1.7:1、1.8:1、1.9:1、2.0:1。
22、进一步,所述步骤4)中室温孵育时间为30min。
23、进一步,所述步骤5)中t细胞扩增培养基为含有100-500iu/ml il-2的x-vivotm15培养基。
24、在一些实施方案中,所述步骤5)中t细胞扩增培养基为含有100iu/ml il-2的x-vivotm 15培养基、150iu/ml il-2的x-vivotm 15培养基、200iu/ml il-2的x-vivotm 15培养基、250iu/ml il-2的x-vivotm 15培养基、300iu/ml il-2的x-vivotm 15培养基、350iu/ml il-2的x-vivotm 15培养基、400iu/ml il-2的x-vivotm 15培养基、450iu/ml il-2的x-vivotm 15培养基、500iu/ml il-2的x-vivotm 15培养基。
25、进一步,所述步骤5)中调整细胞密度为1×106个/ml-5×106个/ml。
26、在一些实施方案中,所述步骤5)中调整细胞密度为1×106个/ml、1.5×106个/ml、2×106个/ml、2.5×106个/ml、3×106个/ml、3.5×106个/ml、4×106个/ml、4.5×106个/ml、5×106个/ml。
27、进一步,所述步骤5)中去除磁珠的时间包括细胞培养第2-9天去除。
28、在一些实施方案中,所述步骤5)中去除磁珠的时间包括细胞培养的第2天去除,细胞培养的第3天去除,细胞培养的第4天去除,细胞培养的第5天去除,细胞培养的第6天去除,细胞培养的第7天去除,细胞培养的第8天去除,细胞培养的第9天去除。
29、在具体的实施方案中,所述t细胞的活化方法包括以下步骤:1)血液样本添加淋巴分离液,在2000rpm离心力下离心25min,然后在离心机升速9降速0的方法下分离得到pbmc;2)向步骤1)中pbmc中添加生理盐水,以1800rpm离心力离心10min,收集pbmc,取其中少量pbmc,检测cd3+t细胞比例;3)取适量磁珠,涡旋30s,加入等体积的dpbs并混匀,然后放置于磁力架上1min,弃上清,得到预备使用的磁珠;4)根据步骤2)中cd3+t细胞比例的测量结果,调节cd3+t细胞浓度到1×107个/ml,加入步骤3)中预备好的磁珠,磁珠与细胞数量的比例为1-2:1,混匀,室温孵育30min,然后稀释磁珠与细胞的混合物,然后放置于磁力架上2min,弃上清;5)使用含有100-500iu/ml il-2的x-vivotm 15培养基重悬步骤4)中弃上清的磁珠与细胞的混合物,调整细胞浓度到1×106个/ml-5×106个/ml,然后置于37℃的5%浓度的co2培养箱中培养14天,并在培养后2-9天去除磁珠,最终培养14天后得到活化的t细胞。
30、本发明第二方面提供了一种前面所述活化方法制备得到的活化的t细胞。
31、进一步,所述活化包括经诱导细胞因子表达和分泌、吞噬作用、细胞信号传导、抗原处理和呈递、靶细胞杀伤功能中的一种或多种。
32、术语“活化”是指单核细胞和/或巨噬细胞已经充分刺激以诱导可检测细胞增殖和/或已经刺激以施加其效应功能的状态,所述效应功能是例如经诱导细胞因子表达和分泌、吞噬作用、细胞信号传导、抗原处理和呈递、靶细胞杀伤功能。
33、本发明第三方面提供了前面所述的活化方法在制备高活化t细胞产品中的应用。
34、进一步,所述产品包括遗传工程化细胞、免疫效应细胞。
35、术语“产品”是指包含遗传工程化细胞(例如,免疫效应细胞)的制造的组合物,所述细胞例如细胞群,其中多个细胞被工程化以表达car,例如本文描述的car。制造的产品可以是任何基因工程化的免疫效应细胞(例如,t细胞,nk细胞),例如从受试者的血液获得的遗传工程化的免疫效应细胞,例如制造的car表达细胞产物,例如制造的cd19 car表达细胞产物。在一个实施方案中,可以从活化的冷冻保存的扩增的细胞群(例如扩增的免疫效应细胞群)获得工程化以表达car的细胞(例如,免疫效应细胞)。
36、本发明第四方面提供了一种组合物,所述组合物包括前面所述的活化方法中使用的试剂。
37、术语“组合物”代指能够用于前面所述的活化方法中的试剂,包括分离、提纯、混样、分选t细胞过程中所使用的试剂,包括化学反应试剂与清洗试剂。
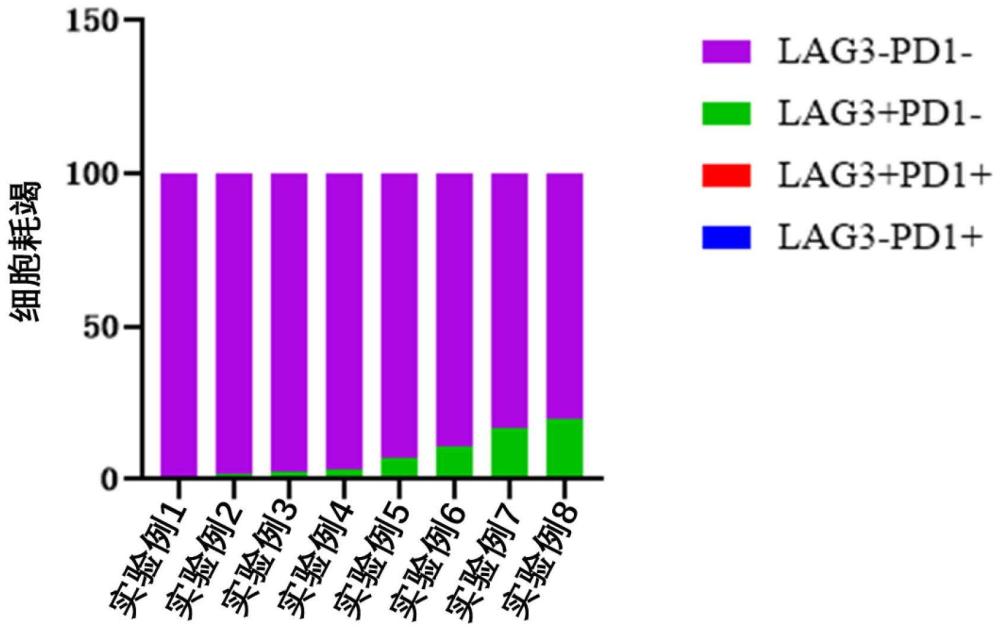
38、本发明第五方面提供了前面所述的活化方法在提高t细胞激活效率、提高t细胞存活率、降低t细胞耗竭程度中的应用。
39、术语“细胞耗竭”是指将期望的细胞与不想要的细胞分离的负向选择的过程。本文使用的细胞样品可以包含血液来源的细胞(例如pbmc)、细胞培养物来源的细胞或组织来源(例如可以在使用前分离的脑或骨)的细胞。适合细胞耗竭的方法包括离心、过滤、磁性细胞分选和荧光细胞分选。本文所用的术语“cd3表达的”和“cd3阳性的”(cd3+)细胞具有可互换的含义并描述表达cd3抗原的细胞。
40、本发明第六方面提供了前面所述的活化方法在计算机模型或装置中的应用。
41、术语“计算机模型”是指应用硬件、软件或它们的组合来实施目的的方案。当在软件中实现时,软件代码可在任何适合的处理器或一批处理器上执行,无论所述处理器是提供在单一计算机中还是分布在多个计算机之中。应当理解,执行上述功能的任何组件或一批组件都可在属类上被视为控制上面所讨论的功能的一个或多个控制器。所述一个或多个控制器可以众多方式实现,诸如采用专用硬件,或者采用使用微代码或软件编程以执行上面叙述的功能的通用硬件(例如,一个或多个处理器)来实现。
42、应当理解一个实现方式包括至少一种用计算机程序(即,多个指令)编码的计算机可读存储介质(即,至少一个有形非暂时计算机可读介质),诸如计算机存储器(例如,硬盘驱动器、闪速存储器、处理器工作存储器等)、软盘、光盘、磁带或其他有形非暂时计算机可读介质,所述计算机程序当在一个或多个处理器上被执行时会执行上面所讨论的功能。计算机可读存储介质可为可移动的,以使其上存储的程序可被加载到任何计算机资源上以实施本文讨论的技术。另外,应当理解对当被执行时会执行上面所讨论的功能的计算机程序的提及不限于在主计算机上运行的应用程序。更确切来说,术语“计算机程序”在本文中以通用含义用于指代可用于对一个或多个处理器编程以实现以上技术的任何类型的计算机代码(例如,软件或微代码)。
43、本发明第七方面提供了一种装置,所述装置包括:单个或多个处理器,和存储器,所述存储器用于存储单个或多个计算机程序,当所述单个或多个计算机程序被所述单个或多个处理器执行时实施前面所述的活化方法的步骤。
44、术语“装置”是指外部或内部应用的、发射、传输或接收信号、能量或数据并用作本发明的治疗的一部分的装置、设备、器件、处理器、传感器。装置可包括但不限于物理、机械、数字、超声、电或磁器件。
45、进一步,所述处理器可单个实施前面所述的活化方法的步骤,也可多个处理器共同实施前面所述的活化方法的步骤。
46、术语“处理器”可以指单个处理器或多个处理器,它们共同实施过程的各种步骤。类似地,“存储装置”或“数据库”可以指分布有编程指令和/或数据的单个装置或数据库或多个装置或数据库。
47、术语“存储器”在本文中以其常规意义使用,以指代存储供处理器随后检索的信息的设备,并且可以包括磁性或光学设备(例如硬盘、软盘、cd或dvd)或固态存储设备(如易失性或非易失性ram)。存储器或存储单元可具有多于一个相同或不同类型的物理存储设备(例如,存储器可具有多个存储设备,如多个硬盘驱动器或多个固态存储设备,或硬盘驱动器和固态存储设备的一些组合)。存储器可以是计算机可读介质或永久性存储器。在实施例中,存储器可以包括具有多种存储标识的一个或多个数据集,该多种存储标识与系统数据库中的每个经标记的生物分子、生物分子、标记、经激活的生物分子、经激活的标记和反应性接头相对应。
48、本发明第八方面提供了前面所述的活化的t细胞在car-t细胞或tcr-t细胞制备中的应用。
49、术语“嵌合抗原受体”(car)通常是指至少包含特异性地结合抗原或靶标的胞外结构域、跨膜结构域以及细胞内信号传导结构域的重组多肽。car的胞外结构域与靶细胞表面上的靶抗原结合导致car聚簇并将激活刺激传送给含car细胞。car重定向免疫效应细胞的特异性,并且触发了增殖、细胞因子产生、能够以不依赖主要组织相容性(mhc)的方式介导表达靶抗原的细胞死亡的分子的吞噬作用和/或产生。
50、术语“car-t”或“car-t细胞”通常是指能够表达car(又称“嵌合抗原受体”)的t细胞。所述car通常是指包含能够结合抗原的胞外结构域和至少一个胞内结构域的融合蛋白。car是嵌合抗原受体t细胞(car-t)的核心部件,其可包括靶向部分(例如,结合肿瘤相关抗原(tumor-associated antigen,taa)的部分)、铰链区、跨膜区和细胞内结构域。
51、术语“t细胞受体”或“tcr”或“工程化tcr”指在t细胞表面上存在的分子,其负责识别在抗原呈递细胞(apc)表面上展示的抗原。每个t细胞都表达独特的tcr,其是通过随机分类基因而产生的,从而确保t细胞可以对几乎任何感染做出反应。tcr还能够从细胞内部识别肿瘤特异性蛋白(抗原)。tcr的结构式由包含α(α)链和β(β)链的两种不同蛋白链构成的。在某些实施方式中,与天然存在的序列相比,tcr可以具有一个或多个氨基酸取代、缺失、插入或修饰,只要所述tcr在转染的t细胞中保持其形成tcr的能力和保持识别抗原的能力,以及参与免疫学相关的细胞因子信号传导即可。工程化tcr还以高亲和力与呈现出相关的肿瘤相关肽的靶细胞结合。
52、本发明第九方面提供了前面所述的活化方法、前面所述的活化的t细胞、前面所述的组合物在提高t细胞的增殖能力、提高t细胞转化效率中的应用。
53、术语“增殖能力”是指细胞增殖的过程,即引起细胞数目增加的过程,并且由细胞分裂与通过细胞死亡或分化引起的细胞损失之间的平衡来定义。
54、本发明的优点和有益效果:
55、本发明方法极大地提高了t细胞的激活效率,增加了t细胞的增殖能力,降低了操作的技术要求,使用该技术制备的t细胞提高了临床应用的安全性和使用的可能性。
- 还没有人留言评论。精彩留言会获得点赞!