一种双苯并菲嵌萘盘状液晶化合物的合成及性能研究
1.本发明涉及双苯并菲嵌萘盘状液晶化合物的合成、凝胶性与光物理性能。
背景技术:
2.目前应用的电导材料,多为非晶或多晶或是微晶与非晶的混合结构,缺陷较多,载流子迁移率多在10-6-10-5 cm2·
v-1
·
s-1
之间。虽然说较好的有机单晶材料电子迁移率可达0.1-1 cm2·
v-1
·
s-1
,但需要苛刻的加工技术且价格昂贵,限制了它们在器件中的应用。然而,盘状液晶作为一种软材料不仅易于加工还价格便宜,其柱状相中载流子迁移率接近于单晶水平,是理想的电荷传输材料。盘状液晶分子容易自组装成柱状相结构,电荷可在柱轴方向上一维高效的传输,而在柱间的传输则被阻断,这是由于盘状液晶分子外围的柔性链的绝缘作用导致的,因此盘状液晶可望成为一类新型的一维有机半导体材料或有机光导体材料。
技术实现要素:
3.基于此我们设计并合成了双苯并菲嵌萘盘状液晶化合物,在合成上主要采用suzuki-miyaura / scholl 串联反应得到该类化合物。首先通过1,6-二溴芘或1,8-二溴芘与3’,4,4’,5-四(烷氧基)联苯-2-频哪醇硼酸酯在pd(pph3)4的催化作用下发生suzuki-miyaura交叉偶联反应,然后在fecl3的催化作用下发生scholl分子内氧化环脱氢反应得到目标化合物双苯并菲嵌萘。研究表明该类化合物能在较宽的温度范围内形成稳定的盘状柱状相,是一种性能优良的有机液晶半导体材料,同时该类化合物还具有凝胶性能和良好的光物理性能。
4.在此,有必要提供一种双苯并菲嵌萘盘状液晶化合物的制备方法,一种权利要求1所述的双苯并菲嵌萘盘状液晶化合物,其特征在于具有通式(ⅰ)、(ⅱ)所示的结构:其中r为c
nh2n+1
,n表示碳原子数为8-16的整数。
5.一种权利要求2所述的通式(ⅲ)、(ⅳ)双(3’,4,4’,5-四(烷氧基)联苯-2-基)芘,其特征在于具有如下合成方法:(a)、1,6-双(3’,4,4’,5-四(烷氧基)联苯-2-基)芘(ⅲ)的合成:
按1 : 3 : 30 : 0.2的摩尔比依次称取1,6-二溴芘,3’,4,4’,5-四(烷氧基)联苯-2-频哪醇硼酸酯,k2co3,pd(pph3)4于50 ml反应管中,并加入混合溶剂thf (9 ml) / h2o (3 ml),脱气并充氩气保护,最后在氩气保护下于70 ℃搅拌反应48 h,反应结束后将反应体系冷却至室温,用乙酸乙酯和饱和食盐水进行萃取,有机相用无水mgso4干燥,过滤,旋干,通过硅胶柱层析(洗脱剂:v
二氯甲烷 : v
石油醚 = 1 : 2),用乙酸乙酯和乙醇重结晶,得到白色固体1,6-双(3’,4,4’,5-四(烷氧基)联苯-2-基)芘(ⅲ);(b)、1,8-双(3’,4,4’,5-四(烷氧基)联苯-2-基)芘(ⅳ)的合成:1,8-双(3’,4,4’,5-四(烷氧基)联苯-2-基)芘(ⅳ)的合成条件及操作过程与1,6-双(3’,4,4’,5-四(烷氧基)联苯-2-基)芘(ⅲ)的合成条件及操作过程一致。
6.双苯并菲嵌萘盘状液晶化合物(ⅰ)、(ⅱ)的制备:(c)、一种权利要求1所示的通式(ⅰ)类双苯并菲嵌萘盘状液晶化合物,其合成方法为:按1 : 6的摩尔比将化合物(ⅲ)和fecl3分别称取于100 ml圆底烧瓶中,加入三氯甲烷(50 ml)和硝基甲烷(1 ml),再套上无水氯化钙填充的干燥管于室温下搅拌反应,每隔10 min点板跟踪反应,半小时后每隔5 min点板跟踪反应,确定反应完毕后加入甲醇终止反应,用三氯甲烷和蒸馏水进行萃取,有机相用无水mgso4干燥,过滤,旋干,通过硅胶柱层析(洗脱剂:v
三氯甲烷 : v
石油醚 = 1 : 2),用乙酸乙酯进行重结晶,得到黄色固体双苯并菲嵌萘(ⅰ);(d)、一种权利要求1所示的通式(ⅱ)类双苯并菲嵌萘盘状液晶化合物,其合成方
法为:盘状液晶化合物双苯并菲嵌萘(ⅱ)的合成条件及操作过程与双苯并菲嵌萘(ⅰ)的合成条件及操作过程一致。
7.上述双苯并菲嵌萘盘状液晶化合物的合成方法,其合成路线简单快捷且反应条件温和,并能以较好的收率获得目标化合物,该类化合物首先通过不同位置二溴芘与3’,4,4’,5-四(烷氧基)联苯-2-频哪醇硼酸酯在pd(pph3)4的催化作用下发生suzuki-miyaura交叉偶联反应,然后再在fecl3的催化作用下发生scholl分子内氧化环脱氢反应得到,通过稠合的方式将多个芳环并在一起组成盘状液晶分子的中心刚性核,在外围多条烷氧基柔性链的调节作用下使得这类盘状液晶化合物在较宽的温度范围内自组装形成稳定的六方柱状液晶中间相,同时还具有良好的光物理性能,这些优异的性质赋予其在有机发光二极管、场效应晶体管和液晶薄膜显示器等多方面有良好的应用价值。
附图说明
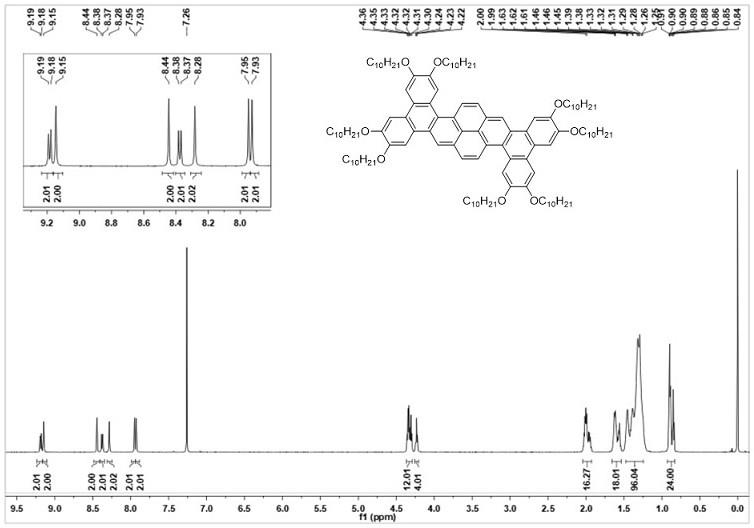
8.图1实施例2中所获r为c
10h21
时通式(ⅰ)的核磁氢谱。
9.图2实施例4中所获r为c
10h21
时通式(ⅱ)的核磁氢谱。
10.图3实施例2中所获r为c
10h21
时通式(ⅰ)的dsc迹线图。
11.图4实施例4中所获r为c
10h21
时通式(ⅱ)的dsc迹线图。
12.图5实施例2中所获r为c
10h21
时通式(ⅰ)在冷却过程中150 ℃时的偏光织构图。
13.图6实施例4中所获r为c
10h21
时通式(ⅱ)在冷却过程中220 ℃时的偏光织构图。
14.图7实施例2中所获r为c
10h21
时通式(ⅰ)在环己烷(cyh)、二氯甲烷(dcm)、四氢呋喃(thf)和n,n-二甲基甲酰胺(dmf)中的紫外吸收光谱图。
15.图8实施例4中所获r为c
10h21
时通式(ⅱ)在环己烷(cyh)、二氯甲烷(dcm)、四氢呋喃(thf)和n,n-二甲基甲酰胺(dmf)中的紫外吸收光谱图。
16.图9实施例2中所获r为c
10h21
时通式(ⅰ)在环己烷(cyh)、二氯甲烷(dcm)、四氢呋喃(thf)和n,n-二甲基甲酰胺(dmf)中的荧光发射光谱图。
17.图10实施例4中所获r为c
10h21
时通式(ⅱ)在环己烷(cyh)、二氯甲烷(dcm)、四氢呋喃(thf)和n,n-二甲基甲酰胺(dmf)中的荧光发射光谱图。
18.图11实施例2和实施例4中所获r为c
10h21
时通式(ⅰ)和通式(ⅱ)在固态薄膜时的荧光发射光谱图。
19.图12实施例2中所获r为c
10h21
时通式(ⅰ)在环己烷中形成的有机凝胶在紫外灯下(左侧)和自然日光下(右侧)的倒置图。
20.下面给出的实例是对本发明的具体描述,必须强调的是下面给出的实施例子只是对本发明的进一步阐述,而不是对本发明的保护范围的一种限制。本领域熟练技术人员根
据上述发明内容在实际实施过程中,涉及到的改进或者调整若不是本质意义上的改变,仍然属于本发明的保护范围。
21.值得说明的是,以下各个实施案例中所用到的3’,4,4’,5-四(烷氧基)联苯-2-频哪醇硼酸酯以及合成方法均为现有技术:j. f. hang, h. lin, k. q. zhao, p. hu, b. q. wang, h. monobe, c. h. zhu, b. donnio, butterfly mesogens based on carbazole, fluorene or fluorenone: mesomorphous, gelling, photophysical, and photoconductive properties, eur. j. org. chem., 2021, 1989-2002.n. miyaura, a. suzuki, palladium-catalyzed cross-coupling reactions of organoboron compounds, chem. rev., 1995, 95, 2457-2483。
22.实施例1。
23.本实施例提供的是通式(ⅲ)类化合物的合成,其中r为c
10h21,
其合成方法如下:按1 : 3 : 30 : 0.2的摩尔比依次称取1,6-二溴芘(60.0 mg),3’,4,4’,5-四(癸氧基)联苯-2-频哪醇硼酸酯(452.6 mg),k2co3(690.9 mg)和pd(pph3)4(38.5 mg)于50 ml反应管中,并加入混合溶剂thf (9 ml) / h2o (3 ml),脱气并充氩气保护,最后在氩气保护下于70 ℃搅拌反应48 h,反应结束后将反应体系冷却至室温,用乙酸乙酯和饱和食盐水进行萃取,有机相用无水mgso4干燥,过滤,旋干,通过硅胶柱层析(洗脱剂:v
二氯甲烷 : v
石油醚 = 1 : 2),用乙酸乙酯和乙醇重结晶,得到白色固体1,6-双(3’,4,4’,5-四(癸氧基)联苯-2-基)芘(ⅲ)(224.0 mg,产率77 % )。
24.实施例2。
25.本实施例提供的是通式(ⅰ)类盘状液晶化合物的合成,其中r为c
10h21,
其合成方法如下:按1 : 6的摩尔比将化合物(ⅲ)(100.0 mg)和fecl3(59.5 mg)分别称取于100 ml圆底烧瓶中,加入三氯甲烷(50 ml)和硝基甲烷(1 ml),再套上无水氯化钙填充的干燥管于室温下搅拌反应,每隔10 min点板跟踪反应,半小时后每隔5 min点板跟踪反应,确定反应
完毕后加入甲醇终止反应,用三氯甲烷和蒸馏水进行萃取,有机相用无水mgso4干燥,过滤,旋干,通过硅胶柱层析(洗脱剂:v
三氯甲烷 : v
石油醚 = 1 : 2),用乙酸乙酯进行重结晶,得到黄色固体双苯并菲嵌萘(ⅰ)(74.7 mg,产率75 %)。
[0026]1h nmr (600 mhz, cdcl3) δ 9.18 (d, j = 9.2 hz, 2h, arh), 9.15 (s, 2h, arh), 8.44 (s, 2h, arh), 8.38 (d, j = 9.3 hz, 2h, arh), 8.28 (s, 2h, arh), 7.95 (s, 2h, arh), 7.93 (s, 2h, arh), 4.36
ꢀ‑ꢀ
4.30 (m, 12h, och2), 4.23 (t, j = 6.5 hz, 4h, och2), 2.04
ꢀ‑ꢀ
1.93 (m, 16h, ch2), 1.65
ꢀ‑ꢀ
1.54 (m, 16h, ch2), 1.47
ꢀ‑ꢀ
1.25 (m, 96h, ch2), 0.91-0.84 (m, 24h, ch3)。
[0027]
实施例3。
[0028]
本实施例提供的是通式(ⅳ)类化合物的合成,其中r为c
10h21,
其合成方法如下:按1 : 3 : 30 : 0.2的摩尔比依次称取1,8-二溴芘(60.0 mg),3’,4,4’,5-四(癸氧基)联苯-2-频哪醇硼酸酯(452.6 mg),k2co3(690.9 mg)和pd(pph3)4(38.5 mg)于50 ml反应管中,并加入混合溶剂thf (9 ml) / h2o (3 ml),脱气并充氩气保护,最后在氩气保护下于70 ℃搅拌反应48 h。反应结束后将反应体系冷却至室温,用乙酸乙酯和饱和食盐水进行萃取,有机相用无水mgso4干燥,过滤,旋干,通过硅胶柱层析(洗脱剂:v
二氯甲烷 : v
石油醚 = 1 : 2),用乙酸乙酯和乙醇重结晶,得到白色固体1,8-双(3’,4,4’,5-四(癸氧基)联苯-2-基)芘(ⅲ)(215.3 mg,产率74 % )。
[0029]
实施例4。
[0030]
本实施例提供的4是通式(ⅱ)类盘状液晶化合物的合成,其中r为c
10h21,
其合成方法如下:按1 : 6的摩尔比将化合物(ⅲ)(150.0 mg)和fecl3(83.1 mg)分别称取于100 ml圆底烧瓶中,加入三氯甲烷(60 ml)和硝基甲烷(1 ml),再套上无水氯化钙填充的干燥管于室温下搅拌反应,每隔10 min点板跟踪反应,半小时后每隔5 min点板跟踪反应,确定反应完毕后加入甲醇终止反应,用三氯甲烷和蒸馏水进行萃取,有机相用无水mgso4干燥,过滤,旋干,通过硅胶柱层析(洗脱剂:v
三氯甲烷 : v
石油醚 = 2 : 3),用乙酸乙酯和乙醇进行重结晶,得到黄色固体双苯并菲嵌萘(ⅱ)(114.4 mg,产率76 %)。
[0031]1h nmr (400 mhz, cdcl3) δ 9.14 (s, 2h, arh), 9.07 (s, 2h, arh), 8.65 (s, 2h, arh), 8.27 (s, 2h, arh), 8.19 (s, 2h, arh), 7.94 (d, j = 12.4 hz, 4h, arh), 4.33 (m, 16h, och2), 2.01
ꢀ‑ꢀ
1.96 (m, 16h, ch2), 1.63
ꢀ‑ꢀ
1.57 (m, 16h, ch2), 1.45
ꢀ‑ꢀ
1.25 (m, 96h, ch2), 0.90
ꢀ‑ꢀ
0.85 (m, 24h, ch3)。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1