黄色系化合物、含有该化合物的着色组合物、滤色器用着色剂以及滤色器的制作方法
1.本发明涉及黄色系化合物、含有该化合物的着色组合物、含有该着色组合物的滤色器用着色剂以及使用该着色组合物的滤色器。
背景技术:
2.迄今为止,开发了喹酞酮颜料、偶氮颜料、二酮吡咯并吡咯颜料等多种颜料(专利文献1~4)。这些颜料用于液晶、场致发光(el)显示装置的滤色器的着色剂。滤色器是通过染色法、颜料分散法、印刷法、电沉积法等使着色层层叠在玻璃等透光性基板上来制造。喹酞酮颜料是通过喹哪啶与邻苯二甲酸酐的缩合而合成的黄色系化合物,由于其鲜明性而用作滤色器用着色剂(专利文献1、2、5、6、非专利文献1)。但是,随着显示器的高画质化,对滤色器所要求的性能提高,需要使着色力、亮度以及对比度进一步提高。
3.颜料通常不溶于溶剂,因此在包含树脂等的滤色器中以微粒状存在。因此,就使用颜料的滤色器而言,已知:由于透射光在颜料粒子表面处进行反射、散射,因此对透明性、色纯度产生影响,另外,由于具有由反射引起的消偏作用,因此彩色液晶显示装置的对比度降低。
4.为了改善对比度降低的问题,提出了仅使用染料作为着色剂的方法或将染料和颜料并用的方法等。由于染料可溶于溶剂,因此,使用染料的滤色器与仅使用颜料作为着色剂的情况相比,消偏作用得到抑制,分光特性优异,可期待对比度、亮度等的提高。
5.现有技术文献
6.专利文献
7.专利文献1:日本特公昭47-3476号公报
8.专利文献2:日本特开2012-193318号公报
9.专利文献3:日本特开2012-12498号公报
10.专利文献4:日本特开2001-220520号公报
11.专利文献5:日本特开2019-104897号公报
12.专利文献6:日本特开2019-123856号公报
13.非专利文献
14.非专利文献1:市村国宏主编、“最尖端滤色器的工艺技术和化学”、株式会社cmc出版、2006年、第80页
技术实现要素:
15.本发明是为了解决上述课题而完成的,其目的在于提供一种黄色系化合物在有机溶剂(丙二醇单甲醚乙酸酯(pgmea)等)中的溶解性以及耐热性提高并含有该化合物且着色力、鲜明性、色相等的色彩特性优异的着色组合物、含有该着色组合物的滤色器用着色剂以及使用该着色剂的滤色器。
16.本发明是为了上述目的而进行深入研究的结果所得到的,主旨如下。
17.1.一种化合物,由下述通式(1)表示,
18.【化1】
[0019][0020]
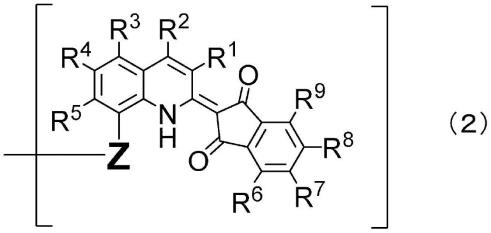
式(1)中,q分别独立地为由下述通式(2)表示的基团,
[0021]
n表示2~10的整数,
[0022]
l表示2~10价的基团。
[0023]
【化2】
[0024][0025]
式(2)中,r1~r9分别独立地表示:
[0026]
氢原子(―h)、羟基(―oh)、卤素原子、氰基(―cn)、硝基(―no2)、
[0027]
能够具有取代基的碳原子数0~25的氨基、
[0028]
能够具有取代基的碳原子数0~25的磺酰基、
[0029]
能够具有取代基的碳原子数1~25的直链状、支链状或环状的烷基、能够具有取代基的碳原子数2~25的直链状、支链状或环状的烯基、
[0030]
能够具有取代基的碳原子数1~25的直链状、支链状或环状的烷氧基、
[0031]
能够具有取代基的碳原子数1~25的酰基、
[0032]
能够具有取代基的碳原子数0~25的醚基、
[0033]
能够具有取代基的碳原子数6~25的芳香族烃基、或者
[0034]
能够具有取代基的成环原子数5~25的杂环基,
[0035]
r1~r9能够在相邻的基团之间彼此键合而形成环。
[0036]
z分别独立地为2价基团或3价基团,并表示:
[0037]
能够具有取代基的碳原子数0~25的氨基、
[0038]
能够具有取代基的碳原子数1~25的直链状、支链状或环状的亚烷基、
[0039]
包含醚基或单键之中的1种或2种以上的基团,
[0040]
多个q经由l或z而彼此键合。
[0041]
2.一种化合物,在上述通式(1)中,l为:
[0042]
能够具有取代基的碳原子数0~25的氨基、
[0043]
能够具有取代基的碳原子数1~25的直链状、支链状或环状的亚烷基、
[0044]
能够具有取代基的碳原子数0~25的醚基、
[0045]
能够具有取代基的碳原子数6~25的芳香族烃基、或者
[0046]
能够具有取代基的成环原子数5~25的杂环基。
[0047]
3.一种化合物,在上述通式(2)中,z为能够具有取代基的碳原子数1~20的氨基。
[0048]
4.一种化合物,在上述通式(2)中,r1~r9为:
[0049]
氢原子、卤素原子、
[0050]
能够具有取代基的碳原子数1~20的直链状或支链状的烷基、能够具有取代基的碳原子数2~20的直链状的烯基、或者
[0051]
能够具有取代基的碳原子数1~20的酰基。
[0052]
5.一种着色组合物,含有上述化合物,所述着色组合物在23℃~27℃下的丙二醇单甲基醚乙酸酯(pgmea)中的溶解度为1质量%以上。
[0053]
6.一种着色组合物,含有上述化合物,所述着色组合物使用含有上述化合物的涂膜而在220℃~240℃下的加热前后的色彩值的色差(δe
*ab
)为3.5以下。
[0054]
7.一种滤色器用着色剂,含有上述化合物或着色组合物。
[0055]
8.一种滤色器,使用了上述滤色器用着色剂。
[0056]
(发明效果)
[0057]
本发明涉及的化合物与以往的黄色系化合物相比,在pgmea等有机溶剂中的溶解性优异,并且制膜时的耐热性优异,因此含有本发明涉及的化合物的着色组合物作为滤色器用着色剂是有用的。
具体实施方式
[0058]
以下,对本发明的实施方式进行详细说明。需要说明的是,本发明并不限定于以下的实施方式,在其主旨的范围内能够进行各种变形进行实施。首先,对于由上述通式(1)表示的化合物进行说明。
[0059]
本发明的化合物由下述通式(1)表示。在通式(1)中,q分别独立地为由下述通式(2)表示的基团,n表示2~10的整数,l表示2~10价的基团。多个q可以分别相同或不同。
[0060]
【化3】
[0061][0062]
【化4】
[0063][0064]
因此,通式(1)可以使用通式(2)如下述通式(1-2)那样进行表示。
[0065]
【化5】
[0066][0067]
其中,在通式(1)中,当在n为2时,将多个q分别表示成q1和q2的情况下,如下述式(1-3)那样,q1和q2经由l如“q1―l―q
2”那样键合。
[0068]
【化6】
[0069]q1-l-q2ꢀꢀ
(1-3)
[0070]
进而,在通式(1)中,当在n为3时,将多个q分别表示成q1、q2以及q3的情况下,如下述式(1-4)那样,q1~q3可以经由l而键合,q1~q3各自可以彼此直接键合,也可以彼此调换。在n为4以上的情况下,同样如下述式(1-4)那样,多个q也可以经由l而彼此键合。
[0071]
【化7】
[0072][0073]
这样,在通式(1)中,即使在n表示2~10的整数、作为多个q存在q1~q
10
的情况下,q1~q
10
各自也可以经由l而键合,q1~q
10
各自可以彼此直接键合,也可以彼此调换。因此,l对应于n而表示2~10的价数的基团。n优选为2~6,更优选为2~4。
[0074]
作为通式(2)中的由r1~r9表示的“卤素原子”,可列举:氟原子、氯原子、溴原子、碘原子等。作为“卤素原子”,优选为氟原子或氯原子。
[0075]
在通式(2)中,由r1~r9表示的“能够具有取代基的碳原子数0~25的氨基”可以具有取代基,也可以不具有取代基,在具有取代基的情况下,包含由“―nr
10r11”表示的“具有取代基r
10
和r
11
的氨基”,可列举:未取代氨基(―nh2)、一取代氨基、二取代氨基等。一取代氨基或二取代氨基中的碳原子数例如为1~25,可以为1~20,也可以为2~10。“能够具有取代基的碳原子数0~25的氨基”也可以为经由―nh―、―n<或―n=ch―而键合后述的“碳原子数1~25的直链状、支链状或环状的烷基”、“碳原子数6~25的芳香族烃基”、“碳原子数0~25的酰基”、“成环原子数5~25的杂环基”的基团。作为一取代氨基,可列举:乙基氨基、丁基氨基、乙酰基氨基、苯基氨基等。作为二取代氨基,可列举:二甲基氨基、二乙基氨基、二丙基氨基、二丁基氨基、二己基氨基等的碳原子数2~25的二烷基氨基;二烯丙基氨基等的碳原子数4~25的二烯基氨基;二苯基氨基、n-乙酰基-n-苯基氨基、(正丁基)-n-苯基氨基等。
[0076]
在通式(2)中,由r1~r9表示的“能够具有取代基的碳原子数0~25的磺酰基”是指由“―so2―r
100”(或“―s(=o)2―r
100”)表示的具有取代基r
100
的磺酰基。“―so2―r
100”也可
以为不包含碳原子的基团,例如,可以为“―so3h”或包含碱金属原子“m”的“―so3m”。本发明中的碱金属原子“m”可列举:锂原子(li)、钠原子(na)、钾原子(k)或铯原子(cs)等,优选为li、na或k,更优选为li或na,特别优选为na。r
100
的碳原子数为0~25,可以为1~20,也可以为1~10。作为能够具有取代基的碳原子数0~25的磺酰基,除了上述的―so3h、―so3m以外,还可列举:磺酰胺基(―s(=o)2―nh2)、甲磺酰基、甲苯磺酰基等。
[0077]
在通式(2)中,作为由r1~r9表示的“能够具有取代基的碳原子数1~25的直链状、支链状或环状的烷基”中的“碳原子数1~25的直链状、支链状或环状的烷基”,具体而言,可列举:甲基、乙基、丙基、丁基、戊基、己基、庚基、辛基、壬基、癸基等的直链状的烷基;异丙基、异丁基、仲丁基、叔丁基、异辛基、2-乙基己基等的支链状的烷基;环丙基、环戊基、环己基、环庚基、环辛基、环壬基、环癸基等的环状的烷基(环烷基);1-金刚烷基、2-金刚烷基;等等。
[0078]
在通式(2)中,作为由r1~r9表示的“能够具有取代基的碳原子数2~25的直链状、支链状或环状的烯基”中的“碳原子数2~25的直链状、支链状或环状的烯基”,具体而言,可列举:乙烯基、1-丙烯基、烯丙基、1-丁烯基、2-丁烯基、1-戊烯基、1-己烯基、异丙烯基、异丁烯基等的直链状或支链状的烯基;环丙烯基、环丁烯基、环戊烯基、环己烯基、环庚烯基等的环状的烯基(环烯基);或者将这些直链状、支链状或环状的烯基键合多个而成的基团。
[0079]
在通式(2)中,作为由r1~r9表示的“能够具有取代基的碳原子数1~25的直链状、支链状或环状的烷氧基”中的“碳原子数1~25的直链状、支链状或环状的烷氧基”,具体而言,可列举:甲氧基、乙氧基、丙氧基、丁氧基、戊氧基、己氧基、庚氧基、辛氧基、壬氧基、癸氧基等的直链状的烷氧基;异丙氧基、异丁氧基、仲丁氧基、叔丁氧基、异辛氧基等的支链状的烷氧基;环丙氧基、环丁氧基、环戊氧基、环己氧基、环庚氧基、环辛氧基、环壬氧基、环癸氧基等的环状的烷氧基(环烷氧基);1-金刚烷基氧基、2-金刚烷基氧基;等等。
[0080]
在通式(2)中,由r1~r9表示的“能够具有取代基的碳原子数1~25的酰基”是指由“―(c=o)―r
101”表示的具有取代基r
101
的基团。取代基r
101
可以为包含碳原子的基团,可以为包含氮原子的基团,或者也可以为不包含碳原子的基团。在取代基r
101
为包含碳原子的基团的情况下,取代基r
101
的碳原子数例如可以为1~25,也可以为1~20。在取代基r
101
为包含氮原子的基团或不包含碳原子的基团的情况下,取代基r
101
的碳原子数例如可以为0~25,也可以为0~20。作为取代基r
101
,例如可列举:―h、―ch3、―ch2ch2ch3、―ch=ch2、―c6h5(苯基)、―nh2、―nhch3、―nhch2ch3、二甲基氨基、二乙基氨基、二(正丙基)氨基、二(正丁基)氨基等,也可以为与由所述r1~r9表示的“能够具有取代基的碳原子数0~25的氨基”同样的基团。作为“能够具有取代基的碳原子数1~25的酰基”中的“碳原子数1~25的酰基”,具体而言,可列举:甲酰基、乙酰基、丙酰基、丙烯酰基、苯甲酰基等。“―(c=o)―r
101”在包含氮原子的情况下也可以为酰胺基、伯酰胺基、仲酰胺基,r
101
也可以为在由所述r1~r9表示的“具有取代基的碳原子数0~25的氨基”中例示的由“―nr
10r11”表示的一取代氨基或二取代氨基。
[0081]
在通式(2)中,由r1~r9表示的“能够具有取代基的碳原子数0~25的醚基”是指由“―o―r
102”表示的具有取代基r
102
的醚基。取代基r
102
可以为包含碳原子的基团,也可以为不包含碳原子的基团。作为“能够具有取代基的碳原子数0~25的醚基”中的“碳原子数0~
25的醚基”,具体而言,可列举:氨基氧基、由“―o―(c=o)―r”表示的酯基(r为任意的烷基或芳香族烃基等)、磷酸基、磷酸酯基等。
[0082]
在通式(2)中,作为由r1~r9表示的“能够具有取代基的碳原子数6~25的芳香族烃基”中的“碳原子数6~25的芳香族烃基”,具体而言,可列举:苯基、联苯基、三联苯基、萘基、蒽基(anthracenyl group、anthryl group)、菲基、芴基、茚基、芘基、苝基、荧蒽基、三亚苯基等的芳香族烃基(本发明中的“芳香族烃基”还包含芳基或稠合多环芳香族基)。
[0083]
在通式(2)中,作为由r1~r9表示的“能够具有取代基的成环原子数5~25的杂环基”中的“成环原子数5~25的杂环基”,具体而言,可列举:吡啶基、嘧啶基、三嗪基、咪唑基、吡唑基、三唑基、噻吩基、呋喃基(furyl group、furanyl group)、吡咯基、喹啉基、异喹啉基、萘啶基、吲哚基、吖啶基、菲咯啉基、苯并呋喃基、苯并噻吩基、吲哚基、咔唑基、噁唑基、苯并噁唑基、噻唑基、苯并噻唑基、喹喔啉基、苯并咪唑基、吡唑基、二苯并呋喃基、二苯并噻吩基、咔啉基等的杂环基(或杂环芳香族烃基)。
[0084]
在通式(2)中,作为由r1~r9表示的
[0085]“具有取代基的碳原子数0~25的氨基”、
[0086]“具有取代基的碳原子数0~25的磺酰基”、
[0087]“具有取代基的碳原子数1~25的直链状、支链状或环状的烷基”、
[0088]“具有取代基的碳原子数2~25的直链状、支链状或环状的烯基”、
[0089]“具有取代基的碳原子数1~25的直链状、支链状或环状的烷氧基”、
[0090]“具有取代基的碳原子数1~25的酰基”、“具有取代基的碳原子数0~25的醚基”、
[0091]“具有取代基的碳原子数6~25的芳香族烃基”、或者
[0092]“具有取代基的成环原子数5~25的杂环基”中的“取代基”,具体而言,可列举:
[0093]
氘原子、羟基、硫醇基、氰基、硝基;氟原子、氯原子、溴原子、碘原子等的卤素原子;
[0094]
碳原子数0~20的氨基;
[0095]
碳原子数0~20的磺酰基;
[0096]
碳原子数1~20的直链状、支链状或环状的烷基;
[0097]
碳原子数2~20的直链状、支链状或环状的烯基;
[0098]
碳原子数1~20的直链状、支链状或环状的烷氧基;
[0099]
碳原子数1~20的酰基;碳原子数1~20的醚基;
[0100]
碳原子数6~20的芳香族烃基或稠合多环芳香族基;
[0101]
成环原子数5~20的杂环基;等等。需要说明的是,在“取代基”包含碳原子的情况下,该碳原子不计入上述的“碳原子数0~25”、“碳原子数1~25”、“碳原子数6~25”中。就这些“取代基”而言,可以仅含有1个,也可以含有多个,在含有多个的情况下,可以彼此相同,也可以彼此不同。另外,这些“取代基”可以进一步具有上述例示的取代基。另外,这些取代基之间可以经由单键、取代或未取代的亚甲基、氧原子(―o―)或硫原子(―s―)彼此键合而形成环。但是,上述的由r1~r9表示的各基团中的“取代基”的数量最大为10个,各基团中的最大的碳原子数为100。
[0102]
需要说明的是,在通式(2)中,由r1~r9表示的具有“取代基”的上述的各基团中,作为被列举为
[0103]“取代基”的“碳原子数0~20的氨基”、
[0104]“碳原子数0~20的磺酰基”、
[0105]“碳原子数1~20的直链状、支链状或环状的烷基”、
[0106]“碳原子数2~20的直链状、支链状或环状的烯基”、
[0107]“碳原子数1~20的直链状、支链状或环状的烷氧基”、
[0108]“碳原子数1~20的酰基”、
[0109]“碳原子数1~20的醚基”、
[0110]“碳原子数6~20的芳香族烃基或稠合多环芳香族基”、或者
[0111]“成环原子数5~20的杂环基”,具体而言,可列举:
[0112]
氨基;甲基氨基、二甲基氨基、二乙基氨基、乙基甲基氨基、二丙基氨基、二叔丁基氨基、二苯基氨基等的具有碳原子数1~20的直链状或碳原子数3~20的支链状的烷基、或者碳原子数6~20的芳香族烃基的一取代或二取代氨基;
[0113]
磺酰胺基(―s(=o)2―nh2)、甲磺酰基、甲苯磺酰基等的具有碳原子数0~20的磺酰基(―s(=o)2―)的基团;―so
3-
、―so3h、―so3m(m为碱金属原子);
[0114]
甲基、乙基、正丙基、异丙基、正丁基、异丁基、仲丁基、叔丁基、正戊基、异戊基、正己基、2-乙基己基、庚基、辛基、异辛基、壬基、癸基等的碳原子数1~20的直链状或碳原子数3~20的支链状的烷基;环丙基、环戊基、环己基、环辛基、环壬基、环癸基等的碳原子数3~20的环状的烷基(环烷基);1-金刚烷基、2-金刚烷基;
[0115]
乙烯基、1-丙烯基、烯丙基、1-丁烯基、2-丁烯基、1-戊烯基、1-己烯基、异丙烯基、异丁烯基、或这些烯基键合多个而成的碳原子数2~20的直链状或碳原子数3~20的支链状的烯基;环丙烯基、环丁烯基、环戊烯基、环己烯基、环庚烯基等的碳原子数3~20的环状的烯基(环烯基);
[0116]
甲氧基、乙氧基、丙氧基、丁氧基、戊氧基、己氧基、庚氧基、辛氧基、壬氧基、癸氧基、异丙氧基、异丁氧基、仲丁氧基、叔丁氧基、异辛氧基等的碳原子数1~20的直链状或碳原子数3~20的支链状的烷氧基;环丙氧基、环丁氧基、环戊氧基、环己氧基、环壬氧基、环癸氧基等的碳原子数3~20的环状的烷氧基(环烷氧基);1-金刚烷氧基、2-金刚烷氧基;
[0117]
甲酰基、乙酰基、丙酰基、丙烯酰基、苯甲酰基等的碳原子数1~20的酰基;醚基(―o―)、氨基氧基、由“―o―(c=o)―r”表示的酯基(r为任意的烷基或芳香族烃基等)、磷酸基、磷酸酯基等的含有碳原子数0~20的醚基(―o―)的基团;
[0118]
苯基、联苯基、三联苯基、萘基、蒽基(anthracenyl group、anthryl group)、菲基、芴基、茚基、芘基、苝基、荧蒽基、三亚苯基等的碳原子数6~20的芳香族烃基或稠合多环芳香族基;
[0119]
吡啶基、嘧啶基、三嗪基、噻吩基、呋喃基(furyl group、furanyl group)、吡咯基、咪唑基、吡唑基、三唑基、喹啉基、异喹啉基、萘啶基、吖啶基、菲咯啉基、苯并呋喃基、苯并噻吩基、噁唑基、吲哚基、咔唑基、苯并噁唑基、噻唑基、苯并噻唑基、喹喔啉基、苯并咪唑基、吡唑基、二苯并呋喃基、二苯并噻吩基、咔啉基等的成环原子数5~20的杂环基;
[0120]
苯氧基、甲苯氧基、联苯氧基、萘氧基、蒽氧基、菲氧基等的碳原子数6~19的芳氧基;等等。
[0121]
在通式(2)中,r1~r9可以在相邻的基团之间经由单键、取代或未取代的亚甲基、氧原子或硫原子彼此键合而形成环。
[0122]
在通式(2)中,作为r1~r9,优选为:
[0123]
氢原子、羟基、卤素原子、硝基、氰基、
[0124]
能够具有取代基的碳原子数1~20的氨基、
[0125]
能够具有取代基的碳原子数1~20的直链状或碳原子数3~20的支链状的烷基、
[0126]
能够具有取代基的碳原子数2~20的直链状或碳原子数3~20的支链状的烯基、
[0127]
能够具有取代基的碳原子数2~20的直链状或碳原子数3~20的支链状的烷氧基、
[0128]
能够具有取代基的碳原子数1~20的酰基、
[0129]
能够具有取代基的碳原子数1~20的醚基、或者
[0130]
能够具有取代基的碳原子数6~20的芳香族烃基,
[0131]
更优选为:
[0132]
氢原子、卤素原子、
[0133]
能够具有取代基的碳原子数1~20的直链状或支链状的烷基、
[0134]
能够具有取代基的碳原子数2~20的直链状的烯基、或者
[0135]
能够具有取代基的碳原子数1~20的酰基。
[0136]
r7或r8进一步优选为氢原子、能够具有取代基的碳原子数1~20的直链状或支链状的烷基、能够具有取代基的碳原子数2~20的直链状的烯基、或者能够具有取代基的碳原子数1~20的酰基,r6或r9进一步优选为氢原子或卤素原子。
[0137]
在通式(1)中,含有n个由通式(2)表示的q。在通式(2)中存在多个(n个)的z可以分别独立地相同或不同,为2价基团或3价基团。
[0138]
在通式(1)中,多个q经由l或z而彼此键合。在z为2价基团的情况下,例如,在所述通式(1)如所述通式(1-3)表示那样表示为“q1―l―q
2”的情况下,可如下述式(2-1)那样来表示。此时,多个r1~r9可以分别独立地相同或不同。另外,在如下述式(2-1)那样来表示的情况下,多个z中的任意1个或多个也可以为3价基团,z也可以为适当的基团、例如具有r
10
、r
11
的3价基团,具体而言,可以如下述式(2-2)那样来表示。
[0139]
【化8】
[0140][0141]
【化9】
[0142]
[0143]
在通式(1)中,在多个q经由z而键合的情况下,例如,如下述式(2-3)那样,各个q可以经由由z表示的2价基团或3价基团而彼此键合。
[0144]
【化10】
[0145][0146]
在通式(1)中,由“l”表示的基团表示2~10价的基团,作为l的具体例,可列举使用如下述那样的任意基团制成2~10价基团而得的基团。另外,l以及多个q可以在下述基团的任意的取代基的部位彼此键合。
[0147]
作为这些基团,可列举:
[0148]“能够具有取代基的碳原子数0~25的氨基”(或亚氨基)、
[0149]“能够具有取代基的碳原子数0~25的磺酰基”、
[0150]“能够具有取代基的碳原子数1~25的直链状、支链状或环状的烷基”、
[0151]“能够具有取代基的碳原子数2~25的直链状、支链状或环状的烯基”、
[0152]“能够具有取代基的碳原子数1~25的直链状、支链状或环状的烷氧基”、
[0153]“能够具有取代基的碳原子数1~25的酰基”、
[0154]“能够具有取代基的碳原子数0~25的醚基”、
[0155]“能够具有取代基的碳原子数6~25的芳香族烃基”、或者
[0156]“能够具有取代基的成环原子数5~25的杂环基”。
[0157]
具体而言,这些基团可列举与通式(2)中的作为r1~r9所列举的基团同样的基团。对于这些“基团”能够具有的“取代基”,也可列举与r1~r9表示的基团能够具有的“取代基”同样的基团。
[0158]
这些基团表示的l可以根据q的数量(n)、或者在任意的能够具有取代基的部位上的与多个q形成的键而形成2~10的任意价数的基团。例如“能够具有取代基的碳原子数1~25的直链状、支链状或环状的烷基”可以为“能够具有取代基的碳原子数1~25的直链状、支链状或环状的亚烷基”,也可以在这些“亚烷基”的一部分基团上键合取代基而形成3价以上的基团。就这些“基团”或“取代基”而言,可以仅含有1个,也可以含有多个,在含有多个的情况下,可以彼此相同,也可以彼此不同。另外,这些“基团”或“取代基”可以进一步具有上述例示的基团或取代基。另外,这些“基团”或“取代基”之间可以经由单键、取代或未取代的亚甲基、氧原子或硫原子彼此键合而形成环。但是,l中所含的上述的“基团”或“取代基”的数量最大为10个,各基团中的最大的碳原子数为100。
[0159]
在通式(1)中,l表示2~10价的基团,在l为可在“能够具有取代基的碳原子数1~25的直链状、支链状或环状的烷基”的任意的取代基的部位彼此键合的基团的情况下,作为l,可表示为“能够具有取代基的碳原子数1~25的直链状、支链状或环状的亚烷基”。具体而言,可列举:亚甲基、亚乙基、―chch3―、亚正丙基(丙烷-1,3-二基)、亚异丙基、丙烷-1,2-二基、丙烷-2,2-二基、亚正丁基、亚异丁基、亚仲丁基、亚叔丁基、亚正戊基、亚新戊基、亚正己基(己烷-1,6-二基、―c6h
12
―)、亚正庚基、亚正辛基、亚正壬基、亚正癸基等的直链状或支链状的亚烷基、或者亚环丙基、亚环戊基、亚环己基等的环状的亚烷基等等键合1个或多个而成的基团,但并不限定于这些基团。
[0160]
在通式(1)中,l优选为:
[0161]
能够具有取代基的碳原子数0~25的氨基、
[0162]
能够具有取代基的碳原子数1~25的直链状、支链状或环状的亚烷基、
[0163]
能够具有取代基的碳原子数0~25的醚基、
[0164]
能够具有取代基的碳原子数6~25的芳香族烃基、或者
[0165]
能够具有取代基的成环原子数5~25的杂环基,
[0166]
更优选为:能够具有取代基的碳原子数1~25的直链状或支链状的亚烷基。
[0167]
在通式(2)中,由z表示的2价基团或3价基团表示:
[0168]
能够具有取代基的碳原子数0~25的氨基、
[0169]
能够具有取代基的碳原子数1~25的直链状、支链状或环状的亚烷基、
[0170]
包含醚基或单键之中的1种或2种以上的基团,包括在适当的部位中将这些基团替代为2价基团或3价基团而得的基团。这些氨基、亚烷基或醚基可以包含多个相同的基团或多个不同的基团。
[0171]
在通式(2)的z中,作为“能够具有取代基的碳原子数0~25的氨基”中的“碳原子数0~25的氨基”,可列举:―n<、―n=ch―、或者将与通式(2)中由r1~r9表示的“能够具有取代基的碳原子数0~25的氨基”同样的基团在任意的取代基的部位替代为2价基团或3价基团而得的基团,通过取代基r
12
,可以表示为―nr
12
―、>n―r
12
―、―r
12
―nr
12
―r
12
―、―r
12
―nh―nr
12
―r
12
―等。作为取代基r
12
,可列举与由r1~r9表示的“能够具有取代基的碳原子数0~25的氨基”中的“取代基”同样的基团。多个r
12
可以相同,也可以不同。需要说明的是,在通式(2)中,z包含多个“能够具有取代基的碳原子数0~25的氨基”的情况下,各个q可以经由z而分别与不同的q键合。
[0172]
在通式(2)中,作为由z表示的“能够具有取代基的碳原子数1~25的直链状、支链状或环状的亚烷基”,可列举从具有与由r1~r9表示的“能够具有取代基的碳原子数1~25的直链状、支链状或环状的烷基”相同的结构的1价基团在任意的位置的取代基中替代为2价基团而得的基团。具体而言,可以为与作为由l表示的“能够具有取代基的碳原子数1~25的直链状、支链状或环状的亚烷基”所列举的亚烷基同样的基团。作为“能够具有取代基的碳原子数1~25的直链状、支链状或环状的亚烷基”中的“取代基”,可列举与由r1~r9表示的“能够具有取代基的碳原子数1~25的直链状、支链状或环状的烷基”中的“取代基”同样的基团。这些亚烷基也可以分支而形成3价基团。
[0173]
在通式(2)中,z为2价基团或3价基团,优选为能够具有取代基的碳原子数1~20的氨基、能够具有取代基的碳原子数1~20的直链状、支链状或环状的亚烷基、或者包含醚基
的基团,更优选为能够具有取代基的碳原子数1~20的氨基。
[0174]
需要说明的是,在上述中,
[0175]“碳原子数1~25的直链状、支链状或环状的烷基”优选为“碳原子数1~25的直链状、或碳原子数3~25的支链状或环状的烷基”。
[0176]“碳原子数2~25的直链状、支链状或环状的烯基”优选为“碳原子数2~25的直链状、或碳原子数3~25的支链状或环状的烯基”。
[0177]“碳原子数1~25的直链状、支链状或环状的烷氧基”优选为“碳原子数1~25的直链状、或碳原子数3~25的支链状或环状的烷氧基”。
[0178]“碳原子数1~25的直链状、支链状或环状的亚烷基”优选为“碳原子数1~25的直链状、或碳原子数3~25的支链状或环状的亚烷基”。
[0179]
本发明的化合物由下述基团构成:
[0180]
1个2~10价的基团l(与通式(1)中的l同义)、
[0181]
n个相同或不同且由下述通式(3)表示的1价基团r0、
[0182]
n个相同或不同的1价基团r
12
(与通式(2)中的取代基同义或者为氢原子)、以及
[0183]
n个相同或不同的2价或3价的基团z(与通式(2)中的z同义),
[0184]
n表示2~10的整数,
[0185]
l仅与z键合,
[0186]
r0仅与z键合,
[0187]r12
仅与z键合,
[0188]
z与r0键合、并且与选自l、r
12
以及其它z组成的组中的一者或两者键合。
[0189]
【化11】
[0190][0191]
(式(3)中,r1~r9与上述同义)
[0192]
由通式(1)表示的化合物(以下,简称为化合物(1))包含可生成的所有的立体异构体、互变异构体。化合物(1)的具体例如以下所示,但是,本发明并不限定于这些化合物。需要说明的是,在下述结构式中,省略了一部分氢原子。
[0193]
【化12】
[0194][0195]
【化13】
[0196][0197]
【化14】
[0198][0199]
【化15】
[0200][0201]
【化16】
[0202][0203]
【化17】
[0204][0205]
【化18】
[0206]
[0207]
【化19】
[0208][0209]
【化20】
[0210][0211]
【化21】
[0212][0213]
【化22】
[0214][0215]
【化23】
[0216][0217]
【化24】
[0218][0219]
【化25】
[0220][0221]
【化26】
[0222][0223]
【化27】
[0224][0225]
【化28】
[0226][0227]
【化29】
[0228][0229]
【化30】
[0230][0231]
【化31】
[0232][0233]
由通式(1)表示的化合物可以利用以下的方法来合成。以下,示出了在通式(1)中n为2、z为具有任意的取代基r
10
的氨基、l由―c6h
12
―表示的情况的合成例。
[0234]
利用适合的溶剂、温度,使具有相应取代基的8-氨基-2-甲基喹啉衍生物与1,6-二碘己烷进行反应,从而得到具有相应取代基的下述中间体(x-1)。
[0235]
【化32】
[0236][0237]
进而,利用适合的溶剂、温度,使所得的中间体(x-1)与具有相应取代基的偏苯三酸酐进行脱水缩合反应,从而可以得到由通式(1)表示的本发明的化合物。
[0238]
在本发明中,作为对生成物进行纯化的方法,可列举:采用柱色谱的纯化;采用硅
胶、活性炭、活性白土等的吸附纯化;采用溶剂的重结晶、晶析法等的公知的方法。另外,在这些化合物的鉴定、分析中,可以进行核磁共振分析(nmr)、采用分光光度计的吸光度测定、紫外可见吸收光谱(uv-vis)测定、热重量测定-差示热分析(tg-dta)等。这些分析方法也可以用于所得化合物的溶解性、色彩评价、耐热性评价。
[0239]
本发明的化合物的溶解性以溶解度来表示,溶解度表示物质在特定的溶剂中可以溶解的最大量的比例,例如以“质量%(溶剂名,温度)”等的单位来表示。溶解度例如通过将试样混合至特定的溶剂中,在一定温度下搅拌溶剂一定时间,测定所调制的饱和溶液的浓度而得到,也通过溶解部的基于液相色谱(lc)、吸光度测定等的浓度测定而得到。
[0240]
通过进行本发明的化合物的热重量测定-差示热分析(tg-dta),从而可以对热分解温度进行分析,可以作为耐热性的指标。在着色组合物中,色素部分的化合物的热分解温度优选为250℃以上。在应用于滤色器的情况下,热分解温度越高越优选。
[0241]
通过将本发明的化合物与丙烯酸类树脂等的滤色器用着色剂中所使用的各种树脂溶液进行混合,利用旋涂法等的方法涂布在玻璃基板上,进行加热并干燥,从而可以制作涂膜。对于所得的涂膜,使用分光光度计进行测色,得到涂膜的色彩值,由此可以进行色彩特性的评价。色彩值一般使用cie l
*a*b*
表色系等。具体而言,测定膜试样的色彩值l
*a*b*
,通过在适当的温度下的加热前后的色彩值的色差(δe
*ab
),可以判断耐热性。在应用于滤色器的情况下,可以将在230℃前后(例如,220℃~240℃的范围内)的温度下的色差用作耐热性的指标。就δe
*ab
而言,其值与比较对象相比越小越优选,意味着因热分解引起的颜色的变色少。δe
*ab
优选为3.5以下,更优选为3以下。越是由热分解引起的颜色的变色少的色素化合物,越可以得到着色力、鲜明性、色相等的色彩特性优异的着色组合物、滤色器用着色剂。
[0242]
就滤色器用着色剂中所含有的着色组合物而言,由于需要使色素化合物良好地溶解或分散于树脂以及有机溶剂中,因此优选为这些着色组合物中所含有的化合物对有机溶剂的溶解度高。作为有机溶剂,具体而言,可列举:乙酸乙酯、乙酸正丁酯等的酯类;二乙基醚、丙二醇单甲基醚(pgme)等的醚类;丙二醇单甲基醚乙酸酯(pgmea)等的醚酯类;丙酮、环己酮等的酮类;甲醇、乙醇等的醇类;二丙酮醇(daa)等;苯、甲苯、二甲苯等的芳香族烃类;n,n-二甲基甲酰胺(dmf)、n-甲基吡咯烷酮(nmp)等的酰胺类;二甲基亚砜(dmso)等。这些溶剂可以单独使用,也可以混合2种以上使用。它们当中,本发明涉及的化合物在pgme、pgmea中的溶解性优异,例如,对在室温25
±
2℃的温度范围(23℃~27℃的范围内的温度)的pgmea的溶解度(质量%)(溶剂pgmea,25
±
2℃)优选为0.1质量%以上,更优选为1质量%以上,特别优选为2质量%以上。
[0243]
由通式(1)表示的化合物在溶液中的可见光区域、例如350nm~700nm的范围的最大吸收波长优选在400nm~500nm的范围。
[0244]
本发明的着色组合物含有由通式(1)表示的本发明的化合物,可以含有1种结构的化合物,也可以含有2种以上结构的化合物。在本发明中,化合物的结构优选为1种。
[0245]
为了提高作为滤色器用着色剂的性能,本发明的着色组合物可以添加表面活性剂、分散剂、消泡剂、流平剂、其它滤色器用着色剂的制造时混合的添加剂等作为化合物的其它成分。但是,着色组合物中的这些添加剂的含有率优选为适量,优选为不使着色组合物的溶解性降低、或者使着色组合物的溶解性提高至所需以上、或者不影响滤色器制造的范
围的含有率。这些添加物可以在制备着色组合物的任意时机投入。
[0246]
本发明的滤色器用着色剂包含:含有由通式(1)表示的化合物的着色组合物;和在滤色器的制造中一般使用的成分。一般的滤色器通过以下方式得到:例如,在利用了光刻工序的方法的情况下,将染料、颜料等色素与树脂成分(包含单体、低聚物、粘结剂成分、抗蚀剂成分)、溶剂进行混合而调制液体,将调制成的液体涂布在玻璃、树脂等的基板上,使用光掩模进行光聚合,制作在溶剂中可溶/不溶的色素-树脂复合膜的着色图案,清洗后进行加热。本发明的化合物由于溶解性优异,因此与这些滤色器的制造中所使用的材料之间的分散性优异,因此可以根据需要与其它材料进行混合、制膜,并进行耐热性、吸光特性的评价。另外,在电沉积法、印刷法中,也可以使用将色素与树脂、其它成分混合而成的混合物来制作着色图案。因此,作为本发明的滤色器用着色剂中的具体成分,可列举由通式(1)表示的化合物、其它染料、颜料等色素、树脂成分、有机溶剂以及光聚合引发剂等其它添加剂。另外,可从这些成分进行取舍选择,或者根据需要追加其它成分。
[0247]
在使用本发明的着色组合物作为滤色器用着色剂的情况下,可以作为黄色系滤色器来使用,但是也可以与红色、绿色等其它颜色用的滤色器混合使用。另外,可以将本发明的着色组合物单独使用,为了调整色相,也可以混合其它染料或颜料等公知的色素。例如,可列举:碱性染料;酸性染料;分散染料;spilon染料;偶氮系、双偶氮系、喹啉系、芪系、(聚)次甲基系、花青系、靛蓝系、酞菁系、蒽醌系、吖啶系、三芳基甲烷系、阴丹士林系、噁嗪系、二噁嗪系、萘酚as系、苯并咪唑酮系、吡唑啉酮系、苝系、紫环酮系、喹吖啶酮系、异吲哚啉酮系、呫吨系、二酮吡咯并吡咯系等的染料或颜料等。
[0248]
本发明的着色组合物以及滤色器用着色剂中的其它色素的混合比相对于由通式(1)表示的化合物优选为5质量%~2000质量%,更优选为10质量%~1000质量%。液状的滤色器用着色剂中的染料等的色素成分的混合比相对于着色剂整体优选为0.5质量%~70质量%,更优选为1质量%~50质量%。
[0249]
作为本发明的着色组合物以及滤色器用着色剂中的树脂成分,只要具有在使用它们所形成的滤色器树脂膜的制造方式、使用时所需的性质,就可以使用公知的树脂成分。例如,可列举:丙烯酸类树脂、烯烃树脂、苯乙烯树脂、聚酰亚胺树脂、聚氨酯树脂、聚酯树脂、环氧树脂、乙烯基醚树脂、酚醛(清漆)树脂、其它透明树脂、光固化性树脂、热固化性树脂、粘结剂树脂、光致抗蚀剂树脂,可以将它们适当组合使用。另外,也可以将这些树脂的共聚物组合使用。这些滤色器用着色剂中的树脂的含量在液态的着色剂的情况下优选为5质量%~95质量%,更优选为10质量%~50质量%。
[0250]
作为本发明的着色组合物以及滤色器用着色剂中的其它添加剂,可列举:光聚合引发剂、交联剂等的在树脂的聚合、固化中所需要的成分,另外,可列举为了使液态的滤色器用着色剂中的成分的性质稳定所需要的表面活性剂、分散剂等。它们均可以使用公知的添加剂,并无特别限定。这些添加剂的总量在滤色器用着色剂的固体成分整体中的混合比优选为5质量%~60质量%,更优选为10质量%~40质量%。
[0251]
【实施例】
[0252]
以下,通过实施例对本发明的实施方式进行具体说明,但本发明并不限定于以下的实施例。需要说明的是,在合成实施例中,化合物的鉴定通过1h-nmr分析(bruker公司制造、核磁共振装置、ascend
tm 400)来进行。
[0253]
【合成实施例1】化合物(a-5)的合成
[0254]
向反应容器中加入8-氨基-2-甲基喹啉48.0g、三乙基胺40.2g、二氯甲烷384ml,在冰浴中冷却至5℃以下。缓缓地加入2,4,6-三甲基苯甲酰氯82.8g,在25℃下搅拌7小时。向反应液中加入水,用二氯甲烷进行萃取。将萃取液进行减压浓缩,用柱色谱进行纯化(载体:硅胶、溶剂:庚烷/二氯甲烷/乙酸乙酯=10/3/1(体积比))。向反应液中加入庚烷,进行过滤,得到n-(2,4,6-三甲基苯甲酰基)-8-氨基喹哪啶(70.8g、收率77%)。
[0255]
接着,向反应容器1中加入氢化钠(60%、分散于液体石蜡中)17.5g、脱水dmf 300ml,在冰浴中冷却至5℃以下。用另一反应容器2,制备将上述的n-(2,4,6-三甲基苯甲酰基)-8-氨基喹哪啶60.6g用脱水dmf300ml溶解而得的溶液。将该反应容器2的溶液缓缓地滴加至反应容器1中,在25℃下搅拌2小时。加入1,6-二碘己烷33.6g,在25℃下搅拌2小时。向反应液中加入二氯甲烷600ml,缓缓地滴加水600ml,用二氯甲烷进行萃取。将萃取液进行减压浓缩,用柱色谱进行纯化(载体:硅胶、溶剂:二氯甲烷/庚烷=1/1(体积比)),得到下述中间体(100)(68.8g、收率100%)。
[0256]
【化33】
[0257][0258]
接着,向反应容器中加入上述得到的中间体(100)68.8g、偏苯三酸酐57.4g、苯甲酸36.5g、1,2,4-三氯苯130ml,在180℃下搅拌8小时。冷却至25℃后,向反应液中加入甲苯680ml,进行过滤,得到下述中间体(101)(95.0g、收率92%)。
[0259]
【化34】
[0260][0261]
接着,向反应容器中加入上述得到的中间体(101)25.0g、二丁基胺8.1g、三乙基胺7.3g、dmf 200ml、1-[双(二甲基氨基)亚甲基]-1h-1,2,3-三唑并[4,5-b]吡啶鎓3-氧化物六氟磷酸盐(hatu)23.8g,在25℃下搅拌5小时。向反应液中添加水,用二氯甲烷进行萃取。将萃取液减压浓缩,用柱色谱进行纯化(载体:硅胶、溶剂:二氯甲烷/丙酮=10/1(体积比)),得到黄色粉末(15.0g、收率49%)。
[0262]
对所得的黄色粉末进行nmr测定,检测出以下88个氢的信号,鉴定为由上述式(a-5)表示的化合物的结构。
[0263]1h-nmr(400mhz、cdcl3):δ(ppm)=13.80-14.60(2h)、8.50-8.80(2h)、7.90-8.20(2h)、7.40-7.80(10h)、6.30-7.20(6h)、3.00-5.20(12h)、2.50-2.70(2h)、2.20-
2.50(6h)、1.80-2.10(6h)、0.70-1.80(40h)。
[0264]
【合成实施例2】化合物(a-11)的合成
[0265]
向反应容器1中加入氢化钠(60%、分散于液体石蜡中)8.6g、脱水dmf 160ml,在冰浴中冷却至5℃以下。用另一反应容器2,制备将合成实施例1中得到的n-(2,4,6-三甲基苯甲酰基)-8-氨基喹哪啶32.7g用脱水dmf160ml溶解而得的溶液。将该反应容器2的溶液缓缓地滴加到反应容器1中,在25℃下搅拌2小时。加入1,10-二碘十二烷21.2g,在25℃下搅拌2小时。向反应液中加入二氯甲烷320ml,缓缓滴加水320ml,用乙酸乙酯进行萃取。将萃取液进行减压浓缩,用柱色谱进行纯化(载体:硅胶、溶剂:二氯甲烷/庚烷=1/1(体积比)),得到下述中间体(102)(30.7g、收率82%)。
[0266]
【化35】
[0267][0268]
接着,向反应容器中加入上述得到的中间体(102)30.7g、2,3-萘二甲酸酐24.4g、苯甲酸15.0g、1,2,4-三氯苯80ml,在180℃下搅拌8小时。冷却至25℃后,用柱色谱进行纯化(载体:硅胶、溶剂:二氯甲烷/丙酮=10/1(体积比)),得到黄色粉末(7.7g、收率17%)。
[0269]
对所得的黄色粉末进行nmr测定,检测出以下66个氢的信号,鉴定为由下述式(a-11)表示的化合物的结构。
[0270]1h-nmr(400mhz、cdcl3):δ(ppm)=14.50-15.00(2h)、8.70-8.90(2h)、7.80-8.30(6h)、7.40-7.80(8h)、6.80-7.30(8h)、6.30-6.80(2h)、3.20-5.20(4h)、2.20-2.80(14h)、1.80-2.10(6h)、0.80-1.50(14h)。
[0271]
【合成实施例3】化合物(a-19)的合成
[0272]
向反应容器中加入合成实施例2中得到的中间体(102)30.7g、3-氯邻苯二甲酸酐24.0g、苯甲酸16.1g、1,2,4-三氯苯60ml,在180℃下搅拌8小时。冷却至25℃后,用柱色谱进行纯化(载体:硅胶、溶剂:二氯甲烷/丙酮=10/1(体积比)),得到黄色粉末(20.7g、收率51%)。
[0273]
对所得的黄色粉末进行nmr测定,检测出以下60个氢的信号,鉴定为由下述式(a-19)表示的化合物的结构。
[0274]1h-nmr(400mhz、cdcl3):δ(ppm)=14.00-14.60(2h)、8.40-8.70(4h)、7.30-8.10(12h)、6.40-7.10(4h)、3.50-4.90(4h)、2.50-2.70(2h)、2.20-2.50(12h)、1.70-2.20(6h)、0.70-1.70(14h)。
[0275]
【合成实施例4】化合物(a-20)的合成
[0276]
向反应容器中加入合成实施例1中得到的中间体(100)27.2g、4-甲基邻苯二甲酸酐20.4g、苯甲酸15.4g、1,2,4-三氯苯50ml,在180℃下搅拌8小时。冷却至25℃后,用柱色谱进行纯化(载体:硅胶、溶剂:二氯甲烷/丙酮=10/1(体积比)),得到黄色粉末(24.8g、收率64%)。
[0277]
对所得的黄色粉末进行nmr测定,检测出以下58个氢的信号,鉴定为由下述式(a-20)表示的化合物的结构。
[0278]1h-nmr(400mhz、cdcl3):δ(ppm)=13.80-14.50(2h)、7.80-8.80(4h)、7.30-7.70(8h)、6.80-7.20(6h)、6.30-6.70(2h)、3.00-5.20(4h)、2.50-2.70(4h)、2.20-2.50(12h)、1.80-2.10(6h)、0.70-1.70(10h)。
[0279]
【合成实施例5】比较例化合物(b-1)的合成
[0280]
向反应容器中加入用与上述合成实施例1同样的方法得到的n-(2,4,6-三甲基苯甲酰基)-n-丙基-8-氨基喹哪啶47.4g、4-甲基邻苯二甲酸酐17.8g、苯甲酸13.4g、1,2,4-三氯苯80ml,在180℃下搅拌8小时。冷却至25℃后,用柱色谱进行纯化(载体:硅胶、溶剂:庚烷/二氯甲烷/乙酸乙酯=10/3/1(体积比)),得到黄色粉末(b-1)(24.0g、收率36%)。
[0281]
对所得的黄色粉末进行nmr测定,检测出以下30个氢的信号,鉴定为由下述式(b-1)表示的化合物的结构。
[0282]1h-nmr(400mhz、cdcl3):δ(ppm)=13.90-14.50(1h)、8.60-8.80(1h)、7.99-8.10(1h)、7.30-7.80(5h)、6.90-7.25(2h)、6.40-6.80(1h)、3.20-5.20(2h)、2.30-2.50(6h)、1.90-2.10(3h)、0.60-1.40(8h)。
[0283]
【化36】
[0284][0285]
【实施例1】
[0286]
对合成实施例1中得到的化合物(a-5),测定了在室温(23℃~27℃的范围)的pgmea溶剂中的溶解度(质量%)(溶剂pgmea,25
±
2℃)。将结果示于表1中。
[0287]
将甲基丙烯酸、丙烯酸酯以及苯乙烯的共聚物的25质量%dmf-pgmea混合溶液5.0g和合成实施例1中得到的化合物(a-5)20mg加入样品瓶中,搅拌混合30分钟。将所得的着色树脂溶液1g涂布(旋涂法、1000rpm-6秒)在5cm
×
5cm的玻璃基板上,在100℃下加热2分钟进行制膜。对所得的膜,使用分光光度计(konica minolta株式会社制造、cm-5),测定了色彩值。之后,在230℃下进行2次20分钟的加热,同样地测定了色彩值。以在230℃下加热前后的色彩值的色差(δe
*ab
)作为耐热性的指标,将结果一并示于表1中。
[0288]
【实施例2~实施例4】
[0289]
作为化合物,代替(a-5)而使用了合成实施例2~4中得到的化合物(a-11)、(a-19)以及(a-20),除此以外,用与实施例1同样的方法测定在室温的pgmea溶剂中的溶解度(质量%)(溶剂pgmea,25
±
2℃),另外,对制成的膜,测定了在230℃下加热前后的色彩值的色差(δe
*ab
),并进行了评价。将结果归纳示于表1中。
[0290]
【比较例1以及比较例2】
[0291]
作为化合物,代替(a-5)而使用作为不属于本发明的色素化合物的、合成实施例5中得到的化合物(b-1)和由下述式(b-2)表示的作为以往的色素化合物的c.i.溶剂黄33,
除此以外,与实施例1同样地测定了在室温的pgmea溶剂中的溶解度(质量%)(溶剂pgmea,25
±
2℃)。另外,对制成的膜,测定了在230℃下加热前后的色彩值的色差(δe
*ab
),并进行了评价。将结果归纳示于表1中。
[0292]
【化37】
[0293][0294]
【表1】
[0295][0296]
如表1所示,本发明的实施例的化合物显示出在pgmea中的高溶解性以及在制膜时的高耐热性,含有本发明的化合物的着色组合物作为滤色器用着色剂,在实用上没有问题。另外,在制膜时具有高于比较例的耐热性,作为滤色器用着色剂是优异的。
[0297]
(产业上可利用性)
[0298]
含有本发明涉及的化合物(黄色系化合物)的着色组合物在有机溶剂(pgmea等)中的溶解性优异,并且制膜时的耐热性优异,因此作为滤色器用着色剂等各种用途的色素材料是有用的。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1