铜纳米团簇荧光探针的制备及水环境中次氯酸根检测方法与流程
1.本发明属于水样检测分析技术领域,涉及一种铜纳米团簇荧光探针及水环境中次氯酸根的荧光检测方法,尤其涉及一种基于碘离子增强的铜纳米团簇荧光材料的水样中次氯酸根的高灵敏度检测方法。
背景技术:
2.人体中的活性氧是在巨噬细胞线粒体中产生的,起到抵御有害刺激的作用。作为众多活性氧类物质的一种,内源性次氯酸(hclo)是通过氯离子和过氧化氢在髓过氧化物酶的催化下发生过氧化反应形成的,在人体免疫系统中扮演着十分重要的角色。机体内髓过氧化物酶水平的变化能够引起次氯酸病理学浓度异常,过量的次氯酸往往会引起多种疾病,包括心血管疾病、阿尔茨海默病、神经退行性病变、肾病、类风湿关节炎和癌症等。次氯酸盐是一种广泛应用于饮用水、游泳池和回用水的氯化消毒剂。在工业、纺织、木浆、食品和奶业上,次氯酸通常作为一种漂白剂。2017年国际癌症研究机构(iarc)将次氯酸定义为第三类致癌物质。然而,它通常作为一种添加剂被加入到一些食品和药物中,如婴儿配方、汤和滴眼液。因此,次氯酸的生物成像以及对环境中次氯酸浓度的痕量检测是一个极其重要的研究领域。
3.目前,人们已开发出大量的次氯酸测定方法,这些方法主要包括比色法、碘量滴定法、化学发光法、电化学法、高效液相色谱法和荧光法等。但是大多数的分析方法都需要复杂的探针和样品的准备程序,或者需要精密的仪器,这些缺点使得它们不适合现场检测活性物质次氯酸。近年来,荧光分析法因其实时监测、高选择性和良好的生物成像能力而备受科研工作者的青睐,其应用范围已遍及生命科学、食品科学、医药等多个领域。到目为止前,报道了很多带有荧光集团的有机小分子荧光探针的研制,例如罗丹明类、荧光素类、喹啉类和咔唑类。但是上述探针具有一定的局限性,例如具有疏水性和生物系统特异性差。基于以上因素,开发出一种具有高灵敏度、高选择性的用于次氯酸检测的发光无机纳米探针具有重大的意义。
技术实现要素:
4.本发明的目的就是提供一种铜纳米团簇荧光探针及水环境中次氯酸根的荧光检测方法。
5.本发明的目的可以通过以下技术方案来实现:
6.一种铜纳米团簇荧光探针的制备方法,包括以下步骤:
7.将聚乙烯吡咯烷酮、抗坏血酸、铜源于溶液中混合,经透析处理后,取截留液冻干处理,即得到铜纳米团簇荧光探针。
8.进一步地,所述的聚乙烯吡咯烷酮、抗坏血酸、铜源的投料比为1g:(1.5~2.5)
×
10-4
mol:(1.5~2.5)
×
10-5
mol。
9.进一步地,所述的聚乙烯吡咯烷酮、抗坏血酸、铜源的混合过程包括:
10.将聚乙烯吡咯烷酮水溶液、抗坏血酸水溶液、铜源水溶液混合,再恒温孵育,得到混合溶液;
11.其中,恒温孵育过程中,孵育温度为常温,孵育时间为6~7天
12.进一步地,所述的聚乙烯吡咯烷酮水溶液的浓度为0.05g/ml,ph为6~7;所述的抗坏血酸水溶液的浓度为100mm;所述的铜源水溶液为100mm的硫酸铜溶液。进一步地,透析处理过程中,透析膜的截留分子量为7000~14000。
13.一种水环境中次氯酸根的荧光检测方法,包括以下步骤:
14.s1:将铜纳米团簇荧光探针配制为水溶液,得到荧光探针溶液;
15.s2:将荧光探针溶液与待测溶液混合均匀,得到待检测液;
16.s3:分别测定荧光探针溶液与待检测液在紫外激发下的荧光强度,并分别记为f0与f;
17.s4:计算荧光强度比f/f0,再根据荧光强度比f/f0与次氯酸根浓度的标准曲线,获得待测溶液中次氯酸根浓度;
18.其中,所述的铜纳米团簇荧光探针,采用如上所述的方法制备得到。
19.进一步地,步骤s1中,所述的荧光探针溶液中,铜纳米团簇荧光探针的浓度为0.4mg ml-1
;溶剂为磷酸缓冲液,浓度为25~75mm,ph=5.8~6.2;
20.步骤s2中,所述的待检测液中,次氯酸根的浓度不大于8μm。
21.进一步地,步骤s2中,所述的荧光探针溶液与待测溶液混合前,先向荧光探针溶液中加入碘源,使得荧光探针溶液的碘离子浓度为8~9μm。
22.进一步地,步骤s3中,紫外激发波长为340~365nm,所述的荧光强度为发射波长410~420nm处的荧光强度。
23.进一步地,步骤s4中,所述的标准曲线的绘制方法包括以下步骤:
24.s4-1:将荧光探针溶液与次氯酸混合,得到不同次氯酸浓度的标准溶液;
25.s4-2:分别测定荧光探针溶液与标准溶液在紫外激发下的荧光强度,并分别记为f0与f’;
26.s4-2:计算荧光强度比f’/f0,再分别以荧光强度比、次氯酸浓度为横纵坐标作图,即得到所述的标准曲线。
27.响应机理:次氯酸能够氧化铜纳米团簇表面的还原性铜从而使其荧光猝灭。在微量hclo存在下,cuncs自发进行如式(1)所示的氧化反应
28.cu+hclo+h
+
→
cu
2+
+cl-+h2o
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
(1)
29.在过量碘离子(i-)的存在下,过量的碘离子、次氯酸和铜纳米团簇之间存在如式(2)~(5)的相互作用,进而使得铜纳米团簇对次氯酸响应增强。
30.hclo+2i-+h
+
→
i2+cl-+h2o
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
(2)
[0031][0032]i3-+2cu
→
2cui
↓
+i-ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
(4)
[0033]i3-+cu
+
→
cui
↓
+i2ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
(5)
[0034]
在酸性条件下,当过量的碘离子存在时,加入的次氯酸首先与其发生反应。由此产生的i
3-会与团簇上的还原性铜发生反应,形成碘化亚铜沉淀并依附在探针的表面,导致其表面产生缺陷。这些表面缺陷可以显著降低探针的荧光强度,导致探针对次氯酸的响应增
强。此外根据在荧光检测时改变次氯酸和碘离子的加入顺序的实验结果可知,只有在加入次氯酸之前加入碘离子,碘离子才会起到这种“增敏作用”。这是因为先加入的次氯酸能够直接氧化探针,之后再加入碘离子则不再影响探针的荧光强度,因此过量的碘离子和次氯酸的加入顺序会同时影响探针的线性范围和检测限。
[0035]
与现有技术相比,本发明具有以下特点:
[0036]
1)本发明中的一种铜纳米团簇(cuncs)荧光探针,最佳激发波长为365nm,最佳发射波长为416nm,在紫外灯下呈蓝色荧光,具有量子产率高、毒性低、水溶性好等优点;
[0037]
2)水体中常见的阴离子,如oh-、i-、co
32-等均无法使荧光探针产生显著的荧光猝灭现象,表明荧光探针具有较高的选择性;
[0038]
3)本发明可通过在荧光探针溶液与待测溶液混合前,先向荧光探针溶液中加入碘源,从而显著降低次氯酸检测限,具有较好的检测灵敏度。
附图说明
[0039]
图1为实施例1所制备铜纳米团簇(cuncs)荧光探针的扫描电镜图(上图)和高分辨扫描电镜图(下图,对应于上图中白色方框处);
[0040]
图2为实施例1所制备铜纳米团簇(cuncs)荧光探针和硫酸奎宁在380nm~550nm范围内的荧光曲线积分面积与相应光密度之间的关系图;
[0041]
图3为实施例1所制备铜纳米团簇(cuncs)荧光探针的高分辨cu(2p)xps谱图;
[0042]
图4为实施例2中cuncs探针与次氯酸反应后的高分辨cu(2p)xps谱图;
[0043]
图5为实施例5中cuncs探针在过量碘离子存在下与次氯酸反应后的高分辨cu(2p)xps谱图;
[0044]
图6为实施例2中不同次氯酸浓度下cuncs探针的荧光谱图(次氯酸浓度分别为0、0.5、1、1.5、2、2.5、3、3.5、4、4.5、5、5.5、6、6.5、7、7.5和8μm);
[0045]
图7为实施例2中次氯酸加入前后的荧光强度比f/f0与次氯酸浓度c[μm]之间的关系图;
[0046]
图8为实施例4中i-掺杂后不同次氯酸浓度下cuncs探针的荧光谱图(次氯酸浓度分别为0、0.3、0.6、0.9、1.2、1.5、1.8、2.1、2.4、2.7、3.0、3.3、3.6和3.9μm);
[0047]
图9为实施例4中i-掺杂下次氯酸加入前后的荧光强度比f/f0与次氯酸浓度c[μm]之间的关系图;
[0048]
图10为实施例3中水体中不同离子类型加入前后的荧光强度比f/f0对比图(其中碘离子浓度为6μm,次氯酸浓度为3μm,其他离子浓度均为10μm);
[0049]
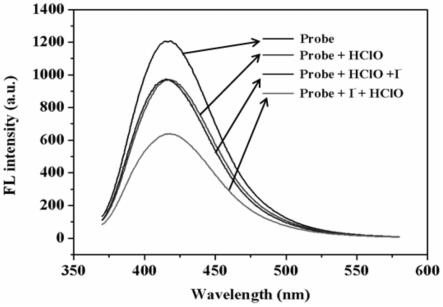
图11为实施例5中i-是否掺杂以及不同掺杂顺序下次氯酸加入后cuncs探针的荧光谱图(碘离子和次氯酸的浓度分别为3nm和1.5μm)。
具体实施方式
[0050]
下面结合附图和具体实施例对本发明进行详细说明。
[0051]
一种铜纳米团簇荧光探针的制备方法,包括以下步骤:
[0052]
将0.05g/ml、ph为6~7的聚乙烯吡咯烷酮水溶液、100mm抗坏血酸水溶液、100mm铜源水溶液,以聚乙烯吡咯烷酮、抗坏血酸、铜源的投料比为1g:(1.5~2.5)
×
10-4
mol:(1.5~
2.5)
×
10-5
mol进行混合,再在常温下恒温孵育6~7天,经截留分子量为7000~14000的透析膜进行透析处理后,取截留液冻干处理,即得到铜纳米团簇荧光探针。
[0053]
一种水环境中次氯酸根的荧光检测方法,包括以下步骤:
[0054]
s1:将铜纳米团簇荧光探针与磷酸缓冲液混合配制为水溶液,得到浓度为0.4mg ml-1
的荧光探针溶液;
[0055]
s2:将荧光探针溶液与待测溶液混合均匀,得到待检测液;其中,待检测液中,次氯酸根的浓度不大于8μm;
[0056]
s3:分别测定荧光探针溶液与待检测液在波长为340~365nm紫外激发下,在发射波长410~420nm处的荧光强度,并分别记为f0与f;
[0057]
s4:计算荧光强度比f/f0,再根据荧光强度比f/f0与次氯酸根浓度的标准曲线,获得待测溶液中次氯酸根浓度;
[0058]
优选的,步骤s2中,所述的荧光探针溶液与待测溶液混合前,先向荧光探针溶液中加入碘源,使得荧光探针溶液的碘离子浓度为8~9μm。
[0059]
步骤s4中,标准曲线的绘制方法包括以下步骤:
[0060]
s4-1:将荧光探针溶液与次氯酸混合,得到不同次氯酸浓度的标准溶液;
[0061]
s4-2:分别测定荧光探针溶液与标准溶液在紫外激发下的荧光强度,并分别记为f0与f’;
[0062]
s4-2:计算荧光强度比f’/f0,再分别以荧光强度比、次氯酸浓度为横纵坐标作图,即得到所述的标准曲线。
[0063]
本实施例以本发明技术方案为前提进行实施,给出了详细的实施方式和具体的操作过程,但本发明的保护范围不限于下述的实施例。
[0064]
实施例1:
[0065]
一种铜纳米团簇(cuncs)荧光探针的制备:
[0066]
1)将1g聚乙烯吡咯烷酮(pvp)加入到100ml烧瓶中,加入20ml超纯水,超声处理至pvp溶解;之后滴加适量的氢氧化钠溶液(1.0m),至溶液ph调整到6.0;
[0067]
2)将2ml 100mm的抗坏血酸(aa)水溶液与0.2ml 100mm的五水合硫酸铜(cuso4·
5h2o)水溶液混合,并加入至步骤1)所得溶液中;在摇床中恒温(25℃)孵育6天后,溶液在太阳光下由最初的无色变为澄清透明的淡黄色,并且在365nm紫外灯的照射下可观察到较强的蓝色荧光,表明cuncs的形成;
[0068]
3)采用截留分子量为7000的透析袋进行为期三天的透析处理,取截留液冻干处理,得到固体cuncs,并置于冰箱中在4℃下冷藏以备后续使用。
[0069]
如图1所示为本实施例所制备铜纳米团簇(cuncs)荧光探针的透射电镜图和高分辨透射电镜图(比例尺分别为20nm和2nm),可以清楚地看出本实验合成的铜纳米团簇近乎球形,条纹晶格间距约为
[0070]
如图2所示为cuncs探针和硫酸奎宁在380nm~550nm范围内的荧光曲线积分面积与相应光密度之间的关系。以0.1m硫酸中的硫酸奎宁(qr=0.54)为对照溶液,通过控制溶液紫外吸光度的数值,分别获得了cuncs和硫酸奎宁的荧光积分面积与紫外吸光度之间的线性回归方程。cuncs的量子产率经式(6)计算为9.39%。
[0071]
q=qr[m/mr][n2/n
r2
]
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
(6)
[0072]
式中,q为待测样品的荧光量子产率,qr为硫酸奎宁标准物质的荧光量子产率,m和mr分别为待测样品和硫酸奎宁参比样图2曲线的斜率,n和nr分别为待测样品和硫酸奎宁参比样的折射率。
[0073]
如图3所示为本实施例所制备铜纳米团簇(cuncs)荧光探针的高分辨cu(2p)xps谱图,从图中可以看出,cuncs形成后表面具有还原价态铜。
[0074]
实施例2:
[0075]
本实施例通过光谱滴定实验测试表征实施例1所制备的铜纳米团簇荧光探针对水样中次氯酸根的有效检测范围,具体过程包括以下步骤:
[0076]
s1:将cuncs加入至磷酸缓冲液中,得到浓度为0.4mg ml-1
荧光探针溶液;其中,磷酸缓冲液的浓度为50mm,ph=6.2;
[0077]
s2:向cuncs检测液中加入次氯酸,并混合均匀,得到次氯酸浓度为0~8μm的待检测液;
[0078]
s3:使用荧光光谱仪在波长为340nm下对步骤s1制得的荧光探针溶液以及步骤s2制得的待检测液,进行信号的采集,得到如图6所示的荧光谱图,从图中可以看出,cuncs在416nm处的荧光强度随着次氯酸浓度(0.5~8μm)的增加逐渐降低。
[0079]
如图4所示为本实施例步骤s2制得的待检测液中,cuncs探针与次氯酸反应后的高分辨cu(2p)xps谱图,次氯酸浓度为8μm,对比图3可以看出,探针表面的还原性铜被次氯酸氧化生成了二价铜。
[0080]
本实施例还根据如图6所示的荧光谱图中416nm处的荧光强度,定量考察荧光强度与次氯酸浓度之间的关系,具体过程如下:
[0081]
将步骤s1制得的荧光探针溶液在416nm处的荧光强度,记为f0;将步骤s2制得的待检测液在416nm处的荧光强度,记为f;
[0082]
计算f/f0,并以f/f0为纵坐标,次氯酸浓度c[μm]为横坐标作图,结果如图7所示,从图中可以看出,f/f0与c[μm]之间表现出较好的线性关系,其通过拟合得到的线性回归方程为f/f0=-0.134c[μm]+1.005(r2=0.998)。
[0083]
根据下式,计算出本实施例中cuncs探针检测次氯酸的检出限(lod)为55nm(3σ)。
[0084]
lod=3σ/k
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
(7)
[0085]
式中,σ:10次测试中荧光强度值的标准方差;k:线性拟合标准曲线的斜率。
[0086]
实施例3:
[0087]
本实施例用于考察实施例1所制备铜纳米团簇(cuncs)荧光探针对h2o2、tbph、
·
oh、tbo
·
、o2·-、hco
3-、co
32-、br-、fe
2+
、fe
3+
、cu
2+
、hg
2+
、pb
2+
、i-、hclo的检测选择性,具体过程如下:
[0088]
m1:将cuncs加入至磷酸缓冲液中,得到浓度为0.4mg ml-1
荧光探针溶液;其中,磷酸缓冲液的浓度为50mm,ph=6.2;
[0089]
m2:向多个cuncs检测液中分别加入h2o2:10μm;tbph:10μm;
·
oh:6μm;tbo
·
:6μm;o2·-:10μm;hco
3-:10μm;co
32-:10μm;br-:10μm;fe
2+
:10μm;fe
3+
:10μm;cu
2+
:10μm;hg
2+
:10μm;pb
2+
:10μm;i-:6μm;hclo:3μm;i-+hclo:6μm,3μm;
[0090]
m3:使用荧光光谱仪在波长为340nm下对步骤m1制得的荧光探针溶液以及步骤m2制得的待检测液,进行信号的采集,并计算荧光探针溶液在416nm处的荧光强度f0,与待检
测液在416nm处的荧光强度f之比f/f0,结果如图10所示。
[0091]
从图10中可以看出,相较于hclo,对于水体中常见的大部分粒子,实施例1所制备铜纳米团簇(cuncs)荧光探针均没有产生明显的荧光强度变化,充分说明了探针对于检测次氯酸具有特异性。此外,在掺杂碘离子的情况下,加入同等浓度的hclo后探针的荧光淬灭程度更加剧烈。本方法具备应用于环境中次氯酸选择性检测的潜力。
[0092]
实施例4:
[0093]
本实施例用于考察i-掺杂对次氯酸浓度与探针荧光强度变化率之间的影响,具体过程同实施例2,不同之处仅在于:步骤s2加入次氯酸前,先加入碘化钾溶液,使得溶液中i-的浓度为8μm。所得荧光谱图如图8所示,所得i-掺杂下的标准曲线如图9所示,线性回归方程为f/f0=-0.34c[μm]+1.03(r2=0.997),cuncs-碘离子-次氯酸体系的线性检测范围为0.3~3.9μm,计算出的检出限低至19nm。
[0094]
结合实施例3可以看出,虽然碘离子本身几乎不影响cuncs的荧光强度,但在与上述条件相同的情况下,过量浓度的i-可以增强次氯酸对cuncs探针荧光发射的猝灭效果,从而使得探针荧光强度更大幅度的降低。即酸性条件下过量碘离子的存在很大程度上提高了该检测方法的灵敏度,故碘离子在响应体系中起到“增敏”作用。
[0095]
实施例5:
[0096]
本实施例用于研究了碘离子和次氯酸的不同添加顺序对荧光强度变化的影响,实验过程包括:
[0097]
probe:同实施例2中荧光探针溶液;
[0098]
probe+hclo:同实施例2中次氯酸浓度为1.5μm的待检测液;
[0099]
probe+i-+hclo:同实施例4(i-浓度为8μm,次氯酸浓度为1.5μm);
[0100]
probe+hclo+i-:与probe+i-+hclo相比仅i-、hclo引入顺序对调;
[0101]
所得待检测液,即cuncs探针在过量碘离子存在下与次氯酸反应后的高分辨cu(2p)xps谱图如图5所示,对比图3可以看出,加入的次氯酸直接与碘离子反应导致探针的表面缺陷。
[0102]
结果如图11所示,表明只有在次氯酸前加入过量的碘离子,才能提高cuncs检测次氯酸的灵敏度。在加入次氯酸后加入碘离子,探针的荧光强度并不发生变化。上述过程亦可视为过量碘离子和次氯酸的加入顺序会影响到探针的线性范围和检测限,直接在探针溶液中加入次氯酸会具有较大的线性范围,而在过量碘离子存在时该体系具有较高的灵敏度。
[0103]
上述的对实施例的描述是为便于该技术领域的普通技术人员能理解和使用发明。熟悉本领域技术的人员显然可以容易地对这些实施例做出各种修改,并把在此说明的一般原理应用到其他实施例中而不必经过创造性的劳动。因此,本发明不限于上述实施例,本领域技术人员根据本发明的揭示,不脱离本发明范畴所做出的改进和修改都应该在本发明的保护范围之内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1