反应器的制作方法
1.荣多反应器,属于化学反应仪器。
背景技术:
2.在化学教学中,化学反应都需要用到化学仪器或仪器的组合,这样,我们才能更好地观察实验现象,利用实验分析问题、解决问题;无疑,好的化学仪器或仪器的组合能起到事半功倍的效果;目前,常用的化学仪器如试管、烧杯、集气瓶、锥形瓶、漏斗、坩埚、蒸发皿等单件仪器只能完成一些简单的实验,较复杂的如蒸馏烧瓶、冷凝器等必须与其他仪器配合才能使用;气体发生器是一种能制取气体的仪器,但它所能解决的问题很有限,只是方便了块状固体与液体之间不需要加热的就能发生反应制取气体而已,它只是一个气体的制取装置;我们都知道,要完成氧气、氢气、二氧化碳等气体的性质实验,就需要用到多样仪器的组合,分别做成气体的制取装置和气体的收集装置,只有气体被制取、被收集了才能进行下一步的实验;想一想就知道,这有多麻烦,多耗时间;那么,能不能设计一套化学仪器或新的整体反应平台,把气体的制取装置和气体的收集装置合二为一,让多个化学反应在整体反应平台上一次性完成呢,答案是肯定的,下面将介绍的就是本人设计制作的这样的一个整体反应平台,为了便于说明,我把这样的一个整体反应平台暂时命名为荣多反应器。
技术实现要素:
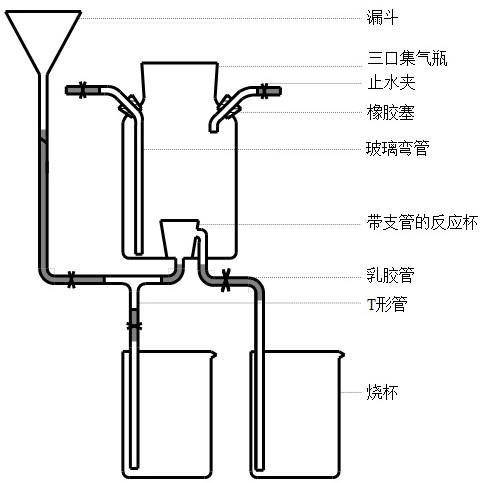
3.一、发明的内容:荣多反应器一物多能,能解决很多实际问题:1.块状固体与液体之间不需要加热就能发生反应生成的气体都可用荣多反应器来制取,且气体的制取装置和气体的收集装置可合二为一;在教学实际中,利用荣多反应器可制取氧气、氢气、二氧化碳、二氧化氮、硫化氢气体;2.可让氧气与铁、氧气与硫、氧气与木炭、氧气与红磷、氧气与蜡烛等多个化学反应在荣多反应器内一次性依次完成,且实验过程中不需要收集氧气,损时损力;氧气与硫、氧气与木炭、氧气与红磷、氧气与蜡烛反应后的产物二氧化硫、二氧化碳、五氧化二磷都能被吸收利用,不会造成空气污染;3.荣多反应器可控制为一个密闭的反应空间,利用它可完成物质燃烧条件的探究实验、二氧化氮气体的扩散实验、可完成氯气与钠、氯气与氢气的实验,可彻底控制或消除化学反应污染,实现化学反应绿色化;4.可依次连续完成氢气的性质实验;5.可依次连续完成二氧化碳气体的化学性质实验;6.可完成分子在不停地运动的实验;二、荣多反应器的组成:荣多反应器是一个整体化学反应平台,属于化学反应仪器;它由底部开有孔的三口集气瓶和底部开有孔侧面带支管的反应杯熔接在一起形成的反应器、乳胶管、止水夹、玻璃弯管、t形管、漏斗、烧杯、配件包组成;图1是它的简易示意图;图中:底部开有孔的三口集气瓶和底部开有孔侧面带支管的反应杯通过底孔紧紧熔接在一起形成
了一个大容器里粘上一个可与外界相通的小容器的反应器,通过导管(一般将橡胶塞、玻璃管、乳胶管连接在一起的组合简称为导管)可实现液体物质的进入、流出;若是高温液体物质的进入、流出则能把热传导给与反应器配合使用的带三脚的不锈钢平台,从而给反应器内带三脚的不锈钢平台上需要加热的固体物质加热;在这里,需要加热的固体物质限于白磷和钠;三口集气瓶的设计是为了方便气体的收集,不管要收集的气体的密度是大于空气还是小于空气,由于三口集气瓶两边导管中玻璃弯管长度的不同,都可收集,只是收集时,密度大的气体与密度小的气体从导管进入的方向不同罢了;反应杯上的支管的设计是为了让液体物质可进入和流出,这解决了反应杯体积小有可能导致液体反应物量的不足问题,通过液体物质的不断进入和流出也避免了反应一段时间后液体反应物变少或变稀而使反应变慢产生的气体变少的问题;还解决了如何给带三脚的不锈钢平台上需要加热的固体物质加热的问题;三、配件包里的仪器组合有:1.仪器组合1——带三脚的不锈钢平台;它是用不锈钢材料按设计图样焊接而成;不锈钢材料多种多样,氯气的化学性质非常活泼,能与很多金属发生反应,只是金属活动性不同,金属与氯气发生反应的条件不同;所以,焊接前要经过实验证实所用材料在本实验条件下不与氯气发生反应;另外,为了避免不必要的腐蚀,在做完实验后,要将带三脚的不锈钢平台从液体中拿出来洗净晾干,以备下次使用;若发现它已经有腐蚀了,应更换新的;图2是它的简易示意图;2.仪器组合2——底侧面钻有孔,孔内有细线通过,瓶口塞有带液封装置的集气瓶;注意:液封装置内的液体或固态糊状物应选择不能溶解二氧化氮也不能与二氧化氮发生化学反应的液体或固态糊状物;液封装置是用中空的双壁大试管套上短试管制成的,液封装置的作用是阻止气体逸出;拉细线(细线最好用钓鱼丝,它是透明的,不影响实验现象的观察),短试管位置上升,液封解除,气体通道被打开,气体就能从下面的集气瓶扩散进入上面的集气瓶;图3是它的简易示意图;3.仪器组合3——塞有大玻璃管(此玻璃管的下端用涂有凡士林的塑料帽密封)的橡胶塞;塑料帽的作用相当于橡胶塞,起到防止气体外逸的作用,但它的另一个作用更好,那就是:在氢气能在氯气中燃烧的实验中,它能被仪器组合5中的尖嘴弯管轻易挤掉,让氢气能与氯气接触而燃烧;图4是它的简易示意图;4.仪器组合4——底侧面带导管的细口瓶;通过改变底侧面带导管的细口瓶的位置高低能让其中的液体流出或流进;它的作用有两个,一个是:通过选择合适的液体可彻底控制或消除化学反应污染,实现化学反应绿色化;另一个是:液体流出或流进能改变所流出或流进的容器内部的压强,控制容器内气体的流向;图5是它的简易示意图;5.仪器组合5——带尖嘴弯管的橡胶塞;弯管尖嘴化的设计是为了方便氢气的燃烧,橡胶塞能起到防止氯气、氯化氢等气体外逸的作用;在氢气能在氯气中燃烧的实验中,实际使用时,它是先挤掉塑料帽打开通道后又用所带的橡胶塞堵住通道;图6是它的简易示意图;6.仪器组合6——带燃烧匙的大橡胶塞;大橡胶塞的作用是防止燃烧匙中的物质燃烧生成的有害气体外逸污染空气;图7是它的简易示意图;7.仪器组合7——洗气瓶;它的作用是通过洗气瓶内所装的液体来吸收特定的气体而让其它的气体通过;图8是它的简易示意图;
8.仪器组合8——氢气与空气中氧气反应的实验装置;它是在一个水槽的底部紧紧粘贴两个打有多个孔的广口瓶,这些孔用带导管的橡胶塞连接,导管上有止水夹,不同位置上的止水夹各自有不同的用途,通过打开或紧闭这些止水夹可控制不同实验的进行;广口瓶的瓶口连接活塞,左边的活塞上连接不锈钢小针管,针管的口径不能太小也不能太大,合适口径的针管才能保证氢气燃烧时出现淡蓝色火焰(在实际使用中,10g不锈钢针管效果最好,它的针管管嘴内径是2.70
±
0.02mm,管身外径是3.43
±
0.02mm);右边的活塞上连接底部钻有三个孔的透明杯,这三个孔,一个用于与活塞相连,一个用于通空气,另一个用于固定电子点火装置,透明杯上可套上塑料罩,点火时,氢气与空气的混合气体发生爆炸,塑料罩炸飞;水槽外连接一个底侧面带导管的细口瓶,通过改变底侧面带导管的细口瓶的位置高低能让其中的水流出或流进;它的作用是:水流进能增大广口瓶内部的压强,把氢气从广口瓶经过活塞压向套有塑料罩的透明杯,使氢气与透明杯内的空气混合,同时,流进的水封住活塞的下端口,这样,点火,氢气爆炸时整个装置更安全;图9是它的简易示意图;四、荣多反应器和配件包里不同的仪器组合配合使用,再应用一些适当的技术可实现不同的功能:1. 利用把二氧化锰粉末变成块状固体的技术,可实现制取氧气并完成氧气的化学性质实验的功能:在荣多反应器内放入配件包里的仪器组合1——带三脚的不锈钢平台;在此平台上放入熔粘上二氧化锰的塑料块(把二氧化锰粉末变成块状固体的技术是:将塑料棍或块加热至其开始熔化时马上拿开并快速插入二氧化锰粉末中,扭动,冷却后,二氧化锰就紧紧熔粘在塑料棍或块上了,这时,再按需要剪成合适大小的块状就行了;若担心熔粘上二氧化锰的塑料块会堵住反应杯的底孔,可把塑料块适当做大块一点,也可在反应杯的底孔上预先放一块有小孔的塑料板之后再放熔粘上二氧化锰的塑料块,这样就不会堵住反应杯的底孔了),再往漏斗中倒入30%的过氧化氢溶液,过氧化氢在二氧化锰的催化下马上分解放出氧气,此时就可做氧气的化学性质实验了;注意:此处不能使用稀的过氧化氢溶液,因为塑料块上附着的二氧化锰的量有限,另外,反应器内的反应杯体积也小,不能放入大量的附着有二氧化锰的塑料块;所以,为保证能快速得到大量氧气,应使用浓的过氧化氢溶液;浓的过氧化氢溶液不断从漏斗中补充进入,稀的过氧化氢溶液不断从反应杯的支管流出,保证了反应物过氧化氢的充足,二氧化锰只做催化剂质量没有损失,从而保证了氧气的大量及时产生;图10就是氧气的化学性质之一,细铁丝在氧气中燃烧的示意图;图11就是氧气的化学性质之一,木炭在氧气中燃烧的示意图;图12就是木碳燃烧后,提升细口瓶的位置,氢氧化钠溶液流入吸收生成的二氧化碳,实现实验尾气排放低碳化的示意图;图13就是氧气的化学性质之一,硫在氧气中燃烧的示意图;图14就是硫燃烧后,提升细口瓶的位置,氢氧化钠溶液流入吸收燃烧生成的二氧化硫,消除二氧化硫对空气污染的示意图;图15就是氧气的化学性质之一,红磷在氧气中燃烧的示意图;图16就是红磷燃烧完后,提升细口瓶的位置,氢氧化钠溶液流入吸收燃烧生成的五氧化二磷,消除五氧化二磷对空气污染的示意图;图17就是氧气的化学性质之一,蜡烛在氧气中燃烧的示意图;图18就是蜡烛燃烧后,提升细口瓶的位置,氢氧化钠溶液流入吸收生成的二氧化碳,实现实验尾气排放低碳化的示意图;2. 利用大橡胶塞内带液封装置的技术,可实现制取二氧化氮并完成二氧化氮气体的扩散实验的功能:
在荣多反应器的反应杯内放入金属铜片,在荣多反应器的瓶口处连接上配件包上的仪器组合2——底侧面钻有孔,孔内有细线通过,瓶口塞有带液封装置的集气瓶;再往漏斗中倒入浓硝酸,铜与浓硝酸马上反应产生二氧化氮气体,图19就是此时的示意图;待荣多反应器内充满了二氧化氮气体时,停止倒入浓硝酸,待放掉反应液后,把导管上的止水夹和反应杯支管上的止水夹都夹紧,此时,铜与浓硝酸不接触,反应停止,三口集气瓶内充满了红棕色的二氧化氮气体,而上面的集气瓶还是空的,是无色的,对比很明显;拉细线,集气瓶瓶口处的液封装置被打开,可看到二氧化氮气体慢慢从下面的三口集气瓶扩散到上面的集气瓶;图20就是二氧化氮气体的扩散实验的示意图;图21是二氧化氮气体扩散实验完成后,提升细口瓶的位置,氢氧化钠溶液流入吸收二氧化氮气体以免二氧化氮气体逸出造成空气污染的示意图;在以上丙个实验中,荣多反应器既是很好的气体制取装置又是很好的气体收集装置,真正实现了气体制取装置和气体收集装置的合二为一;3. 利用带三脚的不锈钢平台给块状固体加热的技术,可实现收集氯气并完成氯气与钠反应、氯气与氢气反应的实验功能:
①
氯气与钠反应:在荣多反应器内放入配件包中的仪器组合1——带三脚的不锈钢平台;在此平台上放入黄豆粒大小的金属钠,橡胶塞塞紧瓶口,用此荣多反应器收集满氯气后,在其右边的导气管上连接配件包中的仪器组合4——底侧面带导管的细口瓶,图22就是用荣多反应器收集满氯气的示意图;因为温度没有达到钠的着火点,此时,钠与氯气接触也不会燃烧;再往漏斗中倒入热水,热水浸没带三脚的不锈钢平台下端,将热传递给它,使其温度升高,从而使在其上的金属钠温度也升高,随着热水不断地从漏斗加入又从反应杯的支管流出,金属钠的温度越来越高,钠表面熔化的越来越多,当达到着火点时,钠在氯气中燃烧起来(钠的熔点为97.81℃,开水的温度随当地大气压的不同而不同,温度小于等于100℃;为使实验成功,应尽可能使用刚烧开的水,热水要不断地从漏斗加入;所使用的热水温度越高等待钠燃烧的时间就越短);图23就是荣多反应器内带三脚的不锈钢平台上的钠在氯气中燃烧的示意图;图24就是钠在氯气中燃烧完后,提升细口瓶的位置,氢氧化钠溶液流入,吸收多余的氯气以免氯气逸出造成空气污染的示意图;
②
氯气与氢气反应:在荣多反应器的瓶口处连接上配件包上的仪器组合3——塞有大玻璃管(此玻璃管的下端用涂有凡士林的塑料帽密封)的橡胶塞;用此荣多反应器收集满氯气,图25就是用荣多反应器收集满氯气的示意图;图26就是收集满氯气后,连接好吸收氯化氢的装置示意图;点燃已经验纯的氢气,并将通氢气的配件包上的仪器组合5——带尖嘴弯管的橡胶塞塞入仪器组合3的大玻璃管内,挤掉玻璃管下端用于密封的涂有凡士林的塑料帽,此时氢气在氯气中继续燃烧,图27就是氢气在氯气中继续燃烧的示意图;生成的氯化氢气体可被氢氧化钠溶液吸收,不用担心氢气在氯气中继续燃烧时发生爆炸,也不用担心多余的氯气或生成的氯化氢气体逸出造成空气污染;4. 利用带三脚的不锈钢平台给块状固体加热的技术,可实现探究物质燃烧条件的实验功能:在荣多反应器内放入配件包中的仪器组合1——带三脚的不锈钢平台;在此平台上放入黄豆粒大小的白磷,大橡胶塞塞紧瓶口,右边的导管上连接配件包上的仪器组合4——底侧面带导管的细口瓶,此时,白磷与空气中的氧气接触,但温度没有达到白磷的着火点,白磷没有燃烧,图28就是将白磷放在带三脚的不锈钢平台上并连接底侧面带导管的细口瓶的
示意图;往漏斗中倒入热水,热水浸没带三脚的不锈钢平台下端,将热传递给它,使其温度升高,从而使在其上的白磷温度也升高,当达到着火点时,白磷在空气中燃烧起来,图29就是荣多反应器内带三脚的不锈钢平台上的白磷在空气中燃烧的示意图;图30就是白磷燃烧完后,提升细口瓶的位置,氢氧化钠溶液流入吸收生成的五氧化二磷以免五氧化二磷逸出造成空气污染的示意图;5.可实现制取氢气并完成氢气的性质实验的功能:
①
纯净的氢气在空气中安静燃烧的实验:在荣多反应器的反应杯内放入锌粒(若担心锌粒太小或发生反应后锌粒变小会堵住反应杯的底孔,可在反应杯的底孔上预先放一块有小孔的塑料板之后再放锌粒,这样就不会堵住反应杯的底孔了),用橡胶塞塞紧瓶口,在右边的导管上连接好配件包上的仪器组合8——氢气与空气中氧气反应的实验装置;往水槽里加约三分之一的水,夹好c止水夹,打开连通a活塞的橡胶塞,往广口瓶内注满水后再塞紧橡胶塞,再往漏斗中倒入稀盐酸或稀硫酸,锌与稀盐酸或稀硫酸马上反应产生氢气,验纯氢气后,打开b和c止水夹,氢气进入广口瓶中排出水,打开a活塞,点火,就可看到小针管口处氢气在安静燃烧,产生淡蓝色火焰;在火焰上方罩一个干燥的小烧杯,烧杯内壁有小水珠出现;若要停止实验,关闭a活塞或夹紧b止水夹放开a、d止水夹,氢气停止进入,氢气的燃烧马上就会停止;图31就是连接好氢气与空气中氧气反应的实验装置后,氢气在安静燃烧的实验示意图;不用产生氢气时,只要停止倒入稀盐酸或稀硫酸,待放掉反应液后,把导管上的止水夹和反应杯支管上的止水夹都夹紧,此时,锌与稀盐酸或稀硫酸不接触,反应即停止,跟气体发生器制取气体一样方便;
②
不纯净的氢气点燃爆炸:在荣多反应器的反应杯内放入锌粒(若担心锌粒太小或发生反应后锌粒变小会堵住反应杯的底孔,可在反应杯的底孔上预先放一块有小孔的塑料板之后再放锌粒,这样就不会堵住反应杯的底孔了),用橡胶塞塞紧瓶口,在右边的导管上连接好配件包上的仪器组合8——氢气与空气中氧气反应的实验装置;往水槽里加约三分之一的水,夹好d止水夹,打开连通b活塞的橡胶塞,往广口瓶内注满水后再塞紧橡胶塞,再往漏斗中倒入稀盐酸或稀硫酸,锌与稀盐酸或稀硫酸马上反应产生氢气,夹紧b和c止水夹,打开a和d止水夹,氢气进入广口瓶中排出水,当广口瓶中氢气的体积达到一定量后,打开b活塞,提升底侧面带导管的细口瓶的位置,细口瓶内的水进入,将氢气经b活塞压往透明杯并与那里的空气混合,按动电子点火开关,氢气爆炸,一声巨响,塑料罩炸飞;若要再做一次氢气的爆炸实验,就要打开b和c止水夹,夹紧 a和d止水夹,往透明杯上套一个新的塑料罩,关闭b活塞,降低底侧面带导管的细口瓶的位置,往细口瓶中补加好水,打开连通b活塞的橡胶塞,往广口瓶内注满水后再塞紧橡胶塞,再往漏斗中倒入稀盐酸或稀硫酸,锌与稀盐酸或稀硫酸马上反应产生氢气,打开a和d止水夹,夹紧b和c止水夹,氢气进入广口瓶中排出水,当氢气的体积达到一定量后,打开b活塞,提升底侧面带导管的细口瓶的位置,细口瓶内的水进入,将氢气经b活塞压往透明杯并与那里的空气混合,按动电子点火开关,氢气爆炸,一声巨响,塑料罩炸飞;若要停止实验,关闭b活塞或夹紧a止水夹放开b止水夹,氢气停止进入,就不能做氢气的爆炸实验了;图32就是氢气的性质实验,氢气与空气混合点燃爆炸的示意图;在上面的实验中,氢气的燃烧和氢气的爆炸实验都可反复进行,解决了过去做氢气的燃烧和氢气的爆炸实验时没有专门的实验仪器,每次实验都需要临时拚凑组合仪器才能做实验的问题;
6.可实现制取二氧化碳气体并完成二氧化碳气体化学性质实验的功能:
①
二氧化碳的制取和二氧化碳与水的反应:在荣多反应器的反应杯内放入大理石或石灰石(若担心大理石或石灰石颗粒太小或发生反应后大理石或石灰石颗粒变小会堵住反应杯的底孔,可在反应杯的底孔上预先放一块有小孔的塑料板之后再放大理石或石灰石颗粒,这样就不会堵住反应杯的底孔了),用橡胶塞塞紧瓶口,再往漏斗中倒入稀盐酸,大理石或石灰石与稀盐酸马上反应产生二氧化碳气体;不用产生二氧化碳气体时,只要停止倒入稀盐酸,待放掉反应液后,把t形管上的止水夹和反应杯支管上的止水夹都夹紧,此时,大理石或石灰石与稀盐酸不接触,反应即停止,跟气体发生器制取气体一样方便;在荣多反应器的导管上连接上二个内部分别放有一朵用滤纸自制的花的塑料瓶,其中一朵花喷有紫色石蕊试液,另一朵花则干燥没有喷紫色石蕊试液,通二氧化碳后,可看到喷有紫色石蕊试液的花变红,而干燥没有喷紫色石蕊试液的花则无变化,这证明二氧化碳能与水反应;图33就是二氧化碳与水反应的性质实验示意图;
②
二氧化碳与碱的反应:在荣多反应器的导管上连接好两组塑料软瓶,图34就是在荣多反应器的导管上用t形管连接好两组塑料软瓶并在有缺口的塑料软瓶中收集二氧化碳气体的示意图,反应杯内放入大理石或石灰石,用橡胶塞塞紧瓶口,再往漏斗中倒入稀盐酸,大理石或石灰石与稀盐酸马上反应产生二氧化碳气体;待两个空塑料软瓶收集满二氧化碳气体后,取出导管,用透明胶封往两个空塑料软瓶上的缺口,图35就是用透明胶密封缺口的示意图;图36就是打开止水夹,氢氧化钠和水分别流入塑料软瓶后,再夹紧止水夹,观察倒入有水的塑料软瓶和倒入有氢氧化钠溶液的塑料软瓶变瘪的程度是否相同的示意图;通过此实验可证明二氧化碳能与碱溶液反应;
③
二氧化碳与澄清石灰水的反应:在荣多反应器的导管上连接两个装有澄清石灰水的相同的烧杯,在反应杯内放入大理石或石灰石,用橡胶塞塞紧瓶口,再往漏斗中倒入稀盐酸,大理石或石灰石与稀盐酸马上反应产生二氧化碳气体,通过控制止水夹,先让二氧化碳短时间通入左边的烧杯,结果烧杯内的澄清石灰水变浑浊了;停止向左边的烧杯通入二氧化碳,让二氧化碳较长时间通入右边的烧杯,结果右边烧杯内的澄清石灰水先变浑浊后来又变澄清了;图37就是二氧化碳与澄清石灰水反应时间长短不同的对比实验示意图;通过此实验说明,二氧化碳能与澄清石灰水反应生成碳酸钙沉淀,若二氧化碳过量,则生成的碳酸钙沉淀能与二氧化碳、水反应生成碳酸氢钙,沉淀消失;
④
制取二氧化碳使用浓盐酸和稀盐酸有什么不同的对比实验:在荣多反应器的导管上连接四个洗气瓶,四个洗气瓶两两为一组,用乳胶管连接起来,通过止水夹控制二氧化碳的通入;首先看看用稀盐酸制取二氧化碳的结果:在反应杯内放入大理石或石灰石,用橡胶塞塞紧瓶口,再往漏斗中倒入稀盐酸,大理石或石灰石与稀盐酸马上反应产生二氧化碳气体,通过控制止水夹,先让气体通入左边的一组洗气瓶,结果第二个洗气瓶内装的澄清石灰水变浑浊了,第一个洗气瓶内装的硝酸银溶液无变化;然后再来看看用浓盐酸制取二氧化碳的结果:停止倒入稀盐酸,打开t形管下乳胶管上的止水夹,放掉反应液之后再夹好止水夹,这样,稀盐酸与大理石或石灰石就不接触,反应自然停止了,然后往漏斗中倒入浓盐酸,大理石或石灰石与浓盐酸马上反应产生二氧化碳气体,通过控制止水夹,让气体通入右边的一组洗气瓶,结果第三个洗气瓶内装的澄清石灰水无变化,第四个洗气瓶内装的硝酸银溶液变浑浊了;图38就是用浓盐酸、稀盐酸分别和大理石反应制取二氧化碳的对比实验示意
图;通过这个实验可证明为什么制取二氧化碳气体要用稀盐酸而不用浓盐酸;以上四个对比实验也顺利地验证二氧化碳的化学性质,还梳理了二氧化碳的制取及复分解反应的相关知识,一举多得;因此,将利用荣多反应器可实现制取二氧化碳气体并完成二氧化碳气体化学性质实验的功能引入综合复习阶段,学生会看到不同的实验,通过实验现象对比加深对所学知识的理解和应用,会起到良好的效果;7.可实现制取硫化氢气体的功能:在荣多反应器的反应杯内放入块状硫化亚铁固体(若担心块状硫化亚铁固体太小或发生反应后块状硫化亚铁固体颗粒变小会堵住反应杯的底孔,可在反应杯的底孔上预先放一块有小孔的塑料板之后再放块状硫化亚铁固体,这样就不会堵住反应杯的底孔了),用橡胶塞塞紧瓶口,再往漏斗中倒入稀盐酸,块状硫化亚铁固体与稀盐酸马上反应产生硫化氢气体;不用产生硫化氢气体时,只要停止倒入稀盐酸,待放掉反应液后,把t形管下乳胶管上的止水夹和反应杯支管上的止水夹都夹紧,此时,块状硫化亚铁固体与稀盐酸不接触,反应即停止,跟气体发生器制取气体一样方便;制取硫化氢气体和制取二氧化碳气体一模一样,只是所用的药品不同而已;事实上,一切块状固体与液体之间不需要加热就能发生反应而产生的气体都可用荣多反应器来制取;二氧化锰是粉末不是块状固体,但我有办法通过简单的手段把二氧化锰粉末变成块状固体,因此,过氧化氢溶液用二氧化锰做催化剂制取氧气的反应也可用荣多反应器;8.可用于验证分子在不停地运动的实验:
①
用无色的酚酞溶液和浓氨水做实验:在荣多反应器的反应杯外三口集气瓶内的空间滴入几滴无色的酚酞溶液,用橡胶塞塞紧瓶口,再往漏斗中倒入少量浓氨水,夹好各处的止水夹,不一会,无色的酚酞溶液变红,这实验现象说明氨分子在不停地运动;
②
用浓盐酸和浓氨水做实验:在荣多反应器的反应杯外三口集气瓶内的空间滴入几滴浓盐酸,用橡胶塞塞紧瓶口,再往漏斗中倒入少量浓氨水,夹好各处的止水夹,不一会,荣多反应器内白烟滚滚,这实验现象说明分子在不停地运动;五、附图说明:图1:是荣多反应器的简易介绍示意图;图2:是带三脚的不锈钢平台的简易示意图;图3:是底侧面钻有孔,孔内有细线通过,瓶口塞有带液封装置的集气瓶的简易示意图;图4:是塞有大玻璃管(此玻璃管的下端用涂有凡士林的塑料帽密封)的橡胶塞的示意图;图5:是底侧面带导管的细口瓶的简易示意图;图6: 是带尖嘴弯管的橡胶塞的简易示意图;图7: 是带燃烧匙的大橡胶塞的简易示意图;图8: 是洗气瓶的简易示意图;图9: 是氢气与空气中氧气反应的实验装置的简易介绍示意图;图10:是细铁丝在氧气中燃烧的示意图;图11:是木炭在氧气中燃烧的示意图;图12:是木碳燃烧后,提升细口瓶的位置,氢氧化钠溶液流入吸收生成的二氧化碳,实现实验尾气排放低碳化的示意图;图13:是硫在氧气中燃烧的示意图;
图14:是硫燃烧后,提升细口瓶的位置,氢氧化钠溶液流入吸收燃烧生成的二氧化硫,消除二氧化硫对空气污染的示意图;图15:是红磷在氧气中燃烧的示意图;图16:是红磷燃烧完后,提升细口瓶的位置,氢氧化钠溶液流入吸收燃烧生成的五氧化二磷,消除五氧化二磷对空气污染的示意图;图17:是蜡烛在氧气中燃烧的示意图;图18:是蜡烛燃烧后,提升细口瓶的位置,氢氧化钠溶液流入吸收生成的二氧化碳,实现实验尾气排放低碳化的示意图;图19: 是往漏斗中倒入浓硝酸,铜与浓硝酸马上反应产生二氧化氮气体的示意图;图20: 是拉细线,集气瓶瓶口处的液封装置被打开,二氧化氮气体慢慢从下面的三口集气瓶扩散到上面的集气瓶的示意图;图21: 是二氧化氮气体扩散实验完成后,提升细口瓶的位置,氢氧化钠溶液流入吸收二氧化氮气体以免二氧化氮气体逸出造成空气污染的示意图;图22: 是在带三脚的不锈钢平台上放好黄豆粒大小的金属钠并收集满氯气的示意图;图23: 是荣多反应器内带三脚的不锈钢平台上的钠在氯气中燃烧的示意图;图24: 是钠在氯气中燃烧完后,提升细口瓶的位置,氢氧化钠溶液流入,吸收多余的氯气以免氯气逸出造成空气污染的示意图;图25: 是在荣多反应器的瓶口处连接上塞有大玻璃管(此玻璃管的下端用涂有凡士林的塑料帽密封)的橡胶塞,并用此荣多反应器收集满氯气的示意图;图26: 是收集满氯气后,连接好吸收氯化氢的装置示意图;图27: 是氢气在氯气中继续燃烧,反应剩余的氯气、生成的氯化氢气体可被氢氧化钠溶液吸收不会造成空气污染的示意图;图28:是将白磷放在带三脚的不锈钢平台上并在荣多反应器上连接底侧面带导管的细口瓶的示意图;图29:是荣多反应器内带三脚的不锈钢平台上的白磷在空气中燃烧的示意图;图30:是白磷燃烧完后,提升细口瓶的位置,氢氧化钠溶液流入吸收生成的五氧化二磷以免五氧化二磷逸出造成空气污染的示意图;图31: 是连接好氢气与空气中氧气反应的实验装置后,氢气在安静燃烧的实验示意图;图32: 是连接好氢气与空气中氧气反应的实验装置后,氢气与空气混合点燃爆炸的示意图;图33: 是用自制纸花验证二氧化碳与水是否反应的实验示意图;图34:是在荣多反应器的导管上用t形管连接好两组塑料软瓶并在有缺口的塑料软瓶中收集二氧化碳气体的示意图;图35:是用透明胶密封塑料软瓶缺口的示意图;图36:是观察倒入有水的塑料软瓶和倒入有氢氧化钠溶液的塑料软瓶变瘪的程度是否相同的示意图;图37:是二氧化碳与澄清石灰水反应时间长短不同的对比实验示意图;图38:是用浓盐酸、稀盐酸分别和大理石反应制取二氧化碳的对比实验示意图。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1