一种磁性MgO吸附剂及其制备方法和应用
一种磁性mgo吸附剂及其制备方法和应用
技术领域
1.本发明涉及吸附材料技术领域,特别涉及一种磁性mgo吸附剂及其制备方法和应用。
背景技术:
2.我国具有丰富的地热资源,几乎在每个省份均有地热资源的分布。高温地热带常分布在我国西藏和云南两地。据报道,西藏储层温度高于150℃的水热系统有129处,其中储层温度高于200℃的有12处。地热水作为一种廉价、清洁、丰富的新型能源和宝贵水资源,其开发和应用已受到国家和地方的大力支持与发展。
3.地热水中常含有高浓度的氟、砷等有害物质,以羊八井热田为例,水体中总砷的浓度高达5.7mg/l,氟离子浓度高达18mg/l,远远高于地表水环境质量标准(gb2828-2002)和生活饮用水水质标准(gb5749-2006)中对氟和砷的限量规定。直接将地热水尾水排入到受纳水体中,不仅会造成流域生态环境的影响,而且会对生物体和人类带来不利的影响。因此,解决地热水除氟、砷问题迫在眉睫,地热水的处理以实现安全排放对生态环境保护具有重要的意义。
4.目前,地热水中氟、砷离子的去除主要采用吸附剂吸附的方式,常见的吸附剂为氧化物吸附剂,主要有mgo、fe2o3、al2o3和tio2等,然而,这些氧化物吸附剂的吸附效果不佳,以商品化的mgo举例,其对氟的吸附效率仅有66%,吸附以后的氟剩余浓度不能满足地表水和饮用水中氟的限量标准。
技术实现要素:
5.有鉴于此,本发明目的在于提供一种磁性mgo吸附剂及其制备方法和应用,本发明提供的磁性mgo吸附剂能够有效去除水中的氟、砷离子。
6.为了实现上述发明目的,本发明提供以下技术方案:
7.本发明提供了一种磁性mgo吸附剂的制备方法,包括以下步骤:
8.将可溶性三价铁源、柠檬酸镁和水混合,加热蒸发,得到前驱体混合物;
9.对所述驱体混合物进行煅烧,得到磁性mgo吸附剂。
10.优选的,所述可溶性三价铁源为fecl3、fe(no3)3和fe2(so4)3中的一种或几种。
11.优选的,所述前驱体溶液中fe离子、mg离子的摩尔比为1:1~5。
12.优选的,所述加热蒸发的温度为60~90℃。
13.优选的,所述煅烧的温度为600~800℃,保温时间为1~5h。
14.本发明提供了上述制备方法制备得到的磁性mgo吸附剂,成分包括mgo和fe3o4。
15.优选的,所述磁性mgo吸附剂的bjh孔径分布为3.062~20nm,比表面积为8.81~28.07m2/g,孔体积为0.115~0.234cm3/g。
16.本发明提供了上述磁性mgo吸附剂在水处理中的应用,所述水中含有氟离子和/或砷离子。
17.优选的,所述水为地热水。
18.优选的,所述应用的方法包括以下步骤:
19.调节待处理水的ph值为2~11,加入磁性mgo吸附剂,在加热条件下进行吸附。
20.本发明提供了一种磁性mgo吸附剂的制备方法,包括以下步骤:将可溶性三价铁源、柠檬酸镁和水混合,加热蒸发,得到前驱体混合物;对所述前驱体混合物进行煅烧,得到磁性mgo吸附剂。柠檬酸根在煅烧的过程中起到造孔剂作用,高温煅烧过程中能形成多孔mgo和fe3o4,即fe3o4@mgo,此磁性吸附剂用于水处理时能够水解形成mg(oh)2,与f-和as(v)发生离子交换吸附,从而去除水中的氟、砷离子。在煅烧的过程中,磁性mgo吸附剂能够形成微孔结构,bjh孔径分布在3.062~20nm范围,比表面积为8.81~28.07m2/g,孔体积为0.115~0.234cm3/g,增大氟、砷离子的吸附容量。同时,由于磁性mgo吸附剂中含有fe3o4,便于吸附剂从水中的磁分离去除。实施例结果表明,本发明提供的磁性mgo吸附剂对f的吸附率为99.9%,对as(v)的吸附率为99.9%,对f和as(v)的吸附容量分别为98.4mg/g和123mg/g。
21.同时,本发明提供的磁性mgo吸附剂具有ph值适应性强的优势,在ph值2~11的范围内可以分别实现f和as(v)99.9%和98.7%的吸附效率;本发明提供的磁性mgo吸附剂具有吸附速度快的优势,对as(v)表现出极快速动力学,在2min内就能实现96.1%的吸附,反应到10min以后,可以实现99.9%吸附;对氟而言,120min后浓度即低于限量标准值1mg/l。
附图说明
22.图1是本发明的吸附剂fe3o4@mgo的制备及其去除地热水中氟和砷的流程示意图;
23.图2是不同fe/mg摩尔比对f离子吸附效果的影响;
24.图3是不同煅烧温度对f离子吸附效果的影响;
25.图4是不同fe/mg摩尔比吸附剂的磁强度表征图;
26.图5是fe/mg比为1/5的fe3o4@mgo的透射电镜微观图;
27.图6是水处理前后fe3o4@mgo的xrd图;
28.图7为fe3o4@mgo及其他氧化物对f离子吸附效果比较;
29.图8为不同ph值对氟的吸附效果影响;
30.图9为不同ph值对砷的吸附效果影响
31.图10为不同吸附时间下氟的吸附效率;
32.图11为不同吸附时间下砷的吸附效率;
33.图12为fe3o4@mgo对f和as(v)的吸附动力学拟合结果;
34.图13为不同起始浓度下fe3o4@mgo对f和as(v)的吸附容量
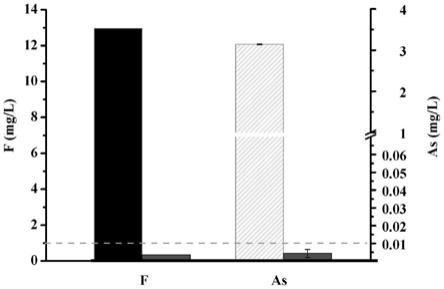
35.图14为fe3o4@mgo处理地热水时吸附前后的氟和砷浓度。
具体实施方式
36.本发明提供了一种磁性mgo吸附剂的制备方法,包括以下步骤:
37.将可溶性三价铁源、柠檬酸镁和水混合,加热蒸发,得到前驱体混合物;
38.对所述前驱体混合物进行煅烧,得到磁性mgo吸附剂。
39.本发明将可溶性三价铁源、柠檬酸镁和水混合,加热蒸发,得到前驱体混合物。在本发明中,所述可溶性三价铁源优选为fecl3、fe(no3)3和fe2(so4)3中的一种或几种。
40.在本发明中,所述柠檬酸镁优选为九水柠檬酸镁。
41.在本发明中,所述可溶性三价铁源、柠檬酸镁中,fe、mg的摩尔比优选为1:1~5,优选为1:3。
42.在本发明中,所述柠檬酸镁与水的质量比优选为1:20。
43.在本发明中,所述混合的方式优选为搅拌混合。在本发明中,所述加热蒸发的温度优选为60~90℃,更优选为70~80℃;本发明对所述加热蒸发的温度没有特殊的要求,能够将混合液中的水分蒸干即可。在本发明中,所述加热蒸发优选在搅拌、水浴的条件下进行。在所述加热蒸发的过程中,柠檬酸镁得到所述前驱体混合物后,本发明对所述前驱体混合物进行煅烧,得到磁性mgo吸附剂。本发明优选在马弗炉中进行所述煅烧。在本发明中,所述煅烧的气氛优选为空气。
44.在本发明中,所述煅烧的温度优选为600~800℃,更优选为700℃;保温时间优选为1~5h,更优选为2~4h。在本发明中,升温至所述煅烧温度的升温速率优选为5℃/min。
45.在本发明中,所述煅烧的过程中,前驱体混合物中的fe离子、mg离子形成mgo、fe3o4复合物,即fe3o4@mgo,此复合物具有微孔结构。
46.在本发明中,所述煅烧后,本发明优选对所得煅烧产物进行洗涤和干燥,以去除杂质成分。在本发明中,所述洗涤用洗涤剂优选为去离子水,所述洗涤的次数优选为3~5次。在本发明中,所述干燥的方式优选为烘干。
47.本发明提了上述制备方法制备得到的磁性mgo吸附剂,成分包括mgo和fe3o4;在本发明中,所述磁性mgo吸附剂中mgo、fe3o4以纳米颗粒的形式团聚、复合在一起。在本发明中,所述磁性mgo吸附剂具有微孔结构,bjh孔径分布在3.062~20nm,比表面积为8.81~28.07m
2/
g,优选为28.07m
2/
g,孔体积为为0.115~0.234cm3/g,优选为0.234cm3/g。
48.本发明提供了上述磁性mgo吸附剂在水处理中的应用,所述水中含有f离子和/或as(v)离子。在本发明中,含氟、砷水中氟的浓度优选为0~20mg/l,更优选为2~15mg/l,进一步优选为5~10mg/l;砷的浓度优选为0~5mg/l,更优选为1~4mg/l,进一步优选为2~3mg/l。
49.在本发明中,所述水优选为地热水。
50.在本发明中,所述应用的方法包括以下步骤:
51.调节待处理水的ph值为2~11,加入磁性mgo吸附剂,进行吸附。
52.本发明对所述调节ph值的方式没有特殊的要求,采用本领域技术人员熟知的调节ph值的方式即可。
53.在本发明中,所述磁性mgo吸附剂的加入量优选为0.5~3g/l水,更优选为1~2g/l水。
54.在本发明中,所述吸附时水的温度优选为30~90℃,更优选为50~80℃。
55.下面结合实施例对本发明提供的磁性mgo吸附剂及其制备方法和应用进行详细的说明,但是不能把它们理解为对本发明保护范围的限定。
56.实施例1
57.将fecl3与柠檬酸镁加入到10ml水中,保持fe/mg的摩尔比分别为1/1、1/3和1/5,60~90℃条件下水浴搅拌挥发,在转移至马弗炉中煅烧1~5h,煅烧温度分别为600、700和800℃,升温速率为5℃/min,得到磁性mgo吸附剂fe3o4@mgo。
58.为了性能对比,省略fecl3的加入,制备了单一柠檬酸镁衍生的mgo材料。
59.图1是本发明的吸附剂fe3o4@mgo的制备及其去除地热水中氟和砷的流程示意图。
60.测试例1
61.分别取不同fe/mg的摩尔比的fe3o4@mgo(其煅烧温度为700℃,时间为2h)60mg,加入到30ml(固液比为2g/l)ph为7的氟离子溶液中,起始浓度为20mg/l,在80℃恒温水浴摇床以180转/分钟保持3小时,磁分离后取上清液采用离子选择性电极测定剩余f离子浓度,并计算其去除效率。所得结果见图2。由图2可以看出,随着fe/mg摩尔比从1/1增加到1/5,材料的吸附性能接近纯mgo,溶液中氟的剩余浓度满足我国饮用水限量标准(1mg/l)。
62.分别取不同煅烧温度下的fe3o4@mgo(fe/mg摩尔比为1:5,煅烧时间为700℃),按照上述方法测试对f的吸附效率。所得结果见图3。由图3可以看出,随着温度增加,材料的性能没有差异,说明600~800℃煅烧温度范围,所制备的材料对吸附性能没有影响。
63.图4是不同fe/mg摩尔比吸附剂的磁强度表征图。随着fe/mg比从1/1减小到1/5,所制备的材料磁性大小分别为20.45、11.45和8.06emu/g。因引入了mgo成分,随着mgo成分比例增强,磁强度减弱趋势越显著。以fe/mg为1/5材料为例,吸附后的溶液经5min后,能得到澄清溶液,表明本工作所制备的材料磁性能满足磁分离要求。
64.图5为fe/mg比为1/5的fe3o4@mgo的透射电镜微观图,由图5可以看出,fe3o4@mgo的粒径为100nm,粒径分布均匀。对其孔结构进行brunner-emmet-teller(bet)表征美国康塔仪器(quadrasorb si)测试,结果显示,bjh孔径分布为3.062nm,比表面积为28.07m2/g,孔体积为0.234cm3/g。
65.为了研究材料的晶型结构和fe3o4@mgo在溶液中的水解过程机理,对所制备的材料进行了xrd表征,所得结果见图6。由图6可以看出,制备的fe3o4@mgo与mgo标准pdf卡片(jcpds 45-0946)和fe3o4标准pdf卡片(jcpds 19-0629)的出峰位置完全一致。水解后的fe3o4@mgo分别在峰1、2、3、4、5和6处出现了新峰,分别对应于mg(oh)2标准卡片(jcpds 44-1482)中(001)、(101)、(102)、(110)、(103)和(201)晶面,此外,mgo峰在2=36.9、74.6和78.6
°
时峰消失,在42.9
°
和62.3
°
时峰减弱,表明在水溶液中,mgo与水发生反应生成mg(oh)2。吸附f和as后,mg(oh)2峰略有减弱。
66.测试例2
67.将fe3o4@mgo(fe/mg的摩尔比1:5)60mg加入到30ml(固液比为2g/l)ph为7的氟离子溶液中,起始浓度为20mg/l,在80℃恒温水浴摇床以180转/分钟保持3小时,磁分离后取上清液采用离子选择性电极测定剩余f离子浓度。并计算其去除效率。为了评价所制备的材料的去除性能,在同一条件下,对比了商品化的mgo和传统氧化物(fe2o3、fe3o4、al2o3、tio2)的性能。所得结果见图7。
68.由图7可以看出,本发明所制备的fe3o4@mgo对氟的吸附效率高达95%,远远高于传统氧化物(fe2o3、fe3o4、al2o3和tio2);而商品化的mgo对氟的吸附效率仅有66%,吸附以后的氟剩余浓度不能满足地表水和饮用水中氟的限量标准。而可以看出,本发明所制备的材料对高氟地热水吸附具有突出优势。
69.测试例3
70.分别考察氟和砷的起始浓度为20mg/l和5mg/l时,固液比为3g/l,fe3o4@mgo(fe/mg的摩尔比1:5)在ph 2~12范围内对氟和砷的吸附性能。
71.其中,不同ph值对氟的吸附效果影响见图8,对砷的吸附效果影响见图9。
72.由图8、9可以看出,在2~12范围内,材料对砷的吸附效率近100%。当ph升至12时,溶液中剩余砷的浓度超过饮用水中砷的限量标准,而其它ph范围内,溶液中剩余砷的浓度均低于饮用水中砷的限量标准。表明材料对as具有良好的吸附性能。ph在2~11之间,氟的去除效率约为96%,处于较高水平。当ph升高至12时,氟吸附效率降低至50%。由于碱性条件下,材料表面去质子化,并不适合负电荷的氟离子吸附。当ph在2~11之间,吸附后的溶液中氟离子浓度满足我国规定的饮用水中氟的限量标准。
73.此外,本发明制备的材料去除地热水中f和as的吸附ph范围为2~11,ph吸附范围宽,综合实际地热水ph范围为8~10,因而在实际应用中,水样可以不用调ph,可以避免调节ph的繁琐操作。
74.测试例4
75.考察氟和砷的起始浓度分别为20mg/l和5mg/l时,固液比为3g/l,fe3o4@mgo(fe/mg的摩尔比1:5)在ph 7条件下,吸附平衡时间的影响。
76.不同吸附时间下氟的吸附效率见图10,砷的吸附效率见图11。
77.由图10、11可以看出,材料对as(v)和f表现出较快的吸附动力学。对as(v)表现出极快速动力学,在2min内就能实现96.1%的去除,反应到10min以后,可以实现99.9%吸附,10min后,as的浓度低于饮用水限量标准。对氟而言,120min后浓度低于限量标准值。文献中大多报道的mgo平衡时间为30min左右,也有的材料的平衡时间长达24h。可见,本方法制备的材料对as和f具有较快的动力学,在实际应用中具有广阔前景。
78.分别用准一级和准二级动力学模型对上述吸附结果进行拟合,拟合后的数据见图12。fe3o4@mgo对f和as(v)的吸附动力学符合准二级,材料对f和as(v)的吸附是基于化学吸附。
79.测试例5
80.向一系列已知浓度的f和as(v)离子中加入fe3o4@mgo(fe/mg的摩尔比1:5),固液比为3g/l,80℃反应180min后磁分离,测定其吸附容量。
81.图13是不同起始浓度下fe3o4@mgo对f和as(v)的吸附容量,fe3o4@mgo对f和as(v)的吸附容量分别高达98.4mg/g和123mg/g。将本发明与功能化的活性炭(f:27.8;as:30.3mg/g)吸附材料相比,本方法所制备的吸附剂显著优于功能化的活性炭吸附剂,与mgo基吸附剂处于同一居高水平(f:120mg/g),具有良好的实际利用价值。
82.测试例6
83.考察所制备的fe3o4@mgo(fe/mg的摩尔比1:5)对实际地热水的去除效果。实际地热水采集于西藏羊八井,ph值为8.6,实际地热水中f和as的初始浓度分别高达12.95和3.14mg/l。30ml地热水中加入90mg所制备的吸附剂后,吸附前后的氟和砷浓度如图14所示,
84.由图14可以看出,材料可以实现地热水中f和as高达97.3%和99.9%的去除效率,吸附f和as后所剩余的浓度分别为0.35mg/l和4.4ng/ml。
85.我国规定饮用水中砷的含量<10ng/ml,氟的含量<1mg/l。因此,经本发明磁性mgo吸附剂处理后地热水中剩余的氟和砷的浓度满足我国饮用水对f和as的限量标准。
86.以上所述仅是本发明的优选实施方式,应当指出,对于本技术领域的普通技术人员来说,在不脱离本发明原理的前提下,还可以做出若干改进和润饰,这些改进和润饰也应
视为本发明的保护范围。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1