Au-MoS2-CdS复合光催化剂的制备方法
au-mos
2-cds复合光催化剂的制备方法
技术领域
1.本公开涉及纳米材料及光催化领域,具体地,涉及一种au-mos
2-cds复合光催化剂的制备方法。
背景技术:
2.利用太阳能驱动分解水,将太阳能转化为可储存和运输的氢气燃料,是缓解能源压力的理想途径之一。悬浮颗粒光催化体系能够实现太阳光的长穿透距离和载流子的短扩散路径,但存在光催化剂重复利用率低的缺点。
3.cds是一种可见光驱动光催化剂,它具有窄带隙、合适的导带位置、高效的激子生成和良好的电子亲和力等与光催化产氢相关的有益特性。目前,基于cds的复合光催化剂仍受限于其低合成产率和窄光谱响应。传统地,人们广泛研究水热法合成结晶度高的cds纳米棒(cds nrs),而水热法也存在一些缺点,如能耗高、反应周期长、合成效率低,且安全性差。化学沉淀法制备的多晶cds nrs却很少受到关注,该方法克服了水热法的一些缺点,具有反应条件温和易控制、反应周期短、收率高等优点。使用简便的cds基光催化剂合成方法实现拓宽的响应光谱和增强电荷分离是实际应用的关键问题。
4.此外,由于太阳光中仅有少于5%的紫外光组成,大范围的光捕获尤其是大范围可见光的捕获是限制实际光催化分解水的重要问题。一维金纳米棒(au nrs)具有在可见及近红外区域可调节的纵向局域表面等离激元吸收特性,为拓宽半导体的光吸收提供了新的思路。
技术实现要素:
5.有鉴于此,本公开提供了一种au-mos
2-cds复合光催化剂的制备方法,以解决上述以及其他方面的至少一种技术问题。
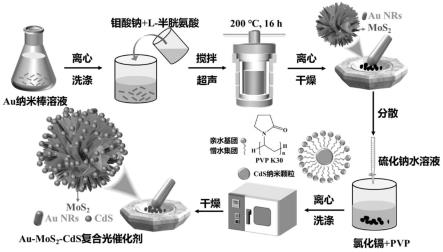
6.为了实现上述目的,本公开的一个方面,提供了一种光催化剂的制备方法,包括以下步骤:步骤s1:将硼氢化钠溶液加入氯金酸溶液还原得到纳米金溶液;步骤s2:配置金纳米棒生长溶液,加入纳米金溶液得到一定长径比的金纳米棒,离心后复溶成金纳米棒溶液待用;步骤s3:将金纳米棒溶液分散在l-半胱氨酸和钼酸钠的混合溶液中,使金纳米棒与二硫化钼(mos2)结合,经处理制得au-mos2复合粉末;步骤s4:将au-mos2分散在氯化镉和聚乙烯吡咯烷酮的混合溶液中,滴加硫化钠水溶液,持续搅拌,生成多晶cds纳米颗粒包覆在mos2外围,经处理得到au-mos
2-cds复合光催化剂。其中,au-mos
2-cds复合光催化剂中mos2在金纳米棒外层,通过au-s键实现金纳米棒与mos2紧密接触,制得au-mos2;多晶cds纳米颗粒包覆在au-mos2的mos2外围,分布均匀,au-mos
2-cds复合光催化剂整体结构呈花球状,mos2介于au-cds之间。
7.根据本公开的实施例,步骤s2中,二硫化钼带正电,采用水热法工艺包覆金纳米棒。
8.根据本公开的实施例,步骤s4中生成多晶cds纳米颗粒采用化学沉淀法。
9.根据本公开的实施例,纳米金溶液的配置过程包括:将0.6ml的10mm nabh4冰水溶液添加到0.25ml的10mm haucl4溶液与9.75ml的0.1m十六烷基三甲基溴化铵混合溶液中,快速摇动5秒钟,在25℃水浴锅中老化两小时形成纳米金溶液;
10.金纳米棒溶液的制备过程包括:在配置好的金纳米棒生长溶液中加入96μl的纳米金溶液,混合后缓慢上下颠倒10次,置于35℃水浴锅中生长金纳米棒,离心后复溶形成金纳米棒溶液;
11.优选地,金纳米棒生长溶液的组成为40ml的0.1m ctab溶液、2ml的10mm haucl4溶液、0.1-0.6ml的10mm agno3溶液、800μl的0.1mm hcl溶液和350μl的0.1m抗坏血酸。
12.根据本公开的实施例,步骤s2中:金纳米棒的长径比为2.9-3.8;离心转速为6000-10000rpm,离心时间为10-20min,得到金纳米棒原液;复溶时将1-5份金纳米棒原液复溶为20ml金纳米棒溶液。
13.根据本公开的实施例,步骤s3中,钼酸钠与l-半胱氨酸的物质的量比为1:1-1:3.5,在15ml去离子水中混合均匀,并加入20ml金纳米棒溶液。
14.根据本公开的实施例,步骤s3中,制备au-mos2采用水热法,在特氟隆内衬的水热反应釜中进行反应,反应温度为200℃,反应时间为16小时。
15.根据本公开的实施例,步骤s4中,cdcl2与na2s水溶液浓度为0.01mol/l,剂量为70~280ml,加入的au-mos2粉末质量为15-30mg,pvp的加入量为0.05-0.1g;
16.优选地,cdcl2与na2s水溶液剂量为93ml,au-mos2粉末质量为20mg,pvp的加入量为0.08g。
17.根据本公开的实施例,步骤s4中,硫化钠水溶液的滴加使用一次性输液器,滴入速度为每分钟5-10滴。
18.根据本公开的实施例,步骤s4中,得到au-mos
2-cds复合光催化剂还需要的处理过程包括:离心,离心转速为4000-6000rpm,离心时间为5-10min;洗涤,洗涤试剂选用去离子水和无水乙醇;干燥,干燥温度60-70℃,时间8-10小时;以及研磨,研磨时间至少持续10-15min,无需过筛。
19.根据本公开的上述实施例的光催化剂的制备方法,利用静电结合作用及au-s键修饰mos2及au nrs,使金纳米棒与二硫化钼紧密接触,制得au-mos2,再通过化学沉淀法制备多晶cds纳米颗粒,包覆在au-mos2的二硫化钼外围,分布均匀;所述au-mos
2-cds复合光催化剂整体结构呈花球状,mos2介于au-cds之间,形成了具有密切接触的三元复合光催化剂,实现在整个可见光区域均能够光捕获及分解水析氢。
附图说明
20.图1是本公开实施例的光催化剂的制备过程示意图;
21.图2是本公开实施例的光催化剂的制备过程流程图;
22.图3是本公开实施例的au-mos
2-cds复合光催化剂的形貌模型图;
23.图4a是本公开实施例的光催化剂的透射电镜图;
24.图4b是本公开实施例的光催化剂的mos2和cds的高分辨率透射电镜图;
25.图5是本公开实施例的金纳米棒的透射电镜图;
26.图6a是本公开实施例的光催化剂的mos2表面的zeta电位分布图;
mos
2-cds复合光催化剂。其中,au-mos
2-cds复合光催化剂中mos2在金纳米棒外层,通过au-s键实现金纳米棒与mos2紧密接触,制得au-mos2;多晶cds纳米颗粒包覆在au-mos2的mos2外围,分布均匀,au-mos
2-cds复合光催化剂整体结构呈花球状,mos2介于au-cds之间。
39.根据本公开的实施例,步骤s2中在纳米金表面选择性附着银离子控制金颗粒呈棒状生长,以制备得到具有一定长径比的金纳米棒。
40.根据本公开的实施例,步骤s2中制得的金纳米棒长径比为2.9-3.8。
41.根据本公开的实施例,步骤s2中二硫化钼带正电,呈花球状,采用水热法工艺包覆金纳米棒。
42.根据本公开的实施例,步骤s2中离心过程离心转速为9000rpm,时间15min。
43.根据本公开的实施例,步骤s3中l-半胱氨酸、钼酸钠分别作为硫源和钼源,其中l-半胱氨酸提供au-s键以增强au与mos2的紧密结合。
44.根据本公开的实施例,步骤s3中得到au-mos2复合粉末还需要的处理过程包括:洗涤,洗涤试剂选用乙醇;离心,离心转速为5000-7000rpm,离心时间为5-10min;干燥,干燥温度60-70℃,时间8-10小时;以及研磨,研磨时间至少持续10-15min,无需过筛。
45.根据本公开的实施例,步骤s4中生成多晶cds纳米颗粒采用化学沉淀法。
46.根据本公开的实施例,纳米金溶液的配置过程包括:将0.6ml的10mm nabh4冰水溶液添加到0.25ml的10mm haucl4溶液与9.75ml的0.1m十六烷基三甲基溴化铵(ctab)混合溶液中,快速摇动5秒钟,在25℃水浴锅中老化两小时形成纳米金溶液;
47.金纳米棒溶液的制备过程包括:在配置好的金纳米棒生长溶液中加入96μl的纳米金溶液,混合后缓慢上下颠倒10次,置于35℃水浴锅中生长金纳米棒,离心后复溶形成金纳米棒溶液。
48.根据本公开的实施例,金纳米棒生长溶液的组成为40ml的0.1mctab溶液、2ml的10mm haucl4溶液、0.1-0.6ml的10mm agno3溶液、800μl的0.1mm hcl溶液和350μl的0.1m抗坏血酸。
49.根据本公开的实施例,步骤s2和s3中金纳米棒的长径比为2.9-3.8,;离心过程转速为6000-10000rpm,离心时间为10-20min,得到金纳米棒原液;复溶时将1-5份金纳米棒原液复溶为20ml金纳米棒溶液。
50.在一些实施例中,金纳米棒生长溶液的组成为40ml的0.1m ctab溶液、2ml的10mm haucl4溶液、0.4ml的10mm agno3溶液、800μl的0.1mm hcl溶液和350μl的0.1m抗坏血酸,得到的金纳米棒的长径比为3.0。
51.根据本公开的实施例,复溶时优选4份金纳米棒原液进行复溶,选用磁子搅拌的方式分散处理15min,并超声处理20min。
52.根据本公开的实施例,步骤s3中钼酸钠与l-半胱氨酸的物质的量比为1:1-1:3.5,在15ml去离子水中混合均匀,并加入20ml上述复溶的金纳米棒溶液。
53.根据本公开的实施例,步骤s3中钼酸钠与l-半胱氨酸的添加量优选对应15ml去离子水分别加入1.0mmol和2.0mmol。
54.根据本公开的实施例,步骤s3中制备au-mos2采用水热法,在特氟隆内衬的水热反应釜中进行反应,反应温度为200℃,反应时间为16小时。
55.根据本公开的实施例,步骤s4中cdcl2与na2s水溶液浓度为0.01mol/l,剂量为70~
280ml,加入的au-mos2粉末质量为15-30mg,pvp的加入量为0.05-0.1g,pvp起到控制cds形貌并分散纳米颗粒的作用;
56.在一些实施例中,cdcl2与na2s水溶液剂量为93ml,au-mos2粉末质量为20mg,pvp的加入量为0.08g。
57.根据本公开的实施例,步骤s4中硫化钠水溶液的滴加使用一次性输液器缓慢滴加,滴入速度为每分钟5-10滴,优选地,滴入速度为每分钟8滴。
58.根据本公开的实施例,步骤s4中得到au-mos
2-cds复合光催化剂还需要的处理过程包括:离心,离心转速为4000-6000rpm,离心时间为5-10min;洗涤,洗涤试剂选用去离子水和无水乙醇;干燥,干燥温度60-70℃,时间8-10小时;以及研磨,研磨时间至少持续10-15min,无需过筛。
59.图3是本公开实施例的au-mos
2-cds复合光催化剂的形貌模型图。
60.如图3所示,au nrs如西瓜籽状分布在mos2的花球状结构中,多晶cds纳米颗粒包裹在mos2外廓,mos2被cds纳米颗粒充分包裹,整体呈花球状,制得的au-mos
2-cds复合光催化剂在整个可见光区域均能够实现光捕获及分解水析氢,且所得光催化剂粉末能够通过静置与水溶液完全分离。
61.图4a是本公开实施例的光催化剂的透射电镜图;图4b是本公开实施例的光催化剂的mos2和cds的高分辨率透射电镜图。
62.如图4a所示,在光催化剂的透射电镜标尺为50nm时,可以清晰看到单个花球状au-mos
2-cds复合光催化剂结构,微米花球的直径分布在300~400nm之间,其中标记处可以看到au nrs的分布及大小。
63.如图4b所示,在光催化剂的透射电镜标尺为5nm时,可以看到au-mos
2-cds复合光催化剂表面两类纳米粒子的分布,其中,可观察到mos2粒子的晶格间距为0.63nm,cds粒子的晶格间距为0.29nm。
64.如图4a和图4b结合来看,水热法制备的mos2分布在直径300~400nm之间的微米花球中,mos2少层片状结构像花瓣一样从中心向边缘伸展,构成了花球,花球边缘均是暴露的片状结构边缘,采用pvp辅助的化学沉淀法制备的多晶cds颗粒的尺寸小于10nm。pvp分子之间缔合为胶束,这时憎水的非极性基团互相吸引,包埋在胶束的内部,而亲水的极性基团则伸向水相,形成球形结构,从而得到尺寸分布均匀的cds纳米颗粒。
65.图5是本公开实施例的金纳米棒的透射电镜图。
66.如图5所示,在金纳米棒的透射电镜形貌图中,可观察到金纳米棒的平均长径比为3.0。
67.图6a是本公开实施例的光催化剂的mos2表面的zeta电位分布图;
68.图6b是本公开实施例的光催化剂的cds表面的zeta电位分布图。
69.如图6a所示,zeta电位表征结果说明分散在水溶液中的mos2颗粒表面具有+41.75mv的正zeta电位。如图6b所示,zeta电位表征结果说明分散在水溶液中的cds颗粒表面具有-14.09mv的负zeta电位。从而证实了mos2与cds之间的紧密结合得益于二者表面相反的zeta电位及静电吸引作用。
70.根据本公开的实施例,au-mos
2-cds复合光催化剂中,au、mos2和cds三者之间的紧密接触得益于au-s键与颗粒表面相反的zeta电位引起的静电相互作用,将mos2介入au与
cds之间代替原有的肖特基势垒从而促进au和cds之间的电荷传输。
71.图7是本公开实施例的光催化剂的x射线衍射图。
72.如图7所示,光催化剂的x射线衍射(xrd)测试对材料结构进行分析,以看到制得的au nrs结晶性良好,衍射峰比较尖锐,而mos2与cds由于特殊的花球形貌和较小的尺寸,衍射峰发生宽化,进一步证明了cds纳米颗粒的多晶状态。
73.图8是本公开实施例的光催化剂在波长》420nm入射光下的析氢曲线图。
74.如图8所示,制得的au-mos
2-cds复合光催化剂粉末分散在100ml0.3m的na2s与0.3m的na2so3的混合溶液中,在可见光下测试其析氢性能,测试时的光功率为300mw/cm2,从析氢曲线得该au-mos
2-cds复合光催化剂表现出2.38mmol/g/h的析氢效率。
75.图9是本公开实施例的光催化剂在各单色光下的表观量子产率曲线图。
76.如图9所示,实验过程中使用滤光片只透过单色光,即相对窄范围的波长范围光。单色光下的表观量子产率(aqy)证实了上述au-mos
2-cds复合光催化剂在整个可见光波段均具有捕获光并将其吸收转换为氢能的能力。复合光催化剂在波长450nm处实现了最高的aqy为8.42%。已知cds的吸收边为520nm,而au-mos
2-cds复合光催化剂在波长大于520nm的550nm、600nm、650nm和700nm单色光下仍具有析氢活性。制备的多晶cds的复合光催化剂相对其他cds基光催化剂具有更宽的光谱响应,能够实现可见光区全波段的光捕获;这得益于au nrs的纵向局域等离激元特性与mos2作为电荷传输通道的协同作用,在大于cds吸收边仍具有析氢活性。
77.图10是本公开实施例的光催化剂在波长》420nm入射光下的稳定性评估曲线图。
78.如图10所示,稳定性测试是在波长》420nm,光功率为300mw/cm2的光照下进行,20小时内没有二次添加牺牲剂,反应以4h作为一个反应周期。在连续20小时的稳定性测试中,验证了au-mos
2-cds复合光催化剂具有良好的稳定性和可重复使用性,从图中可以看出,后三个反应周期几乎保持大致相同的析氢效率,前两周期析氢效率的降低是因为实验过程石英光窗上的溅射物遮挡了入射光,前两周期由于悬浮液处于真空条件并伴随不断搅拌,持续有液体溅射到石英光窗,后三个周期到达液面的入射光相对稳定。
79.根据本公开的上述实施例的光催化剂的制备方法,利用静电结合作用及au-s键修饰mos2及au nrs,使金纳米棒与二硫化钼紧密接触,制得au-mos2,再通过化学沉淀法制备多晶cds纳米颗粒,包覆在au-mos2的二硫化钼外围,分布均匀,所述au-mos
2-cds复合光催化剂整体结构呈花球状,mos2介于au-cds之间,形成了具有密切接触的三元复合光催化剂,实现在整个可见光区域均能够光捕获及分解水析氢,且该光催化剂粉末能够通过静置与水溶液完全分离,克服了光催化悬浮颗粒体系难以回收的缺点。
80.还需要说明的是,实施例中提到的方向用语,例如“上”、“下”、“前”、“后”、“左”、“右”等,仅是参考附图的方向,并非用来限制本公开的保护范围。贯穿附图,相同的元素由相同或相近的附图标记来表示。在可能导致对本公开的理解造成混淆时,将省略常规结构或构造。
81.并且图中各部件的形状和尺寸不反映真实大小和比例,而仅示意本公开实施例的内容。再者,单词“包含”不排除存在未列在权利要求中的元件或步骤。位于元件之前的单词“一”或“一个”不排除存在多个这样的元件。
82.类似地,应当理解,为了精简本公开并帮助理解各个发明方面中的一个或多个,在
上面对本公开的示例性实施例的描述中,本公开的各个特征有时被一起分组到单个实施例、图、或者对其的描述中。然而,并不应将该发明的方法解释成反映如下意图:即所要求保护的本公开要求比在每个权利要求中所明确记载的特征更多的特征。更确切地说,如下面的权利要求书所反映的那样,发明方面在于少于前面发明的单个实施例的所有特征。因此,遵循具体实施方式的权利要求书由此明确地并入该具体实施方式,其中每个权利要求本身都作为本公开的单独实施例。
83.以上所述的具体实施例,对本公开的目的、技术方案和有益效果进行了进一步详细说明,应理解的是,以上所述仅为本公开的具体实施例而已,并不用于限制本公开,凡在本公开的精神和原则之内,所做的任何修改、等同替换、改进等,均应包含在本公开的保护范围之内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1