一种双金属析氢催化剂及其制备方法
1.本发明涉及一种催化剂,特别涉及一种双金属析氢催化剂及其制备方法。
背景技术:
2.化石燃料的使用,给我们带来了很多的便利,化石燃料已经成为了人类所需能源的主要供给体,与此同时化石燃料的使用也带来了严重的污染问题。化石能源是一种不可再生能源,因此找到替代化石能源的新能源以及清洁能源是必不可少的。在核能、太阳能、风能、生物质能、地热能、海洋能、氢能等新能源和清洁能源中,氢能是一种燃烧性能好、无毒、无污染、利用率高、储量丰富的新的含能体能源。但是氢能的利用也存在一些问题,比如制取比较麻烦,需要寻求廉价且能大规模制取的方法,其次氢能在运输和存储方面存在一定的困难。到目前为止,全球96%的氢气来自化石燃料。目前较为成熟的化石能源制氢及电催化水分解制氢技术存在碳排放量大、制氢成本高等问题,而利用太阳能直接分解水制氢是一种理想的、无污染的绿色能源制备技术,被认为是更为理想的未来制氢路线,可以将大量的太阳能直接转化为氢燃料进行存储。但该途径太阳能转化利用效率较低。目前突破该技术瓶颈的核心是开发具有高效催化产氢性能及稳定性的材料,进而实现氢能大规模推广的最终目的。
3.利用太阳能进行光催化产氢的机理为:当半导体材料受到能量相当于或高于催化剂半导体禁带宽度的太阳光辐射时,半导体内的电子受激发,从价带跃迁到导带,迁移到半导体表面的电子与h
+
发生还原反应生成h2,空穴与反应体系中的牺牲剂进行反应,从而实现电子与空穴的分离。实现太阳能光催化产氢的关键即为寻找合适带隙的半导体材料,实现电子和空穴的快速有效分离。
4.目前有各种类型的光催化剂,例如tio2、cds等已被用于制氢,然而由于各种限制,这些材料的制氢性能并不理想,需要进一步研究提高光催化水分解产生氢气的效率。众多学者研究了氮化碳材料在光催化产氢领域的应用,氮化碳是非金属材料因其合适的带隙(2.7ev)和稳定性而引起了广泛关注,它被应用于co2还原、水分解和有机污染物降解等领域。最重要的是,氮化碳满足光催化产氢的标准热力学要求,然而它的可见光吸收效率低和光生载流子复合率高等缺点限制了它在光催化领域的应用。现有研究已采用构建异质结、表面改性、形貌调控、掺杂、负载助催剂等策略来提高原始氮化碳的性能。通过负载au、pt、pd等贵金属做助催剂产氢效果的提高是明显的,但是它们的高成本限制了大规模使用,因此迫切需要寻找高效且廉价的助催剂。
5.已有研究者把co负载在p掺杂氮化碳上改性,co与氮化碳在界面处相互作用且促进电子传输,但是co以纳米粒子存在具有利用率低,比表面积小,活性位点少等缺点。对应所形成的co-pcn催化剂用于高效的光催化水分解产氢是有限的,其催化活性仍然较低,阻碍了商业应用。
elemental mapping)图;
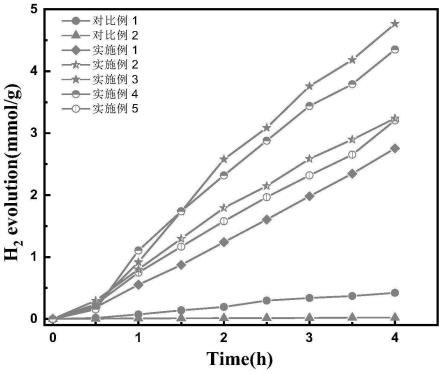
24.图6为实施例1~5和对比例1~2制备的析氢催化剂的光催化制氢速率图;
25.图7为实施例3和对比例1~2制备的析氢催化剂的固体紫外(drs)图;
26.图8为实施例3制备的析氢催化剂的稳定性测试图。
具体实施方式
27.下面结合实施例对本发明的技术方案作进一步说明。
28.实施例1
29.本发明的双金属析氢催化剂,其制备方法包括以下步骤:
30.(1)saag-cn的制备
31.分别将1.323g三聚氰胺和1.032g三聚氰酸加入80ml、100ml水中,加热至90℃搅拌至溶液透明形成溶液a和b;将0.077g柠檬酸(0.4mmol)和0.034g硝酸银(0.2mmol,其中ag 0.0216g)溶于10ml水中,形成溶液c;将溶液c加入溶液b中搅拌均匀,然后将混合液加入溶液a中,20℃条件下搅拌5h,用去离子水和乙醇分别洗涤3次,收集固体,在70℃的烘箱中干燥12小时;将干燥后的样品研磨后,氮气氛围下煅烧,煅烧温度550℃,升温速率5℃/min,煅烧时间3.5h,得到saag-cn;
32.(2)saco-ag-pcn的制备
33.将saag-cn0.5g、氯化钴0.012g(0.09mmol,其中co 0.005g)和0.008g次亚磷酸钠(0.09mmol)加入50ml n-甲基吡咯烷酮,制备分散液,进行水热反应,反应温度155℃,反应时间2h,待冷,洗涤,收集固体样品,干燥,得到saco-ag-pcn。
34.通过icp测试,催化剂中含ag 2.42wt%,含钴0.08wt%。
35.实施例2
36.本发明的双金属析氢催化剂,其制备方法包括以下步骤:
37.(1)saag-cn的制备
38.分别将1.386g三聚氰胺和1.096g三聚氰酸加入80ml、100ml水中,加热至95℃搅拌至溶液透明形成溶液a和b;将0.0884g柠檬酸(0.46mmol)和0.039g硝酸银(0.23mmol,其中ag 0.025g)溶于10ml水中,形成溶液c;将溶液c加入溶液b中搅拌均匀,然后将混合液加入溶液a中,22℃条件下搅拌5h,用去离子水和乙醇分别洗涤3次,收集固体,在70℃的烘箱中干燥12小时;将干燥后的样品研磨后,氮气氛围下煅烧,煅烧温度560℃,升温速率6℃/min,煅烧时间4h,得到saag-cn;
39.(2)saco-ag-pcn的制备
40.将saag-cn 0.5g、氯化钴0.047g(0.36mmol,其中co 0.021g)和0.026g次亚磷酸钠(0.3mmol)加入50ml n-甲基吡咯烷酮,制备分散液,进行水热反应,反应温度155℃,反应时间2h,待冷,洗涤,收集固体样品,干燥,得到saco-ag-pcn。
41.通过icp测试,催化剂中含ag 2.42wt%,含钴0.09wt%。
42.实施例3
43.本发明的双金属析氢催化剂,其制备方法包括以下步骤:
44.(1)saag-cn的制备
45.分别将1.260g三聚氰胺和1.226g三聚氰酸加入80ml、100ml水中,加热至95℃搅拌
至溶液透明形成溶液a和b;将0.096g柠檬酸(0.5mmol)和0.042g硝酸银(0.25mmol,其中ag0.027g)溶于10ml水中,形成溶液c;将溶液c加入溶液b中搅拌均匀,然后将混合液加入溶液a中,25℃条件下搅拌4h,用去离子水和乙醇分别洗涤3次,收集固体,在70℃的烘箱中干燥12小时;将干燥后的样品研磨后,氮气氛围下煅烧,煅烧温度600℃,升温速率5℃/min,煅烧时间4h,得到saag-cn;
46.(2)saco-ag-pcn的制备
47.将saag-cn 0.5g、氯化钴0.091g(0.7mmol,其中co 0.041g)和0.062g g次亚磷酸钠(0.7mmol)加入50ml n-甲基吡咯烷酮,制备分散液,进行水热反应,反应温度160℃,反应时间3h,待冷,洗涤,收集固体样品,干燥,得到saco-ag-pcn。
48.通过icp测试,催化剂中含ag 2.42wt%,含钴0.10wt%。
49.实施例4
50.本发明的双金属析氢催化剂,其制备方法包括以下步骤:
51.(1)saag-cn的制备
52.分别将1.323g三聚氰胺和1.161g三聚氰酸加入80ml、100ml水中,加热至95℃搅拌至溶液透明形成溶液a和b;将0.104g柠檬酸(0.54mmol)和0.046g硝酸银(0.27mmol,其中ag 0.029g)溶于10ml水中,形成溶液c;将溶液c加入溶液b中搅拌均匀,然后将混合液加入溶液a中,25℃条件下搅拌5h,用去离子水和乙醇分别洗涤3次,收集固体,在70℃的烘箱中干燥12小时;将干燥后的样品研磨后,氮气氛围下煅烧,煅烧温度580℃,升温速率7℃/min,煅烧时间4h,得到saag-cn;
53.(2)saco-ag-pcn的制备
54.将saag-cn 0.5g、氯化钴0.182g(1.4mmol,其中co 0.083g)和0.123g次亚磷酸钠(1.4mmol)加入50ml n-甲基吡咯烷酮,制备分散液,进行水热反应,反应温度165℃,反应时间4h,待冷,洗涤,收集固体样品,干燥,得到saco-ag-pcn。
55.通过icp测试,催化剂中含ag 2.42wt%,含钴0.19wt%。
56.实施例5
57.本发明的双金属析氢催化剂,其制备方法包括以下步骤:
58.(1)saag-cn的制备
59.分别将1.512g三聚氰胺和1.290g三聚氰酸加入80ml、100ml水中,加热至95℃搅拌至溶液透明形成溶液a和b;将0.086g柠檬酸(0.45mmol)和0.051g硝酸银(0.3mmol,其中ag 0.032g)溶于10ml水中,形成溶液c;将溶液c加入溶液b中搅拌均匀,然后将混合液加入溶液a中,25℃条件下搅拌5h,用去离子水和乙醇分别洗涤3次,收集固体,在70℃的烘箱中干燥12小时;将干燥后的样品研磨后,氮气氛围下煅烧,煅烧温度600℃,升温速率7℃/min,煅烧时间4h,得到saag-cn;
60.(2)saco-ag-pcn的制备
61.将saag-cn 0.5g、氯化钴0.286g(2.2mmol,其中co 0.13g)和0.185g次亚磷酸钠(2.1mmol)加入50ml n-甲基吡咯烷酮,制备分散液,进行水热反应,反应温度165℃,反应时间4h,待冷,洗涤,收集固体样品,干燥,得到saco-ag-pcn。
62.通过icp测试,催化剂中含ag 2.42wt%,含钴0.28wt%。
63.对比例1
64.在实施例3的基础上不进行第二步,得到saag-cn析氢催化剂。
65.对比例2
66.在实施例3的基础上,第一步不加入柠檬酸和硝酸银,其他条件不变,得到saco-pcn析氢催化剂。
67.结构表征
68.对实施例1~5和对比例1~2的析氢催化剂进行x射线衍射(xrd)表征,如图1所示。通过图1可以看出所有样品均表现出氮化碳的特征峰,说明成功合成了石墨相氮化碳,saag-cn和saco-ag-pcn样品也表现出ag的特征峰,ag的含量少,峰强度很弱,co的含量低,检测不到。
69.对实施例3制备的催化剂采用扫描电镜(sem),透射电镜(tem),球差电镜,haadf-stem和stem
–
edx elemental mapping进行表征,结果如图2~5所示。通过sem(图2)和tem(图3)图可以看出氮化碳呈现片状,对氮化碳负载co和ag双金属原子后,氮化碳表现出管状形貌。通过球差电镜,haadf-stem(图4)和stem
–
edx elemental mapping(图5)可以看出co以单原子的状态分散在p掺杂氮化碳基体上,ag大部分以单原子状态存在,由于co和p的加入使少部分ag原子团聚以纳米颗粒的状态存在,材料总体形貌是co和ag双金属以原子分散态分布在p掺杂氮化碳基体上。
70.性能表征
71.对实施例1~5和对比例1~2制备的析氢催化剂的光催化产氢性能进行测试,测试方法包括以下步骤:
72.(1)在容积为100m l的烧杯中加入20mg析氢催化剂,8ml三乙醇胺,72ml超纯水,超声30min;
73.(2)将超声后的反应溶液转移到反应器中;
74.(3)将反应器装在光催化装置上,启动真空泵抽真空20min;
75.(4)然后用ar气对整个反应装置洗气3次,去除装置中的空气,避免干扰;
76.(5)开磁力搅拌器,开氙灯电源,开气相色谱;
77.(6)光催化反应4h。
78.结果如6所示,可以看出,实施例1~5随着co含量的增加,产氢效果呈现先增加后下降的趋势,对比例1和2相对实施案例3的催化剂的产氢效果显著降低,实施例3制备的催化剂的产氢速率最高为1191umol/g/h。
79.对实施例3和对比例1~2制备的析氢催化剂做固体紫外(drs)表征,结果如图7所示。通过uv-vis drs图可以看出所有样品在370nm波长处表现出最强的吸收,这与该催化剂在365nm波长处得到的aqy值最大是一致的。实施例3制备的析氢催化剂比对比例1和2制备的析氢催化剂的吸收强度大,其在365nm处的aqy为1.49%,与产氢活性的变化规律也是相吻合的。
80.对实施例3的析氢催化剂做稳定性测试,结果如8所示。通过图8可以看出,在经过20h的产氢测试保持良好的稳定性,其中第四个循环产氢量有所下降,在体系中加入3mlteoa后,产氢量增加至最初的产量,证明材料依旧保持良好的稳定性,牺牲剂的消耗是导致产氢量下降的主要原因。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1