一种用于吸附水中硝酸盐的MIL-101(Fe)及其制备方法与应用
一种用于吸附水中硝酸盐的mil-101(fe)及其制备方法与应用
技术领域
1.本发明涉及污水处理技术领域,尤其涉及一种用于吸附水中硝酸盐的mil-101(fe)及其制备方法与应用。
背景技术:
2.随着社会经济的快速发展,人类对自然环境的开发利用愈频繁,许多含氮废水未经完全处理就排入水体,导致水体中硝酸盐(no
3-)的富集。大量no
3-会破环水体生态平衡,污染水体环境,导致水体富营养化,进而危害人类健康。因此,去除水中的no
3-具有重要的意义。
3.目前,去除水中no
3-的主要方法有生物法、化学沉淀法、吸附法等。但生物法受温度、进水cod浓度以及溶解氧等因素的限制,影响处理效果,且占地面积大、投资成本高。化学沉淀法常用磷酸镁铵(mgnh4po4)沉淀,操作方便,不受场地和环境的限制,但对沉淀剂的投加量有严格要求,且产物不易回收。吸附法具有运行方式简单、成本较低、适用条件广泛等优点,逐渐受到研究者的青睐。研究者们采用改性活性炭、改性玉米秸秆、改性活性碳纤维等多种吸附剂吸附去除水中的硝酸盐,均取得了较为理想的效果。然而上述采用的吸附剂普遍存在再生能力不高和选择性吸附能力较差的弊端。
技术实现要素:
4.本发明的目的在于提供一种用于吸附水中硝酸盐的mil-101(fe)及其制备方法与应用,以克服现有技术存在的缺陷。
5.为了实现上述发明目的,本发明提供以下技术方案:
6.本发明提供了一种mil-101(fe)的制备方法,包括以下步骤:
7.(1)将fecl3、n,n-二甲基甲酰胺、对苯二甲酸和乙酸混合后进行水热反应,所得产物体系分离得到中间产物;
8.(2)将所得中间产物和甲醇混合后进行水热反应,生成mil-101(fe)。
9.优选的,所述步骤(1)中fecl3、n,n-二甲基甲酰胺、对苯二甲酸、乙酸的用量比为2.05~2.14g:70~90ml:0.6~0.65g:1ml。
10.优选的,所述步骤(1)水热反应的时间为17~19h,水热反应的温度为105~115℃。
11.优选的,所述步骤(2)甲醇与步骤(1)对苯二甲酸的体积比为5~7:7~9。
12.优选的,所述步骤(2)水热反应的时间为2.5~4h,水热反应的温度为65~75℃。
13.本发明还提供了一种由上述制备方法制备得到的mil-101(fe)。
14.本发明还提供了一种mil-101(fe)在吸附水中硝酸盐的应用方法,其所述mil-101(fe)在吸附初始浓度为25~35mg/l的no
3-废水时的投加量为0.18~0.22g/l。
15.优选的,所述mil-101(fe)吸附水中的硝酸盐的时间为25~35min,吸附的温度为22~28℃,待吸附的水体的ph值为7.5~8.5。
16.经由上述技术方案可知,与现有技术相比,本发明的技术方案具有如下的有益效果:
17.本发明制备的mil-101(fe)材料具有可调节的孔径、多样的孔道结构和特定的活性位点,其对no
3-的吸附量最高可达14.10mg/g。且,该材料吸附效率高,在30min左右即可达到吸附平衡。
附图说明
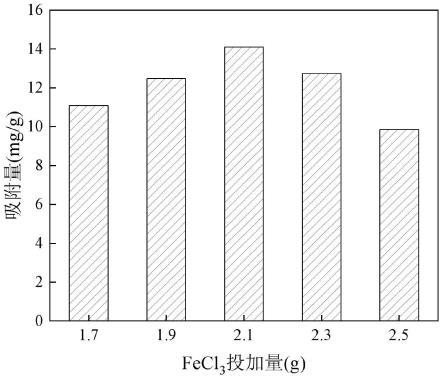
18.图1为实施例1与对比例1制备的mil-101(fe)材料的测试结果;
19.图2为对比例2与实施例1制备的mil-101(fe)材料的测试结果;
20.图3为对比例3与实施例1制备的mil-101(fe)材料的测试结果;
21.图4为测试实施例1制备得到的mil-101(fe)材料的用量(0.1、0.2、0.3、0.4、0.5g)对no
3-的吸附效果的测试结果;
22.图5为测试实施例1制备得到的mil-101(fe)材料在no
3-浓度分别为30mg/l、50mg/l、100mg/l时,吸附时间对吸附性能的影响的测试结果;
23.图6为测试ph在3.0~12.0范围内对实施例1制备得到的mil-101(fe)材料吸附性能的影响的测试结果。
具体实施方式
24.本发明提供了一种mil-101(fe)的制备方法,包括以下步骤:
25.(1)将fecl3、n,n-二甲基甲酰胺、对苯二甲酸和乙酸混合后进行水热反应,所得产物体系分离得到中间产物;
26.(2)将所得中间产物和甲醇混合后进行水热反应,生成mil-101(fe)。
27.在本发明中,所述步骤(1)中fecl3、n,n-二甲基甲酰胺、对苯二甲酸、乙酸的用量比为2.05~2.14g:70~90ml:0.6~0.64g:1ml,优选为2.08~2.12g:75~85ml:0.61~0.63g:1ml。
28.在本发明中,所述步骤(1)水热反应的时间为17~19h,优选为17.5~18.5h,水热反应的温度为105~115℃,优选为108~112℃。
29.在本发明中,所述步骤(2)甲醇与步骤(1)对苯二甲酸的体积比为5~7:7~9,优选为6~7:8~9。
30.在本发明中,所述步骤(2)水热反应的时间为2.5~4h,优选为3~3.5h,水热反应的温度为65~75℃,优选为68~72℃。
31.本发明还提供了一种由上述制备方法制备得到的mil-101(fe)。
32.本发明还提供了一种mil-101(fe)在吸附水中硝酸盐的应用方法,其所述mil-101(fe)在吸附初始浓度为30mg/l的no
3-废水时的投加量为0.18~0.22g/l,优选为0.19~0.21g/l。
33.在本发明中,所述mil-101(fe)吸附水中的硝酸盐的时间为25~35min,优选为28~32min,吸附的温度为22~28℃,优选为24~26℃,待吸附的水体的ph值为7.5~8.5,优选为7.8~8.2。
34.下面结合实施例对本发明提供的技术方案进行详细的说明,但是不能把它们理解
为对本发明保护范围的限定。
35.实施例1
36.一种mil-101(fe)的制备方法,包括以下步骤:
37.(1)将fecl3、n,n-二甲基甲酰胺、对苯二甲酸和乙酸按照用量比为2.1g:80ml:0.62g:1ml混合后加入聚四氟乙烯水热反应釜中,在110℃反应18h,反应结束后冷却至室温,所得产物体系分离得到中间产物;
38.(2)将所得中间产物和60ml甲醇混合后入聚四氟乙烯水热反应釜中,在70℃反应3h,抽滤烘干,研磨得到橘黄色粉末,即为mil-101(fe);
39.(3)称取1.6304g kno3配制1000mg/l的no
3-标准溶液,取3ml no
3-标准溶液加入150ml的锥形瓶中,加水稀释至100ml(此时no
3-的浓度为30mg/l),加入0.2g的mil-101(fe),25℃、200r/min条件下振荡30min,过滤,采用aquion型离子色谱仪测定no
3-浓度。每组实验设置3组平行实验,结果取其平均值。
40.采用式(1)计算no
3-的吸附量qe(mg/g):
[0041][0042]
式中:c0表示no
3-的初始浓度,mg/l;ce表示no
3-的平衡浓度,mg/l;v为溶液的体积,ml;m为吸附剂的质量,g。
[0043]
实施例2
[0044]
一种mil-101(fe)的制备方法,包括以下步骤:
[0045]
(1)将fecl3、n,n-二甲基甲酰胺、对苯二甲酸和乙酸按照用量比为2.08g:70ml:0.61g:1ml混合后加入聚四氟乙烯水热反应釜中,在105℃反应17.5h,反应结束后冷却至室温,所得产物体系分离得到中间产物;
[0046]
(2)将所得中间产物和58ml甲醇混合后入聚四氟乙烯水热反应釜中,在65℃反应2.5h,抽滤烘干,研磨得到橘黄色粉末,即为mil-101(fe);
[0047]
(3)称取1.6304g kno3配制1000mg/l的no
3-标准溶液,取2.5ml no
3-标准溶液加入150ml的锥形瓶中,加水稀释至100ml(此时no
3-的浓度为25mg/l),加入0.19g的mil-101(fe),22℃、200r/min条件下振荡28min,过滤,采用aquion型离子色谱仪测定no
3-浓度。每组实验设置3组平行实验,结果取其平均值。最终mil-101(fe)材料对no
3-吸附量为13.9mg/g。
[0048]
实施例3
[0049]
一种mil-101(fe)的制备方法,包括以下步骤:
[0050]
(1)将fecl3、n,n-二甲基甲酰胺、对苯二甲酸和乙酸按照用量比为2.12g:90ml:0.64g:1ml混合后加入聚四氟乙烯水热反应釜中,在115℃反应18.5h,反应结束后冷却至室温,所得产物体系分离得到中间产物;
[0051]
(2)将所得中间产物和60ml甲醇混合后入聚四氟乙烯水热反应釜中,在75℃反应4h,抽滤烘干,研磨得到橘黄色粉末,即为mil-101(fe);
[0052]
(3)称取1.6304g kno3配制1000mg/l的no
3-标准溶液,取3.5ml no
3-标准溶液加入150ml的锥形瓶中,加水稀释至100ml(此时no
3-的浓度为35mg/l),加入0.21g的mil-101(fe),28℃、200r/min条件下振荡32min,过滤,采用aquion型离子色谱仪测定no
3-浓度。每组实验设置3组平行实验,结果取其平均值。最终mil-101(fe)材料对no
3-吸附量为14mg/g。
[0053]
对比例1
[0054]
对比例1与实施例1相比改变了fecl3投加量(1.9、2.3、2.5、2.7、2.9g),其余与实施例1相同。
[0055]
实施例1与对比例1的测试结果见图1,由图1可知,当fecl3投加量由1.9g增加到2.1g,mil-101(fe)对no
3-的吸附性能随之提高,继续增大fecl3投加量,no
3-的吸附量出现下降趋势,因为fecl3与有机配体形成的材料骨架变化,无法形成有利于no
3-吸附的孔洞结构所致。
[0056]
对比例2
[0057]
对比例2与实施例1相比改变了对苯二甲酸的投加量(0.42、0.62、0.82、1.02g),其余与实施例1相同。
[0058]
对比例2与实施例1的测试结果见图2,由图2可知,当对苯二甲酸投加量提高至0.62g时,mil-101(fe)对no
3-的吸附性能达到最佳值,继续提高对苯二甲酸投加量,no
3-的吸附量急剧降低,因为对苯二甲酸投加量过高时,有可能导致材料骨架的多孔结构和活性位点均受到抑制。
[0059]
对比例3
[0060]
对比例3与实施例1相比改变了步骤(1)的反应时间(16、20、22h),其余与实施例1相同。
[0061]
对比例3与实施例1的测试结果见图3,由图3可知,mil-101(fe)的合成反应时间直接影响了材料的吸附性能。合成反应时间过短,导致反应不完全,而无法生成合适的mil-101(fe)框架结构;合成反应时间过长,过度反应下使得mil-101(fe)材料有可能发生变性,破坏其框架结构。
[0062]
测试例1
[0063]
测试实施例1制备得到的mil-101(fe)材料的用量(0.1、0.2、0.3、0.4、0.5g)对no
3-的吸附效果。
[0064]
测试结果见图4,由图4可知,随着mil-101(fe)投加量从0.1g增大到0.5g,其对no
3-的去除率逐渐提高,继续增大mil-101(fe)投加量至0.5g,no
3-去除率变化趋于平缓;而随着mil-101(fe)投加量增大,no
3-吸附量降低。这可能是因为,适量的mil-101(fe)对水中no
3-离子具有较好的吸附能力,而mil-101(fe)过量会导致吸附剂之间互相碰撞粘合,从而减少其吸附位点,降低对no
3-的吸附性能。当mil-101(fe)投加量为0.2g时,no
3-吸附量为14.10mg/g,符合环境要求。
[0065]
测试例2
[0066]
测试实施例1制备得到的mil-101(fe)材料在no
3-浓度分别为30mg/l、50mg/l、100mg/l时,吸附时间对吸附性能的影响。
[0067]
测试结果见图5,由图5可知,当吸附时间在1~5min时吸附速率较快,在5min时速率开始变缓慢,此后随时间的增加,吸附量变化较缓慢,在30min之后吸附达到平衡。在前5min内,mil-101(fe)表面的吸附位点较多,对no
3-的吸附速率较快,5min之后,吸附位点被占据,吸附速率变缓,但mil-101(fe)有较为丰富的孔道结构,可以与内部cl-进行离子交换而吸附,在30min左右,达到平衡状态。
[0068]
测试例3
[0069]
测试ph在3.0~12.0范围内对实施例1制备得到的mil-101(fe)材料吸附性能的影响,测试结果见图6。
[0070]
由图6可知,mil-101(fe)对no
3-的吸附量随ph值的增大而增大,在ph等于8时达到最高,在ph值大于8时下降,大于10时急剧下降,在过酸或者过碱的条件下都会使材料的孔道结构发生变化,甚至变性,降低对no
3-的吸附能力。当溶液ph值为8的条件下,吸附效果最佳。
[0071]
以上所述仅是本发明的优选实施方式,应当指出,对于本技术领域的普通技术人员来说,在不脱离本发明原理的前提下,还可以做出若干改进和润饰,这些改进和润饰也应视为本发明的保护范围。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1