超分子手性催化剂、其制备方法及其催化D-A反应的应用
超分子手性催化剂、其制备方法及其催化d-a反应的应用
技术领域
1.本发明涉及有机化学合成催化技术领域,具体涉及一种超分子手性催化剂、其制备方法及其催化d-a反应的应用。
背景技术:
2.随着人们对手性化合物的需求日益增加,不对称催化合成是获得手性物质的最有效的方法。对优异的手性催化剂而言,需要具备催化速率快、高立体选择性和优异循环催化性能的特点。
3.金属有机配体催化剂通常在有机溶剂中进行均相催化,虽能够达到较高的选择性,但回收却困难,欠缺循环催化能力。将均相催化剂与载体相结合是解决不能循环催化问题的有效方式。中国发明专利(cn 105195228a)报道了一种fe3o4负载型手性催化剂,将手性小分子负载在具有磁性的fe3o4纳米粒子上,该催化剂在diels-alder环加成反应中获得了高产率和高立体选择性,通过磁分离达到了可循环催化的效果,但该催化剂存在制备工艺复杂,催化时间较长的缺点。
4.近年来,超分子手性催化剂因具有活性位点紧密有序排列、手性微环境的特点,在不对称催化领域表现出优异的效果。目前为止,超分子手性催化剂大都集中在超分子水凝胶体系,能够进行3~5次的循环不对称催化。然而相对于超分子水凝胶有机催化剂而言,超分子手性金属催化剂虽具有优异的高效不对称催化性能,但其循环催化能力却始终是一个难题。刘鸣华课题组(j.am.chem.soc.,2016,138,15629-15635.)制备了一系列超分子手性金属催化剂,对diels-alder和mukaiyama aldol具有优异的选择性催化,但却不具备循环催化性能。
5.因此,发明一种既能高效不对称催化,又能循环使用的超分子手性金属离子催化剂是一项重大挑战。这对将来具有循环不对称催化能力的超分子手性金属催化剂的制备具有重要的指导意义,对手性药物的不对称合成中具有潜在的应用价值。
技术实现要素:
6.针对现有技术中的不足之处,本发明旨在提供一种可高效循环不对称催化的超分子手性金属催化剂,用于选择性催化diels-alder(d-a)反应。
7.为实现上述目的,本发明提供如下技术方案:
8.一种超分子手性催化剂的制备方法,包括如下步骤:
9.1)将单手性苯甘氨酸烷基衍生物溶解在水溶性有机溶剂中,室温下搅拌得到l-phgc
8~20
或d-phgc
8~20
的水溶性有机溶剂溶液;
10.2)向步骤1)的体系中加入超纯水继续搅拌,得到超分子组装体(m)-l-phgc
8~20-nr或(p)-d-phgc
8~20-nr;
11.3)向步骤2)中加入金属离子化合物,继续搅拌得到(m)-l型或(p)-d型超分子手性催化剂。
12.进一步地,所述步骤1)中水溶性有机溶剂选自甲醇、乙醇、异丙醇、丙三醇、丙酮、乙腈和四氢呋喃中的一种;单手性苯甘氨酸烷基衍生物的浓度为1~10mm。
13.进一步地,所述步骤2)中超纯水与有机溶剂的体积比为9:1~3:7。
14.进一步地,所述金属离子化合物选自cu(no3)2·
3h2o、cuso4、cucl2、cu(otf)2、fe(no3)3·
9h2o、fecl3、fe(otf)3、bi(otf)3、sc(otf)3、zncl2、zn(otf)2中的一种;浓度为0.1mm。
15.本发明进一步提供一种如上所述的制备方法制得的超分子手性催化剂。
16.本发明进一步提供如上所述的超分子手性催化剂用于选择催化diels-alder的反应,将得到的超分子手性催化剂降温至0~5℃,加入反应物环戊二烯和查尔酮衍生物,搅拌0.25~4h进行diels-alder反应,(m)-l型催化得到s型产物,(p)-d型催化得到r型产物。
17.进一步地,所述查尔酮衍生物为查尔酮、甲氧基取代查尔酮、氯取代查尔酮、溴取代查尔酮、2-噻吩查尔酮、糠醛查尔酮或1-萘甲醛查尔酮。
18.本发明的有益效果是:本发明提供的超分子手性金属催化剂可高效循环不对称催化diels
–
alder反应,超分子内部基元紧密有序的排列以及金属离子在其表面配位后具有的手性微环境,使得diels
–
alder反应产率和ee值分别高达95%和92%。超分子手性催化剂(m)-l-phgc
16-cu(ⅱ)-nr催化得到(s)-endo产物,而(p)-d-phgc
16-cu(ⅱ)-nr催化得到(r)-endo产物。该超分子催化体系是一种悬浮液,通过离心可进行催化剂的分离,在溶剂极性不变的条件下,催化剂具备结构稳定的优势,并且在保持高产率和高ee值的前提下,能够完成4次循环不对称催化。这将对制备可循环不对称催化的新型催化剂具有重要的指导意义。
附图说明
19.为了更清楚地说明本发明具体实施方式或现有技术中的技术方案,下面将对具体实施方式或现有技术描述中所需要使用的附图作简单地介绍,显而易见地,下面描述中的附图是本发明的一些实施方式,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据这些附图获得其他的附图。
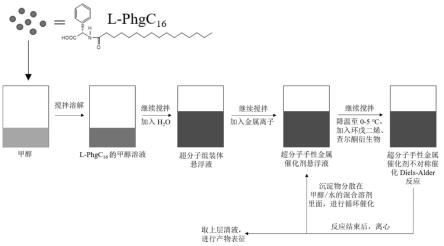
20.图1为超分子手性催化剂的制备过程及催化流程图。
21.图2是手性超分子纳米带(m)-l-phgc
16-nr(a)、(m)-l-phgc
16-cu(ⅱ)-nr(b)、(p)-d-phgc
16-nr(d)、(p)-d-phgc
16-cu(ⅱ)-nr(e)的sem图;(m)-l-phgc
16-cu(ⅱ)-nr(c)、(p)-d-phgc
16-cu(ⅱ)-nr(f)的tem图。
22.图3是l-phgc
16
的uv-vis谱图(a)、l/d-phgc
16
的cd谱图(b)、l-phgc
16-cu(ⅱ)、d-phgc
16-cu(ⅱ)、(m)-l-phgc
16-nr、(p)-d-phgc
16-nr、(m)-l-phgc
16-cu(ⅱ)-nr、(p)-d-phgc
16-cu(ⅱ)-nr的cd谱图(c)。
23.图4为实施例1-3制得的催化剂不对称催化diels-alder反应效果对比图。
24.图5是(m)-l-phgc
16-cu(ⅱ)-nr循环不对称催化diels-alder反应效果图。
具体实施方式
25.下面将结合附图对本发明的技术方案进行清楚、完整地描述,显然,所描述的实施例是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术
人员在没有做出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
26.此外,下面所描述的本发明不同实施方式中所涉及的技术特征只要彼此之间未构成冲突就可以相互结合。
27.实施例1:超分子手性金属催化剂(m)-l-phgc
16-cu(ⅱ)-nr
28.15.6mg l-phgc
16
溶解至4ml的甲醇中,搅拌条件下,向上述体系中加入6ml的h2o,继续搅拌15min后获得超分子组装体(m)-l-phgc
16-nr。
29.向所得的超分子组装体(m)-l-phgc
16-nr体系中加入1μmol cu(no3)2·
3h2o,继续搅拌15min后得到超分子手性催化剂(m)-l-phgc
16-cu(ⅱ)-nr。
30.实施例2:超分子手性金属催化剂(p)-d-phgc
16-cu(ⅱ)-nr
31.同实施例1,区别在于将l-phgc
16
替换为d-phgc
16
,分别得到(p)-d-phgc
16-nr、(p)-d-phgc
16-cu(ⅱ)-nr。
32.实施例3:小分子手性l-phgc
16-cu(ⅱ)、d-phgc
16-cu(ⅱ)催化剂
33.分别将15.6mg的l-phgc
16-cu(ⅱ)、d-phgc
16-cu(ⅱ)溶解至10ml的甲醇中,搅拌均匀后,各加入1μmol cu(no3)2·
3h2o,15min后分别得到l-phgc
16-cu(ⅱ)、d-phgc
16-cu(ⅱ)。
34.应用:用实施例1-3的催化剂催化d-a反应,具体步骤如下:
35.将催化剂悬浮液降至0~5℃,加入环戊二烯、查尔酮衍生物,搅拌0.25~4h,进行d-a反应。反应完成后离心,取上清液进行产物表征,沉淀物则继续分散在甲醇/水的混合溶剂中进行循环催化d-a反应。
36.上述超分子手性催化剂的制备过程及催化流程如图1所示。
37.对催化剂和d-a产物进行表征:
38.由图2(a)和2(d)可见,(m)-l-phgc
16-nr和(p)-d-phgc
16-nr均表现出纳米带形貌,随着cu
2+
的加入,在图2(b)和2(e)中可以发现一些左螺旋和右螺旋纳米带的形貌,从tem中(图2c、f)也可以发现除了纳米带之外的螺旋形貌,这与材料的cd表征相吻合。
39.图3(a)为l-phgc
16
的uv-vis光谱,该小分子在211nm和259nm处出现两个紫外吸收峰;图3(b)为l/d-phgc
16
的cd光谱,l/d-phgc
16
两个小分子在216nm处分别显示出正/负的cotton效应,对应于紫外211nm处的吸收;图3(c)中l/d-phgc
16-cu(ⅱ)同样在216nm处分别显示出正/负的cotton效应,表明cu
2+
的加入并未出现新的手性信号;而超分子组装体(m)-l-phgc
16-nr和(p)-d-phgc
16-nr在231nm处出现新的超分子手性信号,这与紫外吸收中259nm处的吸收相对应,并且超分子手性催化剂(m)-l-phgc
16-cu(ⅱ)-nr和(p)-d-phgc
16-cu(ⅱ)-nr在231nm处依然存在超分子手性信号。
40.小分子手性催化剂l-phgc
16-cu(ⅱ)、d-phgc
16-cu(ⅱ)以及超分子手性催化剂(m)-l-phgc
16-cu(ⅱ)-nr、(p)-d-phgc
16-cu(ⅱ)-nr催化d-a反应的产率和ee值如图4所示,其中小分子手性催化剂的产率和ee值均较低,产率为42~45%,ee值仅6.4~7%,说明小分子手性催化剂对d-a反应的催化活性和选择性效果较差。相反地,超分子手性催化剂极大的提升了催化活性和选择性,反应产率和ee值分别高达95%和92%。
41.图5表明超分子手性催化剂(m)-l-phgc
16-cu(ⅱ)-nr具有优异的循环不对称催化效果,循环不对称催化4次后,产率和选择性依然保持在90%以上。
42.尽管本发明的实施方案已公开如上,但其并不仅仅限于说明书和实施方式中所列运用,它完全可以被适用于各种适合本发明的领域,对于熟悉本领域的人员而言,可容易地
实现另外的修改,因此在不背离权利要求及等同范围所限定的一般概念下,本发明并不限于特定的细节和这里示出与描述的图例。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1