一种无溶剂干法合成除氧催化剂的方法
1.本发明属于催化剂合成领域,涉及一种除氧催化剂的合成方法,具体涉及一种无溶剂干法合成除氧催化剂的方法。
背景技术:
2.催化除氧在生物技术和工业合成中有着至关重要的作用。在有机合成中,许多涉及易被氧化试剂的反应对氧气敏感,严格控制气氛中的无氧条件才能得到理想结果。在工业气体管路运输当中,气体中低的氧气浓度可以减少管路腐蚀,延长管路寿命。半导体制造及加工行业中超高纯度气体要求氧气浓度低于0.01ppm;锂离子电池行业需要氧气浓度低于0.1ppm的惰性气体,来保证无水无氧的操作环境;燃料电池及绿氢行业标准要求氧浓度低于5ppm;仪器分析需要低于0.5ppm氧气的高纯气体,以实现更高精度的分析测试。在不同类型的除氧方法中,多相催化除氧由于易分离、长寿命等优点广泛应用。除氧催化剂合成方法的合理设计变得尤为重要。但是,目前实验室生产的除氧催化剂产量仍与大规模应用开发及商业部署的需求存在较大差距。
3.一般合成除氧催化剂的方法分为湿法合成和干法合成。传统湿法合成包括共沉淀法、水热合成法和浸渍法。共沉淀法首先制备活性组分复合氧化物,再利用胶溶剂和扩孔剂进行捏合、成型、干燥和焙烧制成除氧催化剂;水热合成法是在高温高压的环境中,以水为反应介质合成除氧催化剂;浸渍法是将活性金属以离子或化合物的形式附着在多孔载体上合成高效催化剂。peppel报道了一种合成方法,采用湿法浸渍合成将贵金属(pt、pa、rh、cu、ag/al2o3)负载在三氧化二铝(al2o3)上合成除氧催化剂(peppel,t.,seeburg,d.,fulda,g., kraus,m.,trommler,u.,roland,u.and wohlrab,s.,chem.eng.technol 2017,40:153-161.)。然而,这些基于溶液的湿法合成方法不可避免的导致大量溶剂废物产生,且随后的煅烧步骤也会逸出有毒气体,需要额外的废气处理步骤。此外,湿法合成涉及多个步骤,费时费力,能耗及成本难以控制在较低范围,限制了其规模化生产催化材料。因此,高效、绿色、简单、安全、廉价的可扩展规模化无溶剂干法合成除氧催化剂的方法研究具有非常重要的价值。
技术实现要素:
4.本发明针对上述现有技术存在的缺陷,提供了一种无溶剂干法合成除氧催化剂的方法。
5.为达到上述目的,本发明提供一种无溶剂干法合成除氧催化剂的方法,包括通过机械化学合成法使金属前驱体与有机配体充分反应,合成具有多孔结构的除氧催化剂的步骤,所述金属前驱体为金属、合金、金属氧化物、金属氮化合物、金属硫化物和金属盐中的一种或多种组成的混合物,所述有机配体为选自对苯二甲酸、2-氨基对苯二甲酸、2,5-二羟基对苯二甲酸、1,3,5-苯三甲酸、富马酸、2-甲基咪唑盐、聚苯乙烯磺酸盐、联苯酚、三苯基膦、四苯醛基卟啉、四苯羧基卟啉和乙酸钠中的一种或多种组成的混合物。
6.优化地,所述机械化学合成法为使用研磨、反应挤出或球磨使物料在机械力诱发和作用下发生反应的方法。
7.进一步地,包括以下步骤:(a)将所述金属前驱体与所述有机配体进行分散,得混合粉末;(b)使所述混合粉末在球磨机中以1-10000hz的频率进行研磨反应并控制反应温度为10~500℃;或,使所述混合粉末在挤出机中进行反应,保持螺杆转速为1-10000rpm、扭矩为最大值的0.1%-100%且反应温度为10~500℃;反应为0.5-10天。
8.更进一步地,所述金属前驱体的用量为0.1-100mol,所述有机配体的用量为0.1-100mol。
9.优化地,所述金属前驱体为金属氧化物、金属氮化合物、金属硫化物和金属盐中的一种或多种组成的混合物。
10.进一步地,所述有机配体为选自对苯二甲酸和均苯三酸中的一种或两种组成的混合物。
11.进一步地,还包括:(c)利用步骤(b)的产物对待除氧气体进行处理使对氟苯酚与氧气进行反应,所述待除氧气体为氧气与选自氦气、氩气、氮气、二氧化碳、一氧化碳、氢气、氨气、甲烷、乙烷、丙烷、乙烯、丙烯、丁烯、乙炔、丙炔、硅烷、磷烷、砷烷、乙硼烷、氯化氢、氟化氢、氢化锑、三氟化硼、三氟化氮、三氟化磷、四氟化硅和四氟化碳中的一种或多种的混合气体。
12.更进一步地,所述待除氧气体中氧气的体积含量为0.0001%-30%。
13.由于上述技术方案运用,本发明与现有技术相比具有下列优点:本发明无溶剂干法合成除氧催化剂的方法,以金属前驱体和有机配体为原料,采用机械化学合成法(如填入球磨机、球磨机、挤出机中等)即可快速产出除氧催化剂产品,该产品可将待除氧气体(催化对氟苯酚与氧气反应)在常温常压下快速脱氧达到极低浓度(《0.001ppm);该无溶剂干法规模化合成除氧催化剂的方法技术具有无毒、安全、产率稳定、易操作等优点。
14.本发明提供了一种无溶剂干法合成除氧催化剂的方法,通过机械化学合成法,使金属前驱体与有机配体反应,合成多孔催化剂材料,可以用于代替生产除氧催化剂的体系,具有高效、温和、低成本、长效稳定的优点,适合工业大规模应用。
附图说明
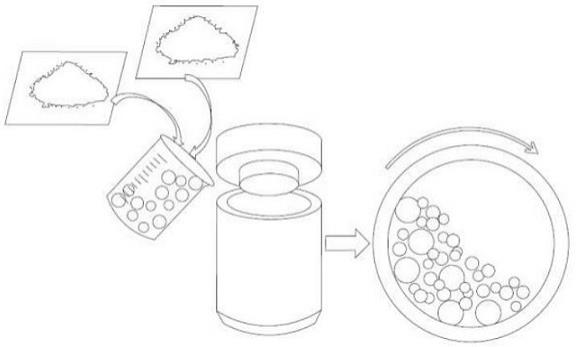
15.图1为本发明无溶剂干法合成除氧催化剂的方法的流程示意图;图2为实施例1中除氧催化剂(oz-1)的sem表征图;图3为实施例1中除氧催化剂(oz-1)与商业氧捕集井性能对比图。
具体实施方式
16.本发明无溶剂干法合成除氧催化剂的方法,包括通过机械化学合成法使金属前驱体与有机配体充分反应,合成具有多孔结构的除氧催化剂的步骤,所述金属前驱体为金属、合金、金属氧化物、金属氮化合物、金属硫化物和金属盐中的一种或多种组成的混合物,所述有机配体为选自对苯二甲酸、2-氨基对苯二甲酸、2,5-二羟基对苯二甲酸、1,3,5-苯三甲酸、富马酸、2-甲基咪唑盐、聚苯乙烯磺酸盐、联苯酚、三苯基膦、四苯醛基卟啉、四苯羧基卟
啉和乙酸钠中的一种或多种组成的混合物。该方法以金属前驱体和有机配体为原料,采用机械化学合成法(如填入研钵、球磨机、挤出机中等)即可快速产出除氧催化剂产品,该产品可将待除氧气体(催化对氟苯酚与氧气反应)在常温常压下快速脱氧达到极低浓度(《0.01ppm);该无溶剂干法规模化合成除氧催化剂的方法技术具有无毒、安全、产率稳定、易操作等优点。即通过机械化学合成法,使金属前驱体与有机配体反应,合成多孔催化剂材料,可以用于代替生产除氧催化剂的体系,具有高效、温和、低成本、长效稳定的优点,适合工业大规模(可达1.5kg/h)应用。
17.所述机械化学合成法为使用研磨、反应挤出或球磨使物料在机械力诱发和作用下发生反应的方法。具体包括以下步骤:(a)将所述金属前驱体与所述有机配体进行分散,得混合粉末;(b)使所述混合粉末在球磨机中以1-10000hz的频率进行研磨反应并控制反应温度为10~500℃;或,使所述混合粉末在挤出机中进行反应,保持螺杆转速为1-10000rpm、扭矩为最大值的0.1%-100%且反应温度为10~500℃;反应为0.5-10天。本技术还包括将上述方法制得的除氧催化剂进行应用步骤:利用步骤(b)的产物对待除氧气体进行处理,所述待除氧气体为氧气与选自氦气、氩气、氮气、二氧化碳、一氧化碳、氢气、氨气、甲烷、乙烷、丙烷、乙烯、丙烯、丁烯、乙炔、丙炔、硅烷、磷烷、砷烷、乙硼烷、氯化氢、氟化氢、氢化锑、三氟化硼、三氟化氮、三氟化磷、四氟化硅和四氟化碳中的一种或多种的混合气体(即上述方法还包括步骤(c):利用步骤(b)的产物对待除氧气体进行处理,所述待除氧气体为氧气与选自氦气、氩气、氮气、二氧化碳、一氧化碳、氢气、氨气、甲烷、乙烷、丙烷、乙烯、丙烯、丁烯、乙炔、丙炔、硅烷、磷烷、砷烷、乙硼烷、氯化氢、氟化氢、氢化锑、三氟化硼、三氟化氮、三氟化磷、四氟化硅和四氟化碳中的一种或多种的混合气体)。所述待除氧气体中氧气的体积含量为0.0001%-30%。
18.所述金属前驱体的用量优选为0.1-100mol,更优选为5-20mol;所述有机配体的用量优选为0.1-100mol,更优选为5-20mol;金属前驱体和有机配体摩尔比为优选为1:0.5~2最优为1:1。
19.所述金属前驱体优选为金属氧化物、金属氮化合物、金属硫化物和金属盐中的一种或多种组成的混合物,最优为金属盐或金属氧化物,如氯化铝、醋酸钴、氯化锌、氯化亚铁、碱式碳酸铜、硝酸铜、硝酸锌、醋酸镍、氯化钌、醋酸钴、醋酸铁和氧化亚铜等。所述有机配体优选为选自对苯二甲酸和均苯三甲酸中的一种或两种组成的混合物。
20.下面对本发明优选实施方案进行详细说明。
21.实施例1本实施例提供一种无溶剂干法合成除氧催化剂的方法,如图1所示,包括以下步骤:(a)将10mol醋酸钴与10mol对苯二甲酸进行分散预混合10min,得混合粉末;(b)将混合粉末填入球磨机中,以50hz的频率在100℃反应90min,收集样品;将得到的样品用乙醇洗涤3次,随后放置在真空干燥箱中于60℃干燥12h得到除氧催化剂3.43kg(命名为o
z-1),其形貌见图2。
22.(c)将25g除氧催化剂与25g对氟苯酚混合,研磨混匀装入除氧管中;于室温下,以50ml/min的流速通入氮氧混合反应气体,其中氧含量为500ppm;3h后通过质谱分析:反应气体的氧气体积含量从500ppm降至<0.01ppm(0.009ppm)。如图3所示,反应的前期已经能达
到很低的氧浓度了,3h后测是为了保证除氧性能的稳定性,使除氧性能更具说服力,即3h还是能降至<0.01ppm。
23.实施例2本实施例提供一种无溶剂干法合成除氧催化剂的方法,它与实施例1中的基本一致,不同的是:步骤(b)中,将混合粉末倒入挤出机中于100℃进行挤压反应,螺杆速度保持在300rpm、扭矩保持在最大值的80%,干燥后获得除氧催化剂3.43kg;最终通过微氧传感器分析:反应气体的氧气体积含量从500ppm降至0.01ppm。
24.实施例3本实施例提供一种无溶剂干法合成除氧催化剂的方法,它与实施例1中的基本一致,不同的是:步骤(a)中,将1mol醋酸钴与1mol对苯二甲酸进行分散预混合;步骤(b)中,将混合粉末倒入研钵中充分研磨反应,干燥后获得除氧催化剂0.34kg;最终通过微氧传感器分析:反应气体的氧气体积含量从500ppm降至1ppm。
25.实施例4本实施例提供一种无溶剂干法合成除氧催化剂的方法,它与实施例1中的基本一致,不同的仅是:步骤(c)中,通入二氧化碳和氧气的混合反应气体,其中氧含量为500ppm;3h后通过质谱分析:反应气体的氧气体积含量从500ppm降至0.01ppm。
26.实施例5本实施例提供一种无溶剂干法合成除氧催化剂的方法,它与实施例1中的基本一致,不同的是:步骤(c)中,通入氦氧混合反应气体,其中氧含量为500ppm;3h后通过质谱分析:反应气体的氧气体积含量从500ppm降至0.01ppm。
27.实施例6本实施例提供一种无溶剂干法合成除氧催化剂的方法,它与实施例1中的基本一致,不同的是:步骤(c)中,通入四氟化碳和氧气的混合反应气体,其中氧含量为500ppm;3h后通过质谱分析:反应气体的氧气体积含量从500ppm降至0.03ppm。
28.实施例7本实施例提供一种无溶剂干法合成除氧催化剂的方法,它与实施例1中的基本一致,不同的仅是:步骤(a)中,将10mol醋酸镍与10mol对苯二甲酸进行分散预混合,干燥后获得除氧催化剂3.42kg;最终通过微氧传感器分析:反应气体的氧气体积含量从500ppm降至1.3ppm。
29.实施例8本实施例提供一种无溶剂干法合成除氧催化剂的方法,它与实施例7中的基本一致,不同的是:步骤(c)中,通入二氧化碳和氧气的混合反应气体,其中氧含量为500ppm;3h后通过质谱分析:反应气体的氧气体积含量从500ppm降至1.8ppm。
30.实施例9本实施例提供一种无溶剂干法合成除氧催化剂的方法,它与实施例7中的基本一致,不同的是:步骤(c)中,通入氦氧混合反应气体,其中氧含量为500ppm;3h后通过质谱分析:反应气体的氧气体积含量从500ppm降至1.2ppm。
31.实施例10
本实施例提供一种无溶剂干法合成除氧催化剂的方法,它与实施例7中的基本一致,不同的是:步骤(c)中,通入四氟化碳和氧气的混合反应气体,其中氧含量为500ppm;3h后通过质谱分析:反应气体的氧气体积含量从500ppm降至1.2ppm。
32.实施例11本实施例提供一种无溶剂干法合成除氧催化剂的方法,它与实施例1中的基本一致,不同的是:步骤(a)中,将10mol氯化亚铁与10mol对苯二甲酸进行分散预混合,干燥后获得除氧催化剂2.93kg;最终通过微氧传感器分析:反应气体的氧气体积含量从500ppm降至0.7ppm。
33.实施例12本实施例提供一种无溶剂干法合成除氧催化剂的方法,它与实施例11中的基本一致,不同的是:步骤(c)中,通入二氧化碳和氧气的混合反应气体,其中氧含量为500ppm;3h后通过质谱分析:反应气体的氧气体积含量从500ppm降至0.6ppm。
34.实施例13本实施例提供一种无溶剂干法合成除氧催化剂的方法,它与实施例11中的基本一致,不同的是:步骤(c)中,通入氦氧混合反应气体,其中氧含量为500ppm;3h后通过质谱分析:反应气体的氧气体积含量从500ppm降至0.7ppm。
35.实施例14本实施例提供一种无溶剂干法合成除氧催化剂的方法,它与实施例11中的基本一致,不同的是:步骤(c)中,通入氦氧混合反应气体,其中氧含量为500ppm;3h后通过质谱分析:反应气体的氧气体积含量从500ppm降至0.9ppm。
36.实施例15本实施例提供一种无溶剂干法合成除氧催化剂的方法,它与实施例1中的基本一致,不同的是:步骤(a)中,将10mol醋酸钴与10mol均苯三甲酸进行分散预混合,干燥后获得除氧催化剂3.87kg;最终通过微氧传感器分析:反应气体的氧气体积含量从500ppm降至0.09ppm。
37.实施例16本实施例提供一种无溶剂干法合成除氧催化剂的方法,它与实施例7中的基本一致,不同的是:步骤(a)中,将10mol醋酸镍与10mol均苯三甲酸进行分散预混合,干燥后获得除氧催化剂3.86kg;最终通过微氧传感器分析:反应气体的氧气体积含量从500ppm降至2.2ppm。
38.实施例17本实施例提供一种无溶剂干法合成除氧催化剂的方法,它与实施例11中的基本一致,不同的是:步骤(a)中,将10mol氯化亚铁与10mol均苯三甲酸进行分散预混合,干燥后获得除氧催化剂3.36kg;最终通过微氧传感器分析:反应气体的氧气体积含量从500ppm降至1.2ppm。
39.实施例18本实施例提供一种无溶剂干法合成除氧催化剂的方法,它与实施例1中的基本一致,不同的是:步骤(a)中,反应温度为10℃,干燥后获得除氧催化剂3.43kg;最终通过微氧传感器分析:反应气体的氧气体积含量从500ppm降至5ppm。
40.实施例19本实施例提供一种无溶剂干法合成除氧催化剂的方法,它与实施例1中的基本一致,不同的是:步骤(a)中,反应温度为室温,干燥后获得除氧催化剂3.43kg;最终通过微氧传感器分析:反应气体的氧气体积含量从500ppm降至0.01ppm。
41.实施例20本实施例提供一种无溶剂干法合成除氧催化剂的方法,它与实施例1中的基本一致,不同的是:步骤(a)中,反应温度为500℃,干燥后获得除氧催化剂2.83kg;最终通过微氧传感器分析:反应气体的氧气体积含量从500ppm降至0.001ppm。
42.实施例21本实施例提供一种无溶剂干法合成除氧催化剂的方法,它与实施例1中的基本一致,不同的是:步骤(c)中,氮氧混合反应气体中氧气体积含量为1%,6h后通过质谱分析:反应气体的氧气体积含量从1%降至0.005%。
43.实施例22本实施例提供一种无溶剂干法合成除氧催化剂的方法,它与实施例1中的基本一致,不同的是:步骤(c)中,氮氧混合反应气体中氧气体积含量为10%,6h后通过质谱分析:反应气体的氧气体积含量从10%降至0.01%。
44.对比例1本例与实施例1中的基本一致,不同的是:使用的方法为水热合成法:117mg醋酸钴和166mg对苯二甲酸分散于5mln,n
’‑
二甲基甲酰胺(dmf)中,室温下磁力搅拌30min,磁性搅拌至透明溶液后,转至聚四氟乙烯高压釜中,在烘箱内150℃保持12h;自然冷却后,将得到的样品离心,分别用dmf、甲醇和去离子水洗涤3次;最后,将得到的橙色粉末放置真空干燥箱120℃干燥24h,干燥后获得除氧催化剂283mg;最终通过微氧传感器分析:反应气体的氧气体积含量从500ppm降至0.1ppm。
45.上述实施例只为说明本发明的技术构思及特点,其目的在于让熟悉此项技术的人士能够了解本发明的内容并据以实施,并不能以此限制本发明的保护范围。凡根据本发明精神实质所作的等效变化或修饰,都应涵盖在本发明的保护范围之内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1