微流控芯片及利用该微流控芯片进行细胞检测的方法与流程
1.本发明是关于生物医学微流控细胞分选技术领域,特别是关于一种利用阻抗学检测细胞活性的微流控芯片及利用该微流控芯片进行细胞检测的方法。
背景技术:
2.判断细胞活性的一般方法为形态学鉴别和特异性荧光染色检测,这些基本方法在流式细胞术、显微镜技术、图像流式细胞术等方法中大量应用,细胞活性检测也是生命科学、医学诊断非常基础的一种检测应用。
3.形态学检测细胞活性的方法主要应用在显微镜平台或者高端图像流式检测平台,显微镜平台提供了细胞计数板的经典检测方案,但该方法检测通量很低,细胞计数板上检测区域覆盖的细胞样本只占到总加样量的1%不到。高端流式细胞仪提供了全部通量下的细胞形态学检测能力,但该技术方法有赖于非常昂贵的检测器和软件。
4.特异性荧光染色主要基于特异性细胞染料对细胞核或者细胞内部新陈代谢产物进行特异性荧光染色,经过染色后的细胞样本,在流式细胞仪平台上实现了检测。该方法需要大量的样本前操作,且染料等试剂成本和流式细胞仪设备较为昂贵,整体操作要求较高。
5.公开于该背景技术部分的信息仅仅旨在增加对本发明的总体背景的理解,而不应当被视为承认或以任何形式暗示该信息构成已为本领域一般技术人员所公知的现有技术。
技术实现要素:
6.本发明的目的在于提供一种利用阻抗学检测细胞活性的微流控芯片及利用该微流控芯片进行细胞检测的方法,其能够简单高效且更加全面的对细胞进行活性检测。
7.为实现上述目的,本发明的实施例提供了一种微流控芯片,用于细胞检测,所述微流控芯片包括芯片本体以及检测电极组。所述芯片本体内形成有一流体通道,所述流体通道内沿流体的流动方向依次形成有第一检测通道和第二检测通道,所述第二检测通道的直径小于所述第一检测通道的直径;检测电极组包括形成于所述第一检测通道两端的第一组检测电极,以及形成于所述第二检测通道两端的第二组检测电极。
8.在本发明的一个或多个实施方式中,所述第一检测通道以及所述第二检测通道的直径均小于所述流体通道的直径。
9.在本发明的一个或多个实施方式中,所述第一检测通道的直径大于待检测细胞的直径。
10.在本发明的一个或多个实施方式中,所述第二检测通道的直径不大于待检测细胞的直径。
11.在本发明的一个或多个实施方式中,所述第一组检测电极包括检测电极一和检测电极二,所述检测电极一位于所述第一检测通道在流体的流动方向的前端,所述检测电极二位于所述第一检测通道在流体的流动方向的后端。
12.在本发明的一个或多个实施方式中,所述第二组检测电极包括检测电极三和检测
电极四,所述检测电极三位于所述第二检测通道在流体的流动方向的前端,所述检测电极四位于所述第二检测通道在流体的流动方向的后端。
13.在本发明的一个或多个实施方式中,所述第一检测通道的直径为50微米。
14.在本发明的一个或多个实施方式中,所述第二检测通道的的直径为20微米。
15.本发明的实施例还提供了一种利用上述的微流控芯片进行细胞检测的方法,包括:使待检测细胞流经第一检测通道;获取待检测细胞流经第一检测通道时、第一检测通道两端的第一组检测电极的第一检测信号;使待检测细胞流经第二检测通道;获取取待检测细胞流经第二检测通道时、第二检测通道两端的第二组检测电极的第二检测信号;将所述第二检测信号与所述第一检测信号作比较,判断待检测细胞的活性。
16.在本发明的一个或多个实施方式中,获取所述第一检测信号后,根据所述第一检测信号判断待检测细胞的大小。
17.在本发明的一个或多个实施方式中,所述第一检测信号为:待检测细胞通过所述第一检测通道时所引起的阻抗变化信号,其中,该阻抗变化由待检测细胞本身大小所引起;获取所述第一检测信号,根据所述第一检测信号判断待检测细胞的大小,包括:根据第一组检测电极获取的阻抗变化情况,判断通过第一检测通道的待检测细胞的大小。
18.在本发明的一个或多个实施方式中,所述第二检测信号为:待检测细胞通过所述第二检测通道时所引起的阻抗变化信号,其中,该阻抗变化由待检测细胞本身大小以及待检测细胞活性所引起;获取第二检测信号,将第二检测信号与第一检测信号作比较,判断待检测细胞的活性,包括:根据第二组检测电极获取的阻抗变化情况,与第一组检测电极获取的阻抗变化情况做比对,通过比对结果判断通过第二检测通道的待检测细胞的活性。
19.与现有技术相比,本发明实施方式的微流控芯片及细胞检测方法,集成度高,应用成本底,设备简单,是典型的无标记检测方案,相比现有的细胞活性检测技术,无需复杂的细胞样前的手工操作,且提供了更加全面的阻抗学信息,甚至可以联合现有的荧光特异性检测技术,达到更多角度的细胞活性或者其他特性的检测。
附图说明
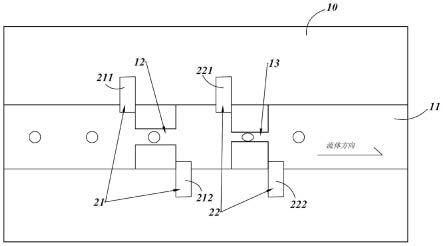
20.图1是本发明一实施方式的微流控芯片的结构示意图;
21.图2是本发明一实施方式的利用微流控芯片进行细胞检测的方法的流程示意图。
具体实施方式
22.下面结合附图,对本发明的具体实施方式进行详细描述,但应当理解本发明的保护范围并不受具体实施方式的限制。
23.除非另有其它明确表示,否则在整个说明书和权利要求书中,术语“包括”或其变换如“包含”或“包括有”等等将被理解为包括所陈述的元件或组成部分,而并未排除其它元件或其它组成部分。
24.如背景技术所言,现有的判断细胞活性的方法为形态学鉴别和特异性荧光染色检测,这两种方法均有赖于非常昂贵的设备或材料或软件,且需要大量的样本前操作,检测方法相对繁琐。
25.为了解决上述问题,本发明创造性的提出了一种利用阻抗学检测细胞活性的微流
控芯片及利用该微流控芯片进行细胞检测的方法,其能够简单高效且更加全面的对细胞进行活性检测。
26.如图1所示,本发明一实施方式提供了一种用于细胞检测的微流控芯片,包括芯片本体10以及检测电极组。
27.芯片本体10内形成有一流体通道11,流体通道11提供了待检测细胞流动的通道。流体通道11内沿流体的流动方向依次形成有第一检测通道12和第二检测通道13,第一检测通道12以及第二检测通道13的直径均远小于流体通道11的直径。
28.检测电极组包括形成于第一检测通道12两端的第一组检测电极21,以及形成于第二检测通道13两端的第二组检测电极22。
29.当待检测细胞流经第一检测通道12以及第二检测通道13时,会引起第一检测通道12以及第二检测通道13的电阻变化,第一检测通道12两端的第一组检测电极21以及第二检测通道13两端的第二组检测电极22分别进行检测,通过信号的放大、采集和分析,从而得到了待检测细胞的大小等阻抗信息。
30.在本实施例中,第二检测通道13的直径小于第一检测通道12的直径。其中,第一检测通道12的直径大于待检测细胞的直径;第二检测通道13的直径不大于待检测细胞的直径。示例性的,第一检测通道12的直径为50微米,第二检测通道13的直径为20微米,待检测细胞在通过第一检测通道12和通过第二检测通道13引起的阻抗变化会有一定的不同。在通过第一检测通道12过程中,待检测细胞直径(一般不超过20微米)较第一检测通道12直径较小,待检测细胞受到的流体的压迫相对较小,发生较小的形变,此时第一检测通道12得到的阻抗信号为细胞的粒径大小成正相关的电阻变化信号。而当待检测细胞经过第二检测通道13时,待检测细胞直径和第二检测通道13直径较为接近,造成待检测细胞受到较大压迫通过该通道,此时待检测细胞整体的形变引起了细胞膜表面的电荷的变化,则在该第二检测通道13测到的电压变化不但包含了待检测细胞本身大小的基本阻抗,也包含了细胞膜由于受压迫引起的表面电荷变化。同时,细胞膜受压迫引起的表面电荷变化在死细胞条件上不会发生或者不显著,则可以由此区分待检测细胞的活性。
31.待检测细胞在通过第一检测通道12时引起的阻抗变化为v1;待检测细胞在通过第二检测通道13时引起的阻抗变化为v2+δv2。其中,v1、v2是待检测细胞本身大小引起的阻抗变化,δv2指的是待检测细胞受压迫引起的细胞膜表面电荷的变化信号。如果细胞已经死亡,则δv2信号为非常微弱的变化或者无变化。
32.上位机通过时间轴的标定,将所有通过第一检测通道12和第二检测通道13产生的阻抗变化关系对应起来,并通过第一检测通道12的信号判断细胞大小,通过第二检测通道13的信号判断该大小细胞条件下,是否发生了细胞膜电荷的变化,通过该变化水平判断待检测细胞的活性。
33.在本实施例中,第一组检测电极21包括检测电极一211和检测电极二212,检测电极一211位于第一检测通道12在流体的流动方向的前端,检测电极二212位于第一检测通道12在流体的流动方向的后端。第二组检测电极22包括检测电极三221和检测电极四222,检测电极三221位于第二检测通道13在流体的流动方向的前端,检测电极四222位于第二检测通道22在流体的流动方向的后端。
34.如图2所示,本发明的实施例还提供了一种利用上述的微流控芯片进行细胞检测
的方法,包括:s1,使待检测细胞流经第一检测通道;s2,获取待检测细胞流经第一检测通道时、第一检测通道两端的第一组检测电极的第一检测信号,根据第一检测信号判断待检测细胞的大小;s3,使待检测细胞流经第二检测通道;s4,获取取待检测细胞流经第二检测通道时、第二检测通道两端的第二组检测电极的第二检测信号;s5,将第二检测信号与第一检测信号作比较,判断待检测细胞的活性。
35.第一检测信号为:待检测细胞通过第一检测通道时所引起的阻抗变化信号,其中,该阻抗变化由待检测细胞本身大小所引起。在通过第一检测通道12过程中,待检测细胞直径(一般不超过20微米)较第一检测通道12直径较小,待检测细胞受到的流体的压迫相对较小,发生较小的形变,此时第一检测通道12得到的阻抗信号为细胞的粒径大小成正相关的电阻变化信号。获取第一检测信号,根据第一检测信号判断待检测细胞的大小,具体可以包括:根据第一组检测电极获取的待检测细胞通过第一检测通道时产生的阻抗变化情况,判断通过第一检测通道的待检测细胞的大小。
36.第二检测信号为:待检测细胞通过第二检测通道时所引起的阻抗变化信号,其中,该阻抗变化由待检测细胞本身大小以及待检测细胞活性所引起。当待检测细胞经过第二检测通道13时,待检测细胞直径和第二检测通道13直径较为接近,造成待检测细胞受到较大压迫通过该通道,此时待检测细胞整体的形变引起了细胞膜表面的电荷的变化,则在该第二检测通道13测到的电压变化不但包含了待检测细胞本身大小的基本阻抗,也包含了细胞膜由于受压迫引起的表面电荷变化。获取第二检测信号,将第二检测信号与第一检测信号作比较,判断待检测细胞的活性,具体可以包括:根据第二组检测电极获取的待检测细胞通过第二检测通道时产生的阻抗变化情况,将其与第一组检测电极获取的待检测细胞通过第一检测通道时产生的阻抗变化情况做比对,通过比对结果判断通过第二检测通道的待检测细胞是否发生了细胞膜电荷的变化,并通过该变化水平判断待检测细胞的活性,如果细胞已经死亡,则待检测细胞受压迫引起的细胞膜表面电荷的变化信号为非常微弱的变化或者无变化。
37.与现有技术相比,本发明实施方式的微流控芯片及细胞检测方法,集成度高,应用成本底,设备简单,是典型的无标记检测方案,相比现有的细胞活性检测技术,无需复杂的细胞样前的手工操作,且提供了更加全面的阻抗学信息,甚至可以联合现有的荧光特异性检测技术,达到更多角度的细胞活性或者其他特性的检测。
38.前述对本发明的具体示例性实施方案的描述是为了说明和例证的目的。这些描述并非想将本发明限定为所公开的精确形式,并且很显然,根据上述教导,可以进行很多改变和变化。对示例性实施例进行选择和描述的目的在于解释本发明的特定原理及其实际应用,从而使得本领域的技术人员能够实现并利用本发明的各种不同的示例性实施方案以及各种不同的选择和改变。本发明的范围意在由权利要求书及其等同形式所限定。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1