一种微流控芯片及其在分离鸭肌原细胞上的应用
本发明涉及细胞分离领域,特别涉及一种微流控芯片及其在分离鸭肌原细胞上的应用。
背景技术:
1、鸭肌原细胞是鸭骨骼肌形成的物质基础,在骨骼肌的发生、分化和成熟三个阶段中,成肌细胞起关键作用。鸭肌原细胞的研究在禽类养殖、禽类疾病诊断、治疗和细胞生理、基因调控等研究方面具有重要意义。鸭肌原细胞分离技术是进行鸭肌原细胞水平研究的基础,用经济简便的方法获得大量鸭肌原细胞是研究的关键。
2、目前鸭肌原细胞的分离方法有流式细胞术分离法、差速离心法等。流式细胞术分离法根据流体动力聚焦效应,流式细胞术将细胞排成一列形成细胞流,利用光激发并捕捉细胞特定的信号进行细胞分离,但流式细胞术需依靠流式细胞仪,该仪器结构复杂,价格昂贵;差速离心法利用肌原细胞与其他细胞类型在密度上的差异,通过不同离心速度和离心时间,将肌原细胞与其他细胞类型分离,该方法简单易行,但分离效果有限。
技术实现思路
1、鉴以此,本发明提出一种微流控芯片及其在分离鸭肌原细胞上的应用。
2、本发明的技术方案是这样实现的:
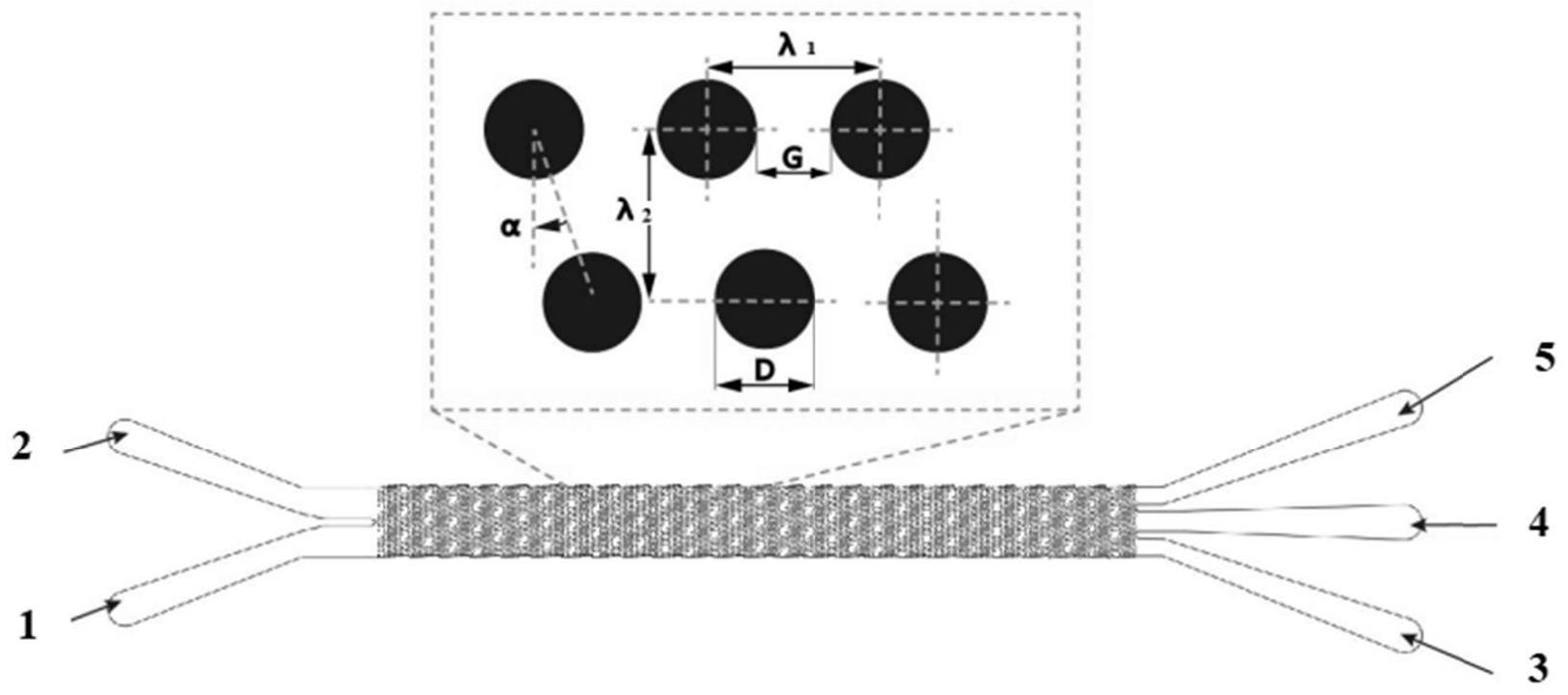
3、一种微流控芯片,由基体和载玻片两部分构成;所述基体由进样通道、输出通道和分离通道构成;所述进样通道包括入口ⅰ和入口ⅱ,输出通道包括出口ⅰ、出口ⅱ和出口ⅲ。
4、进一步的,所述基体材质为聚二甲基硅氧烷。
5、进一步的,所述进样通道和输出通道的深度为40~70μm;所述分离通道由分离微柱构成;分离通道的宽度为1~2mm,长度为3~5mm。
6、进一步的,所述微流控芯片的临界尺寸为10μm。
7、进一步的,所述分离微柱为圆形微柱或三角形微柱。
8、进一步的,所述圆形微柱的直径为47~51μm,偏转角为2~3°,纵向中心距为89~91μm,横向中心距为89~91μm,微柱间隙为38~42μm,微柱的偏转周期为n=21~23;所述三角形微柱的边长为53~56μm,偏转角4~5°,纵向中心距89~90μm,横向中心距89~90μm,微柱间隙39~41μm,微柱的偏转周期n=11~13。
9、微流控芯片在分离鸭肌原细胞上的应用。
10、微流控芯片在分离鸭肌原细胞上的应用,包括以下步骤:
11、(1)取微流控芯片,浸润、去除气泡后备用,入口ⅰ和入口ⅱ与两个注射器分别连接,出口ⅰ、出口ⅱ和出口ⅲ分别与三个收集瓶连接;
12、(2)从入口ⅰ通入含鸭肌原细胞的悬浊液、入口ⅱ通入鞘液,调整悬浊液和鞘液的流速使其通过分离通道,经出口ⅰ、出口ⅱ、出口ⅲ分别流入三个收集瓶,得到鸭肌原细胞。
13、进一步的,所述含鸭肌原细胞的悬浊液、鞘液的体积比为1~2:1~2。
14、进一步的,步骤(2)中,所述悬浊液和鞘液的流速为10~20μl/min。
15、与现有技术相比,本发明的有益效果是:
16、(1)本发明的微流控芯片不仅灵敏度高,分离效果好,而且对细胞无损伤,保证鸭肌原细胞的完整性和生理性。
17、(2)本发明的微流控芯片体积小、样品试剂使用量小,价格便宜,操作简便,易于大规模生产和使用。
18、(3)本发明首次报道了微流控芯片在分离鸭肌原细胞上的应用,为大量制备鸭肌原细胞、研究鸭肌原细胞增殖和基因调控提供了基础。
技术特征:
1.一种微流控芯片,其特征在于:由基体和载玻片两部分构成;所述基体由进样通道、输出通道和分离通道构成;所述进样通道包括入口ⅰ和入口ⅱ,输出通道包括出口ⅰ、出口ⅱ和出口ⅲ。
2.如权利要求1所述一种微流控芯片,其特征在于,所述基体材质为聚二甲基硅氧烷。
3.如权利要求1所述一种微流控芯片,其特征在于,所述进样通道和输出通道的深度为40~70μm;所述分离通道由分离微柱构成;分离通道的宽度为1~2mm,长度为3~5mm。
4.如权利要求1所述的微流控芯片,其特征在于,所述微流控芯片的临界尺寸为10μm。
5.如权利要求3所述的微流控芯片,其特征在于,所述分离微柱为圆形微柱或三角形微柱。
6.如权利要求5所述的微流控芯片,其特征在于,所述圆形微柱的直径为47~51μm,偏转角为2~3°,纵向中心距为89~91μm,横向中心距为89~91μm,微柱间隙为38~42μm,微柱的偏转周期为n=21~23;所述三角形微柱的边长为53~56μm,偏转角4~5°,纵向中心距89~90μm,横向中心距89~90μm,微柱间隙39~41μm,微柱的偏转周期n=11~13。
7.如权利要求1-6任一项所述的微流控芯片在分离鸭肌原细胞上的应用。
8.如权利要求7所述的应用,其特征在于,包括以下步骤:
9.如权利要求8所述的应用,其特征在于,所述含鸭肌原细胞的悬浊液、鞘液的体积比为1~2:1~2。
10.如权利要求8所述的应用,其特征在于,步骤(2)中,所述悬浊液和鞘液的流速为10~20μl/min。
技术总结
本发明提供一种微流控芯片及其在分离鸭肌原细胞上的应用,所述的微流控芯片由基体和载玻片两部分构成;所述基体由进样通道、输出通道和分离通道构成;所述进样通道包括入口Ⅰ和入口Ⅱ,输出通道包括出口Ⅰ、出口Ⅱ和出口Ⅲ。本发明中应用微流控技术分离鸭肌原细胞,不仅具有通量高、反应快、集成度高和灵敏度高、不需要额外施加作用力场的优点,而且降低样品和试剂使用量、操作简便、价格低廉。
技术研发人员:顾丽红,刘宏举,史留勇,郑心力,晁哲
受保护的技术使用者:海南省农业科学院畜牧兽医研究所
技术研发日:
技术公布日:2024/1/16
- 还没有人留言评论。精彩留言会获得点赞!