一种循环连续电解铝酸钠溶液制备氧化铝的方法与流程
本发明属于氧化铝生产技术领域,尤其涉及一种氧循环连续电解铝酸钠溶液制备氧化铝,属于有色金属工业和化学工业领域。
发明背景
铝及其铝合金在导电、导热、抗磁性等方面拥有很多优秀的特性,成为当前最广泛应用的有色金属,其电解原料——氧化铝的产量和消耗量也是逐年增长。据统计,2014年上半年,全球氧化铝产量为5346万吨,其中我国氧化铝产量为2490万吨,占全球总产量的46.58%。
目前国内外氧化铝生产的方法主要有拜耳法(Bayer)、烧结法和联合法。拜耳法作为世界氧化铝生产的经典方法,广泛应用于从铝土矿中制备氧化铝。该方法的原理是利用铝酸钠溶液自身水解体系的平衡,也就是在高温高压条件下,实现NaOH-NaAlO2溶液从铝土矿中浸出氧化铝的溶出过程,然后在较低温度下,高浓度的NaAlO2溶液水解为NaOH和氢氧化铝产品。分解后得到NaOH-NaAlO2混合溶液返回溶解工序继续下一批矿物的浸出,沉淀得到得氢氧化铝经过焙烧得到氧化铝产品。虽然拜尔工艺成熟,具有过程简单、能耗低、产品质量高、成本低等优点,但是由于受水解相图限制,分解率仅有46-50%,导致循环液中仍有大量铝酸钠没有分解为氢氧化铝,并且该方法一般限于处理富铝的铝矿,即含硅量比较低的高品位铝土矿(A/S>8),不适合我国高硅铝土矿的处理。近年来,伴随着进口矿物和人力成本价格的增高,如何实现氧化铝生产的节能增效已经成为 了氧化铝行业的重要研究方向。
直接电解铝酸钠溶液制备氧化铝的研究一直曾广受人们关注。其中比较典型工作如中南大学陶涛等(铝酸钠溶液离子膜电解方法制备氢氧化铝,中南大学学报,2007,38(1),102-106)采用离子膜电解种分铝酸钠溶液得到氢氧化铝。该工作采取钝化钛板为阳极、不锈钢为阴极直接电解铝酸钠溶液。阳极析氧过程产生的H+使铝酸钠溶液酸化,进而析出氢氧化铝。阴极析氢过程产生OH-提高NaOH溶液浓度。研究者们在论文中表明该方法在3V的电解槽压下,经过7小时电解,可以种分48.89%的氧化铝,而同等条件的拜尔法仅有1.58%。该工艺经过改进和两次种分后,可以达到71.7%的种分效率。该方法存在的主要问题如下:
1,电解过程槽压高达3V,超过1.7V经济电解水平,导致电耗成本较高。
2,电解过程中阳极析氧同时不断酸化,导致部分氢氧化铝直接絮凝在阳离子交换膜上,堵塞阳离子交换膜的离子通道,使得离子膜寿命提前终结,并加剧了电解过程离子扩散的阻力,进一步增加能耗。
为了克服铝酸钠直接电解产生的氢氧化铝絮凝物堵塞离子交换膜的问题,北京化工大学钮因健等提出了“一种碱溶碳分生产氧化铝的工艺ZL200710178670.2”,主要原理是利用电解碳酸钠溶液阳极产生的NaHCO3溶液来酸化铝酸钠溶液,得到氢氧化铝和碳酸钠,该碳酸钠溶液经过分离氢氧化铝后可以继续返回电解。阴极产生的氢氧化钠溶液可以再次用于铝土矿的浸出过程,从而实现原料的循环利 用。该方法存在的问题是:
1,需要增加额外碳酸钠作为中间过渡介质,增加了物料循环量。
2,由于铝酸钠溶液含有过量的NaOH,该工艺在利用NaHCO3来酸化NaAlO2过程中,需要额外的NaHCO3来中和这部分NaOH,导致能耗和物料循环压力增加。
2,电解能耗较高,电解效果在100mA/cm2的电流密度下槽压在2.6V左右,导致系统能耗较高,每吨氧化铝的电解能耗高达1700度电,大大增加了生产成本。
虽然离子膜直接电解铝酸钠或者间接电解碳酸钠工艺可以显著提高铝酸钠溶液的种分效率。如何从现有两种工艺出发,克服现有工艺的缺点,发明一种新的节能高效的铝酸钠电解工艺成为氧化铝行业亟待攻克的技术关键。
技术实现要素:
本发明是针对拜耳法、离子膜电解铝酸钠溶液、碱溶碳分法等氧化铝工艺所存在的不足,提供一种既能显著提高氧化铝种分效率又可以实现碱液循环利用,且槽压较低、能源清洁的生产工艺,并最终得到质量高的氢氧化铝产品。
一种连续循环连续电解铝酸钠溶液制备氧化铝的方法,其特征在于,包括以下步骤:
(1)在阳极室通入铝酸钠溶液并在阳极发生氧化反应,在阴极室通入氢氧化钠溶液并在阴极发生还原过程;
(2)步骤(1)电解后的铝酸钠溶液经种分后析出氢氧化铝,分 离氢氧化铝后的铝酸钠母液返回阳极室继续电解;如此循环;所得氢氧化铝经过煅烧得到氧化铝。
上述优选,在每循环过程中,基于铝酸钠溶液中Na2O-Al2O3-H2O三相平衡的连续电解方式,通过控制电解深度(如改变电流密度、电流时间等条件),在氢氧化铝刚好析出时停止电解反应,即为临界点时停止电解反应,然后进行种分。在电解过程铝酸钠溶液苛性比αk不断变小,在氢氧化铝刚好析出时对应的铝酸钠溶液状态的αk,即为临界点的K0。
所述的铝酸钠溶液电解过程的临界值K0为铝酸钠中的[Na2O]:[Al2O3]的质量比,温度为T℃,铝酸钠溶液中[Na2O]质量浓度为Nk,苛性比αk=1.5~3.0时,在达到临界点时临界值K0其特征如下:(1)当T1<T≤T2,100<Nk≤200g/L时,K0为(1.7-T1/200)-(1.95-T2/200);
(2)当T1<T≤T2,200<Nk≤300g/L时,K0为(1.65-T1/200)-(1.9-T2/200);
(3)当T1<T≤T2,300<Nk≤400g/L时,K0为(1.55-T1/200)-(1.8-T2/200);
T1、T2的范围是40℃~100℃。
上述种分是将电解后的铝酸钠溶液降温并搅拌促进氢氧化铝的析出。
优选电解过程采用恒温恒流的电解方式,电解装置采用的是循环 装置。
电解后阴极室氢氧化钠溶液可用于浸渍铝矿制备铝酸钠溶液,继续电解。
优选在上述循环电解的过程中,阳极液还可以不断补充新的铝酸钠溶液,此新的铝酸钠溶液指的是未曾电解过的铝酸钠溶液。即铝酸钠溶液来源于上一循环电解后分离氢氧化铝得到的母液和浸渍铝土矿得到未电解过的铝酸钠溶液。
所述的阳极氧化反应是指铝酸钠溶液在阳极发生析氧反应或者来自外部的氢气在阳极发生氧化反应;所述的阴极还原反应是指NaOH溶液中的水发生阴极析氢过程,或者来自外部的氧气发生氧还原反应。
所述的阳极氧化反应和阴极还原反应,包括以下几种情况:
(1)当铝酸钠溶液在阳极发生析氧过程的氧化反应,且NaOH溶液在阴极发生析氢反应时,电解过程分别在阳极和阴极获得氧气和氢气;
(2)当铝酸钠溶液在阳极发生析氧过程的氧化反应,且NaOH溶液在阴极发生氧气的还原反应时,阳极产生的氧气可以导入到阴极消耗,电解过程为氧循环过程;
(3)当铝酸钠溶液和外部的氢气发生氢气的氧化反应,且NaOH溶液在阴极发生析氢还原反应时,阴极产生的氢气导入到阳极消耗,电解过程为氢循环过程。
一种连续循环连续电解铝酸钠溶液制备氧化铝的方法,具体情况如下:
(1)将氢氧化钠溶液a浸渍铝矿制备铝酸钠溶液,然后将铝酸钠溶液和氢氧化钠溶液b分别引入到氧循环装置的阳极室和阴极室,恒温恒流进行电解,电解到临界点时停止;在电解的过程中,铝酸钠溶液在阳极发生氧化反应消耗OH-,NaOH浓度降低,降低了Al2O3在阳极室铝酸钠溶液中的溶解度,使得αk不断变小;阴极液氢氧化钠溶液b在阴极发生还原反应生成OH-,氢氧化钠溶液b碱度不断升高;(2)当步骤(1)电解到临界点时,停止电解;将阳极液导出直接搅拌并利用温差进行种分促进氧化铝的析出,固液分离后的母液,母液由于氧化铝的析出,母液αk相对于临界点时的αk变大,母液返回步骤(1)阳极室继续电解;阴极液碱度作为返回步骤(1)作为氢氧化钠溶液a浸渍铝矿制备铝酸钠溶液;
(3)不断重复步骤(1)和(2)的电解和种分过程;一般直至阳极液没有氧化铝的析出。
氢氧化钠溶液a的浓度大于氢氧化钠溶液b的浓度。
电解过程为可控深度电解,其电解时间优选以达到阳极室电解液中氢氧化铝刚好不析出的临界点为止,此时的阳极室电解液直接在分解槽中进行种分。
电解过程中不仅是利用铝酸钠溶液中氢氧化钠浓度的降低促使氢氧化铝的析出,而且还利用了晶种、搅拌和温差等外界因素加速氢氧化铝的析出,根据铝酸钠溶液的相图,升温可促使氧化铝在氢氧化 钠溶液中溶解,同理,降温则利于氢氧化铝的析出,搅拌条件更利于晶体的生长和聚沉。
采用氧循环连续电解铝酸钠溶液生产氢氧化铝为例,其基本原理及工艺简单描述如下:
作为阳极电解溶液,碱性条件下在阳极电极表面发生OH-氧化生成O2:
4OH--4e→O2+2H2O(阳极室)
或者H2氧化中和OH-:
H2+2OH--2e→2H2O(阳极室)
阳极室电解液由于OH-减少,从而达到阳极液碱度降低的目的,电解结束后阳极室电解液需要进入分解槽,利用搅拌和温度差的条件,析出氢氧化铝。所以在电解过程中需要控制其电解时间,基于Na2O-Al2O3-H2O三相平衡的相图,以及所探究的不同氢氧化铝开始析出的氢氧化钠浓度,将电解结果刚好控制在此临界点,如此可防止氢氧化铝固体对电极和离子交换膜的粘覆。
电解装置中阴极室电解液为低浓度的氢氧化钠溶液,发生还原反应:
O2+2H2O+4e→4OH-(阴极室)
或者:
2H2O→H2+2OH-(阴极室)
阴极室电解液由于还原生成OH-,达到了阴极液碱度升高的目的。电解结束后的阴极室氢氧化钠溶液可用于氧化铝生产工艺中的氧 化铝浸出工序,碱液的循环使用,不仅可以节省资源,也可以达到节能减耗的目标。
而阳极富余的钠离子根据离子平衡原则需要迁移至阴极,所以需要使用阳离子交换膜,达到钠离子迁移的目标:
Na+(阳极室)→Na+(阴极室)
从上述阳极、阴极的电极反应看出,采用循环装置连续电解可减小槽压。
为了确保连续电解制备氧化铝工艺在槽压较低的条件下可以长时间稳定的进行,且保持节电节能效果,电解条件需要控制:过程中电解液温度范围为45℃~95℃,电解过程中电流密度为10~100mAcm-2;电解时间是以所探究的不同浓度氢氧化铝刚好不析出时氢氧化钠浓度临界点为依据;阳极室通入的电解液铝酸钠浓度控制在[Na2O]=100~400g/L,苛性比αk=1.5~3.0;阴极室通入的电解液为浓度不大于10M NaOH溶液;阳极电解液初始αk为1.5~3.0,首次电解终点时αk为1.1~1.6,然后进行种分固液分离后铝酸钠溶液的αk回到1.50~3.0,然后阳极液返回电解槽继续电解,电解至再次的临界点,苛性比为1.2~1.8;电解时不增加额外新的偏铝酸钠溶液时,一般下一次循环时临界点时的αk大于上一循环时临界点时的αk。
本发明一种连续电解铝酸钠溶液制备氧化铝的方法,电解过程:
1,恒温恒流电解时,阳极液为铝酸钠溶液,溶液中溶质有NaOH和NaAlO2,电解过程中阳极发生析氧反应消耗OH-生成O2,NaOH浓度降低,从而降低了Al2O3在碱液中的溶解度,析出氢氧化铝固体。
2,阴极液为相对低浓度的NaOH溶液,阴极发生O2的还原反应生成OH-,所以阴极液碱度得到较大幅度升高,可用于铝矿浸出工序,与氧化铝反应生成铝酸钠,形成阴极液的循环再利用。
3,电解结束后,阳极液在分解槽中进行种分,固液分离后的母液中溶质仍为NaOH和NaAlO2,返回阳极室继续电解,形成阳极液连续电解,提高分解率。
本发明提供的连续电解铝酸钠溶液制备氧化铝的方法,其优点在于:
1.单位质量碱液的溶出效率提高。拜耳法溶出铝土矿中氧化铝时用的是种分后的铝酸钠溶液,其中含有约50%未分解的铝酸钠;而本发明中溶出氧化铝的是种分后的铝酸钠溶液(其中大约含有少量未分解的铝酸钠)以及由于电解碱度升高的阴极液氢氧化钠溶液,所以理论上每千克Na2O可溶出0.89Kg氧化铝,大于拜耳法中每千克Na2O可溶出的氧化铝。
2.氧化铝浸出工序中用溶出剂氢氧化钠溶液通过氧循环电解方法实现循环使用的目的。
3.阳极铝酸钠溶液实现连续电解,不仅可以减少流入铝矿浸出时溶液中的氧化铝含量,而且可以提高分分解率。
4.利用氢氧化铝析出临界点,可避免电解过程中析出的氢氧化铝损伤离子交换膜,影响循环电解过程的正常进行。
附图说明
图1为氧循环电解铝酸钠溶液的氧循环装置图(a)及流程图(b);
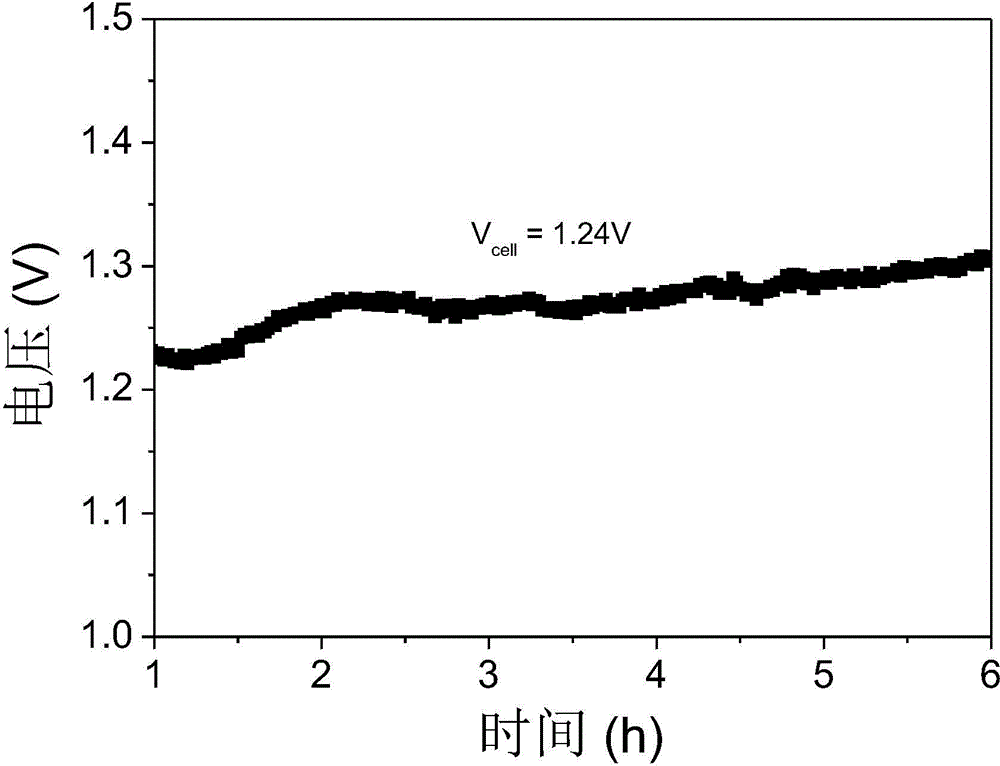
图2实施例1阳极液为铝酸钠溶液[Na2O]=308g/L,苛性比2.0电解温度85℃、电流密度为50mA cm-2时的槽压时间图;
图3实施例2阳极液为[Na2O]=189g/L,[Al2O3]=193g/L,电解温度为45℃,电流密度为50mA cm-2时槽压时间图;
图4实施例2阳极液为[Na2O]=189g/L,[Al2O3]=193g/L,电解温度为45℃,电流密度为50mA cm-2时产品的扫描电子显微镜图。
具体实施方法
以氧循环装置为例,装置见图1,并且在阳极产生的氧气作为阴极所需氧气的来源。
氧循环装置中,阳极为具有高催化活性、耐腐蚀非牺牲型析氧阳极,阴极为电催化性能高的氧阴极。其电解槽被钠离子交换膜分为阳极室和阴极室,钠离子交换膜为Nafion离子膜。如阳极基体为钛基或镍基,其表面催化剂主要种类有Co3O4、NiCo2O4、RuO2、IrO2的一种或几种,或者同时加入Ni、Co、Sn、Fe、La系、Ta中的一种或者几种进行复合。阴极催化剂主要有贵金属催化剂铂、铂碳、铂合金、钙钛矿型氧化物、金属有机螯合物等的一种。
在进行氧循环电解之前,首先要确定一下该氢氧化铝浓度下的临界点,以确定电解时间,使得氢氧化铝刚好不析出。进一步,用高浓度的氢氧化钠溶液在加热状态下溶解铝矿,将矿中氧化铝浸出,出液为铝酸钠溶液,由于在实际电解过程中所需铝酸钠溶液浓度控制在[Na2O]=100~400g/L,苛性比αk=1.5~3.0,所以出液需要经过稀释, 达到所需浓度,然后通入阳极室。
一种氧循环连续电解铝酸钠溶液生产氧化铝,是将铝酸钠溶液(将浓度相对较高的氢氧化钠溶液浸渍铝矿制备铝酸钠溶液,)、相对低浓度的NaOH溶液通入析氧阳极、氧电极为阴极、以对钠离子具有选择性的阳离子交换膜的电解槽中的阳极室、阴极室。恒温恒流电解后阳极室碱度降低的铝酸钠溶液在分解槽中种分,搅拌的条件下自然降温析出氢氧化铝;阴极液碱度升高的氢氧化钠溶液用于氧化铝的浸出,实现氢氧化钠溶液的再利用。而阳极液经过固液分离后,仍返回阳极室继续电解,重复多次电解、种分的过程,实现连续电解。其中电解液温度范围为45℃~95℃,电解过程中电流密度为10~100mAcm-2。
而寻找此临界点的方法有两种,电化学方法和化学方法。
电化学方法,即利用恒流电解的方法,可利用氧循环装置,也可使传统阴极析氢、阳极析氧的电极电解装置,也可以使用氢循环的电解装置。本发明以氧循环电解装置为例需找一定苛性比的铝酸钠溶液中氧化铝析出的临界点,其具体的操作步骤如下:
A、将待电解铝酸钠溶液,利用滴定法测得其中每种组分的具体浓度,以及αk的值;并配置一定浓度的氢氧化钠溶液;
B、将步骤A铝酸钠溶液、氢氧化钠溶液分别通入阳极室、阴极室,在一定的电解温度、电流密度下进行恒温恒流电解,αk不断变小;
C、当溶液刚出现浑浊现象时停止电解;
D、取出步骤C的阳极液,测定此时铝酸钠溶液的αk值,即为此待电解铝酸钠溶液在该电解温度时临界点的苛性比。
优选步骤A中铝酸钠溶液和氢氧化钠溶液与待电解的铝酸钠溶液和氢氧化钠溶液浓度分别相同,步骤B的电解温度、电流密度分别与氧循环连续电解铝酸钠溶液制备氧化铝的电解温度、电流密度相同。
而化学方法的基本原理与氢循环电解相似,是利用铝酸钠溶液酸化,降低溶液中氢氧化钠的浓度,其具体的操作步骤如下:
A、配制待电解铝酸钠溶液,利用滴定法测得其中每种组分的具体浓度,以及αk的值;已知浓度的稀酸溶液,例如HCl、HNO3、H2SO4等。
B、恒定铝酸钠溶液的温度,利用蠕动泵将稀酸溶液缓慢注入铝酸钠溶液中,同时并强烈搅拌,这是为了防止由于局部酸化现象而引起氢氧化铝聚沉现象,在与酸反应过程中αk不断变小。
C、当铝酸钠溶液中刚出现浑浊现象时停止加入酸溶液;
D、测定步骤C此时铝酸钠溶液的αk值,即为步骤(1)中待电解铝酸钠溶液临界点时的苛性比。
其中达到临界点时根据电解时间计算的,根据临界点计算电解时间的方法,是以测得的临界点时的苛性比为依据,得到临界点时即电解结束时钠离子的浓度,再结合初始铝酸钠溶液中游离态NaOH浓度、离子交换膜Na+的迁移率、电流密度等,计算出电解时间。
为了更好的说明本发明的结果特征,下面通过具体的实施例进行 说明,但本发明并不限于以下实施例。
实施例1
配制一定浓度的铝酸钠溶液,离心取得上清液,测定铝酸钠溶液的各组分的含量:其中[Na2O]=308g/L,[Al2O3]=253g/L,苛性比是2.0。将此铝酸钠溶液恒温至85℃,用蠕动泵将0.01M HCl溶液缓慢滴加如铝酸钠溶液中,转速为6r/min,为了防止由于局部酸化而导致聚沉,所以在加入盐酸的同时需要强烈搅拌。由于盐酸溶液浓度较低,所以需要耗时较长,并不断观察溶液现象,考虑到加入盐酸出现的体积变化,且由于在85℃恒温,水溶液也会出现挥发现象,所以在加酸的过程中应注意体积变化,需要时可加入等温度的蒸馏水,尽量减少溶液体积变化属对氢氧化铝析出的影响。当有稍微的浑浊出现时,立即停止加入盐酸,认为达到临界点,利用化学滴定法分析此时铝酸钠溶液中各组分的含量,[Na2O]=179.9g/L,苛性比为1.17。
以Ti/NiCo2O4为阳极,氧电极为阴极,利用氧循环装置进行电解。本实施例中阳极液为铝酸钠溶液(将氢氧化钠溶液浸渍铝矿制备铝酸钠溶液,其中[Na2O]=308g/L,[Al2O3]=253g/L,苛性比是2.0,阴极液为质量浓度20%NaOH溶液,电解温度为85℃,电解时电流密度为50mA cm-2,电解时间为6h,([Na2O]=179.9g/L和苛性比临界点K0为1.17,再结合初始铝酸钠溶液中游离态NaOH浓度、离子交换膜Na+的迁移率、电流密度等,计算出电解时间,以下实施例同理),本实施例中槽压结果如图2,槽压大约为1.24V,其氢氧化铝产品粒径为2~10μm,然后800℃煅烧后得到氧化铝,质量分数为99.64%。 固液分离后的母液苛性比为2.07,返回阳极室继续电解,阴极液可用于浸出氧化铝,配成[Na2O]=308g/L,[Al2O3]=253g/L的氧化铝溶液,通入阳极室进行电解。
实施例2
以Ti/NiCo2O4为阳极,氧电极为阴极,利用氧循环装置进行电解,阳极液为[Na2O]=189g/L,[Al2O3]=193g/L的铝酸钠溶液,体积为200mL,阴极液为10%氢氧化钠溶液,电解温度为65℃,电流密度为50mA cm-2,在电解过程中每隔30min~1h取点测定其苛性比,在出现氢氧化铝细小微粒时停止电解,其电解时间为6h,电解过程中槽压与时间的关系如图3,第一次电解6h达到临界点K0为1.45,槽压为1.43V,种分时自然降至室温并搅拌,可得到19.96g氢氧化铝,焙烧后氧化铝含量达到99.64%;固液分离后铝酸钠溶液苛性比为2.19,母液返回阳极室继续电解,槽压相比降低0.1V。经过连续两次循环电解后,铝酸钠的分解率达到75%以上。而阴极液导出用于配置[Na2O]=189g/L,[Al2O3]=193g/L的铝酸钠溶液,通入阳极室电解。
实施例3
以泡沫镍为阳极、氧电极为阴极,电极有效使用面积为2.4*3.4cm2,采用氧循环电解装置电解,阳极液为[Na2O]=189g/L、[Al2O3]=149g/L、苛性比为2.0的铝酸钠溶液,体积为100mL,阴极液为10%氢氧化钠溶液。电解液温度分别为55℃,化学法测定其临界点值K0为1.46,电解过程中恒流电解的电流密度为50mA cm-2,通过计算得到时间约为10h,电流效率为85%,种分后得到8.19g氢氧 化铝,其电镜图如图4所示,可看出样品具有较好的分散性,粒径在2~8μm。焙烧后得到的产品氧化铝含量为99.7%。固液分离后的母液苛性比为2.09,返回阳极室继续电解阴极液浓度升高可用于配制[Na2O]=189g/L,[Al2O3]=149g/L的铝酸钠溶液,通入阳极室进行连续电解。
实施例4
以氢电极为阳极、泡沫镍电极为阴极,电极有效使用面积为2.4*3.4cm2,采用氢循环电解装置电解,阳极液为[Na2O]=249g/L、[Al2O3]=228g/L、苛性比为1.8的铝酸钠溶,体积为200mL,阴极液为15%氢氧化钠溶液。电解液温度分别为90℃,化学法测定其临界点值K0为1.23,电解过程中恒流电解的电流密度为50mA cm-2,通过计算得到时间约为17.7h,电流效率为89%,种分后得到13.95g氢氧化铝,焙烧后得到的产品氧化铝含量为99.6%。固液分离后的母液苛性比2.7返回阳极室继续电解阴极液浓度升高可用于配制[Na2O]=249g/L,[Al2O3]=228g/L的铝酸钠溶液,通入阳极室进行连续电解。
- 还没有人留言评论。精彩留言会获得点赞!