一种检测生鲜乳中4种巴比妥类镇静药物的方法与流程
本发明属于食品领域,涉及一种食品的安全检测方法,具体来说是一种检测生鲜乳中4种巴比妥类镇静药物的方法。
背景技术:
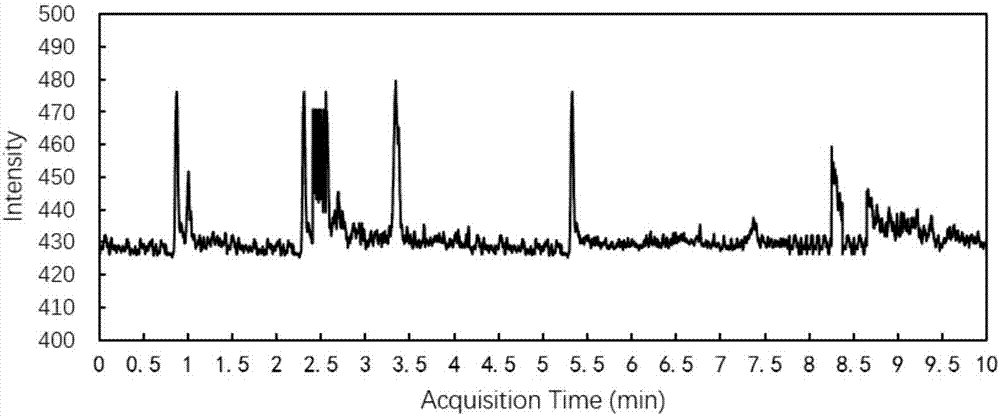
:巴比妥类(barbiturates)是普遍性中枢抑制药,包括苯巴比妥(phenobarbital)、戊巴比妥(pentobarbital)、异戊巴比妥(amobarbital)、司可巴比妥(secobarbital)等安眠镇静药物,兽药临床用作镇静剂和化学保定,可引起近似生理性睡眠,主要表现在对中枢神经系统的抑制,还能抑制延脑的呼吸中枢及血管运动中枢。抑制中枢神经的深度,一般与剂量成比例。小剂量起镇静作用,中等剂量有催眠作用,大剂量起麻醉作用。量大时对循环系统和呼吸系统也产生抑制作用,服用过量易造成急性死亡,致死期一般多在服药后10天左右,长期服用易产生药物积累,导致死亡。人食入残留有巴比妥类药物的动物组织,可导致头晕、恶心、呕吐,长期摄入可能产生耐受性和成瘾性。许多国家严禁将巴比妥药物用于人类,也禁止其作为饲料添加剂,我国的农业部第178号公告中就明确规定严禁将巴比妥、苯巴比妥、苯巴比妥钠、戊巴比妥、戊巴比妥钠添加到饲料和动物饮用水中。此外,兽药临床规定了巴比妥药物的休药期,防止动物体内该类药物蓄积浓度过高而影响食用者安全。牛奶的安全质量问题关系国计民生,其中生鲜乳的质量控制是牛奶生产的重要前提。然而,从我国国内养殖环境来看,在我国大部分地区,特别是广大农村地区的动物和饲料生产过程中仍存在使用违禁兽药的情况。为了防止巴比妥类药物在产品化过程中的传播与积累,将生鲜乳作为重要的一种生物检材并对其巴比妥类药物进行检测对于保障乳制品安全具有重要意义。目前,现有技术公开的测定巴比妥类药物残留的生物检材主要是人血、血清、血浆、饲料、尿液等其他生物组织。方法主要有薄层色谱法、毛细管电泳法、高效液相色谱法、气相色谱法、气相色谱-质谱联用法、液相色谱-质谱联用法等。其中,液相色谱法以及液相色谱-质谱联用法对于巴比妥类药物的检测制备要求较低,只要能将巴比妥类药物制备成溶液且净化后,就能用于液相分析。另外,液相色谱相对气相色谱而言,灵敏度高,分析范围广,分析时间短等优点,近年来已经广泛运用于巴比妥等类别兽药化合物的分析,且涵盖的生物检材也十分广泛。除此之外,由于不同样品的基质特点不同,预处理方法会有很大的差异。然而,目前还没有将生鲜乳作为生物检材并检测其中巴比妥类药物的方法报导。由于生鲜乳中富含蛋白质和脂肪,如何对其中可能含有的巴比妥类兽药化合物进行提取、净化,提高其在生鲜乳中的回收率和灵敏度已经成为亟待解决的问题。技术实现要素:针对现有技术中的上述技术问题,本发明提供了一种检测生鲜乳中4种巴比妥类镇静药物的方法,所述的这种检测生鲜乳中4种巴比妥类镇静药物的方法要解决现有技术在检测生鲜乳中巴比妥类镇静药物困难的技术问题。本发明提供了一种检测生鲜乳中4种巴比妥类镇静药物的方法,包括如下步骤:1)一个对待测新鲜乳中的巴比妥类镇静药物进行预提取的步骤,将生鲜乳和乙腈溶液混合,震荡,超声,加入无机盐a,离心,所述的生鲜乳、乙腈溶液、无机盐a的物料比为10~20ml:5~20g:2~10g;上清液采用氮气吹干,用乙腈水溶液定容,待净化用;所述无机盐a为无水硫酸镁、无水硫酸钠、无水氯化钠、无水碳酸钠中的任意一种或两种以上的组合;2)一个净化的步骤,先用甲醇和乙腈水溶液预洗柱,将待净化定容液过柱后,超纯水洗柱,真空抽干;然后采用二氯甲烷洗脱,控制流速,洗脱液于氮气吹干,乙腈水溶液定容,待上机用;净化所用柱为spe柱;3)将预处理方法得到的溶液进行高效液相色谱-质谱联用检测分析;所述的高效液相色谱法检测的流动相为:流动相a:水;流动相b:乙腈;所述的高效液相色谱法检测的柱温为25~35℃;所述的高效液相色谱法检测的待测样品的流速为0.3~0.6ml/min;所述的高效液相色谱法检测的进样体积为5~15μl;所述的高效液相色谱法检测的梯度洗脱的条件为:所述的质谱检测条件为:离子源:电喷雾离子源;扫描模式:负离子模式;毛细管电压:3.5kv;离子源温度:100℃;去溶剂温度:350℃。进一步的,在一个对待测新鲜乳中的巴比妥类镇静药物进行预提取的步骤中,将生鲜乳样品、乙腈溶液混合,震荡混匀,超声后加入无机盐a,离心;取上清液10ml于15ml离心管中,50℃氮气吹干,用2ml含乙腈水溶液定容,待净化用;进一步的,在一个净化的步骤中,将步骤(1)中定容待净化溶液用spe柱净化,先用甲醇和乙腈水溶液过柱,控制流速0.5ml/min;将2ml待净化液过柱后,用超纯水洗柱,真空抽干;用二氯甲烷洗脱,控制流速,洗脱液于50℃氮气吹干,1ml乙腈水溶液定容,过滤,待上机用。进一步的,步骤(1)中,所述的乙腈的添加量为每5~20g待测样品添加10~20ml;步骤(1)中,所述无机盐a的添加量为2~10g。进一步的,所述的乙腈溶液中还添加酸;所述的酸为甲酸和/或乙酸;所述酸的添加量为所述乙腈添加量的0.1~0.3%,所述百分比为占乙腈的体积百分比。进一步的,步骤(1)中,所述的震荡的时间为0.5~3min;步骤(1)中,所述的超声时间为20~40min;步骤(1)中,所述的离心的转速为5000~10000rpm;步骤(1)中,所述的离心时间为5~15min;进一步的,步骤(2)中所述的spe柱规格为6ml或150mg;步骤(2)中,所述甲醇、乙腈水、超纯水为5~10ml;所述二氯甲烷体积为10~30ml;所述乙腈水溶液浓度为30~50%;所述百分比为占水溶液的体积百分比;步骤(2)中,所述的过滤方法为将溶液经有机微孔滤膜过滤。进一步的,步骤(2)中所述的spe柱购买厂家为besep,步骤(2)中,所述的有机微孔滤膜的孔径为0.22μm。进一步的,所述的高效液相色谱法检测的色谱柱为hplccshc18柱;所述的色谱柱的规格为2.1×100mm,1.7μm;所述的高效液相色谱法检测的待测样品的流速为0.3ml/min;所述的高效液相色谱法检测的进样体积5μl;所述的高效液相色谱法检测的柱温为25℃。进一步的,所述的质谱检测过程中,目标检测化合物母离子、子离子、碰撞能、保留时间为:其中,a代表定量离子。进一步的,所述的待测样品较佳的可能含有苯巴比妥和/或戊巴比妥和/或异戊巴比妥和/或司可巴比妥的生鲜乳。较佳的,所述的生鲜乳为不含有固体颗粒的生鲜乳。进一步的,步骤(1)中,所述的震荡是为了利于提取,使乙腈进一步提取苯巴比妥和/或戊巴比妥和/或异戊巴比妥和/或司可巴比妥。所述的震荡的方法和条件为本领域常规的方法和条件,所述的震荡的时间较佳的为0.5~3min。进一步的,步骤(1)中,所述的超声是为了利于提取,使乙腈进一步提取苯巴比妥和/或戊巴比妥和/或异戊巴比妥和/或司可巴比妥。所述的超声的方法和条件为本领域常规的方法和条件,所述的超声的时间较佳的为30~60min。本发明中,所述的高效液相色谱-质谱联用检测的方法为本领域常规的方法,本领域技术人员均知道,所述的高效液相色谱-质谱联用方法为高效液相色谱-电喷雾质谱方法。所述的质谱的检测方式为多反应监测模式。在符合本领域常识的基础上,上述各优选条件,可任意组合,即得本发明各较佳实例。本发明所用试剂和原料均市售可得。本发明解决了复杂基质生鲜乳中巴比妥类兽药化合物提取、净化的难题,所设计的预处理方法能较好地将生鲜乳中杂质去除,高效地提取生鲜乳中巴比妥类药物,具有较好的回收率;同时该检测方法对两种巴比妥类同分异构体进行了较好的分离,具有高效、快速、成本低、操作简便等优势,净化效果好,灵敏度高,准确度和精确度均符合多残留分析方法的要求。本发明方法采用的检测方法,能同时高效、快速、精确地同时对生鲜乳中苯巴比妥、戊巴比妥、异戊巴比妥、司可巴比妥4种巴比妥类兽药化合物进行测定,尤其是对戊巴比妥和异戊巴比妥两个同分异构体具有较高的分辨率。本发明和已有技术相比,其技术进步是显著的。本发明弥补现有检测生鲜乳中巴比妥类化合物的方法的缺失,提供一种灵敏、简便、快速而准确的能同时测定生鲜乳中多种巴比妥类兽药化合物的方法。本发明检测方法中的预处理方法能有效地提高生鲜乳中巴比妥类药物的提取率,且显著提高了巴比妥类药物在生鲜乳中的回收率,方法简便、经济、可靠,有效地降低了生鲜乳的基质影响,灵敏度、重复率和回收率好。附图说明图1是高效液相色谱-质谱检测加入苯巴比妥、戊巴比妥、异戊巴比妥、司可巴比妥的生鲜乳的色谱图。图2是高效液相色谱-质谱检测生鲜乳空白样的色谱图。图3是高效液相色谱-质谱检测加入苯巴比妥、戊巴比妥、异戊巴比妥、司可巴比妥的生鲜乳的色谱图。具体实施方式下面通过实施例的方式进一步说明本发明,但并不因此将本发明限制在所述的实施例范围之中。下列实施例中未注明具体条件的实验方法,按照常规方法和条件,或按照商品说明书选择。实施例1标准曲线的制备将苯巴比妥、戊巴比妥、异戊巴比妥和司可巴比妥用甲醇配制成10μg/ml的母液,于-20℃储藏。临用时各精确吸取1ml,用甲醇配制成浓度为1μg/ml的混合标准溶液10ml,于-20℃储藏。使用前称取0μl,50μl,100μl,200μl,500μl,1000μl混合标准溶液,50℃氮气吹干,用空白生鲜乳样品提取液1ml定容。进样检测,制得标准曲线。色谱柱:acquitycshc18(2.1×100mm,1.7μm);柱温:25℃;流速为0.3ml/min;进样量:5μl;流动相a:水;流动相b:乙腈;梯度洗脱条件如表1所示表1液相色谱线性梯度洗脱条件时间(min)%a(水)%b(乙腈)0.0090.0010.000.5090.0010.000.6073.5026.504.0073.5026.504.1075.0025.005.5073.5026.506.0073.5026.509.0020.0080.009.1090.0010.0010.0090.0010.00质谱检测条件为:离子源:电喷雾离子源;扫描模式:负离子模式;毛细管电压:3.5kv;离子源温度:100℃;去溶剂温度:350℃;检测方式:多反应监测模式;目标检测化合物母离子、子离子、碰撞能、保留时间如表2所示:表24种巴比妥类药物母离子、子离子、碰撞能、保留时间信息检测结果:图1是高效液相色谱-质谱检测加入苯巴比妥、戊巴比妥、异戊巴比妥、司可巴比妥的生鲜乳的色谱图。测定图1中所对应化全物峰面积,以浓度c(ng/ml)为横坐标,峰面积a为纵坐标,绘制苯巴比妥、戊巴比妥、异戊巴比妥、司可巴比妥的标准溶液工作曲线,得标准曲线方程及其相关系数,如表3所示。表34种巴比妥类药物线性方程、相关系数和线性范围实施例2待测样品的预处理(1)将10.0g生鲜乳(牧场a),置于50ml聚丙烯离心管中,加入20ml0.1%乙酸乙腈溶液,震荡30s,超声20min;加入2g无水氯化钠,震荡3min;5000rpm,离心5min;取10ml上清液于15ml聚丙烯离心管中,50℃氮气吹干,2ml30%的乙腈水溶液定容,待净化。(2)将上述定容液过spe小柱。先用5ml甲醇和5ml30%乙腈水溶液预处理。上述定容液过柱,控制流速在0.5ml/min左右。然后用5ml超纯水洗柱,真空抽干15min;用10ml二氯甲烷洗脱,收集洗脱液,于50℃氮气吹干;1ml30%乙腈水溶液定容,过0.22μl有机滤膜,用于hplc-ms/ms分析。待测样品中苯巴比妥、戊巴比妥、异戊巴比妥、司可巴比妥的检测方法如实施例1所示,经过上述预处理方法和检测方法,能够检测出待测样品中的苯巴比妥、戊巴比妥、异戊巴比妥、司可巴比妥。实施例3待测样品的预处理(1)将10.0g生鲜乳(牧场b),置于50ml聚丙烯离心管中,加入20ml0.1%乙酸乙腈溶液,震荡1min,超声30min;加入5g无水氯化钠,震荡3min;8000rpm,离心10min;取10ml上清液于15ml聚丙烯离心管中,50℃氮气吹干,2ml30%的乙腈水溶液定容,待净化。(2)将上述定容液过spe小柱。先用8ml甲醇和8ml30%乙腈水溶液预处理。上述定容液过柱,控制流速在0.5ml/min左右。然后用8ml超纯水洗柱,真空抽干15min;用20ml二氯甲烷洗脱,收集洗脱液,于50℃氮气吹干;1ml30%乙腈水溶液定容,过0.22μl有机滤膜,用于hplc-ms/ms分析。待测样品中苯巴比妥、戊巴比妥、异戊巴比妥、司可巴比妥的检测方法如实施例1所示,经过上述预处理方法和检测方法,能够检测出待测样品中的苯巴比妥、戊巴比妥、异戊巴比妥、司可巴比妥。实施例4待测样品的预处理(1)将10.0g生鲜乳(牧场c),置于50ml聚丙烯离心管中,加入20ml0.1%乙酸乙腈溶液,震荡3min,超声40min;加入10g无水氯化钠,震荡3min;10000rpm,离心15min;取10ml上清液于15ml聚丙烯离心管中,50℃氮气吹干,2ml30%的乙腈水溶液定容,待净化。(2)将上述定容液过spe小柱。先用10ml甲醇和10ml30%乙腈水溶液预处理。上述定容液过柱,控制流速在0.5ml/min左右。然后用10ml超纯水洗柱,真空抽干15min;用30ml二氯甲烷洗脱,收集洗脱液,于50℃氮气吹干;1ml30%乙腈水溶液定容,过0.22μl有机滤膜,用于hplc-ms/ms分析。待测样品中苯巴比妥、戊巴比妥、异戊巴比妥、司可巴比妥的检测方法如实施例1所示,经过上述预处理方法和检测方法,能够检测出待测样品中的苯巴比妥、戊巴比妥、异戊巴比妥、司可巴比妥。对比例1利用sn/t2217中方法检测生鲜乳中巴比妥类药物。sn/t2217方法检测生鲜乳中巴比妥类药物步骤如下:(1)称取2g(精确至0.01g)经检测不含目标待测物的生鲜乳,置于50ml聚丙烯离心管中,加入200μl1.0μg/ml的混合标准工作液静置5min。加入5g无水硫酸钠,混匀;加入10ml0.1%乙酸乙腈溶液,涡旋混合3min,超声10min;4000rpm,离心2min;取上清液于另一50ml聚丙烯离心管中,下层溶液用10ml0.1%的乙酸乙腈重复提取一次,合并上清液。在提取液中加入5ml乙腈饱和的正己烷,涡旋混合,离心,弃去上层正己烷,下层乙腈氮气吹干,5ml的0.1mol/l乙酸胺缓冲液:甲醇(90+10,体积比)溶解定容,待净化。(2)将上述定容液过hlb小柱。先用5ml甲醇和5ml0.1mol/l乙酸胺缓冲液预处理。上述定容液过柱,控制流速在0.5ml/min左右。然后用5ml0.1mol/l乙酸胺缓冲液:甲醇(90+10,体积比)洗柱,真空抽干15min;随后用5ml正己烷和5ml正己烷:乙酸乙酯(95+5,体积比)淋洗;最后用10ml正己烷:乙酸乙酯(50+50,体积比)洗脱,氮气吹干,用1.0ml甲酸溶解残渣,过0.45μm有机滤膜,供hplc-ms/ms分析。分析条件如实施例1。实验设计3个平行。实验结果以回收率为指标对sn/t2217方法和本发明方法进行对比,结果见表5。由表5可以看出,本发明方法对生鲜乳中巴比妥类药物的回收率远高于sn/t2217方法,说明本方法更加适用于生鲜乳类复杂基质中巴比妥类药物的检测。效果例1检出限的测定将实施例1中制备的混合标准溶液摇匀,从高浓度往低浓度稀释,进样5μl,按实施例1中hplc色谱条件分析。信噪比s/n=3时所测浓度作为检出限,信噪比s/n=10时所测浓度作为定量限。其检出限和定量限如表4所示。表44种巴比妥类药物的检出限和定量限效果例2加标回收率的测定称取10g经检测不含目标兽药化合物的生鲜乳,分别加入1μg/ml的混合标准工作液100μl,200μl,400μl,制成10、20、40ng/g生鲜乳三个质控浓度水平,每个浓度水平做6个平行样品,用本发明方法分别进行样品前处理和hplc-ms/ms分析,并按照标准品色谱峰面积和添加标准品提取后测定峰面积计算回收率,结果见表5。图2为高效液相色谱-质谱检测生鲜乳空白样的色谱图。图3为高效液相色谱-质谱检测加入苯巴比妥、戊巴比妥、异戊巴比妥和司可巴比妥的生鲜乳的色谱图。检测得到苯巴比妥、戊巴比妥、异戊巴比妥、司可巴比妥浓度在误差允许范围内。由表5可以看出,4种巴比妥类兽药化合物在生鲜乳中的回收率在85.04%和111.37%之间,而sn/t2217方法检测生鲜乳中巴比妥类药物的回收率在23.65%和43.24%之间,远远低于本发明方法,说明本发明方法适用于复杂基质生鲜乳中巴比妥类药物的检测。表5回收率检测结果与对比效果例3精密度的测定按效果例2中同样实验设计,测定并计算回收率。精密度以相对标准偏差(rsd)计算,生鲜乳中4种巴比妥类兽药的相对标准偏差见表6。由表6可看知,批内相对标准偏差在1.09%和9.85%之间,批间相对标准偏差在3.88%和7.28%之间,符合多残留分析的要求。表6精密度实验结果以上结果表明,本方法的预处理方法是一种对生鲜乳中巴比妥类药物提取和净化的良好方法,在待测样品中苯巴比妥、戊巴比妥、异戊巴比妥、司可巴比妥残留检测中具有重要的应用价值。效果例4实际样品中巴比妥类药物的检测将本发明方法应用到不同牧场,共50个生鲜乳盲样中巴比妥类药物的检测,具体实验步骤按照实施例3进行(标准曲线的制作按照实施例1进行)。具体检测结果如下:50个生鲜乳盲样中,共48个阴性产品,检测出2个阳性产品。结果见表7(阴性结果未列出),此结果表明,本发明可有效地检测生鲜乳中巴比妥类药物。表7实际生鲜乳盲样中4种巴比妥类药的检测结果注:nd代表未检出。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1