利用牛血清蛋白--金银合金纳米簇检测碱性磷酸酶的用途的制作方法
本发明属于分析化学领域,涉及一种利用牛血清蛋白--金银合金纳米簇检测碱性磷酸酶的用途。
背景技术:
近年来,水体富营养化已经成为水污染的主要原因之一,因此受到越来越来人的关注。众所周知,水体富营养化是由于水中氮和磷等营养物质含量过高造成的。河流湖泊中大量磷的流入导致富营养化和藻类爆发。因此,对水体中磷的监测常常被用来监控水体富营养化程度。现如今,因为湖水中的浮游植物可直接利用的无机磷含量通常不到总磷浓度的5%,所以通过简单地测量水中的总磷浓度,来辨别磷和富营养化之间的关系是非常困难的。碱性磷酸酶(alkalinephosphatase,alp)是自然界中广泛存在的酶,催化水解一系列单磷酸酯基团,为水中的浮游植物提供了生存能量,因此在生物系统中起着至关重要的作用。大量文献表明,当水体中缺少溶解性活性磷时,浮游植物会诱导alp含量增加,将有机磷转化为溶解性活性磷。相对地,高水平的溶解性活性磷也会抑制alp得表达。因此,对碱性磷酸酶活性的监测也可以清楚地掌握水体中的溶解性活性磷的水平,进而间接地了解水生生态系统的富营养化程度。这也意味着,alp可以作为富营养化的指标之一。
到目前为止,alp的检测方法已有许多报道,如:比色、色谱、荧光、表面增强拉曼光谱、免疫分析和电化学法。这些方法中,大多数方法都受到自身低敏感度、低选择性和分析过程太耗时的限制。而荧光法由于其灵敏度高和方便快捷的优势,被认为是一种较好的方法。目前,alp检测的荧光分析方法中多采用有机染料、荧光聚合物和量子点作为荧光指标。但是,由于有机染料的荧光不稳定性和较差的水溶性、荧光聚合物的合成复杂和量子点的高毒性,这些荧光分析技术存在一些不可忽视的问题。近年来,由于贵金属纳米簇独特光学特性、合成简单、无毒和良好的生物相容性等优点引起了广泛地关注。目前,荧光传感器由于灵敏度高、选择性好和操作简单等优点,已经成为实时检测的有效手段。因此,开发一种碱性磷酸酶荧光传感器具有非常重要的意义,更重要的是,alp的荧光检测分析方法基本专注于血清研究,而环境中的alp检测却鲜有人问津。
技术实现要素:
本发明的目的是建立一种利用牛血清蛋白--金银合金纳米簇检测碱性磷酸酶的用途,并用于检测环境水体中的碱性磷酸酶。
一种利用牛血清蛋白--金银合金纳米簇检测碱性磷酸酶的用途,包括如下步骤:
(1)制备牛血清蛋白--金银合金纳米簇(bsa-au/agncs)水溶液:
将4ml的氯金酸(10mm)和1ml的硝酸银(10mm)混合(金银摩尔比为4:1),加入到5ml的牛血清蛋白溶液(0.75mm)中,强有力搅拌混合5分钟后,用氢氧化钠调节溶液的酸碱度,然后置于37℃的恒温油浴锅反应12小时,反应结束后用超纯水透析纯化48小时,得到bsa-au/agncs水溶液;
牛血清蛋白为保护剂和还原剂。
(2)在步骤(1)制得的bsa-au/agncs水溶液中加入kmno4水溶液淬灭其荧光,制得混合溶液a,检测荧光强度为i1。
其中,bsa-au/agncs水溶液和kmno4水溶液的体积比为2:1,bsa-au/agncs水溶液的浓度为20nmol/l,kmno4水溶液的浓度为1~5mmol/l。
(3)配置一系列不同浓度的碱性磷酸酶溶液,然后利用碱性磷酸酶催化抗坏血酸2-磷酸酯生成抗坏血酸。
其中,碱性磷酸酶溶液的浓度为0~3.125u/l,抗坏血酸2-磷酸酯的浓度为0.5~600nmol/l,碱性磷酸酶溶液与抗坏血酸2-磷酸酯的体积比为1:1。
所述的利用碱性磷酸酶催化抗坏血酸2-磷酸酯的反应是在tris-hcl缓冲液中进行的,ph为7~10.5;催化温度为27~57℃;催化时间为10~50分钟。
(4)将步骤(2)制得的制得混合溶液a和步骤(3)制得的抗坏血酸混合反应,反应温度为27~57℃,时间为5~60分钟,制得混合溶液b,检测荧光强度i。
其中,混合溶液a和步骤(2)制得的抗坏血酸的体积比为3:2。
(5)建立(i-i1)/i和碱性磷酸酶浓度的标准曲线。
(6)将抗坏血酸2-磷酸酯加入待测样品中,催化完成后,再与混合溶液a混合反应,反应完成后,检测其荧光强度i'。根据(i'-i1)/i'的值对照标准曲线,得出样品中的碱性磷酸酶浓度。
本发明的有益效果为:
(1)本发明基于kmno4可以氧化bsa使得bsa-au/agncs的结构被破坏,从而导致bsa-au/agncs荧光淬灭。同时,由于抗坏血酸具有相对较强的还原性,所以可以有效地恢复被破坏的bsa结构,从而导致bsa-au/agncs的荧光恢复。而抗坏血酸2-磷酸脂可被碱性磷酸酶催化水解为抗坏血酸和磷酸酯,因此可依据上述原理建立碱性磷酸酶荧光传感器。
(2)本发明所构建的碱性磷酸酶荧光传感器检测方法简单便捷、灵敏度高,为环境水体中的碱性磷酸酶检测提供了一条有效的新途径。
附图说明
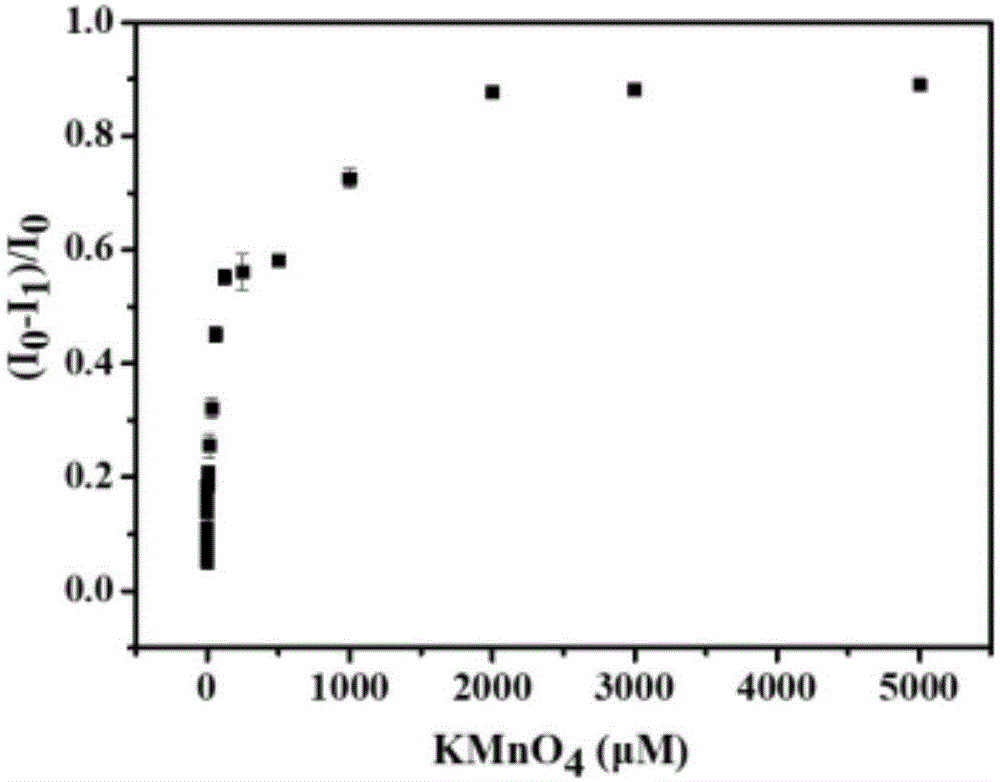
图1为不同浓度的kmno4水溶液(0~5mmol/l)对bsa-au/agncs的荧光淬灭率((i0-i1)/i0)与kmno4浓度的关系图(i0为bsa-au/agncs的原始荧光强度,i1为bsa-au/agncs被kmno4淬灭后的荧光强度)。
图2为不同浓度的碱性磷酸酶水溶液(0~3.125u/l)作用下的荧光恢复率((i-i1)/i)与碱性磷酸酶浓度的关系图。
图3为碱性磷酸酶水溶液(0.006-0.1u/l)与荧光恢复率((i-i1)/i)的标准曲线。
图4为不同干扰物质对碱性磷酸酶荧光传感器的影响。
具体实施方式
下面用实例来进一步说明本发明,但本发明并不受其限制。下列实例中未标明具体条件的实验中,均按照常规条件,或制造厂商建议条件。
实例1
(1)制备牛血清蛋白--金银合金纳米簇(bsa-au/agncs)水溶液:
将4ml的氯金酸(10mm)和1ml的硝酸银(10mm)混合(金银摩尔比为4:1),加入到5ml的牛血清蛋白溶液(0.75mm)中,强有力搅拌混合5分钟后,用氢氧化钠调节溶液的酸碱度,然后置于37℃的恒温油浴锅反应12小时,反应结束后用超纯水透析纯化48小时,得到bsa-au/agncs水溶液;
(2)在步骤(1)制得的bsa-au/agncs水溶液中加入kmno4水溶液淬灭其荧光,制得混合溶液a,检测荧光强度为i1。其中,bsa-au/agncs水溶液和kmno4水溶液的体积比为2:1,bsa-au/agncs水溶液的浓度为20nmol/l,kmno4水溶液的浓度为5mmol/l。
(3)碱性磷酸酶催化抗坏血酸2-磷酸酯生成抗坏血酸;
配置一系列不同浓度的碱性磷酸酶溶液,然后利用碱性磷酸酶催化抗坏血酸2-磷酸酯生成抗坏血酸。碱性磷酸酶溶液的浓度为0~3.125u/l,抗坏血酸2-磷酸酯的浓度为300nmol/l,碱性磷酸酶溶液与抗坏血酸2-磷酸酯的体积比为1:1。
所述的利用碱性磷酸酶催化抗坏血酸2-磷酸酯的反应是在tris-hcl缓冲液中进行的,ph为9.0;催化温度为37℃;催化时间为30分钟。
(4)将步骤(2)制得的制得混合溶液a和步骤(3)制得的抗坏血酸混合反应,反应温度为37℃,时间为25分钟,制得混合溶液b,检测荧光强度i。
(5)建立(i-i1)/i和碱性磷酸酶浓度的标准曲线。
(6)特异性分析:
由于本发明旨在开发检测水样中碱性磷酸酶的浓度,我们测定了一些常见的潜在干扰物质,包括相关金属离子(k+,na+),水中常见的酶(葡萄氧化酶、乙酰胆碱酯酶、辣根过氧化物酶、脂肪酶)。结果表明,碱性磷酸酶荧光传感器具有很强的抗干扰能力和检测碱性磷酸酶的高度特异性。
(7)环境水样中碱性磷酸酶的检测:
收集湖泊水样,采用0.22μm的滤膜去除水样中的悬浮颗粒物,用tris-hcl缓冲液稀释10倍,待用。
将抗坏血酸2-磷酸酯(300nmol/l)加入待测水样中,催化完成后,再与混合溶液a混合反应,反应完成后,检测其荧光强度i'。根据(i'-i1)/i'的值对照标准曲线,得出样品中的碱性磷酸酶浓度。
图1为不同浓度的kmno4水溶液(0~5mmol/l)对bsa-au/agncs的荧光淬灭率((i0-i1)/i0)与kmno4浓度的关系图(i0为bsa-au/agncs的原始荧光强度,i1为bsa-au/agncs被kmno4淬灭后的荧光强度)。
图2为不同浓度的碱性磷酸酶水溶液(0~3.125u/l)作用下的荧光恢复率((i-i1)/i)与碱性磷酸酶浓度的关系图。
图3为碱性磷酸酶水溶液(0.006-0.1u/l)与荧光恢复率((i-i1)/i)的标准曲线。
图4为不同干扰物质对碱性磷酸酶荧光传感器的影响。
实例2
(1)制备牛血清蛋白--金银合金纳米簇(bsa-au/agncs)水溶液步骤同实施例1。
(2)混合溶液a制备步骤同实施例1,检测荧光强度为i1。
(3)碱性磷酸酶催化抗坏血酸2-磷酸酯生成抗坏血酸步骤同实施例1。
(4)混合溶液b制备步骤同实施例1,检测荧光强度为i。
(5)建立(i-i1)/i和碱性磷酸酶浓度的标准曲线。
(6)水样1中碱性磷酸酶的检测:
收集湖泊水样1,采用0.22μm的滤膜去除水样中的悬浮颗粒物,用tris-hcl缓冲液稀释10倍,待用。
将抗坏血酸2-磷酸酯(300nmol/l)加入待测水样中,催化完成后,再与混合溶液a混合反应,反应完成后,检测其荧光强度i'。计算(i'-i1)/i'的值,对照标准曲线得水样1中的碱性磷酸酶浓度为0.009u/l。
实例3
(1)制备牛血清蛋白--金银合金纳米簇(bsa-au/agncs)水溶液步骤同实施例1。
(2)混合溶液a制备步骤同实施例1,检测荧光强度为i1。
(3)碱性磷酸酶催化抗坏血酸2-磷酸酯生成抗坏血酸步骤同实施例1。
(4)混合溶液b制备步骤同实施例1,检测荧光强度为i。
(5)建立(i-i1)/i和碱性磷酸酶浓度的标准曲线。
(6)水样2中碱性磷酸酶的检测:
收集湖泊水样1,采用0.22μm的滤膜去除水样中的悬浮颗粒物,用tris-hcl缓冲液稀释10倍,待用。
将抗坏血酸2-磷酸酯(300nmol/l)加入待测水样中,催化完成后,再与混合溶液a混合反应,反应完成后,检测其荧光强度i'。计算(i'-i1)/i'的值,对照标准曲线得水样1中的碱性磷酸酶浓度为0.017u/l。
实例4
(1)制备牛血清蛋白--金银合金纳米簇(bsa-au/agncs)水溶液步骤同实施例1。
(2)混合溶液a制备步骤同实施例1,检测荧光强度为i1。
(3)碱性磷酸酶催化抗坏血酸2-磷酸酯生成抗坏血酸步骤同实施例1。
(4)混合溶液b制备步骤同实施例1,检测荧光强度为i。
(5)建立(i-i1)/i和碱性磷酸酶浓度的标准曲线。
(6)水样3中碱性磷酸酶的检测:
收集湖泊水样3,采用0.22μm的滤膜去除水样中的悬浮颗粒物,用tris-hcl缓冲液稀释10倍,待用。
将抗坏血酸2-磷酸酯(300nmol/l)加入待测水样中,催化完成后,再与混合溶液a混合反应,反应完成后,检测其荧光强度i'。计算(i'-i1)/i'的值,对照标准曲线得水样1中的碱性磷酸酶浓度为0.019u/l。
- 还没有人留言评论。精彩留言会获得点赞!