用于治疗眼病的预测性生物标记物的制作方法
本发明涉及蛋白质组学领域。更具体地,本发明涉及基于蛋白质组学变化来预测对眼病治疗的响应的装置和方法。
背景技术:
泪膜和底下眼睛表面是眼睛的第一防线,并且眼泪在我们眼睛中具有数个目的;它们从眼睛上皮递送和取走营养物和代谢产物,它们润滑和保护上皮表面并且参与精细控制机制。泪液含有许多不同类型的分子,并且由于眼泪反映了底下眼睛表面的健康并且采集方法是非侵入性的,所以已经持续努力地用蛋白质组学分析眼泪以便鉴定对于各种疾病的潜在生物标记物。近年来,蛋白质组学已经用于各种眼病的研究中,包括干眼、糖尿病视网膜病和年龄相关的黄斑变性(amd)。
蛋白质组学研究中常见的是合并样品以便获得对临床问题的更全面的回答,并且这种方式假设所有患者经历某些类似的蛋白质组学变化。这样,经常没有鉴定患者之间的个体差异。然而,药物试验已经证明患者对于相同治疗反应方式不同,并且潜在原因是复杂的并且仍然大多未知(ginsbury&mccarthy,2001;schork,2015)。随着蛋白质组学领域的最新革新,主要是无标签质谱(ms)法,现在可以在大的临床研究中作为个体治疗每个患者,以便探索不同结果模式的潜在原因。
最近,眼泪蛋白质组学已经显示了其在鉴定关于与青光眼药物治疗相关的炎症响应的生物标记物中的潜力(funke等,2016;wong等,2011)。典型的药物治疗是目前最普遍的降低眼内压(iop)的青光眼管理方法,并且因为病症是不可治愈的,所以患者经常需要数年或数十年使用滴眼液。先前的临床研究已经显示,长期使用局部青光眼药物治疗可诱发眼睛表面疾病的症状和体征,其在一定程度上和与干眼病相关的那些重叠。副作用不仅可以由滴眼液的活性化合物导致,而且可以由它们的防腐剂导致,所述防腐剂诸如苯扎氯铵(bak),苯扎氯铵在局部青光眼药物中以及在其他局部眼药中最著名的和最常用的防腐剂。临床证据提示,在使用防腐的局部治疗同时遭受副反应的患者受益于转换至不含防腐剂的滴眼剂:他们的副反应消失了,而不削弱iop的控制。本发明基于青光眼药物治疗转换对于眼泪蛋白质组学的影响的研究,其采用更个人化的方法。药物试验已经证明,患者对于相同治疗反应方式不同,并且潜在原因是复杂的并且大多未知。因此,存在确定的对于这样的装置和方法的需要,所述装置和方法用于预测对于眼病治疗的个体化响应。
技术实现要素:
本发明的一个目的是提供预测受试者对于眼病药物的响应的装置和方法,以及方法的不同应用。该目的是通过独立权利要求中所述的技术方案实现。本发明的优选实施方案在从属权利要求中公开。
更具体地,本发明提供了一种在需要眼病治疗的受试者中预测对眼病治疗的响应的方法,其中所述方法包括评估从所述受试者获得的样品中一种或多种生物标记物的水平,所述生物标记物包括prol1,所述方法包括比较所述生物标记物的评估水平和对照,并且基于所述比较预测所述受试者对所述治疗的响应。
在该方法中,降低的prol1水平表示所述受试者可能受益于所述治疗。在一些实施方案中,该方法包括评估获自所述受试者的样品的一种或多种另外的生物标记物的水平,所述另外的生物标记物选自由以下组成的组:tf、cst4、hspa8、cst1、ywhaz、rnh1、uchl3、cst2、myl6、s100a6、b2m、gsr、s100a8、hspa5、ywhae、cndp2、csta、cstb、cst5和cst3。优选的另外的生物标记物是tf和/或myl6,以及cts1或者没有cts1。
本发明还提供了本发明方法的不同应用。该应用包括为患有眼病的受试者选择治疗方案,监视患有眼病的受试者对治疗的响应,基于对治疗的预测的响应将受试者分层(stratifying),和将受试者分层用于临床试验。
还提供了生物标记物组合在确定受试者对于眼病治疗的响应中的用途,所述生物标记物组合包括至少prol1,以及tf或myl6之一,或tf和myl6两者。在一些实施方案中,生物标记物组合另外包括一种或多种选自下组的生物标记物:cst4、hspa8、cst1、ywhaz、rnh1、uchl3、cst2、s100a6、b2m、gsr、s100a8、hspa5、ywhae、cndp2、csta、cstb、cst5和cst3。
本发明还提供用于本发明方法中的试剂盒,其中所述试剂盒包括用于特别评估至少prol1以及tf或myl6之一或tf和myl6两者的水平的试剂。在一些实施方案中,试剂盒还包括一种或多种试剂,其用于特别评估生物样品、优选眼泪样品中一种或多种另外的选自下组的生物标记物的水平:cst4、hspa8、cst1、ywhaz、rnh1、uchl3、cst2、s100a6、b2m、gsr、s100a8、hspa5、ywhae、cndp2、csta、cstb、cst5和cst3。适当的试剂在本领域容易获得,并且包括例如这些特异性针对生物标记物的抗体。
本发明的另外的方面、特定实施方案、目的、细节和优势在以下附图、详述和实施例中阐明。
附图说明
以下本发明将通过优选实施方案参考附图更详细地描述,其中
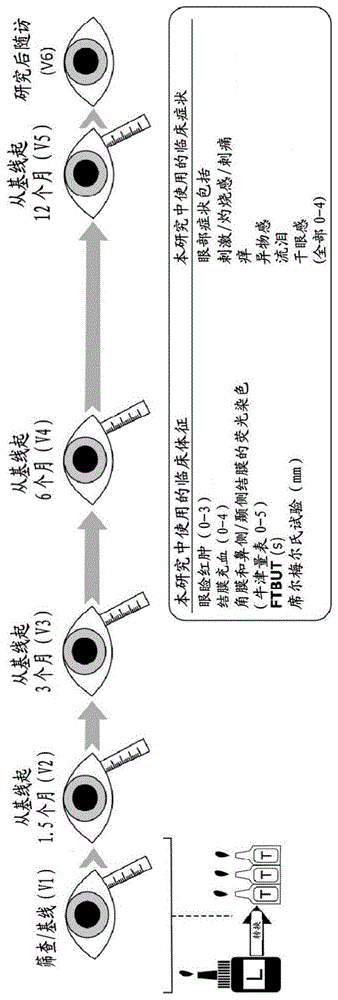
图1图解了研究提纲概要。在筛查/基线随访(v1)期间,将患者在单位剂量分配器中的防腐的拉坦前列素(latanoprost)(l)转换为不含防腐剂的他氟前列素(tafluprost)(t)。在随访v1-v5进行临床测量以及眼泪样品采集。在研究后随访(v6)时,记录最后的临床测量值,但是不再采集眼泪样品。
图2进一步扩展了来自患者分层的分析要点和结果的解释。顶行解释了数据处理、蛋白聚类和患者分层的要点。热图显现了在基线和药物转换后12个月之间蛋白表达的改变。与眼睛炎症相关的两个蛋白簇以灰色行表示,并且与泪腺分泌关联的蛋白以白色行表示。由于基线表达丢失,排除了两名患者。
图3显示了在患者组之间它们的基线log2表达(x-轴)不同的蛋白(y-轴)。所有缺失解释的蛋白(*、
图4显示了席尔梅尔氏试验(schirmer’stest)和荧光泪膜破裂时间(fluoresceintearbreak-uptime,ftbut)与在我们的研究中鉴定的统计学显著的蛋白相关。黑点表示潜在的异常值。图4a显示:当席尔梅尔氏试验结果低时,在基线处的tf、s100a6和ywhaz蛋白表达高。对于prol1、cst4和b2m的情形相反。图4b显示:当ftbut低时,在基线处的tf、hspa8和ywhaz蛋白表达高。
图5图解了显示不同prol1(基线)表达水平的影响的患者实例。图5a显示:与患者003和029(圆圈)相比,患者004和028(正方形)具有高的prol1基线表达。图5b显示:基于大部分临床体征,由正方形表示的具有高prol1基线水平的患者在1年后不受益于所述转换。眼睑红肿和结膜染色增加或保持不变,同时角膜染色保持不变。对于患者004,荧光泪膜破裂时间(ftbut)减少,其也提示恶化迹象。具有低prol1基线表达的患者(由圆圈表示)显示了减少的睑内红肿、角膜染色和结膜染色的体征,同时ftbut增加。结膜红肿在患者之间是类似的。
具体实施方式
本发明是基于新的生物标记物组或表达模式的鉴定,所述生物标记物指示或预测在需要眼病治疗的受试者中对于该治疗的响应。因此,本发明的目的是提供在治疗眼病中用于各种目的的装置和方法。
如本文所用,术语“受试者”是指任何哺乳动物,包括但不限于人和家畜,诸如牲畜、宠物和运动动物。该动物的实例非限制性地包括食肉动物如猫和狗以及有蹄类如马。因此,本发明可以应用于人类医学和兽医学两者。如本文所用,术语“受试者”、“患者”和“个体”可互换。
受试者可以先前已经诊断患有眼病或先前没有诊断患有眼病。此外,所述受试者可以处于眼病治疗方案中或者可以先前处于该方案中。
如本文所用,术语“眼病”是指其中需要长期局部药物治疗的任何眼病,所述眼病包括但不限于任何形式的青光眼、眼高压、眼表疾病、眼部感染、虹膜炎或葡萄膜炎。
如本文所用,术语如“眼病治疗”、“眼病治疗方案”或“眼病疗法”是指任何眼睛疗法,包括但不限于局部滴眼液、软膏、凝胶或任何类型的药物递送植入物。
如本文所用,术语“眼用药物”和“眼药”是指但不限于任何青光眼药物、眼表眼泪替代物、过敏药、皮质类固醇或免疫调节剂。
如本文所用,术语“防腐的”眼用药物或眼药是指包含至少一种防腐剂的制剂。典型地用于眼用制剂中的防腐剂的非限制性实例包括季铵家族成员,如苯扎氯铵(bak)和聚季铵盐(polyquaternium)。
如本文所用,术语“不含防腐剂的”眼用药物或眼药是指不含任何防腐剂的制剂。
如本文所用,术语“治疗(treatment或treating)”意欲包括将眼用药物或眼药施用于受试者,其目的可以不但包括完成疾病治愈,而且包括减轻或改善疾病或与其相关的症状。如本文所用,术语“治疗”和“疗法”可互换。
如本文所用,术语“样品”是指可获自受试者眼睛的任何生物学样品,典型地临床样品。在一些实施方案中,眼泪样品是最优选的样品类型。通常,从受试者获得待分析的样品不是本发明方法的一部分,本发明的方法因此可以称为体外方法。眼泪样品可以通过本领域可用的任何适当装置或方法来获得,例如通过在吸水纸诸如席尔梅尔氏试纸条上采集泪液或者通过用微毛细管采集眼泪。
术语“样品”还包括在它们获取后已经以任何适当方式操作或处理的样品,所述方式包括但不限于提取、离心、过滤、沉淀、渗析、层析、用试剂处理、洗涤或富集样品的特定组分。
如本文所用,术语“生物标记物”和“标记物”是可互换的并且是指这样的分子、优选蛋白:与在获自将不受益于给定眼病治疗或将对该治疗不利响应的受试者的样品中相比,其在获自将受益于该眼病治疗的受试者的样品中差异存在。因此,本发明的生物标记物提供了关于眼病治疗的可能结果的信息。
这里,当应用于生物标记物时,术语“水平”与术语“量”和“浓度”可互换使用,并且可以是指样品中生物标记物的绝对量或相对量。
在一方面,本发明涉及一种在需要眼病治疗的受试者中预测眼病治疗的效果或结果的方法。该方法包括提供获自患有眼病的受试者的样品,优选眼泪样品,和评估所述样品中至少一种下文所述的本发明的生物标记物的水平,和基于所述评估来确定所述受试者对于所述眼病治疗的响应。优选地,所述至少一种生物标记物包括:prol1;prol1和tf;prol1和myl6;prol1、tf和myl6;或prol1和cst1。
该方法不仅可以用于选择对于受试者有效或以其他方式有益的治疗方案(例如,某种药物治疗或药),而且可以用于监视对于治疗的响应。另外,该方法也可以用于筛选眼病的新治疗剂。设想本发明的生物标记物可以用于评估候选药物或干预疗法是否能够将遭受不利治疗效果的受试者的生物标记物表达模式朝向阳性对照或朝向具有有利治疗响应的个体改变。此外,可以将下述个体用作临床试验靶标以鉴定眼病的新治疗药物或其他干预疗法,所述个体基于他们的生物标记物表达模式被鉴定对于某种治疗没有有利响应。因此,本发明的生物标记物也可以用于将个体对于临床试验分层。
在需要眼病治疗的受试者中预测眼病治疗的效果或结果的本发明方法的某些实施方案中,所述眼病治疗包括药物转换。在这样的实施方案中,该方法可以表示为预测眼病治疗中药物转换的效果或结果(即对药物转换的响应)的方法。该方法包括提供获自患有所述眼病的受试者的样品,优选眼泪样品,和评估所述样品中至少一种下文所述的本发明的生物标记物的水平,和基于所述评估来确定所述受试者对于所述药物转换的响应。优选地,所述至少一种生物标记物包括:prol1;prol1和tf;prol1和myl6;prol1、tf和myl6;或prol1和cst1。在一些另外的实施方案中,所述药物转换可以涉及从含防腐剂(例如含bak)的眼药向不含防腐剂的眼药的转换。
在一些实施方案中,预测可以基于分析获自受试者的一个或多个系列样品,例如以确定对于眼病的特定治疗或治疗组合的响应的任何变化。在该情形中,所述预测方法包括分析和比较在不同时间点获自相同受试者的至少两个样品。系列样品的数量和间隔可以根据需要改变。获得的评估结果之间的区别用作对治疗响应的任何变化的指示或者用作施加的治疗或治疗组合的有效性或无效性的指示。
基于生物标记物谱图确定对治疗的响应或对药物转换的响应通常要求将评估的或检测的生物标记物水平与相关对照进行比较。
如本文所用,术语“对照”可以是指获自具有已知眼病史或无眼病史的对照受试者或对照受试者组的可比较样品。术语“对照”也可以是指先前获自相同受试者的样品,其中将要预测所述受试者对于治疗的响应。在一些实施方案中,术语“阴性对照”可以是指获自明显健康和因此不显示任何讨论的眼病体征或已知不受益于治疗的个体或个体组的对照样品。在一些实施方案中,术语“阳性对照”可以是指获自已经患有讨论的眼病或已知受益于治疗的个体或个体组的对照样品。因此,适当的对照受试者可以还包括正在经历或先前用给定眼病治疗处理的个体或个体组。有时可能有益的是在根据本发明的单一方法中使用超过一种类型的对照。
术语“对照”也可以是指源自上述单一对照受试者或对照受试者组的预定的阈值或对照值,该值指示对治疗的响应。用于确定适当阈值或对照值的统计学方法对于本领域普通技术人员将是容易明了的,并且统计学验证的阈值或对照值可以采取各种各样的形式。例如,统计学验证的阈值可以是单个截止值,诸如中值或平均值。备选地,统计学验证的阈值可以等分(或不等分)成各个组,诸如低响应组、中响应组和高响应组,低响应组是最不可能受益于治疗或甚至可能具有副作用的个体,并且高响应组是最可能受益于治疗的个体。此外,阈值可以是绝对值或相对值。然而,如果将绝对值用于测定的生物标记物的水平,则阈值也是基于绝对值。相对值同样如此,其必须是可比较的。在一些实施方案中,在与相关对照比较之前,使用标准方法将生物标记物水平标准化。
在一些实施方案中,相同年龄、人口统计特征和/或疾病状态等的受试者可以用作用于获得可比较对照样品或确定统计学验证的阈值的适当对照受试者。
可以将获自受试者(将预测其对治疗的响应)的样品中的测定的生物标记物的水平与一个或多个单一对照值比较或与一个或多个对照值范围比较,而不管对照值是否是预定值或在实施本发明的方法后获自对照样品的值。患者样品和对照中生物标记物水平的差异的显著性可以使用标准统计学方法评估。
用于本发明的生物标记物包括选自下组的一个或多个生物标记物(以任意组合):tf、cst4、hspa8、prol1、cst1、ywhaz、rnh1、uchl3、cst2、myl6、s100a6、b2m、gsr、s100a8、hspa5、ywhae、cndp2、csta、cstb、cst5和cst3。取决于所讨论的患者组,与相关对照相比,这些生物标记物的水平可以是提高的、正常的或降低的。
如本文所用,术语“提高的水平”是指与相关对照相比,在样品中生物标记物的量增加。所述增加可以根据本领域已知的标准方法定性和/或定量确定。术语“提高的”包括任何水平的提高,但是更具体地是指与相关对照相比大约1.25倍至大约10倍的提高。在一些实施方案中,如果样品中生物标记物的量或水平是对照样品中同一生物标记物的量的例如至少大约1.25倍、1.5倍、2倍、3倍、4倍、5倍、6倍、8倍、9倍或10倍,则表达增加。所述增加可以根据本领域已知的标准方法定性和/或定量确定。在一些实施方案中,术语“提高的水平”是指与相关对照相比,生物标记物的水平或量的统计学显著的增加。
如本文所用,术语“正常的”是指与相关对照样品的生物标记物水平或预定阈值相比,检测的或测定的生物标记物水平基本上相同或基本上未改变。术语“正常的”与术语“未改变的”是可互换的。
如本文所用,术语“降低的水平”是指与相关对照相比,在样品中生物标记物的量降低。所述降低可以根据本领域已知的标准方法定性和/或定量确定。术语“降低的”包括任何水平的降低,但是更具体地是指与相关对照相比大约1.25倍至大约10倍的降低。在一些实施方案中,如果样品中生物标记物的量比对照样品中同一生物标记物的量低例如至少大约1.25倍、1.5倍、2倍、3倍、4倍、5倍、6倍、8倍、9倍或10倍,则表达降低。在一些实施方案中,术语“降低的水平”是指与相关对照相比,生物标记物的水平或量的统计学显著的降低。
如本文所用,术语“指示有利响应”和任何等价表述包括其中可能受试者将显著受益于眼病治疗的情形(这里表示为组1患者)。在一些实施方案中,该表述是指这样的生物标记物:使用常规统计学方法设定置信水平最小值95%,所述生物标记物预测有利的响应,使得发现该生物标记物与不受益于所述治疗的受试者相比在受益于所述治疗的受试者中更经常地处于特定水平(提高的、正常的或降低的)。优选地,发现指示有利响应的预测生物标记物在至少80%的受益于治疗的受试者中处于特定水平,并且发现指示有利响应的预测生物标记物在小于10%的不受益于治疗的受试者中处于该水平。更优选地,发现指示有利响应的预测生物标记物在至少90%、至少95%、至少98%或更多的受益于治疗的受试者中处于特定水平,并且发现指示有利响应的预测生物标记物在小于10%、小于8%、小于5%、小于2.5%或小于1%的不受益于治疗的受试者中处于该水平。
如本文所用,表述“指示不利响应”和任何等价表述包括其中可能受试者将仅在一定程度上受益于眼病治疗的情形(这里表示为组2患者)或将不会受益于眼病治疗或患者可能经历由眼病治疗导致的不利作用的情形(这里表示为组3患者)。在一些实施方案中,该表述是指这样的生物标记物:使用常规统计学方法设定置信水平最小值95%,所述生物标记物预测不利的响应,使得发现该生物标记物与受益于治疗的受试者相比在不受益于治疗的受试者中显著地更经常地处于特定水平(提高的、正常的或降低的)。优选地,发现指示不利响应的预测生物标记物在至少80%的不受益于治疗的受试者中处于特定水平,并且发现指示不利响应的预测生物标记物在小于10%的受益于治疗的受试者中处于该水平。更优选地,发现指示不利响应的预测生物标记物在至少90%、至少95%、至少98%或更多的不受益于治疗的受试者中处于特定水平,并且发现指示不利响应的预测生物标记物在小于10%、小于8%、小于5%、小于2.5%或小于1%的受益于治疗的受试者中处于该水平。
因此,在本发明的一些实施方案中,受试者可以基于他们的生物标记物表达谱分层为:可能对治疗具有明确有利响应或显著受益于所述治疗的那些(组1患者),或可能具有有利响应但是程度较低或者轻微受益于所述治疗的那些(组2患者),或可能对治疗具有不利响应或经历由所述治疗导致的不利作用的那些(组3患者)。换言之,通过观察蛋白质组谱图,可以将患者分层并且预测哪些患者将最受益于治疗或干预。
如上文已经阐述的,可能对于治疗具有明确有利响应或者显著受益于所述治疗的受试者(即组1患者)可以在一些实施方案中称为可能对于所述治疗具有有利响应或者受益于所述治疗的受试者。在这些实施方案中,可能具有有利响应但是程度较低或者轻微受益于所述治疗的那些(即组2患者)和可能对治疗具有不利响应或经历由所述治疗导致的不利作用的那些(即组3患者)可以分组在一起并且简单表示为可能不具有有利响应或不受益于所述治疗的受试者。这适用于本文公开的所有其他实施方案,即使关于那些实施方案没有特别提到。
如图3c所示,降低的prol1水平表示明确的有利响应,而正常的prol1水平表示患者可能在一定程度上受益于所述治疗或者受试者可能不受益于所述治疗或者甚至经历不利作用。因此,prol1可以用于将组1患者与组2或3患者区分开来。由于prol1在本文鉴定的生物标记物中在患者组之间显示最高的倍数变化,因此它至少在一些实施方案中可以被考虑为用于本发明方法的最佳生物标记物。
如图3c表示,提高的tf水平指示明确的有利响应,而正常或降低的tf水平表示患者可能在一定程度上受益于治疗或者受试者可能不受益于所述治疗或者甚至经历不利作用。因此,tf可以用于将组1患者与组2或3患者区分开来。由于tf在本文鉴定的生物标记物中在患者组之间显示第二高的倍数变化,因此它至少在一些实施方案中可以被考虑为用于本发明方法的第二好的生物标记物。
如图3c表示,提高的myl6水平指示明确的有利响应,而正常或降低的myl6水平表示患者可能在一定程度上受益于治疗或者受试者可能不受益于所述治疗或者甚至经历不利作用。因此,myl6可以用于将组1患者与组2或3患者区分开来。由于myl6在本文鉴定的生物标记物之中显示最明确的倍数变化区别,因此它至少在一些实施方案中可以被考虑为用于本发明方法的第三最佳生物标记物。
因此,在一些优选实施方案中,本发明方法是基于确定单独的prol1水平或者其与tf和/或myl6的组合。可能具有明确有利响应的患者显示降低的prol1表达以及增加的tf和myl6表达。在一些其他实施方案中,该方法可以包括测定获自受试者的样品中一种或多种另外的选自下组的生物标记物(以任意组合):cst4、hspa8、cst1、ywhaz、rnh1、uchl3、cst2、s100a6、b2m、gsr、s100a8、hspa5、ywhae、cndp2、csta、cstb、cst5和cst3。
如图3c所示,降低的cst1水平表示明确的有利响应,而正常的cst1水平表示患者可能在一定程度上受益于治疗,而提高的cst1水平表示受试者可能不受益于所述治疗或者经历不利作用。因此,cst1可以用于将组1、2和3的患者彼此区分开来。
在一些优选实施方案中,本发明方法是基于确定prol1和cst1两者的水平。可能具有明确有利响应的患者显示prol1和cst1两者的降低的表达。可能具有有利响应但是程度较小的患者显示prol1和cst1两者的正常水平。可能不受益于治疗或者经历不利作用的患者显示正常的prol1水平和提高的cst1水平。在一些另外的实施方案中,也使用tf和/或myl6并且与prol1和cst1组合使用。在一些还有的其他实施方案中,方法可以包括测定获自受试者的样品的一种或多种另外的选自下组的生物标记物:cst4、hspa8、ywhaz、rnh1、uchl3、cst2、s100a6、b2m、gsr、s100a8、hspa5、ywhae、cndp2、csta、cstb、cst5、cst3。
因此,除了如上所述基于prol1预测,可能显著受益于治疗(诸如药物转换(例如,从含有防腐剂的眼药转换为不含防腐剂的眼药))的受试者(即,患者组1)可以通过与相关对照相比,提高水平的选自tf、hspa8、ywhaz、rnh1、uchl3、myl6、s100a6、gsr、s100a8、hspa5、ywhae和cndp2的一种或多种生物标记物和/或降低水平的选自cst1、cst4、cst2、b2m、cst5和cst3的一种或多种生物标记物和/或正常水平的csta、cstb之一或两者来鉴定。这些另外的生物标记物可以以任何所需组合使用。
因此,除了如上所述基于prol1预测,可能在一定程度上受益于治疗(诸如药物转换(例如,从含有防腐剂的眼药转换为不含防腐剂的眼药))的受试者(即,患者组2)可以通过与相关对照相比,提高水平的选自uchl3、rnh1、cstb、cst5和cst2的一种或多种生物标记物和/或降低水平的myl6和/或正常水平的选自tf、cst4、hspa8、cst1、ywhaz、s100a6、b2m、gsr、s100a8、hspa5、ywhae、cndp2、csta和cst3的一种或多种生物标记物来鉴定。这些另外的生物标记物可以以任何所需组合使用。
因此,除了如上所述基于prol1预测,可能不受益于治疗(诸如药物转换(例如,从含有防腐剂的眼药转换为不含防腐剂的眼药))或者甚至经历由所述治疗导致的不利作用的受试者(即,患者组3)可以通过与相关对照相比,提高水平的选自cst1、cstb、csta、cst3、cst5、cst2和cst4的一种或多种生物标记物和/或降低水平的myl6和/或正常水平的选自tf、hspa8、ywhaz、rnh1、uchl3、s100a6、b2m、gsr、s100a8、hspa5、ywhae和cndp2的一种或多种生物标记物来鉴定。这些另外的生物标记物可以以任何所需组合使用。
根据以上,优选生物标记物组合的非限制性实例在以下表1中列出。
表1.优选生物标记物组合列表
在一些实施方案中,本发明方法可以包括药物转换,即将先前使用的眼用药物改变为不同的眼用药物。优选地,含有防腐剂的药用药物转换为不含防腐剂的眼用药物。在一些实施方案中,本发明的方法可以包括向受试者施用眼用药物、优选不含防腐剂的眼用药物,其中将预测所述受试者对于眼病治疗的响应。
本发明的生物标记物谱图可以通过本领域可用的任何适当技术来确定,所述技术包括但不限于任何质谱法(例如,微型lc-ms/ms)、任何基于抗体的技术(例如,elisa、蛋白质印迹)、任何基于rna的技术(例如,rna-测序或微阵列)。
在一方面,本发明涉及用于实施本发明方法的试剂盒。所述试剂盒可以包括评估本文公开的生物标记物组合的水平所需的任何试剂或测试试剂。本领域技术人员可以容易地确定将包括的试剂,这取决于所讨论的生物标记物组合和实施所述评估的所需技术。在一些实施方案中,试剂盒可以包括适当的对照样品或阈值。试剂盒也可以包括计算机可读介质,其包括计算机可执行的指令,用于实施本发明的任一方法。
如本领域技术人员明白的,关于预测受试者对于眼病治疗的响应的方法的本发明的任何实施方案、细节、优势等相应地适用于本发明的其他方面,包括所公开的生物标记物组合在所述预测中的用途和用于所述预测的试剂盒,反之亦然。
对于本领域技术人员而言显而易见的是,随着技术发展,本发明的构思可以以各种方式实施。本发明及其实施方案不限于下述实施例,而是可以在权利要求的范围内变化。
实施例
实施例1.青光眼药物转换
方法
研究人群
本研究依据国际协调会议药品临床试验指南(internationalconferenceofharmonizationgoodclinicalpracticeguidelines)和赫尔辛基宣言(declarationofhelsinki)进行。临床研究被坦佩雷大学医院伦理委员会批准,并且登记于eu临床试验注册处(eudract号:2010-021039-14)。在进入研究之前每名患者签署了书面知情同意书。
在基线随访期间评估患者,并且合格的患者在一只眼或两只眼中具有原发性开角的囊膜性青光眼或眼高压。包括的患者也已经接受防腐的拉坦前列素治疗达6个月或更长,并且显示至少两个眼睛症状或眼表刺激/炎症的一个症状和一个体征。基于这些纳入标准,选择三十名患者。
排除在研究之外的患者具有色素性或闭角型青光眼、基线高于22mmhg的iop、影响眼压测量的角膜异常,最近(6个月内)已经进行眼部手术(包括激光操作),佩戴隐形眼镜,或正在使用含有防腐剂的人工泪液。另外,排除了孕妇和哺乳期妇女以及没有充分避孕而可能怀孕的妇女。
研究概述
本研究由6次随访组成:筛查/基线随访,在基线后1.5、3、6和12个月时的随访,和12-个月随访后1-4周的随访(图1)。在基线随访中,患者从防腐的拉坦前列素(
泪液采集和样品制备
在没有麻醉的情况下使用席尔梅尔氏试纸条(teartouch,madhuinstruments,newdelhi,印度)采集患者泪液样品。将所述试纸条插入患者下眼睑下并且在5分钟后移出。记录眼泪量(mm),然后将试纸条储存在-80℃直至蛋白质组学分析。
为了提取眼泪蛋白,首先将席尔梅尔氏试纸条切割成小条并且溶解在含有蛋白酶抑制剂混合物(thermofisherscientificinc.,waltham,ma,usa)的50mm碳酸氢铵溶液中达3小时。然后将样品离心并且测量上清液的总蛋白浓度。将来自每个样品的多至50μg的蛋白在快速真空浓缩器中干燥。将蛋白溶解在2%十二烷基硫酸钠(sds)中并且在+60℃通过50mmtris-(2-羧乙基)膦(tcep)还原60min。然后将样品转移到30kda分子量截止值的滤器(pallcorporation,portwashington,纽约,usa)中并用在50mmtris-hcl中的8m尿素(merckkgaa,darmstadt,德国)冲洗两次。在暗处在室温通过碘乙酰胺(iaa)封闭半胱氨酸残基。通过离心终止烷基化,并且将样品用尿素溶液冲洗三次。随后用消化缓冲液进行漂洗三次,之后用胰蛋白酶(sciex,framingham,ma,usa)在+37℃消化16h,胰蛋白酶与蛋白的比率为1:25。将消化物在快速真空浓缩器中干燥,并且用piercec18tips(thermofisherscientific)根据制造商的说明书脱盐。在清理后将样品再次真空干燥并储存在-20℃直至以相同浓度重构至加样溶液(5%acn,0.1%fa)。将hrm肽混合物(biognosys,zurich,瑞士)加入每个样品,之后进行nanorplc-tripletoftmswath分析。除非另外说明,所有试剂购自sigma-aldrich(st.louis,mo,usa)。对每个样品进行两次重复的ms分析。
使用swath-ms分析进行蛋白质鉴定和定量
使用与高速tripletoftm5600+质谱仪(absciex,concord,加拿大)偶联的eksigent425nanolc分析消化的肽。将毛细管rp-lc柱(
在swathid文库分析中的质谱仪的关键参数是:离子喷雾电压浮动(isvf)2300v,气帘气体(cur)30,接口加热器温度(iht)+125℃,离子源气体113,去簇电压(dp)100v。通过信息依赖性获取(ida)方法从相同样品创建用于swath分析的文库,通过swath方法完成相对定量分析。所有方法通过analysttf1.5软件(absciex,usa)拉制。对于ida参数,在质量范围350-1250mz内的0.25sms全扫描(surveyscan),接着是在100-1500da质量范围内的60ms/ms扫描(总循环时间3.302s)。转换标准设定为质荷比(m/z)大于350且小于1250(m/z)的离子,电荷状态2-5和丰度阈值为超过120个计数。前靶离子的排除设定为12s。ida旋转碰撞能量(ce)参数脚本被设定为自动控制ce。swath定量分析参数与swathid相同,除了以下以外:循环时间3.332s和ms参数设定为15da窗口,在质量范围350-1250da之间具有1da重叠,接着在100-1500da的质量范围内40ms/ms扫描。
swath文库创建
使用proteinpilot软件4.6版(sciex,加拿大)创建swath文库,所述软件用于分析ms/ms数据和针对uniprotswissprot秘密文库检索进行蛋白质鉴定。proteinpilot中paragon搜索算法中的一些重要设定如下配置。样品类型:鉴定,cys-烷基化:iaa,消化:胰蛋白酶,仪器:tripletof5600+,检索工作:所有id。在proteinpilot中进行假发现率(fdr)分析,并且设定fdr<1%用于蛋白质鉴定。将来自患者的所有鉴定运行的数据合并为一批并用于文库创建。将具有swath的
数据处理和统计学分析
总共,使用swath-ms方法成功定量了785个蛋白。应用log2-转换来获得更正规分布的数据,并且进行分位数归一化。大多数样品具有两个重复的ms分析并且它们之间的变异通过组内相关(r中的icc包)和通过置换检验使用斯皮尔曼等级相关系数来评估。然后通过取几何平均数来合并重复的ms分析。
对于临床数据,将关于顺序(ordinal)临床体征的连续配对t检验和配对2-组wflcoxon符号秩检验用于检验临床体征和症状在随访期间是如何改变的。对于蛋白质组学数据,使用分级群聚(euclidean距离测量和ward’s方法作为标准)分析基线和其他随访之间的倍数变化(log2)以便鉴定与眼表并发症相关的成簇的蛋白组。使用
对于感兴趣的蛋白实施人工峰核查,因此,由于的肽匹配差,从结果中省略一些统计学显著的蛋白。将benjamini&hochberg校正应用于p-值,并且仅考虑调整的p-值在阈值(α=0.05)之下的蛋白,除非另外指出。使用r软件3.2.3版(rcoreteam.foundationforstatisticalcomputing,vienna,austria)和qiagen’s
结果
研究人群特征和临床结果
因为一名患者在后续跟踪期间死亡和一名患者终止研究,研究人群由28名患者(7个男性和21个女性)组成。二十五名患者诊断有原发性开角型青光眼并且3名具有囊膜性青光眼。研究开始时患者的平均年龄是67.4岁(95%ci:64.5-70.3)。患者平均接受防腐的拉坦前列素治疗达7.7年(95%ci:6.1-9.2)。我们没有发现临床和蛋白质组学结果与患者年龄、性别、诊断和拉坦前列素治疗持续时间之间的关联(数据未显示)。
患者的大多数临床体征和症状在转换后整个12个月期间持续改善(表2和表3)。更具体地,结膜红肿和睑炎减少而ftbut和席尔梅尔氏试验结果增加。这些提示大多数患者经历副作用减轻。尽管角膜和结膜染色得分没有显著改变,但是总体平均值提示该分数下降。在具有最高初始染色得分的患者中发生了角膜和结膜染色的最突出的降低(未显示)。患者经历的所有症状在转换后改善,但是这些改善中的一些不是统计学显著的。
表2.在药物转换后在基线和随访之间临床体征的变化
*p<0.05
**p<0.01
***p<0.001
ci(置信区间)
表3.在药物转换后在基线和随访之间临床症状的变化
*r<0.05
**p<0.01
***p<0.001
2-组wilcoxon符号秩检验
ci(置信区间)
不同相对蛋白表达水平可以用于对患者分层
使用swath-ms从每个眼泪样品中定量总共785个蛋白。蛋白质组学数据显示了良好的质量和可靠性,在89%的重复ms分析中p-值<0.05(置换检验,斯皮尔曼秩相关)并且平均值icc系数为0.97。
我们想确定在12个月治疗期间每个患者的蛋白质谱图是如何变化的。为此,我们首先将在第一次随访和最后一次随访之间的log2倍数变化归簇,并且基于系统树图和结果的视觉观察,我们在7个簇处设定了截止值(图2)。然后我们对于所有7个蛋白簇用ipa进行了路径分析,并且鉴定了三个目标簇,富含炎性蛋白。这三个簇内的蛋白表达水平的变化在图2中表示,包括还来自较早随访的蛋白表达数据并且很好地显示了在12个月的跟踪时间期间如何阐明患者之间的蛋白质谱图。第一个蛋白簇由各种有益的(泪腺分泌蛋白)眼表生物标记物如溶菌酶(lyz)、富含脯氨酸蛋白1(prol1)和各种半胱氨酸蛋白酶抑制剂组成。该簇中总共有71个蛋白,顶部(top)富集的疾病和功能术语包括中性白细胞活化和慢性炎性疾病。第二簇包括炎症生物标记物如白蛋白(alb)、血清转铁蛋白(tf)、蛋白s100a8和膜联蛋白,总共116个蛋白全部显示类似的倍数变化。关于该簇的顶部富集的术语包括器官炎症和细胞死亡。第三簇也包括已知的炎症生物标记物,如补体c3(c3)、α-烯醇化酶(eno1)和蛋白s100a9。该簇中135个类似表达的蛋白具有与细胞死亡、细胞运动和细胞浸润相关的富集。
基于在研究期间蛋白质组谱图的变化,可以将患者分层成三组(图2)。基于他们的蛋白质组谱图,组1和2中的患者显示改善:抗炎蛋白表达增加和促炎蛋白表达降低。组3中的患者经历抗炎蛋白表达的降低和促炎蛋白表达的增加,提示他们没有从药物转换中受益良多。
数个蛋白的基线表达水平指示患者组之间的个体差异
接下来,我们想测试特定蛋白的基线表达水平是否能够解释在v5时三个患者组之间的差异并且进行单向anova。在p-值调整后,在322个归簇蛋白中,31个保持统计学显著(p-值<0.05)。我们排除了一个没有基因符号的蛋白(免疫球蛋白)、两个具有不等方差的蛋白(异方差性,levene’s检验p-值<0.05)和六个具有差的峰匹配的蛋白,获得总共22个在基线处在患者组之间不同的蛋白(图3)。
蛋白表达水平与席尔梅尔氏试验和ftbut值相关
最后,我们想要用三个鉴定的患者组中的眼泪蛋白质组学数据检验临床结果,并且进行了混合效应模型分析。在三个患者组之间有区别的所有促炎蛋白(图3a)与席尔梅尔氏试验结果相关,并且四个与ftbut相关(表4和图4)。各种半胱氨酸蛋白酶抑制剂,prol1和b2m(图3b)与席尔梅尔氏试验正相关,并且酰基-coa-结合蛋白(dbi)(图3c)与席尔梅尔氏试验负相关(图4)。我们观察到低席尔梅尔氏试验值和低ftbut值与有害促炎蛋白的高表达和有益蛋白的低表达相关。
表4.在基线处区分患者组的蛋白,其也与席尔梅尔氏试验和荧光泪膜破裂时间(ftbut)相关。随着临床体征增加,具有负log2(表达)的蛋白减少,对于正值反之亦然。
dv=因变量
实施例2.患者实施例
选择四名在他们的防腐前列腺素类似物眼用药物期间具有类似副作用史的患者作为这里的患者实例。其他的患者特征也是类似的:所有患者是年龄为62-69岁的女性。所有四名患者在研究期间从防腐的前列腺素类似物转换为不含防腐剂的前列腺类似物,然而,如图5所示,在一年后根据蛋白质组谱图和临床体征,患者中的两名(003,029)受益于所述转换,而另外两名(004,028)则没有受益于所述转换。在基线处区分这些患者的蛋白之一是prol1,其在根据临床和蛋白质组谱图变化受益于所述转换的患者中具有降低的表达水平。
本实施例证实了prol1可以用作用于确定对眼病药物治疗的响应的预测性生物标记物。
- 还没有人留言评论。精彩留言会获得点赞!