一种登革病毒NS1抗原检测试纸条、试剂盒及其制备方法与流程
本发明属于体外诊断技术领域,具体涉及生物检测技术领域,特别涉及一种登革病毒ns1抗原检测试剂盒的制备方法。
背景技术:
登革热是由登革热病毒引起的一种急性传染病,以埃及伊蚊和白纹伊蚊为传播媒介,具有传播迅猛、发病率高、人群普遍易感、重症类型死亡率高等特点,被认为是全球最受关注的传染病。目前在非洲、美洲、东地中海、东南亚和西太平洋100多个国家呈地方性流行,东南亚和西太平洋地区受dv(登革病毒)影响更为严重。大约2.5亿人生活在登革热流行国家,感染dv后可发生登革热、登革出血热(dhf)或登革休克综合征(dss)。每年估计有5000万以上的登革热感染发生,其中50万人因患登革热需住院治疗,感染者中约2.5%发生死亡。
在我国,登革热具有典型的输入性和突发性,在发生时常常表现为较大范围、较严重的暴发流行等特点。按照《中华人民共和国传染病防治法》的规定为乙类传染病。近年来,登革热在我国本地暴发流行区域主要集中在广东、云南、浙江、广西、福建省(自治区)等东南沿海和边境省份,而输入病例在我国多数省份有分布。2014年我国登革热爆发时病例的发生数量超过45000例。
登革病毒有四个血清型,在一个地区往往存在不同血清型病毒的交替流行,这更增加了登革出血热和登革休克综合征发生的可能性。登革出血热和登革休克综合征的病死率较高,不仅严重影响人民的身体健康,增加医疗负担,而且严重影响居民生活和旅游业的发展,进而影响当地的经济发展,同时由于控制不当还会造成大量的杀虫剂浪费,导致环境污染,严重影响人类和环境健康,也能诱发媒介生物抗药性。
登革热的检测对象为媒介标本(伊蚊成蚊和幼虫)、疑似和临床诊断病例(按照登革热诊断标准ws216-2008)。媒介标本检测分为核酸检测和病毒分离两种方法。疑似和临床诊断病例检测,包括病原学检测和血清学检测。由于目前尚无特效的抗病毒治疗药物,主要采取支持及对症治疗措施。治疗原则是早发现、早诊断、早治疗、早防蚊隔离。
而目前,市面上缺乏针对登革病毒检测的试剂盒。
技术实现要素:
本发明的目的在于提供一种登革病毒ns1抗原检测试纸条和包括该试纸条的检测卡。该登革病毒ns1抗原检测试纸条和检测卡可特异快速地进行登革病毒早期感染的检测与诊断,减低成本,检测速度快。
本发明的另一目的在于提供上述登革病毒ns1抗原检测试纸条和包括该试纸条的检测卡的制备方法。该制备方法得到的登革病毒ns1抗原检测试纸条和检测卡应用简便,结果准确,为下一步准确治疗由登革病毒引起的疾病提供了依据,适于大规模推广应用。
本发明的另一目的在于提供含有上述登革病毒ns1抗原检测卡的试剂盒。该试剂盒可特异快速地进行登革病毒早期感染的检测与诊断,减低成本,快速检测,有效满足临床使用的需要。
为实现上述目的,本发明提供了一种登革病毒ns1抗原检测试纸条的制备方法采用了如下的技术方案:
a.用氯化金溶液和柠檬酸三钠溶液制备胶体金溶液;
b.碳酸钾调节步骤a得到的胶体金溶液的ph至6.5-8.0,依次加入ns1mab5、牛血清白蛋白溶液,离心得到沉淀,重悬液重悬沉淀得到胶体金标记的ns1mab5溶液;
c.用结合垫处理液均匀喷涂在结合垫上进行预处理,预处理结束后用步骤b得到的胶体金标记的ns1mab5溶液对结合垫喷金得到免疫结合垫,划膜结束后将免疫结合垫置于室温,湿度≤30%条件下干燥1小时;
d.用包被缓冲液稀释ns1mab6得到检测线工作液;用包被缓冲液稀释羊抗鼠igg多抗得到质控线工作液;用检测线工作液和质控线工作液分别在贴于聚氯乙烯底板的硝酸纤维素膜上划线,划膜结束后将膜置于37℃干燥箱中干燥24小时;
e.用样品垫处理液均匀喷涂在样品垫上进行预处理;
f将样品垫和免疫结合垫贴于划膜的硝酸纤维素膜下方,将吸水纸贴于划膜的硝酸纤维素膜的上方得到登革病毒ns1抗原检测试纸条。
优选地,上述技术方案中,胶体金标记用的抗登革病毒ns1单克隆抗体为ns1mab5,硝酸纤维素膜包被用的抗登革病毒ns1单克隆抗体为ns1mab6。
优选地,上述技术方案中,步骤a所述的具体制备步骤为称取990g水于三角烧瓶中,加入10ml浓度为2%的氯化金溶液,即溶液中氯化金的终浓度为0.02%,将烧瓶置于磁力搅拌器上加热至沸腾,迅速加入13ml浓度为2%的柠檬酸三钠溶液,待溶液变为红棕色后继续加热沸腾5分钟,静置至恢复室温,置于4℃保存待用。
优选地,上述技术方案中,步骤b所述的具体步骤是将胶体金溶液中加入0.2m碳酸钾,混匀调节ph至6.5-8.0,然后加入ns1mab5,继续搅拌30min,再加入2ml10%牛血清白蛋白溶液,继续搅拌30min,在4℃、转速为8000g的条件下离心30min得到沉淀,沉淀用1ml重悬液复溶
优选地,上述技术方案中,步骤b所述重悬液为0.01m磷酸盐缓冲液,每100ml磷酸盐缓冲液包含lg牛血清白蛋白和10g海藻糖、0.05%nan3,ph7.0±0.1。
优选地,上述技术方案中,步骤c所述的免疫结合垫采用玻璃纤维膜或聚酯纤维膜。
优选地,上述技术方案中,步骤c所述结合垫处理液为硼酸-硼砂缓冲体系,每100ml结合垫处理液含0.9g硼酸、0.6g四硼酸钠、5g海藻糖、0.5gbsa、10mg阻断剂、0.2%tritonx-100、0.05%nan3,ph8.6±0.1。
优选地,上述技术方案中,步骤d中,所述的包被缓冲液为tris缓冲体系,每100ml包被缓冲液含1.2lgtris、0.5g氯化钠、3g蔗糖、0.05%nan3,ph8.6±0.1。
优选地,上述技术方案中,步骤d中所述检测线工作液浓度为1.0mg/ml;所述质控线工作液浓度为1.5mg/ml。
优选地,上述技术方案中,步骤e中所述样品垫采用玻璃纤维膜或聚酯纤维膜。
优选地,上述技术方案中,步骤e中所述样品垫处理液为tris缓冲体系,每100ml样品垫缓冲溶液中含1.2lgtris、0.4g酪蛋白钠、1%tween80、0.05%nan3,ph8.6±0.1。
本发明提供了一种登革病毒ns1抗原检测卡,其制备方法为:将上述获得的登革病毒ns1抗原检测试纸条置入塑料外壳中,其中,塑料外壳的加样孔在样品垫上方,塑料外壳的观察窗在检测线t和质控线c上方,加样孔和观察窗上方无遮挡物。
本发明提供了一种登革病毒ns1抗原检测试剂盒,其制备方法为:将上述获得的登革病毒ns1抗原检测卡装入铝箔袋,与采样吸管、说明书装盒组成登革病毒ns1抗原检测试剂盒。
一种登革病毒ns1抗原检测试纸条,试纸条自上而下依次由样品垫、免疫结合垫、硝酸纤维素膜和吸水垫粘贴于聚氯乙烯底板上组成,其中,所述免疫结合垫上包被胶体金标记的ns1mab5,硝酸纤维素膜设有检测线t和质控线c,检测线t包被了ns1mab6,质控线包被了羊抗鼠igg多抗。
一种登革病毒ns1抗原检测卡,包括装有上述试纸条的塑料外壳,其中塑料外壳的卡壳上盖上设有加样孔和观察窗,加样孔在样品垫上方,观察窗在检测线t和质控线c上方。
一种登革病毒ns1抗原检测试剂盒,将装有上述检测卡的铝箔袋、采样吸管和说明书装盒得到试剂盒。
本发明采用胶体金免疫层析原理,在结合垫上包被胶体金标记的ns1mab5,在硝酸纤维素膜上分别包被ns1mab6和羊抗鼠igg多克隆抗体。检测阳性标本时,样本中的登革病毒ns1抗原,与金标记的抗体结合形成复合物,经层析作用,被包被有ns1mab6的检测线捕获并显色,其余的金标复合物继续层析与质控线处的羊抗鼠igg捕获并显色。质控线所呈现的红色/粉色反应线是判定层析过程是否正常的标准,同时也作为试剂的内控标准。
与现有技术相比,本发明的有益效果在于:
1、检测灵敏度高;
2、检测时间短,仅需15分钟即可得到检测结果;
3、操作简单,经简单培训即可独立进行操作,无需专业人士;
4、对使用环境要求低,适用各种复杂用户场景。
附图说明:
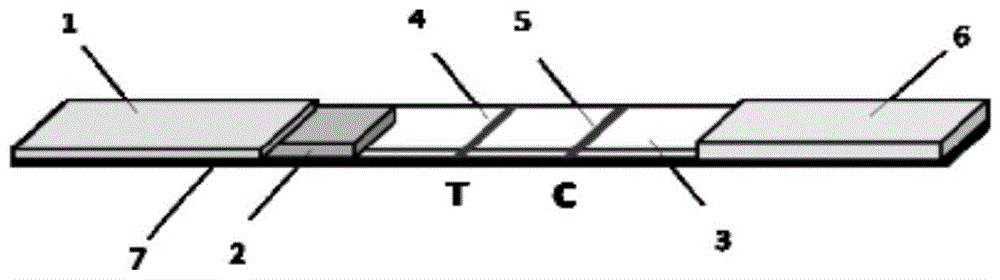
图1为本发明实施例中的登革病毒ns1抗原检测试纸条的结构示意图;
图2为本发明实施例中的登革病毒ns1抗原检测卡的透视图。
图中:1-样品垫;2-免疫结合垫;3-硝酸纤维素膜;4-检测线;5-质控线;6-吸水垫;7-聚氯乙烯底板;8-塑料外壳;9-加样孔;10-观察窗。
具体实施方式:
下为使本发明实施例的目的、技术方案和优点更加清楚,下面将对本发明实施例中的技术方案进行清楚、完整地描述。实施例中未注明具体条件者,按照常规条件或制造商建议的条件进行。所用试剂或仪器未注明生产厂商者,均为可以通过市售购买获得的常规产品。
下列实施例中未注明具体条件的实验方法,通常按照常规条件,例如sambrook等人,分子克隆:实验室手册(newyork:coldspringharborlaboratorypress,1989)中所述的条件,或按照制造厂商所建议的条件。
以下结合实施例对本发明的特征和性能作进一步的详细描述。
实施例1
本实施例提供的登革病毒ns1抗原检测卡的制备方法,具体步骤如下:
本实施例所用喷金划膜仪,型号:xyz3020,生产厂家:上海捷宁生物科技有限公司;
本实施例所用:ns1mab5抗登革病毒ns1单克隆抗体、ns1mab6抗登革病毒ns1单克隆抗体,生产厂家:奥创生物技术(山东)有限公司;羊抗鼠抗体,生产厂家:菲鹏生物股份有限公司。
(1)胶体金溶液的制备
以1l为例,称取990g水于三角烧瓶中,加入10ml浓度为2%的氯化金溶液,即溶液中氯化金的终浓度为0.02%。将烧瓶置于磁力搅拌器上加热至沸腾,迅速加入11ml浓度为2%的柠檬酸三钠溶液,待溶液变为红棕色后继续加热沸腾5分钟,静置至恢复室温,置于4℃保存待用。
(2)胶体金标记ns1mab5
在一个较佳的实施例中,用0.2m碳酸钾溶液调节50ml浓度为0.02%的胶体金溶液ph至7.0,在搅拌的条件下,逐滴缓慢将0.5ml1mg/ml待标记的ns1mab5加入上述胶体金溶液中,继续搅拌30min;
在一个较佳的实施例中,用0.2m碳酸钾溶液调节50ml浓度为0.02%的胶体金溶液ph至6.5,在搅拌的条件下,逐滴缓慢将0.5ml1mg/ml待标记的ns1mab5加入上述胶体金溶液中,继续搅拌30min;
在一个较佳的实施例中,用0.2m碳酸钾溶液调节50ml浓度为0.02%的胶体金溶液ph至8.0,在搅拌的条件下,逐滴缓慢将0.5ml1mg/ml待标记的ns1mab5加入上述胶体金溶液中,继续搅拌30min;
在搅拌的条件下将2ml10%牛血清白蛋白溶液缓慢滴加到上述胶体金溶液中,继续搅拌30min,得到混合溶液;
混合溶液在8000g、4℃条件下离心30min,去上清,留疏松沉淀;沉淀用1ml重悬液复溶,转入2.0ml离心管中,得ns1mab5免疫金浓缩溶液,即胶体金标记的ns1mab5溶液。用紫外分光光度计测最大吸收峰处的吸光度值,即为免疫金浓缩液浓度,即用或4℃保存备用。
所用重悬液为0.01m磷酸盐缓冲液,每100ml磷酸盐缓冲液包含lg牛血清白蛋白和10g海藻糖、0.05%nan3,ph7.0±0.1。
(3)制备免疫结合垫
将20cm*30cm的8964玻璃纤维用结合垫处理液预处理,即将25ml的结合垫处理液均匀喷涂在玻璃纤维上至完全浸润。在湿度≤30%条件下干燥12h,真空干燥箱干燥4h,切刀切成0.5cm*30cm的长条,置于铝箔袋中加干燥剂室温密封保存备用。
所用结合垫处理液为硼酸-硼砂缓冲体系,每100ml结合垫处理液含0.9g硼酸、0.6g四硼酸钠、5g海藻糖、0.5gbsa、10mg阻断剂、0.2%tritonx-100、0.05%nan3,ph8.6±0.1。
设定喷金划膜仪,开启电源,运行喷金模块,设定喷金程序;1号管道为喷金通道;喷金划膜仪初始化:将1号管道置于ns1mab5免疫金溶液中,选择初始化程序,清洗管道10个循环,设置喷量为1.2μl/ml,将预处理后的玻璃纤维按固定位置平放在板面上,开始喷金,条带均匀、连续和贯通整个结合垫的为合格品,两条直线中出现断点为不合格,标出不合格区域;喷金结束,清洗管道。
喷金处理后的免疫结合垫置于室温,湿度≤30%条件下干燥1小时,然后在0.1mpa条件下真空干燥1小时干燥处理后置于铝箔袋中,室温密封保存备用。
(4)制备免疫硝酸纤维素膜
取500μgns1mab6,用包被缓冲液稀释至1mg/ml,得到检测线工作液,相应容器标记t标志,2-8℃保存备用。
取羊抗鼠igg多抗500μg,用包被缓冲液稀释至1.5mg/ml,得到质控线工作液,相应容器标记c标志,2-8℃保存备用。
所用包被缓冲液为tris缓冲体系,每100ml包被缓冲液含1.2lgtris、0.5g氯化钠、3g蔗糖、0.05%nan3,ph8.6±0.1。
设定划膜仪,开启划膜仪的电源,设定划膜程序,划膜喷量为1μl/cm;1号管道为检测线通道,2号管道为质控线通道;划膜仪初始化:将1号管道置于检测线工作液中,将2号管道置于质控线工作液,选择初始化程序,清洗管道10个循环;
将聚氯乙烯底板上较宽部分的保护纸除去,沿上面保护纸的下边缘,将空白的硝酸纤维素膜粘贴于聚氯乙烯底板上,得到贴膜的聚氯乙烯底板。将贴有硝酸纤维素膜的聚氯乙烯底板的按固定位置平放在划膜仪上,开始划膜。检查划好线的硝酸纤维素膜,检测线和质控线为两条均匀、连续和贯通整个硝酸纤维素膜的直线为合格品,两条直线中出现断点区为不合格品,标出不合格区域。
划膜结束,将划膜的硝酸纤维素膜置于37℃干燥箱中,干燥24小时后置于铝箔袋中,加干燥剂密封保存备用。
(5)制备样品垫
将20cm*30cm的8964玻璃纤维用结合垫处理液预处理,即将25ml的样品垫处理液均匀喷涂在玻璃纤维上至完全浸润。在温度37℃-45℃、湿度≤30%条件下干燥12h,真空干燥箱干燥4h,切刀切成1.6cm*30cm的长条,置于铝箔袋中加干燥剂室温密封保存备用。
所用样品垫处理液为tris缓冲体系,每100ml样品垫缓冲溶液中含1.21gtris、0.4g酪蛋白钠、1%tween80、0.05%nan3,ph8.6±0.1。
(6)贴膜、切膜
组装试纸条,将免疫结合垫贴于划膜的硝酸纤维素膜下方,与膜接触1-2mm;样品垫贴在免疫结合垫下方,与免疫结合垫少许接触;接着除去上方保护纸,将吸水纸贴在硝酸纤维素膜的上方,与膜接触1-2mm。
接通裁条机电源,设定切割宽度为4mm;将试纸条合格品平放入切割机平台轨道中,正面朝上,按操作面板上“开始”键,开始切割;每放一片试纸条合格品,按操作面板上“开始”键一次,直至切割完所有试纸条合格品。
切割完成后,将试纸条装入塑料外壳,压卡机压紧,即得到登革病毒ns1抗原检测卡。
本实施例得到的登革病毒ns1抗原检测试纸条的结构如图1所示,检测卡的结构如图2所示,其包括塑料外壳8以及在卡壳上盖上的加样孔9,观察窗10和卡入在外壳内聚氯乙烯底板7,聚氯乙烯底板7上具有自左往右依次搭接的样品垫1、免疫结合垫2、硝酸纤维素膜3和吸水垫6;
样品垫1、免疫结合垫2、硝酸纤维素膜3和吸水垫6均粘附在聚氯乙烯底板7上。
其中,硝酸纤维素膜3上具有检测线4和质控线5,检测线4上包被有ns1mab6,质控线5包被有羊抗鼠igg多抗。免疫结合垫2上含有胶体金标记的ns1mab5。
实施例2试剂盒组装
取铝箔袋和干燥剂;打开热封机,预热;将待装袋的实施例1制得的检测卡、1袋干燥剂装入铝箔袋中;用热封机封好铝箔袋;贴上标签。
装有检测卡的铝箔袋与采样吸管、说明书等装盒即为登革病毒ns1抗原检测试剂盒成品。
实施例3
采用实施例1提供的登革病毒ns1抗原检测卡或实施例2提供的登革病毒ns1抗原检测试剂盒检测样本的方法:
采用登革病毒ns1抗原检测卡在测试时,滴加70μl左右的血清/血浆,水平放置。如样本中含有登革病毒ns1抗原,ns1mab5-胶体金与样本中的登革病毒ns1抗原结合在一起,形成“抗原-抗体-金”复合物,复合物沿着试纸条层析移动,首先到达包被了ns1mab6的检测线,“抗原-抗体-金”复合物将与抗登革病毒ns1mab6结合,并在检测线上滞留下来,形成一条红色的线,这表示阳性结果。线条颜色的深浅同样本中的抗原数量没有比例关系。如果无显色的条带表示样本中不含登革病毒ns1抗原或登革病毒ns1抗原低于本试纸最低检出限,游离的“抗体-金”复合物继续层析,到达包被了羊抗鼠igg抗体的质控线,同羊抗鼠igg结合在一起而富集在对照区,形成一条红色的线。质控线的出现证明试纸条检测功能正常。无论样本中是否含有登革病毒ns1抗原,在有效试验中,试纸条的质控线都应当显色。样本继续移动,到达吸水纸。吸水纸的作用是吸附剩余的复合物,使其在试纸条内移动,并消除本底的颜色。自试纸条加入样本起计时,15分钟左右方可读取结果。
实施例4
采用实施例l提供的登革病毒ns1抗原检测卡或实施例2提供的登革病毒ns1抗原检测试剂盒检测不同浓度梯度的登革i型灭活病毒培养液、登革ii型灭活病毒培养、登革iii型灭活病毒培养、登革iv型灭活病毒培养。
结果显示登革病毒ns1抗原检测卡对4个血清型的登革病毒均有良好的反应性,见表1。
表1登革病毒ns1抗原检测卡对4型登革病毒检出限
实施例5
采用实施例1提供的登革病毒ns1抗原检测卡或实施例2提供的登革病毒ns1抗原检测试剂盒检测不同类型的干扰样本。
结果显示登革病毒ns1抗原检测卡对下列干扰样本无交叉反应,见表2。
表2登革病毒ns1抗原检测卡对不同类型干扰样本的交叉反应
实施例6
采用实施例1提供的登革病毒ns1抗原检测卡或实施例2提供的登革病毒ns1抗原检测试剂盒检测不同病程的登革阳性临床样本。
结果显示登革病毒ns1抗原检测卡对临床样本的检出率达到80%,见表3。
表3登革病毒ns1抗原检测卡与对照试剂(pcr)比对
以上所述仅为本发明的优选实施例而已,并不用于限制本发明,对于本领域的技术人员来说,本发明可以有各种更改和变化。凡在本发明的精神和原则之内,所作的任何修改、等同替换、改进等,均应包含在本发明的保护范围之内。
- 还没有人留言评论。精彩留言会获得点赞!