参倍固肠胶囊中苍术、肉豆蔻和红参的薄层鉴别测定法的制作方法
本发明涉及药物有效成分技术领域,具体涉及是参倍固肠胶囊中苍术、肉豆蔻和红参的薄层鉴别测定法。
背景技术:
参倍固肠胶囊为一种常见中成药,其中包含五倍子、肉豆蔻(煨)、诃子肉(煨)、乌梅、木香、苍术、茯苓、鹿角霜、红参,具有固肠止泻,健脾温肾的作用。用于因脾肾阳虚所致的慢性腹泻,腹痛,肢体倦怠,神疲懒言,形寒肢冷,食少,腰膝酸软;肠易激综合征(腹泻型)见上述症候者。
在药物有效成分分析时需要对其中苍术、肉豆蔻和红参通过薄层鉴别测定法进行鉴定,但是由于参倍固肠胶囊中各成分重量较多,且苍术、肉豆蔻等含有挥发油,现有常规的薄层鉴别测定法较难从参倍固肠胶囊中提取待测定药物,同时受易挥发影响,显色较困难。
技术实现要素:
本发明针对常规的薄层鉴别测定法较难从参倍固肠胶囊中提取待测定目标药物,同时受目标药物易挥发的影响,最终显色较困难的问题,提供一种参倍固肠胶囊中苍术、肉豆蔻和红参的薄层鉴别测定法。
本发明解决上述技术问题,采用的技术方案是,一种参倍固肠胶囊中苍术、肉豆蔻和红参的薄层鉴别测定法,包括苍术薄层鉴别测定方法、肉豆蔻薄层鉴别测定方法和红参薄层鉴别测定方法。
进一步的,苍术薄层鉴别测定方法包括对照组试剂制备、测定组试剂制备和薄层鉴别测定,对照组试剂制备包括以下步骤:
s1,取苍术,将其研细,置具塞锥形瓶中并添加提取试剂,进行提取;
s2,将s1提取后溶液进行超声波处理,并过滤,待滤液挥干,制得残渣;
s3,在残渣中添加提取试剂,使得残渣溶解,制得对照组试剂;
测定组试剂制备包括以下步骤:
s1,取参倍固肠胶囊,将其研细,置具塞锥形瓶中并添加提取试剂,进行提取;
s2,将s1提取后溶液进行超声波处理,并过滤,待滤液挥干,制得残渣;
s3,在残渣中添加提取试剂,使得残渣溶解,制得测定组试剂;
薄层鉴别测定包括以下步骤:
s1,取对照组试剂和测定组试剂,分别点于同一硅胶g薄层板上,并通过展开剂进行展开;
s2,将展开后的硅胶g薄层板取出,晾干,并喷以显影试剂,加热;
s3,加热至适应温度后,在对照组试剂色谱和测定组试剂色谱相应的位置上,得到显示相同的颜色的荧光斑点。
进一步的,苍术薄层鉴别测定方法的对照组试剂制备步骤中,s1和s3中提取试剂均为沸程规格60℃~90℃的石油醚,测定组试剂制备步骤中,s1和s3中提取试剂均为沸程规格60℃~90℃的石油醚,薄层鉴别测定步骤中,s1展开剂为沸程规格60℃~90℃的石油醚,s2显影试剂为茴香醛试液。
可选的,苍术薄层鉴别测定方法的对照组试剂制备步骤中,s1苍术取0.5g,添加提取试剂为15ml,s2超声波处理20min,s3添加提取试剂为1ml,测定组试剂制备步骤中,s1苍术取5g,添加提取试剂为15ml,s2超声波处理20min,s3添加提取试剂为1ml,薄层鉴别测定步骤中,s1取对照组试剂2μl、测定组试剂10μl,s3加热温度为105℃。
进一步的,肉豆蔻薄层鉴别测定方法包括对照组试剂制备、测定组试剂制备和薄层鉴别测定,对照组试剂制备包括以下步骤:
s1,取肉豆蔻,将其研细,置具塞锥形瓶中并添加提取试剂,进行提取;
s2,将s1提取后溶液进行超声波处理,并过滤,收集滤液制得对照组试剂;
测定组试剂制备包括以下步骤:
s1,取参倍固肠胶囊,将其研细,置具塞锥形瓶中并添加提取试剂,进行提取;
s2,将s1提取后溶液进行超声波处理,并过滤,收集滤液制得测定组试剂;
薄层鉴别测定包括以下步骤:
s1,取对照组试剂和测定组试剂,分别点于同一硅胶g薄层板上,并通过展开剂进行展开;
s2,将展开后的硅胶g薄层板取出,晾干,并喷以显影试剂,加热;
s3,加热至适应温度后,在对照组试剂色谱和测定组试剂色谱相应的位置上,得到显示相同的颜色的荧光斑点。
可选的,肉豆蔻薄层鉴别测定方法的对照组试剂制备步骤中,s1中提取试剂为三氯甲烷,测定组试剂制备步骤中,s1中提取试剂为三氯甲烷,薄层鉴别测定步骤中,s1展开剂为按照体积比为9:1的沸程规格60℃~90℃石油醚和乙酸乙酯混合溶剂,s2显影试剂为10%硫酸乙醇溶液。
可选的,肉豆蔻薄层鉴别测定方法的对照组试剂制备步骤中,s1中肉豆蔻取0.5g,添加提取试剂为10ml,s2超声波处理20min,测定组试剂制备步骤中,s1中参倍固肠胶囊取5g,添加提取试剂为15ml,s2超声波处理20min,薄层鉴别测定步骤中,s1取对照组试剂10μl、测定组试剂10μl,s3加热温度为105℃。
进一步的,红参薄层鉴别测定方法包括对照组试剂制备、测定组试剂制备和薄层鉴别测定,对照组试剂制备包括以下步骤:
s1,取人参皂苷rb1、人参皂苷re、人参皂苷rg1,置索氏提取器中并添加提取试剂,加热进行提取,制得对照品提取液,取红参置索氏提取器中并添加提取试剂,加热进行提取,制得对照药材提取液;
s2,将s1中对照品提取液的溶液挥干,并添加回流试剂,加热回流后,过滤,滤液蒸干,制得对照品残渣;将s1中对照药材提取液的溶液挥干,并添加回流试剂,加热回流后,过滤,滤液蒸干,制得对照药材残渣;
s3,在对照品残渣中添加溶剂,待溶解后,进行提取,然后碱洗,碱洗后再提取,制得对照品试剂,在对照药材残渣中添加溶剂,待溶解后,进行提取,然后碱洗,碱洗后再提取,制得对照药材试剂;
测定组试剂制备包括以下步骤:
s1,取参倍固肠胶囊,置索氏提取器中并添加提取试剂,加热进行提取;
s2,将s1提取后溶液挥干,并添加回流试剂,加热回流后,过滤,滤液蒸干,制得残渣;
s3,在残渣中添加溶剂,待溶解后,进行提取,然后碱洗,碱洗后再提取,制得测定组试剂;
薄层鉴别测定包括以下步骤:
s1,取对照品试剂、对照药材试剂和测定组试剂,分别点于同一硅胶g薄层板上,并通过展开剂进行展开;
s2,将展开后的硅胶g薄层板取出,晾干,并喷以显影试剂,加热;
s3,加热至适应温度后,在对照品试剂色谱、对照药材试剂色谱和测定组试剂色谱相应的位置上,分别置于日光及紫外光灯下检视,得到显示相同的颜色的荧光斑点。
可选的,红参薄层鉴别测定方法的对照组试剂制备步骤中,s1中用于制备对照品提取液的提取试剂为甲醇,用于制备对照药材提取液的提取试剂为乙醚,s2中回流试剂为甲醇,s3中溶剂为正丁醇饱和的水,测定组试剂制备步骤中,s1中提取试剂均为乙醚,s2中回流试剂为甲醇,s3中溶剂为正丁醇饱和的水,薄层鉴别测定步骤中,s1中展开剂为在10℃的环境温度下按照体积比为65:35:10的三氯甲烷-甲醇-水的下层溶液,s2中显影试剂为10%硫酸乙醇溶液。
可选的,红参薄层鉴别测定方法的对照组试剂制备步骤中,s1中取人参皂苷rb1、人参皂苷re、人参皂苷rg1各1mg,添加提取试剂为1ml,加热3h,s2中回流试剂为150ml,加热回流时间为3h,s3中在对照品残渣中加正丁醇饱和的水30ml使溶解,转移至分液漏斗中,用水饱和的正丁醇提取3次,每次40ml,合并制得正丁醇提取液,用1%氢氧化钠溶液洗涤2次,其中第一次用50ml,第二次用30ml,碱液用水饱和的正丁醇50ml提取1次,弃去碱液,与上述正丁醇提取液合并,再用正丁醇饱和的水洗至中性,弃去水洗液,回收正丁醇至干,残渣加甲醇2ml使溶解,制得对照品试剂;
s1中取红参1g,添加提取试剂为80ml,加热3h,s2中回流试剂为150ml,加热回流时间为3h,s3中在对照药材残渣中加正丁醇饱和的水30ml使溶解,转移至分液漏斗中,用水饱和的正丁醇提取3次,每次40ml,合并制得正丁醇提取液,用1%氢氧化钠溶液洗涤2次,其中第一次用50ml,第二次用30ml,碱液用水饱和的正丁醇50ml提取1次,弃去碱液,与上述正丁醇提取液合并,再用正丁醇饱和的水洗至中性,弃去水洗液,回收正丁醇至干,残渣加甲醇2ml使溶解,制得对照药材试剂;
测定组试剂制备步骤中,s1中取参倍固肠胶囊12g,添加提取试剂为80ml,加热3h,s2中回流试剂为150ml,加热回流时间为3h,s3中在残渣中加正丁醇饱和的水30ml使溶解,转移至分液漏斗中,用水饱和的正丁醇提取3次,每次40ml,合并制得正丁醇提取液,用1%氢氧化钠溶液洗涤2次,其中第一次用50ml,第二次用30ml,碱液用水饱和的正丁醇50ml提取1次,弃去碱液,与上述正丁醇提取液合并,再用正丁醇饱和的水洗至中性,弃去水洗液,回收正丁醇至干,残渣加甲醇2ml使溶解,制得测定组试剂;
薄层鉴别测定步骤中,s1中取测定组试剂10μl,取对照品试剂和对照药材试剂各2μl,s3加热温度为105℃。
本发明的有益效果至少包括以下之一;
1、通过针对参倍固肠胶囊中各药物成分的特性,再基于苍术、肉豆蔻和红参的薄层鉴定特点,提供相适应的提取制备工艺和所需的制剂,从而能够从参倍固肠胶囊的诸多有效药物成分中分离提取待测定成分。
2、解决了现有的薄层鉴别测定法较难从参倍固肠胶囊中提取待测定目标药物,同时受目标药物易挥发的影响,最终显色较困难的问题。
附图说明
图1为苍术专属性展开测定图;
图2为苍术耐用性硅胶g自制板展开测定图;
图3为苍术耐用性硅胶g预制板展开测定图;
图4为肉豆蔻专属性展开测定图;
图5为肉豆蔻耐用性硅胶g自制板展开测定图;
图6为肉豆蔻耐用性硅胶g预制板展开测定图;
图7为红参专属性日光下检视展开测定图;
图8为红参专属性紫外光灯(365nm)下检视展开测定图;
图9为红参耐用性日光下硅胶g自制板展开测定图;
图10为红参耐用性紫外光灯(365nm)下硅胶g自制板展开测定图;
图11为红参耐用性日光下硅胶g预制板展开测定图;
图12为红参耐用性紫外光灯(365nm)下硅胶g预制板展开测定图;
具体实施方式
为了使本发明的目的、技术方案及优点能够更加清晰明白,以下结合实施例对本发明进行进一步详细说明。应当理解,此处所描述的具体实施例仅仅用以解释本发明,并不用于限定本发明保护内容。
实施例1
参倍固肠胶囊中苍术、肉豆蔻和红参的薄层鉴别测定法,包括苍术薄层鉴别测定方法、肉豆蔻薄层鉴别测定方法和红参薄层鉴别测定方法,其中苍术薄层鉴别测定方法包括对照组试剂制备、测定组试剂制备和薄层鉴别测定,对照组试剂制备包括以下步骤:
s1,取苍术,将其研细,置具塞锥形瓶中并添加提取试剂,进行提取;
s2,将s1提取后溶液进行超声波处理,并过滤,待滤液挥干,制得残渣;
s3,在残渣中添加提取试剂,使得残渣溶解,制得对照组试剂;
测定组试剂制备包括以下步骤:
s1,取参倍固肠胶囊,将其研细,置具塞锥形瓶中并添加提取试剂,进行提取;
s2,将s1提取后溶液进行超声波处理,并过滤,待滤液挥干,制得残渣;
s3,在残渣中添加提取试剂,使得残渣溶解,制得测定组试剂;
薄层鉴别测定包括以下步骤:
s1,取对照组试剂和测定组试剂,分别点于同一硅胶g薄层板上,并通过展开剂进行展开;
s2,将展开后的硅胶g薄层板取出,晾干,并喷以显影试剂,加热;
s3,加热至适应温度后,在对照组试剂色谱和测定组试剂色谱相应的位置上,得到显示相同的颜色的荧光斑点。
其中肉豆蔻薄层鉴别测定方法包括对照组试剂制备、测定组试剂制备和薄层鉴别测定,对照组试剂制备包括以下步骤:
s1,取肉豆蔻,将其研细,置具塞锥形瓶中并添加提取试剂,进行提取;
s2,将s1提取后溶液进行超声波处理,并过滤,收集滤液制得对照组试剂;
测定组试剂制备包括以下步骤:
s1,取参倍固肠胶囊,将其研细,置具塞锥形瓶中并添加提取试剂,进行提取;
s2,将s1提取后溶液进行超声波处理,并过滤,收集滤液制得测定组试剂;
薄层鉴别测定包括以下步骤:
s1,取对照组试剂和测定组试剂,分别点于同一硅胶g薄层板上,并通过展开剂进行展开;
s2,将展开后的硅胶g薄层板取出,晾干,并喷以显影试剂,加热;
s3,加热至适应温度后,在对照组试剂色谱和测定组试剂色谱相应的位置上,得到显示相同的颜色的荧光斑点。
其中红参薄层鉴别测定方法包括对照组试剂制备、测定组试剂制备和薄层鉴别测定,对照组试剂制备包括以下步骤:
s1,取人参皂苷rb1、人参皂苷re、人参皂苷rg1,置索氏提取器中并添加提取试剂,加热进行提取,制得对照品提取液,取红参置索氏提取器中并添加提取试剂,加热进行提取,制得对照药材提取液;
s2,将s1中对照品提取液的溶液挥干,并添加回流试剂,加热回流后,过滤,滤液蒸干,制得对照品残渣;将s1中对照药材提取液的溶液挥干,并添加回流试剂,加热回流后,过滤,滤液蒸干,制得对照药材残渣;
s3,在对照品残渣中添加溶剂,待溶解后,进行提取,然后碱洗,碱洗后再提取,制得对照品试剂,在对照药材残渣中添加溶剂,待溶解后,进行提取,然后碱洗,碱洗后再提取,制得对照药材试剂;
测定组试剂制备包括以下步骤:
s1,取参倍固肠胶囊,置索氏提取器中并添加提取试剂,加热进行提取;
s2,将s1提取后溶液挥干,并添加回流试剂,加热回流后,过滤,滤液蒸干,制得残渣;
s3,在残渣中添加溶剂,待溶解后,进行提取,然后碱洗,碱洗后再提取,制得测定组试剂;
薄层鉴别测定包括以下步骤:
s1,取对照品试剂、对照药材试剂和测定组试剂,分别点于同一硅胶g薄层板上,并通过展开剂进行展开;
s2,将展开后的硅胶g薄层板取出,晾干,并喷以显影试剂,加热;
s3,加热至适应温度后,在对照品试剂色谱、对照药材试剂色谱和测定组试剂色谱相应的位置上,分别置于日光及紫外光灯下检视,得到显示相同的颜色的荧光斑点。
通过针对参倍固肠胶囊中各药物成分的特性,再基于苍术、肉豆蔻和红参的薄层鉴定特定,提供相适应的提取制备工艺,从而能够从参倍固肠胶囊的诸多有效药物成分中分离提取待测定成分。解决了现有的薄层鉴别测定法较难从参倍固肠胶囊中提取待测定目标药物,同时受目标药物易挥发的影响,最终显色较困难的问题。
实施例2
参倍固肠胶囊中苍术、肉豆蔻和红参的薄层鉴别测定法,包括苍术薄层鉴别测定方法、肉豆蔻薄层鉴别测定方法和红参薄层鉴别测定方法,其中苍术薄层鉴别测定方法包括对照组试剂制备、测定组试剂制备和薄层鉴别测定,对照组试剂制备包括以下步骤:
s1,取苍术0.5g,将其研细,置具塞锥形瓶中并添加15ml沸程规格60℃~90℃的石油醚,进行提取;
s2,将s1提取后溶液进行超声波处理20min,并过滤,待滤液挥干,制得残渣;
s3,在残渣中添加1ml沸程规格60℃~90℃的石油醚,使得残渣溶解,制得对照组试剂;
测定组试剂制备包括以下步骤:
s1,取参倍固肠胶囊5g,将其研细,置具塞锥形瓶中并添加15ml沸程规格60℃~90℃的石油醚,进行提取;
s2,将s1提取后溶液进行超声波处理20min,并过滤,待滤液挥干,制得残渣;
s3,在残渣中添加1ml沸程规格60℃~90℃的石油醚,使得残渣溶解,制得测定组试剂;
薄层鉴别测定包括以下步骤:
s1,取对照组试剂2μl和测定组试剂10μl,分别点于同一硅胶g薄层板上,并通过沸程规格60℃~90℃的石油醚进行展开;
s2,将展开后的硅胶g薄层板取出,晾干,并喷以茴香醛,加热;
s3,加热至105℃后,在对照组试剂色谱和测定组试剂色谱相应的位置上,得到显示相同的颜色的荧光斑点。
其中肉豆蔻薄层鉴别测定方法包括对照组试剂制备、测定组试剂制备和薄层鉴别测定,对照组试剂制备包括以下步骤:
s1,取肉豆蔻0.5g,将其研细,置具塞锥形瓶中并添加10ml三氯甲烷,进行提取;
s2,将s1提取后溶液进行超声波处理20min,并过滤,收集滤液制得对照组试剂;
测定组试剂制备包括以下步骤:
s1,取参倍固肠胶囊5g,将其研细,置具塞锥形瓶中并添加10ml三氯甲烷,进行提取;
s2,将s1提取后溶液进行超声波处理20min,并过滤,收集滤液制得测定组试剂;
薄层鉴别测定包括以下步骤:
s1,取对照组试剂和测定组试剂各10μl,分别点于同一硅胶g薄层板上,并通过按照体积比为9:1的沸程规格60℃~90℃石油醚和乙酸乙酯混合溶剂进行展开;
s2,将展开后的硅胶g薄层板取出,晾干,并喷以10%硫酸乙醇溶液,加热;
s3,加热至105℃后,在对照组试剂色谱和测定组试剂色谱相应的位置上,得到显示相同的颜色的荧光斑点。
其中红参薄层鉴别测定方法包括对照组试剂制备、测定组试剂制备和薄层鉴别测定,对照组试剂制备包括以下步骤:
s1,取人参皂苷rb1、人参皂苷re、人参皂苷rg1各1mg,置索氏提取器中并添加1ml甲醇,加热3小时进行提取,制得对照品提取液,取红参1g置索氏提取器中并添加80ml乙醚,加热3小时进行提取,制得对照药材提取液;
s2,将s1中对照品提取液的溶液挥干,并添加150ml甲醇,加热回流3小时后,过滤,滤液蒸干,制得对照品残渣;将s1中对照药材提取液的溶液挥干,并添加150ml甲醇,加热回流3小时后,过滤,滤液蒸干,制得对照药材残渣;
s3,在对照品残渣中加正丁醇饱和的水30ml使溶解,转移至分液漏斗中,用水饱和的正丁醇提取3次,每次40ml,合并制得正丁醇提取液,用1%氢氧化钠溶液洗涤2次,其中第一次用50ml,第二次用30ml,碱液用水饱和的正丁醇50ml提取1次,弃去碱液,与上述正丁醇提取液合并,再用正丁醇饱和的水洗至中性,弃去水洗液,回收正丁醇至干,残渣加甲醇2ml使溶解,制得对照品试剂,在对照药材残渣中加正丁醇饱和的水30ml使溶解,转移至分液漏斗中,用水饱和的正丁醇提取3次,每次40ml,合并制得正丁醇提取液,用1%氢氧化钠溶液洗涤2次,其中第一次用50ml,第二次用30ml,碱液用水饱和的正丁醇50ml提取1次,弃去碱液,与上述正丁醇提取液合并,再用正丁醇饱和的水洗至中性,弃去水洗液,回收正丁醇至干,残渣加甲醇2ml使溶解,制得对照药材试剂;
测定组试剂制备包括以下步骤:
s1,取参倍固肠胶囊12g,置索氏提取器中并添加80ml乙醚,加热3小时进行提取;
s2,将s1提取后溶液挥干乙醚,并添加150ml甲醇,加热回流3小时后,过滤,滤液蒸干,制得残渣;
s3,在残渣中加正丁醇饱和的水30ml使溶解,转移至分液漏斗中,用水饱和的正丁醇提取3次,每次40ml,合并制得正丁醇提取液,用1%氢氧化钠溶液洗涤2次,其中第一次用50ml,第二次用30ml,碱液用水饱和的正丁醇50ml提取1次,弃去碱液,与上述正丁醇提取液合并,再用正丁醇饱和的水洗至中性,弃去水洗液,回收正丁醇至干,残渣加甲醇2ml使溶解,制得测定组试剂;
薄层鉴别测定包括以下步骤:
s1,取对照品试剂2μl、对照药材试剂2μl和测定组试剂10μl,分别点于同一硅胶g薄层板上,并通过10℃的环境温度下按照体积比为65:35:10的三氯甲烷-甲醇-水的下层溶液进行展开;
s2,将展开后的硅胶g薄层板取出,晾干,并喷以10%硫酸乙醇,加热;
s3,加热至105℃后,在对照品试剂色谱、对照药材试剂色谱和测定组试剂色谱相应的位置上,分别置于日光及紫外光灯(365nm)下检视,得到显示相同的颜色的荧光斑点。
实施例3
为了确保本发明的效果,申请人对制剂中苍术、肉豆蔻和红参的鉴别方法进行了相应的试验研究与论证,具体如下:
苍术薄层鉴别测定方法
(1)试剂与试药
参倍固肠胶囊由贵州联盛药业有限公司提供;苍术对照药材(120932-201006)由中国药品生物制品检定所提供;硅胶g薄层板:青岛海洋化工厂分厂生产的硅胶g薄层板及自制硅胶g薄层板;试剂:石油醚(60℃~90℃)为分析纯。
十批样品含量测定结果
(2)专属性
取参倍固肠胶囊、缺苍术阴性样品,同实施例2方法制得测定组试剂和对照组试剂,再通过现有技术制备阴性测定组试剂(不含待检测成分试剂),分别取测定组试剂、阴性测定组试剂、对照组试剂点样、展开、显色,日光下检视,在测定组试剂色谱中,与对照组试剂色谱相应的位置上显相同的主斑点,斑点分离较好,且阴性无干扰。
(3)耐用性
取通过上述10批样品制得测定组试剂、阴性测定组试剂和对照组试剂分别点于硅胶g预制板和硅胶g自制板,展开、显色后,结果斑点分离好,无干扰。
按照实施例2中提供的技术方案测定后得以下内容:
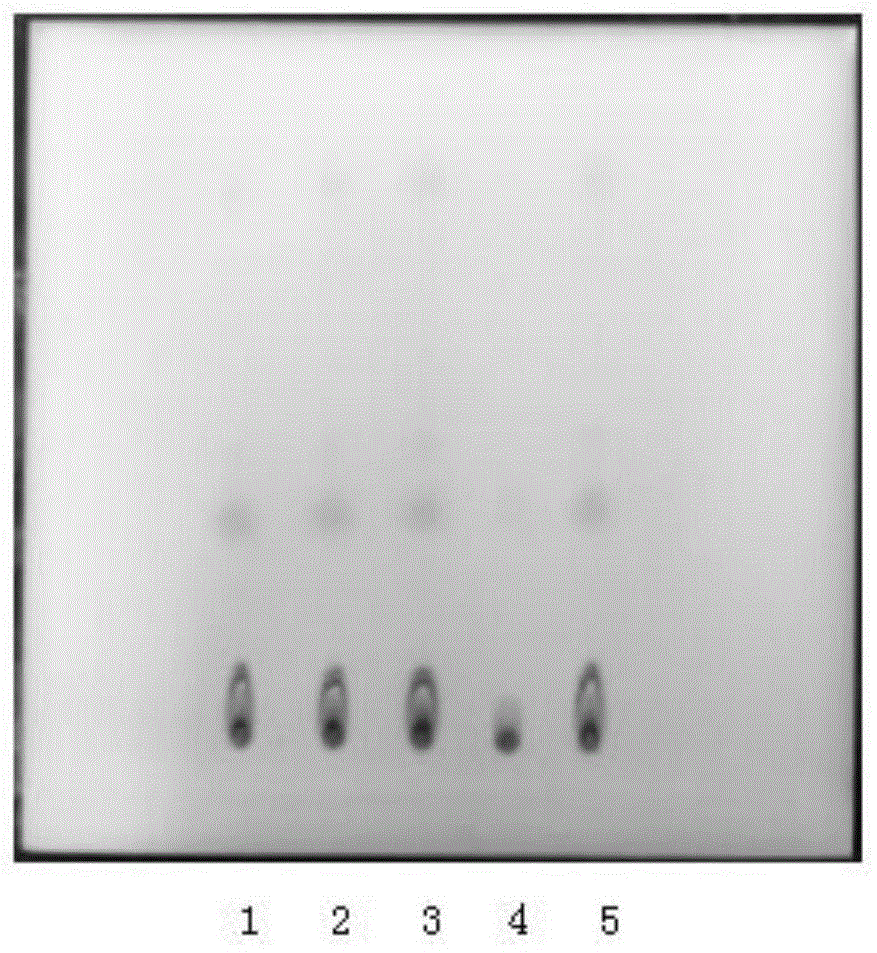
图1中载体为硅胶g板,展开剂为沸程规格60℃~90℃的石油醚,显色为喷以茴香醛试液,105℃加热至斑点显色清晰,日光下检视。
其中标号1对应1511010批号样品测定组试剂,2对应1512010批号样品测定组试剂,3对应1512020批号样品测定组试剂,4对应阴性样品,5对应苍术对照组试剂。
图2和图3中,仅载体存在差异,图2载体为硅胶g自制板,图3载体硅胶g预制板,展开剂均为沸程规格60℃~90℃的石油醚,显色为喷以茴香醛试液,105℃加热至斑点显色清晰,日光下检视。
其中标号1均对应1511010批号样品测定组试剂,2均对应1512010批号样品测定组试剂,3均对应1512020批号样品测定组试剂,4均对应阴性样品,5均对应苍术对照组试剂。
肉豆蔻薄层鉴别测定方法
(1)试剂与试药
参倍固肠胶囊由贵州联盛药业有限公司提供;肉豆蔻对照药材(120926-201307)由中国药品生物制品检定所提供;硅胶g薄层板:青岛海洋化工厂分厂生产的硅胶g薄层板及自制硅胶g薄层板;试剂:石油醚(60℃~90℃)、三氯甲烷和乙酸乙酯为分析纯。
十批样品含量测定结果
(2)专属性
取参倍固肠胶囊、缺肉豆蔻阴性样品,同实施例2方法制得测定组试剂和对照组试剂,再通过现有技术制备阴性测定组试剂(不含待检测成分试剂),分别取测定组试剂、阴性测定组试剂、对照组试剂点样、展开、显色,日光下检视,在测定组试剂色谱中,与对照组试剂色谱相应的位置上显相同的主斑点,斑点分离较好,且阴性无干扰。
(3)耐用性
取通过上述10批样品制得测定组试剂、阴性测定组试剂和对照组试剂分别点于硅胶g预制板和硅胶g自制板,展开、显色后,结果斑点分离好,无干扰。
按照实施例2中提供的技术方案测定后得以下内容:
图4中载体为硅胶g板,展开剂均为按照体积比为9:1的沸程规格60℃~90℃石油醚和乙酸乙酯混合溶剂,显色为喷以10%硫酸乙醇溶液,105℃加热至斑点显色清晰,日光下检视。
其中标号1对应1511010批号样品测定组试剂,2对应1512010批号样品测定组试剂,3对应1512020批号样品测定组试剂,4对应阴性样品,5对应肉豆蔻对照组试剂。
图5和图6中,仅载体存在差异,图5载体为硅胶g自制板,图6载体硅胶g预制板,展开剂均为按照体积比为9:1的沸程规格60℃~90℃石油醚和乙酸乙酯混合溶剂,显色为喷以10%硫酸乙醇溶液,105℃加热至斑点显色清晰,日光下检视。
其中标号1均对应1511010批号样品测定组试剂,2均对应1512010批号样品测定组试剂,3均对应1512020批号样品测定组试剂,4均对应阴性样品,5均对应肉豆蔻对照组试剂。
红参薄层鉴别测定方法
(1)试剂与试药
参倍固肠胶囊由贵州联盛药业有限公司提供;红参对照药材(121045-201105)、人参皂苷re(110754-201324)、人参皂苷rb1(110704-201223)由中国药品生物制品检定所提供;硅胶g薄层板:青岛海洋化工厂分厂生产的硅胶g薄层板及自制硅胶g薄层板;试剂:正丁醇、三氯甲烷、乙醚、甲醇均为分析纯。
十批样品含量测定结果
(2)专属性
取参倍固肠胶囊、缺红参阴性样品,同实施例2方法制得测定组试剂、对照药材试剂和对照品试剂,再通过现有技术制备阴性测定组试剂(不含待检测成分试剂),分别取测定组试剂、阴性测定组试剂、对照药材试剂和对照品试剂点样、展开、显色,日光下检视,在测定组试剂色谱中,与对照组试剂色谱相应的位置上显相同的主斑点,斑点分离较好,且阴性无干扰。
(3)耐用性
取通过上述10批样品制得测定组试剂、阴性测定组试剂、对照药材试剂和对照品试剂分别点于硅胶g预制板和硅胶g自制板,展开、显色后,结果斑点分离好,无干扰。
按照实施例2中提供的技术方案测定后得以下内容:
图7中载体为硅胶g板,展开剂均为在10℃的环境温度下按照体积比为65:35:10的三氯甲烷-甲醇-水的下层溶液,显色为喷以10%硫酸乙醇溶液,105℃加热至斑点显色清晰,日光下检视。
图8中载体为硅胶g板,展开剂均为在10℃的环境温度下按照体积比为65:35:10的三氯甲烷-甲醇-水的下层溶液,显色为喷以10%硫酸乙醇溶液,105℃加热至斑点显色清晰,紫外光灯(365nm)下检视。
其中标号1对应1511010批号样品测定组试剂,2对应1512010批号样品测定组试剂,3对应1512020批号样品测定组试剂,4对应阴性样品,5对应红参对照药材试剂、6对应红参对照品试剂(从上至下为人参皂苷rb1、人参皂苷re、人参皂苷rg1)。
图9和图11中,仅载体存在差异,图9载体为硅胶g自制板,图11载体硅胶g预制板,展开剂均为在10℃的环境温度下按照体积比为65:35:10的三氯甲烷-甲醇-水的下层溶液,显色为喷以10%硫酸乙醇溶液,105℃加热至斑点显色清晰,日光下检视。
图10和图11中,仅载体存在差异,图9载体为硅胶g自制板,图11载体硅胶g预制板,展开剂均为在10℃的环境温度下按照体积比为65:35:10的三氯甲烷-甲醇-水的下层溶液,显色为喷以10%硫酸乙醇溶液,105℃加热至斑点显色清晰,紫外光灯(365nm)下检视。
其中标号1对应1511010批号样品测定组试剂,2对应1512010批号样品测定组试剂,3对应1512020批号样品测定组试剂,4对应阴性样品,5对应红参对照药材试剂、6对应红参对照品试剂(从上至下为人参皂苷rb1、人参皂苷re、人参皂苷rg1)。
- 还没有人留言评论。精彩留言会获得点赞!