一种检测Hg2+的自增强电化学发光适配体传感器的制备方法与流程
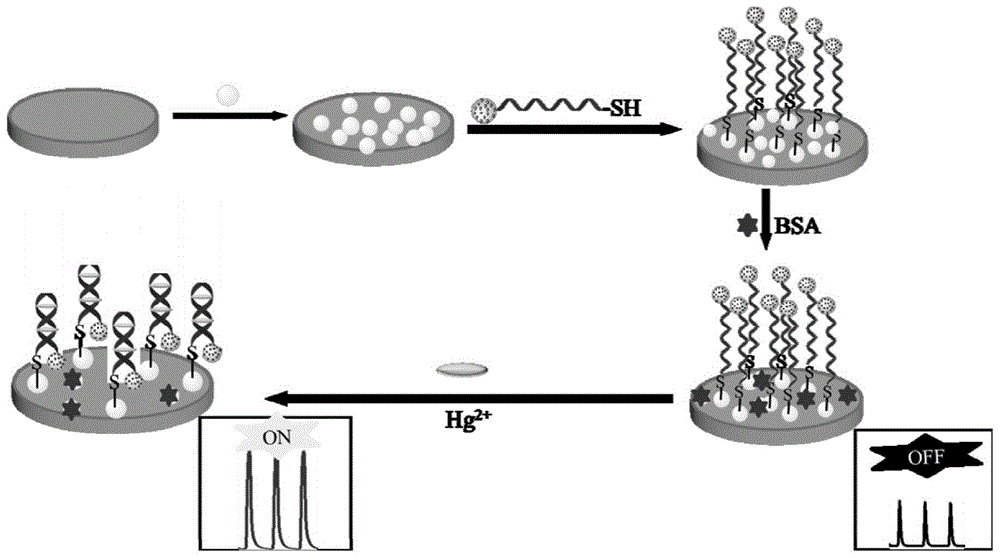
本发明属于生物传感检测技术领域,涉及一种检测hg2+的制备方法,具体涉及一种基于apt-ngqds-nh2-ru@sio2体系的自增强电化学发光适配体传感器的制备方法及应用。
背景技术:
汞离子(hg2+)是一种毒性大,易蓄积的重金属离子。hg2+广泛分布在土壤、农作物、水体、大气中,并且通过生物链进入人体中。当生态环境中hg2+含量过高,会导致土壤甲基化,植物中毒,水源受到污染,侵害鱼虾等水生物,进一步通过食物链进入人体后,会在体内富集,引起四肢变形,甚至是可怕的水俣病。因此对水中hg2+含量进行检测很有必要的,它可以为水质量评估和后续处理提供理论依据。
对于hg2+的检测一直是刻不容缓的事情,目前常用的hg2+分析测定方法有原子吸收光谱法(afs)、电感耦合等离子体质谱法(icp-ms)和原子荧光光谱法等。虽然这些方法准确高效,但是它们依赖于专业人员,仪器昂贵。电化学法、电化学发光法(ecl)、荧光法等,这些方法操作简单且成本低。其中ecl因其灵敏度高,重现性好,可控性强,仪器操作简单等特征引起科学家们广泛的关注。为了进一步缩小电子转移距离,降低能量损失,提高ecl发光效率,自增强ecl逐渐进入人们的视线,并在检测领域占有一席之地。
技术实现要素:
针对目前检测hg2+的方法存在的一些问题,本发明提供了一种成本低、灵敏度高、发光效率高的ecl生物传感器检测hg2+。
一种检测hg2+的自增强电化学发光适配体传感器的制备方法,包括以下步骤:
(1)ru@sio2材料的制备:
首先,将曲拉通、环己烷、1-己醇加入到二次水中,通过反向微乳法得到微乳液,反应结束后,加入三联吡啶钌、硅酸四乙酯、氨水继续进行搅拌反应,反应结束后,得到的产物依次溶于丙酮、乙醇、二次水,离心洗涤,得到下层沉淀,经真空干燥,得到的ru@sio2;溶解在超纯水中,得到ru@sio2分散液;
(2)nh2-ru@sio2复合材料的制备:
首先,将步骤(1)中制备的ru@sio2分散液与aptes混合,搅拌反应,结束后,得到的产物用乙醇溶解,离心,得到的下层沉淀,经真空干燥,得到的nh2-ru@sio2;溶解在乙醇中,得到nh2-ru@sio2分散液;
(3)ngqds-nh2-ru@sio2复合材料的制备:
首先,将步骤(2)中制备的nh2-ru@sio2分散液与ngqds混合,搅拌反应结束后,得到的产物用二次水溶解,离心取上层黄色澄清液,即ngqds-nh2-ru@sio2;
(4)apt-ngqds-nh2-ru@sio2复合材料的制备:
首先,在步骤(3)中制备的ngqds-nh2-ru@sio2中加入含有edc与nhs的pbs缓冲液,反应结束后,加入适配体apt,继续搅拌,得到黄色的apt-ngqds-nh2-ru@sio2,放置4℃备用;
(5)将玻碳电极依次用不同粒径的三氧化二铝粉末打磨,在乙醇和水中超声后于空气中干燥;
(6)将步骤(5)修饰好的电极浸泡在haucl4溶液中,从-0.25v到-0.1v电位下进行电镀,时间控制在15s到30s内,在电极表面修饰上一层au粒子aunps,用于连接步骤(4)所制备的材料;
(7)将步骤(4)制备的自增强发光体材料apt-ngqds-nh2-ru@sio2修饰到步骤(6)制备的玻碳电极表面,通过au-s共价键固定在电极表面,形成自组装电极;
(8)在一定温度下,将步骤(7)制备的自组装电极浸入牛血清白蛋白bsa溶液中孵育,以阻断剩余的非特异性结合位点,制得基于apt-ngqds-nh2-ru@sio2的电化学发光适配体传感器。
步骤(1)中,曲拉通、环己烷、1-己醇和二次水中的用量比例为1.77ml:7.5ml:1.8ml:340μl,反应时间为15min;三联吡啶钌、硅酸四乙酯、氨水的用量比例为80μl:100μl:60μl;搅拌反应时间为24h,离心转速为10000rpm,每次5min,所得ru@sio2分散液的浓度为2mg·ml-1。
步骤(2)中,ru@sio2分散液与aptes的用量比例为1ml:400μl,两者搅拌反应的时间为4h,乙醇离心三次,离心转速为10000rpm,每次5min,所得nh2-ru@sio2分散液的浓度为1mg·ml-1。
步骤(3)中,nh2-ru@sio2分散液与ngqds的用量比例为1ml:5ml,ngqds的浓度为5mg·ml-1,两者搅拌反应的时间为12h。
步骤(4)中,ngqds-nh2-ru@sio2,pbs缓冲液,apt的用量比例为800μl:400μl:800μl,pbs的浓度为0.01m,其中nhs的浓度为0.005m,edc的浓度为0.01m,apt的浓度为2.5μm。
步骤(4)中,适配体apt的序列为:5'-nh2-ttgtttgtcccctctttctta-(ch2)3-sh-3'。
反应时间为15min;加入适配体后继续搅拌的时间为2h。
步骤(5)中,玻碳电极的直径d=3mm;所用的三氧化二铝粉末的粒径依次为0.3μm和0.05μm。
步骤(6)中,haucl4溶液的质量百分浓度为1%。
步骤(7)中,apt-ngqds-nh2-ru@sio2用量为6μl;反应温度为4℃,反应时间为8-12h。
步骤(8)中,牛血清白蛋白bsa溶液的质量百分浓度为1%;孵育的温度为37℃,孵育的时间为10-60min。
在本发明所制得的生物传感器依次浸泡到不同浓度的hg2+溶液中,避光室温下绑定时间为1-2h,hg2+浓度范围为1×10-12~5×10-6mol/l,之后用pbs(ph=7.0)溶液对电极进行清洗。制得的传感器作为工作电极,饱和ag/agcl电极为参比电极,铂电极为对电极,在0.1mpbs(ph=7.4)缓冲溶液中进行测试,得到hg2+浓度与ecl信号强度之间的线性关系。
在本发明所制得的生物传感器浸泡到未知hg2+浓度的待测溶液中,避光室温下绑定时间为1-2h,hg2+浓度未知,之后用pbs(ph=7.0)溶液对电极进行清洗。制得的传感器作为工作电极,饱和ag/agcl电极为参比电极,铂电极为对电极,在0.1mpbs(ph=7.4)缓冲溶液中进行测试,将得到的ecl信号带入上述得到的线性关系中,即可得到待测溶液中hg2+的浓度。
本发明中ecl生物传感器的工作原理:
复合发光材料apt-ngqds-nh2-ru@sio2将发光体nh2-ru@sio2和共反应物ngqds复合成一个发光基团(ngqds-nh2-ru@sio2),可以增强ecl信号强度。当目标物hg2+出现后,与apt形成t-hg2+-t的特异性结构,使得apt弯曲,发光基团ngqds-nh2-ru@sio2靠近电极,电子转移距离缩短,ecl信号强度进一步增强,根据ecl信号强度的变化,达到对hg2+的检测。
本发明的有益效果:
(1)本发明所涉及的自增强ecl生物传感器制备方法简单,简化了实验操作的复杂程度,实现了目标物简单、快速、灵敏的分析检测。用碳点代替有毒易挥发的胺类物质作为发光体ru(bpy)32+的共反应物不仅可以避免有害共反应物的使用,还可以提高体系的稳定性,解决稳定性差的问题。
(2)用新型自增强ecl代替传统的ecl,并且首次应用于hg2+的检测,在实际样品的检测中得到较高的回收率。
(3)本发明构建的自增强ecl适配体传感器用于水体中hg2+的特异性检测,灵敏度高、选择性好、稳定性好,线性范围宽,为5×10-11-1×10-6moll-1;检测限低至1.0×10-12m。
附图说明
图1为自增强ecl适配体传感器构建过程图。
图2(a)为apt-ngqds-nh2-ru@sio2孵育时间与ecl关系图;(b)为目标物孵育时间与ecl关系图。
图3(a)为ru@sio2的tem图;(b)复合材料nh2-ru@sio2的tem图;(c)ngqds的tem图;(d)复合材料apt-ngqds-nh2-ru@sio2的tem图。
图4(a)不同浓度hg2+所对应的ecl信号变化:浓度依次为5×10-11、2×10-10、1×10-9、1×10-8、1×10-7、1×10-6mol/l;(b)不同浓度hg2+对数与电化学发光信号之间构建的线性关系。
图5(a)不同电极之间的自增强ecl适配体传感器的重现性,(b)适配体传感器连续放置7天的稳定性能。
图6自增强ecl适配体传感器的选择性。干扰物分别为mg2+、fe2+、fe3+、na+、ca2+、cd2+、mn2+、pb2+、zn2+、cu2+。
具体实施方式
下面结合具体实施例和说明书附图,进一步阐明本发明。
实施例1
按照图1所述的制备工艺:
(1)apt-ngqds-nh2-ru@sio2复合材料的制备:
首先,将1.77ml曲拉通、7.5ml环己烷、1.8ml1-己醇和340μl二次水混合在一起搅拌15min后,加入80μl三联吡啶钌、100μl硅酸四乙酯、60μl氨水,继续搅拌时间为24h,搅拌结束后,丙酮、乙醇离心,水洗各三次,离心转速为10000rpm,每次5min,最终得到沉淀溶解在超纯水中,备用。
将上述得到的ru@sio2(2mg/ml)4ml与1600μlaptes混合搅拌4h,反应结束后,得到的产物用乙醇溶解,离心三次,离心转速为10000rpm,每次5min,取下层沉淀,经真空干燥,得到nh2-ru@sio2。
将nh2-ru@sio2(1mg/ml)1ml与ngqds(5mg/ml)5ml混合搅拌12h,得到黄色溶液ngqds-nh2-ru@sio2。
在ngqds-nh2-ru@sio2中加入含有0.01medc与0.005mnhs的0.01m缓冲液(pbs,ph=7.4)搅拌15min,使得发生酰胺反应,反应结束后,加入2.5μm适配体apt,继续搅拌,得到apt-ngqds-nh2-ru@sio2,反应结束后,得到的产物离心5min,离心转速为10000rpm,放置4℃备用。
(2)将玻碳电极(d=3mmgce)依次用0.3μm和0.05μm的三氧化二铝粉末打磨,在乙醇和水中超声后在空气中干燥。
(3)将步骤(2)修饰好的电极浸泡在1%haucl4中,从-0.25v到-0.1v电位下进行电镀,时间控制在15s到30s内,在电极表面修饰上一层au纳米粒子aunps,此时传感器表示为aunps/gce;
(4)将自增强发光体材料apt-ngqds-nh2-ru@sio2修饰到步骤(3)制备的玻碳电极表面,apt-ngqds-nh2-ru@sio2用量为6μl,通过au-s共价键固定在电极表面,形成自组装电极,放入4℃,孵育8-12h,此时传感器表示为apt-ngqds-nh2-ru@sio2/aunps/gce;
(5)常温下,将步骤(4)制备的自组装电极用二次水冲洗,并且在37℃浸入1%牛血清白蛋白bsa溶液中孵育10-60min,以阻断剩余的非特异性结合位点,制得基于apt-ngqds-nh2-ru@sio2的电化学发光适配体传感器,此时传感器表示为bsa/apt-ngqds-nh2-ru@sio2/aunps/gce。
将上述制得的传感器浸入到200μl1×10-6mol·l-1hg2+溶液中,室温下绑定时间为60-120min,之后用pbs(ph=7.0)对电极进行清洗。制得的传感器作为工作电极,饱和ag/agcl电极为参比电极,铂丝电极为对电极,采用mpi-eii电化学发光分析仪记录ecl信号。在0.1mpbs(ph=6.0-8.5)缓冲溶液中进行测试。扫描电压范围0.2-1.25v,扫描速度0.1vs,实验中光电倍增管的高压为650v。
图3(a)为ru@sio2的tem图,结果表明ru@sio2呈圆形且大小均匀;(b)复合材料nh2-ru@sio2的代表性tem图,可观察到当ru@sio2氨基化后,粒径变大;(c)ngqds的tem图,结果表明ngqds呈球形分布均匀;(d)复合材料ngqds-nh2-ru@sio2的tem图,可观察到ngqds成功附着在nh2-ru@sio2的表面,证明了ngqds-nh2-ru@sio2自增强材料的成功合成。
实施例2
制备的自增强电化学发光适配体传感器检测hg2+优化实验条件:
将实施例1制备的生物传感器在4℃条件下放置6、8、10、12、14h,检测ecl信号。
图2(a)为apt-ngqds-nh2-ru@sio2孵育时间与ecl关系图;孵育时间从4h增加到8h,ecl信号强度逐渐增加,在8h达到平稳。因此,选择10h为适配体的最佳孵育时间。
实施例3
制备的自增强电化学发光适配体传感器检测hg2+优化实验条件:
在实施例2获得的条件最佳的自增强电化学发光适配体传感器的基础上,于传感器表面修饰目标物hg2+,如图2(b)为目标物孵育时间与ecl关系图,孵育时间从40min增加到70min,ecl信号强度逐渐增加,在80min达到平稳,目标物hg2+在电极表面孵育时间为90min。
实施例4
自增强电化学发光适配体传感器检测hg2+:
分别用5×10-11、2×10-10、1×10-9、1×10-8、1×10-7、1×10-6mol/l的hg2+修饰实施例2所获得的最佳自增强电化学发光适配体传感器,根据实施例3得到的最佳实验条件,用mpi-eii电化学发光分析仪记录ecl信号。随着hg2+浓度的增加,ecl信号增大并且在一定范围内eclintensity与hg2+浓度的对数呈线性关系。
实施例5
自增强电化学发光适配体传感器选择性分析:
根据实施例3探究的最佳自增强电化学发光适配体传感器的实验条件,干扰物mg2+(5×10-7m)、fe2+(5×10-7m)、fe3+(5×10-7m)、na+(5×10-7m)、ca2+(5×10-7m)、cd2+(5×10-7m)、mn2+(5×10-7m)、pb2+(5×10-7m)、zn2+(5×10-7m)、cu2+(5×10-7m)分别与传感器进行孵育,所得ecl响应结果与空白试验结果基本一样,但是,10-8mhg2+与传感器孵育后,ecl信号响应结果明显高于空白。当生物传感器与10-8mhg2+和10种干扰物(5×10-7m)的混合物共同孵育时,其响应与单纯hg2+响应相比,基本保持不变。结果表明,电化学生物传感器具有良好的特异性,可用于hg2+的检测。
从图4(a)可以看出,随着hg2+浓度的增加(浓度依次为5×10-11、2×10-10、1×10-9、1×10-8、1×10-7、1×10-6mol/l),ecl信号逐渐增大,这应归因于hg2+与apt形成t-hg2+-t的特异性结构,使得apt弯曲,从而ngqds-nh2-ru@sio2靠近电极表面。
从图4(b)可以看出,ecl信号与hg2+浓度的对数值(logchg2+)绘制的标准曲线为iecl=559lgchg2++6323(r2=0.9959),线性范围为5.0×10-11-1.0×10-6m,检测限为1.0×10-12m。
从图5(a)中可以看出自增强电化学发光适配体传感器具有良好的重现性。
从图5(b)中可以看出自增强电化学发光适配体传感器具有良好的稳定性。
从图6中可以看出其他重金属离子干扰物以及十种重金属离子的混合所引起的ecl信号的变化可忽略不计,从而证明该自增强电化学发光适配体传感器具有良好的选择性。
- 还没有人留言评论。精彩留言会获得点赞!