一种注射用替加环素中9-硝基米诺环素的检测方法与流程
本发明涉及替加环素质量控制技术领域,具体而言,涉及一种注射用替加环素中9-硝基米诺环素的检测方法。
背景技术:
替加环素(tigecycline),由美国惠氏药物公司开发,是一种新型广谱活性的静脉注射用抗生素,对有抗药性的耐甲氧西林金黄色葡萄球菌也有活性,是甘氨酰四环素类中的首个药品,其化学结构如下:
根据替加环素的合成工艺,替加环素中可能存在的已知杂质包括表米诺环素、米诺环素、9-氨基米诺环素、9-硝基米诺环素、n-叔丁基甘氨酸、差向异构体、氧化物、醌类似物、三环物等,其中9-硝基米诺环素是生产替加环素的关键中间体,而且是一种基因毒杂质。但是,现有技术中通常是对含量较高的杂质进行定量分析,而不是对痕量的9-硝基米诺环素的定量分析,进而导致不能对9-硝基米诺环素的量有效质量控制。
技术实现要素:
本发明的主要目的在于提供一种注射用替加环素中9-硝基米诺环素的检测方法,以解决现有技术中的注射用替加环素中痕量9-硝基米诺环素不能有效定量的问题。
为了实现上述目的,根据本发明的一个方面,提供了一种注射用替加环素中9-硝基米诺环素的检测方法,包括:步骤s1,获取9-硝基米诺环素的高效液相色谱串联质谱的标准曲线,标准曲线的纵坐标为9-硝基米诺环素的特征离子峰面积、横坐标为9-硝基米诺环素的质量含量;步骤s2,将注射用替加环素溶解形成替加环素溶液,并将替加环素溶液进行高效液相色谱串联质谱检测,得到质量色谱图;步骤s3,根据质量色谱图的分析结果确定质量色谱图中9-硝基米诺环素的特征离子峰,并将特征离子峰的峰面积以标准曲线为依据计算得出9-硝基米诺环素的质量含量。
进一步地,上述步骤s1采用不同浓度的9-硝基米诺环素的溶液作为标准溶液获取标准曲线,优选配制标准溶液的溶剂为甲醇。
进一步地,上述标准溶液中9-硝基米诺环素的质量含量为0.0~0.25μg/ml。
进一步地,上述步骤s2中采用稀释剂稀释注射用替加环素形成替加环素溶液,优选稀释剂为甲醇和水的混合物,优选甲醇和水的体积比为40:60~60:40。
进一步地,上述高效液相色谱检测的条件设定包括:色谱柱为c18色谱柱,柱温为30~40℃,流速为0.3~0.8ml/min,流动相a为体积含量为0.05~0.2%的甲酸、流动相b为乙腈,梯度洗脱过程为:0~2min采用70~80%的流动相a和20~30%的流动相b洗脱,2~8min采用1~3%的流动相a和97~99%的流动相b洗脱,8~15min采用70~80%的流动相a和20~30%的流动相b洗脱。
进一步地,上述高效液相色谱检测的条件设定包括:色谱柱为welchxb-c18色谱柱,且色谱柱尺寸为4.6×50mm、5μm,柱温为35℃,流速为0.5ml/min,流动相a为体积含量为0.1%的甲酸、流动相b为乙腈,梯度洗脱过程为:0~2min采用75%的流动相a和25%的流动相b洗脱,2~8min采用2%的流动相a和98%的流动相b洗脱,8~13min采用75%的流动相a和25%的流动相b洗脱。
进一步地,上述质谱检测的条件设定包括:离子源为ajsesi,干燥气温度为280~310℃,干燥气流速为7~9l/min,雾化气压力为30~40psi,鞘流气温度为330~360℃,鞘流气流速为10~12l/min,毛细管端电压为3000~4000v,喷嘴正电压为450~550v,喷嘴负电压为800~1100v。
进一步地,上述质谱检测的条件设定包括:离子源为ajsesi,干燥气温度为300℃,干燥气流速为8l/min,雾化气压力为35psi,鞘流气温度为350℃,鞘流气流速为11l/min,毛细管端电压为3500v,喷嘴正电压为500v,喷嘴负电压为1000v。
进一步地,上述步骤s1和步骤s2中高效液相色谱串联质谱的测试条件相同。
应用本发明的技术方案,本申请通过高效液相色谱和质谱进行串联对注射用替加环素进行测试时,高效液相色谱对注射用替加环素中的各物质进行分离,然后质谱对对应各特征峰的分离物进行进一步的检测得到相应质量色谱图,利用质量色谱图可以确定9-硝基米诺环素以及对应的色谱图中9-硝基米诺环素的特征离子峰,依据该特征离子峰面积和步骤s1建立的标准曲线即可得到9-硝基米诺环素的质量含量。由此可见,本申请在实现了利用高效液相色谱对痕量9-硝基米诺环素充分分离的基础上,利用质谱数据精确对应质量色谱图中9-硝基米诺环素的特征离子峰,从而得到9-硝基米诺环素的精确质量含量,为对9-硝基米诺环素的有效质量控制提供可靠数据基础。
附图说明
构成本申请的一部分的说明书附图用来提供对本发明的进一步理解,本发明的示意性实施例及其说明用于解释本发明,并不构成对本发明的不当限定。在附图中:
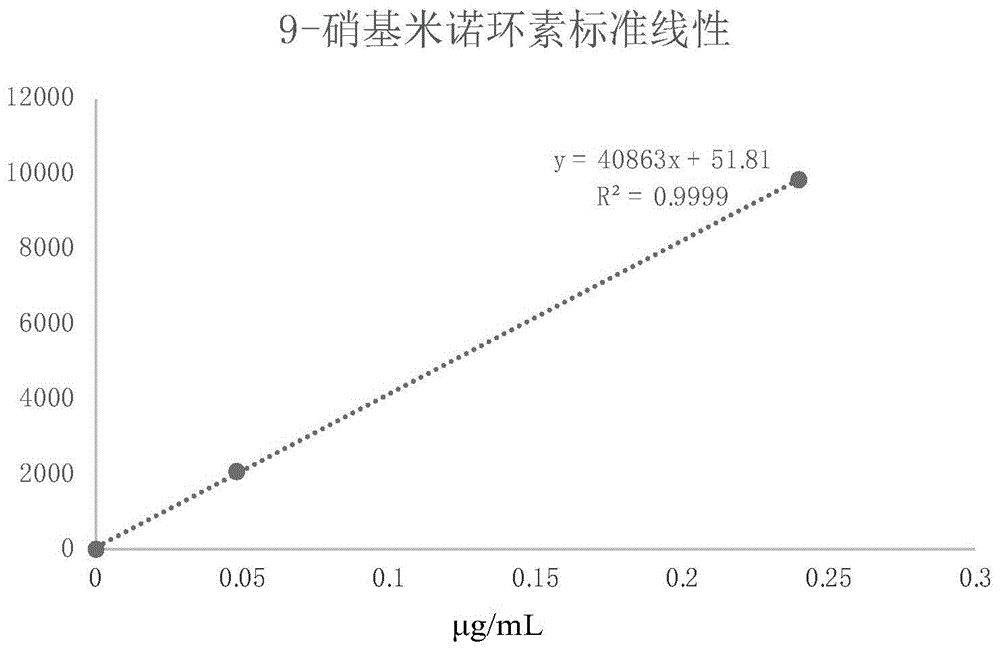
图1示出了根据本发明的实施例1的标准曲线图;
图2示出了根据本发明的实施例1的系统适用性溶液的质量色谱图;
图3示出了根据本发明的实施例1的样品溶液的质量色谱图。
具体实施方式
需要说明的是,在不冲突的情况下,本申请中的实施例及实施例中的特征可以相互组合。下面将参考附图并结合实施例来详细说明本发明。
如本申请背景技术所分析的,现有技术通常是对替加环素中所有杂质进行定量分析,而不是对9-硝基米诺环素的定量分析,进而导致不能对9-硝基米诺环素的有效质量控制,为了解决该问题,本申请提供了一种注射用替加环素中9-硝基米诺环素的检测方法,该检测方法包括:步骤s1,获取9-硝基米诺环素的高效液相色谱串联质谱的标准曲线,标准曲线的纵坐标为9-硝基米诺环素的特征离子峰面积、横坐标为9-硝基米诺环素的质量含量;步骤s2,将注射用替加环素溶解形成替加环素溶液,并将替加环素溶液进行高效液相色谱串联质谱检测,得到质量色谱图;步骤s3,根据质量色谱图的分析结果确定质量色谱图中9-硝基米诺环素的特征离子峰,并将特征离子峰的峰面积以标准曲线为依据计算得出9-硝基米诺环素的质量含量。
本申请通过高效液相色谱和质谱进行串联对注射用替加环素进行测试时,高效液相色谱对注射用替加环素中的各物质进行分离,然后质谱对对应各特征峰的分离物进行进一步的检测得到相应质量色谱图,利用质量色谱图可以确定9-硝基米诺环素以及对应的色谱图中9-硝基米诺环素的特征离子峰,依据该特征离子峰面积和步骤s1建立的标准曲线即可得到9-硝基米诺环素的质量含量。由此可见,本申请在实现了利用高效液相色谱对痕量9-硝基米诺环素充分分离的基础上,利用质谱数据精确对应质量色谱图中9-硝基米诺环素的特征离子峰,从而得到9-硝基米诺环素的精确质量含量,为对9-硝基米诺环素的有效质量控制提供可靠数据基础。
本申请中标准曲线的建立可以参考现有技术中液相色谱测试常用的标准曲线建立的流程,在一种实施例中,上述步骤s1采用不同浓度的9-硝基米诺环素的溶液作为标准溶液获取标准曲线,优选配制标准溶液的溶剂为甲醇。
由于9-硝基米诺环素作为杂质存在于注射用替加环素中,其含量较微,为了更进一步地保证测试结果的准确性,优选上述标准溶液中9-硝基米诺环素的质量含量为0.05~0.25μg/ml。采用上述浓度的标准溶液为测试基础绘制得到的标准曲线的可靠性更好。
为了使注射用替加环素中的9-硝基米诺环素尽可能在短时间内完全溶出,优选上述步骤s2中采用稀释剂稀释注射用替加环素形成替加环素溶液,优选稀释剂为甲醇和水的混合物,优选甲醇和水的体积比为40:60~60:40。
在对注射用替加环素进行高效液相色谱检测时,本申请对检测条件进行了深入研究,尤其是在使用不同色谱柱的前提下,对流动相的组成和梯度洗脱程序的配合进行了试验研究,最终确定高效液相色谱检测的条件设定包括:色谱柱为c18色谱柱,柱温为30~40℃,流速为0.3~0.8ml/min,流动相a为体积含量为0.05~0.2%的甲酸、流动相b为乙腈,梯度洗脱过程为:0~2min采用70~80%的流动相a和20~30%的流动相b洗脱,2~8min采用1~3%的流动相a和97~99%的流动相b洗脱,8~15min采用70~80%的流动相a和20~30%的流动相b洗脱。在上述条件下,尤其是采用c18色谱柱与上述流动相a和流动相b的组合,实现了对9-硝基米诺环素与其它杂质的有效分离,进而实现了对9-硝基米诺环素的质量测定。同时,上述流动相a和流动相b的性质稳定,不会导致替加环素和9-硝基米诺环素的异构化,进一步使得检测结果更加可靠。
进一步地,优选上述高效液相色谱检测的条件设定包括:色谱柱为welchxb-c18色谱柱,且色谱柱尺寸为4.6×50mm、5μm,柱温为35℃,流速为0.5ml/min,流动相a为体积含量为0.1%的甲酸、流动相b为乙腈,梯度洗脱过程为:0~2min采用75%的流动相a和25%的流动相b洗脱,2~8min采用2%的流动相a和98%的流动相b洗脱,8~13min采用75%的流动相a和25%的流动相b洗脱。
为了提高质谱检测结果的准确性,优选上述质谱检测的条件设定包括:离子源为ajsesi,干燥气温度为280~310℃,干燥气流速为7~9l/min,雾化气压力为30~40psi,鞘流气温度为330~360℃,鞘流气流速为10~12l/min,毛细管端电压为3000~4000v,喷嘴正电压为450~550v,喷嘴负电压为800~1100v。
在一种优选的实施例中,上述质谱检测的条件设定包括:离子源为ajsesi,干燥气温度为300℃,干燥气流速为8l/min,雾化气压力为35psi,鞘流气温度为350℃,鞘流气流速为11l/min,毛细管端电压为3500v,喷嘴正电压为500v,喷嘴负电压为1000v。
由于标准曲线建立过程中标准溶液的组成相对简单,因此其高效液相色谱串联质谱测试的条件相对宽泛,为了使标准曲线能够为步骤s2的测试提供更可靠的计算基础,优选上述步骤s1和步骤s2中高效液相色谱串联质谱的测试条件相同。
以下将结合实施例和对比例,进一步说明本申请的有益效果。
以下各实施例和对比例所采用的仪器和试剂如下。
仪器
agilenthplc1260-msqqq6460
试剂
甲醇,色谱级;
甲酸,质谱级;
乙腈,色谱级;
纯化水。
实施例1
标准曲线的建立过程
标准溶液配制过程如下:
标准溶液即系统适应性溶液:采用甲醇将9-硝基米诺环素标准样品14.1mg(相当于含9-硝基米诺环素12mg)逐级稀释,分别配置成浓度为0.05μg/ml,0.25μg/ml的单一标准溶液对标准溶液进行高效液相色谱串联质谱的检测过程如下:
高效液相色谱检测的条件设定如下:色谱柱为welchxb-c18色谱柱,且色谱柱尺寸为4.6×50mm、5μm,柱温为35℃,流速为0.5ml/min,流动相a为体积含量为0.1%的甲酸、流动相b为乙腈,梯度洗脱过程为:0~2min采用75%的流动相a和25%的流动相b洗脱,2~8min采用2%的流动相a和98%的流动相b洗脱,8~13min采用75%的流动相a和25%的流动相b洗脱。
质谱检测的条件设定如下:离子源为ajsesi,干燥气温度为300℃,干燥气流速为8l/min,雾化气压力为35psi,鞘流气温度为350℃,鞘流气流速为11l/min,毛细管端电压为3500v,喷嘴正电压为500v,喷嘴负电压为1000v。
所建立的标准曲线见图1。
检测条件同标准曲线时的检测条件。
回收率与精密度验证采用添加法进行检测。
准确度储备液:称取9-硝基米诺环素对照品14.1mg(相当于含9-硝基米诺环素12mg)置于一个50ml容量瓶中,加甲醇超声5分钟溶解并利用甲醇稀释至刻度,混匀得储备液a;精密移取1ml储备液a于100ml容量瓶中,加甲醇稀释至刻度,混匀得准确度储备液。
100%准确度样品溶液:移取准确度储备液2ml,加稀释剂2至20ml,混匀得准确度储备液1。取注射用替加环素1瓶,用上述20ml准确度储备液1,溶解,混匀,即得100%准确度样品溶液。平行配制三份。
20%准确度样品溶液:移取准确度储备液0.4ml,加稀释剂2至20ml,混匀得准确度储备液2。取注射用替加环素1瓶,用上述20ml准确度储备液2,溶解,混匀,即得20%准确度样品溶液。平行配制三份。
认可标准:每个浓度三份样品的平均回收率在70%~130%。(参考中国药典分析方法验证规程)
结果见下表1。
表1
检出限和定量限验证
(loq)定量限溶液:称取9-硝基米诺环素对照品14.1mg(相当于含9-硝基米诺环素12mg)置于一个50ml容量瓶中,加甲醇超声5分钟溶解并用甲醇稀释至刻度,混匀得储备液a;精密移取1ml储备液a于100ml容量瓶中,加甲醇稀释至刻度,混匀得储备液b;精密移取1ml储备液b,加稀释剂1稀释至10ml,混匀得系统适应性溶液。精密移取系统适应性溶液2ml用稀释剂1稀释至10ml,混匀得定量限溶液。稀释剂1为体积比为1:1的0.1%体积含量的氨水和乙腈的混合液。
(lod)检测限溶液:精密移取定量限溶液5ml,用稀释剂1稀释至10ml,混匀得检测限溶液。
认可标准:
6针loq溶液中9-硝基米诺环素的信噪比均≥10。(参考中国药典分析方法验证规程)6针loq溶液中9-硝基米诺环素峰面积的rsd均≤15%。(根据经验值设定)
3针lod溶液中9-硝基米诺环素的信噪比均≥3。(参考中国药典分析方法验证规程)
结果见表2。
表2
注射用替加环素中9-硝基米诺环素测定过程:
样品溶液:取注射用替加环素(规格50mg)1瓶,用稀释剂2溶解并稀释至20ml,混匀。稀释剂2为体积比为1:1的甲醇和水的混合液。
色谱分析程序:待系统平衡后,连续进6针系统适应性溶液,计算9-硝基米诺环素峰面积的rsd应≤10%;取20%限度溶液进样1针,查看9-硝基米诺环素的信噪比信噪比应≥10。每份样品溶液进1针。每进样不多于12针和序列结束时,分别进一针系统适应性溶液,与连续进样的前6针系统适应性溶液相比,9-硝基米诺环素峰面积的rsd应≤10%,得到系统适应性溶液而后样品溶液的质量色谱图,分别见图2和图3。
将质量色谱图中替加环素的特征离子峰的峰面积以标准曲线为依据计算得出9-硝基米诺环素的质量含量为4.36ppm。
实施例2
与实施例1的检测条件不同,具体如下。
高效液相色谱检测的条件设定如下:色谱柱为welchxb-c18色谱柱,且色谱柱尺寸为4.6×50mm、5μm,柱温为30℃,流速为0.3ml/min,流动相a为体积含量为0.2%的甲酸、流动相b为乙腈,梯度洗脱过程为:0~2min采用70%的流动相a和30%的流动相b洗脱,2~8min采用1%的流动相a和99%的流动相b洗脱,8~13min采用70%的流动相a和30%的流动相b洗脱。
质谱检测的条件设定如下:离子源为ajsesi,干燥气温度为310℃,干燥气流速为9l/min,雾化气压力为30psi,鞘流气温度为330℃,鞘流气流速为10l/min,毛细管端电压为3000v,喷嘴正电压为450v,喷嘴负电压为1100v。
所建立的标准曲线对应的线性回归方程为:y=40879x+50.64,线性相关系数为0.9996。
实施例3
与实施例1的检测条件不同,具体如下。
高效液相色谱检测的条件设定如下:色谱柱为welchxb-c18色谱柱,且色谱柱尺寸为4.6×50mm、5μm,柱温为40℃,流速为0.8ml/min,流动相a为体积含量为0.05%的甲酸、流动相b为乙腈,梯度洗脱过程为:0~2min采用80%的流动相a和20%的流动相b洗脱,2~8min采用3%的流动相a和97%的流动相b洗脱,8~13min采用80%的流动相a和20%的流动相b洗脱。
质谱检测的条件设定如下:离子源为ajsesi,干燥气温度为280℃,干燥气流速为7l/min,雾化气压力为40psi,鞘流气温度为360℃,鞘流气流速为12l/min,毛细管端电压为4000v,喷嘴正电压为550v,喷嘴负电压为800v。
所建立的标准曲线对应的线性回归方程为:y=40857x+51.93,线性相关系数为0.9995。
实施例4
与实施例1所用的稀释剂2的组成不同,具体为甲醇和水的体积比为40:60,最终计算得到的9-硝基米诺环素的质量含量为4.34ppm。
实施例5
与实施例1所用的稀释剂2的组成不同,具体为甲醇和水的体积比为60:40,最终计算得到的9-硝基米诺环素的质量含量为4.36ppm。
从以上的描述中,可以看出,本发明上述的实施例实现了如下技术效果:
本申请通过高效液相色谱和质谱进行串联对注射用替加环素进行测试时,高效液相色谱对注射用替加环素中的各物质进行分离,然后质谱对对应各特征峰的分离物进行进一步的检测得到相应质量色谱图,利用质量色谱图可以确定9-硝基米诺环素以及对应的色谱图中9-硝基米诺环素的特征离子峰,依据该特征离子峰面积和步骤s1建立的标准曲线即可得到9-硝基米诺环素的质量含量。由此可见,本申请在实现了利用高效液相色谱对痕量9-硝基米诺环素充分分离的基础上,利用质谱数据精确对应质量色谱图中9-硝基米诺环素的特征离子峰,从而得到9-硝基米诺环素的精确质量含量,为对9-硝基米诺环素的有效质量控制提供可靠数据基础。
以上所述仅为本发明的优选实施例而已,并不用于限制本发明,对于本领域的技术人员来说,本发明可以有各种更改和变化。凡在本发明的精神和原则之内,所作的任何修改、等同替换、改进等,均应包含在本发明的保护范围之内。
- 还没有人留言评论。精彩留言会获得点赞!