一种pH和AA同时检测一体化微电极传感器及其制备方法和应用与流程
本发明属于微纳米材料在生物传感中应用技术领域,涉及一种ph和aa同时检测一体化微电极传感器及其制备方法和应用。
背景技术:
氧化应激在生命活动中扮演着重要角色,过量的活性氧会导致ph降低,而ph的轻微浮动会导致生物化学、离子传导以及神经电信号传递行为的异常。更重要的是脑环境的酸化反过来还会加剧氧化应激的发生。抗坏血酸(aa)作为一种重要的抗氧化剂,参与体内的各种氧化还原反应清除自由基,维持细胞氧化还原平衡,其含量的异常与各种疾病密切相关,如脑中风、阿尔茨海默病、帕金森病及癌症等。因此,发展同时检测ph和aa新方法对本质上理解ph和aa在疾病中的作用具有十分重要的意义。
传统的ph测定方法主要有ph计测定,ph试纸测定。ph计测定主要利用ph玻璃电极,依据能斯特方程,在零电流下通过电位进行测定,但玻璃电极每次测定前需要校准,并且,ph探头较大,需要体液较多;ph试纸虽然可以快速测定,但其在准确性上大打折扣;除此之外,有文献报道荧光指示剂可以用于测量体液ph,但在人体的安全性评估方面仍有待研究。与ph测定不同,aa常用的检测方法,主要依赖于自身的电化学特性,主要通过电化学方法来检测。然而,迄今为止尚无有效的电化学方法可实现ph和aa同时且准确检测。
技术实现要素:
针对目前的ph测量在体液测量中存在的问题以及同时分析的重要性,本发明的目的在于提供一种可实现微量唾液ph和aa高准确及同时分析的一体化微型传感器。另一目的在于提供其制备方和应用。
为实现本发明目的,所述微型传感器为一种集工作电极、对电极和参比电极为一体的微型传感器,该传感器工作电极以耐尔兰(nb)为ph识别分子,以2,2-连氮-二(3-2基-苯并噻唑-6-磺酸)二铵盐(abts)为参比分子,实现体液ph的高准确分析。与此同时,以碳纳米管作为修饰材料,提高aa的催化活性,实现体液中aa高选择性、高准确度和高灵敏度检测,并实现ph和aa的同时分析。
本发明所述ph和aa同时分析微型一体化传感器的制备方法如下:
(1)通过激光拉制仪制得玻璃毛细管;
(2)将碳纤维连接cu丝导入玻璃管露出碳纤维尖端;
(3)将pt丝导入玻璃管中并露出尖端;
(4)将含有饱和kcl的琼脂糖注入玻璃管尖端;
(5)将ag/agcl电极插入玻璃管中,并注入饱和kcl,玻璃管口用胶帽密封;
(6)将碳纳米材料(cnt)自组装修饰步骤(2)所得电极表面;
(7)将ph识别分子和参比分子按照比例修饰在步骤(6)所得电极的表面,制得所述的ph和aa同时检测微电极cfme/cnt/abts+nb。
步骤(1)所述玻璃毛细管可以用移液枪头替换,优选玻璃毛细管。
步骤(2)所述碳纤维的直径7μm,尖端露出长度为500μm~1mm。
步骤(3)所述pt丝直径为0.05或0.02μm,优选0.05μm;
步骤(5)所述ag丝浸泡于过饱和的fecl3溶液中10~60s,优选30s;所述的ag丝为0.05μm或0.02μm,优选0.05μm;
步骤(6)所述碳纳米材料为单壁碳纳米管、多壁碳纳米管、羧基化碳纳米管、氨基化碳纳米管、氧化石墨烯或石墨烯,优选单壁碳纳米管;
步骤(6)所述碳纳米材料通过π-π堆积吸附的方式修饰于碳纤维表面,吸附时间1min~1h,优选5min;
步骤(7)所述ph识别分子为nb,奈醌、亚甲基蓝、耐尔红、硫瑾或结晶紫,优选nb;
步骤(7)所述内参比分子为abts、巯基二茂铁、氨基二茂铁或羧基二茂铁,优选abts;
步骤(7)所述内参比和ph识别分子的溶剂为水、甲醇、乙醇、乙腈、n,n二甲基甲酰胺或二甲基亚砜,优选乙醇;
步骤(7)所述内参比分子与ph识别分子修饰摩尔比为1:0.1~1,优选1:1;
步骤(7)所述内参比和ph识别分子吸附于碳纤维电极表面,反应时间为1~60min,优选10min;
步骤(1-7)所述整个制备过程在室温下进行。
本发明原理:所述的一体化微传感器中nb的作用为ph特异性识别分子,随着ph的改变,nb分子的氧化还原峰伴随质子参与,其峰电位与ph满足能斯特响应。可以实现ph的高选择性检测。与此同时,所述的碳材料对aa具有良好的电催化性能,aa自身在低电位氧化,避免其他电活性物质干扰,可以实现aa的高选择性分析。这也是本发明实现ph和aa同时分析的基础。另外,所述的abts的作用作为内参比,在aa和ph改变时,其电化学信号(电流和电位)均不发生变化,可以提高本发明一体化微传感器对ph和aa同时检测的准确性。
本发明制备的一体化微传感器是一种集外参比和内参比为一体的比率型电化学传感器,将其用于体液ph和aa的同时分析,通过循环伏安法(cv)测得电极nb分子在不同ph下的氧化峰电位(enb),参比分子abts的峰电位eabts,依据两者的峰电位差δep的值与ph建立线性关系,得到线性范围和灵敏度。与此同时,测定不同aa浓度变化下,其自身的氧化峰电流jaa与abts的峰电流jabts的比值的变化关系,依据(jaa-j0)/jabts与aa浓度建立线性关系,得到线性范围和检测限。该微传感器不仅可以实现ph的高准确检测,而且可以实现aa高准确性检测。
本发明的有益效果在于:(1)本发明制备的微传感器集工作电极、对电极与参比电极为一体,实现微量唾液ph和aa高准确及同时分析。制备简单,成本低。(2)工作电极cfme/cnt/abts+nb以商品化碳纳米管、nb和abts分子为修饰,原料易得,nb和abts分子通过π-π作用共修饰于碳纳米管电极表面,修饰方法简单,快速。(3)以nb作为ph特异性识别电化学探针,ph检测线性范围为4.52~8.83,以abts为内参比,明显提高检测准确度,有效避免实际样品复杂环境带来的测定误差。(4)以cnt作为催化材料,对aa检测具有较宽的线性范围(0.02~8.0mm)。(5)该微传感器重现性好(相同3支电极对ph测定相对标椎偏差不超过4.0%),稳定性高(连续扫描100圈峰电流密度比值下降不超过2.5%)。(6)微电极尖端尺寸直径为7μm,可以实现微量样品的定性、定量测定,对于了解ph和aa在相关疾病中发挥的作用具有重要意义。
附图说明
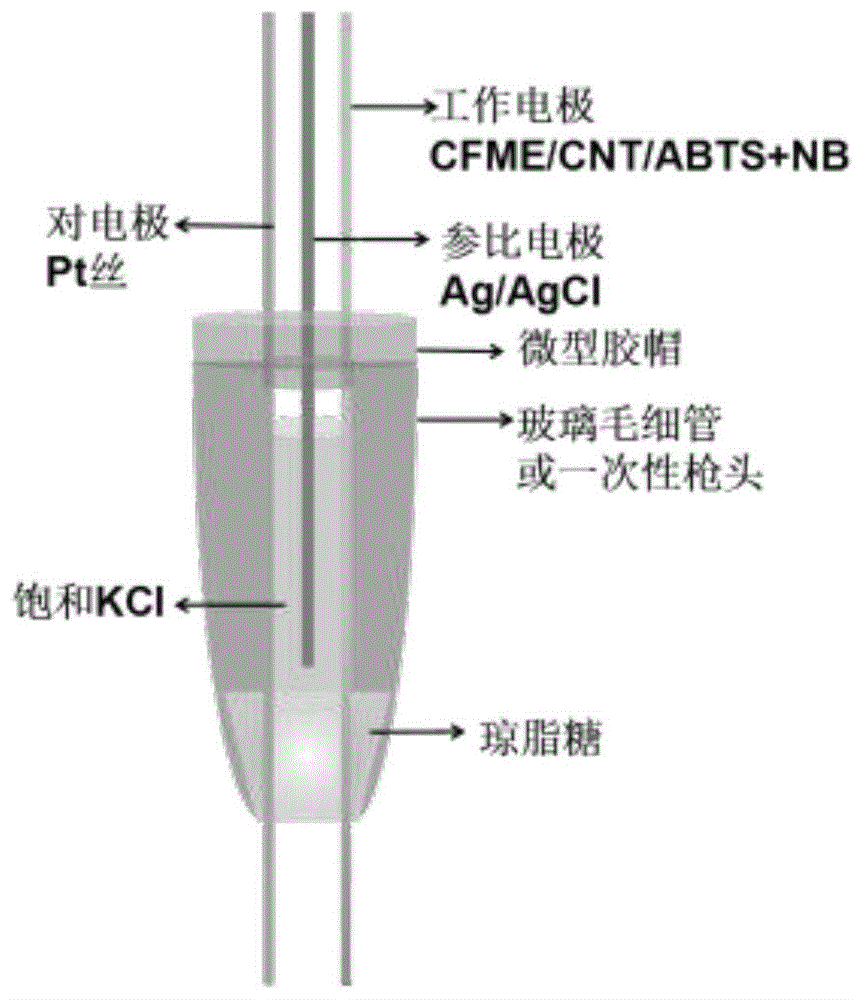
图1为实施例1一体化微电极的结构示意图。
图2为本发明工作电极修饰过程的cv响应,其中a-cfme/cnt,b-cfme/cnt/abts,c-cfme/cnt/nb,d-cfme/cnt/abts+nb。
图3为本发明一体化微电极在不同扫速下的cv响应。
图4为本发明一体化微电极nb分子和abts分子氧化还原峰电流与扫速的关系图,其中a-nb分子,b-abts。
图5为本发明一体化微电极在不同ph的pbs溶液中的cv响应(a)及线性关系图(b)。
图6为本发明一体化微电极在不同aa浓度中的cv响应(a)及线性关系图(b)。
图7为本发明一体化微电极对ph测定(a)和aa测定(b)的抗干扰实验。
图8为本发明一体化微电极扫描100圈的cv图,其中a-第1圈,b-第100圈。
图9为本发明一体化微电极按照相同的制备方法制备三支在相同ph下的cv响应。
图10为本发明一体化微电极对唾液的cv响应,其中a-0.1mpbs(ph7.4),b-唾液。
具体实施方式
结合以下具体实例和附图,对本发明作进一步的详细说明,除以下专门提及的内容之外,均为本领域的普通知识和公知常识,本发明没有特别限制内容。
实施例1:一体化微电极制备及修饰
(1)一体化微电极的制备
首先采用激光拉制硼酸酸盐毛细管,然后将连接碳纤维的cu丝工作电极、pt丝对电极、自制的ag/agcl电极为参比电极穿于毛细管中,然后将含有kcl的热的琼脂糖用注射器注入玻璃尖端,泠却后,继续注入饱和kcl,然后用微型胶帽封塞,得到一体化微电极。
自制的ag/agcl电极:首先将ag丝通过砂纸打磨除去表面氧化膜,然后浸泡于过饱和的fecl3溶液中10~60s,取出,用蒸馏水清洗。
(2)一体化微电极的修饰
将(1)制备的一体化电极浸入0.5㎎/mlcnt中5min取出。用乙醇、蒸馏水依次各清洗3次,得到cnt修饰的碳纤维微电极cfme/cnt,继续将cfme/cnt浸入预配置好的具有参比分子abts和ph识别分子nb的乙醇溶液中(摩尔比1:1)10min。取出用乙醇、蒸馏水依次各洗涤3次,制备的电极为cfme/cnt/abts+nb(图1)。
实施例2:微电极cfme/cnt/abts+nb的电化学表征
利用chi660d电化学工作站对微电极cfme/cnt/abts+nb修饰过程进行cv扫描,扫速:0.1vs-1。如图2所示,a为cfme/cnt,b为abts修饰的cfme/cnt,c为单独nb修饰的cfme/cnt,d为abts和nb共修饰的cfme/cnt电极,分别在0.1m的pbs(ph7.4)中的cv图。从图中看出,cfme/cnt电极只有充电背景电流。单独修饰abts的cfme/cnt电极在0.52v附近有一对明显的氧化峰还原,这说明参比分子abts具有良好的电化学活性。单独nb修饰的cfme/cnt电极的cv能看到在-0.39v附近有一对明显的氧化还原峰,这说明ph识别分子具有良好的电化学活性。当abts和nb共修饰后,由于abts分子中的磺酸基和nb分子中的氨基发生静电作用,所得电极的cv图上能看到在-0.42v与0.52v处有两对氧化还原峰,nb分子的峰电位向左移动,但nb和abts的电化学信号区分好并具有良好的电化学活性。进一步通过改变扫速,nb的氧化和还原峰电流,abts的氧化和峰电流均与扫速具有良好的线性关系(图3和图4),这说明nb分子和abts分子在微电极上是一个表面吸附控制的电化学反应过程。表明abts和nb同时修饰在cfme/cnt电极上。
实施例3:一体化微电极对ph测定
利用chi660d电化学工作站对本发明的一体化微电极在不同的ph的0.1mpbs中进行cv测定,扫速:0.1vs-1。如图5所示,随着ph(4.5~8.8)的改变,该微电极对ph具有良好的响应,nb分子的氧化峰电位epa(nb)随着ph的升高逐渐正移,与此同时,abts的氧化峰电位epa(abts)保持不变,峰电位差δepa与ph在4.5~8.8的范围内呈现良好的线性关系,线性方程为:δepa=0.6053+0.04386ph,灵敏度为43.8mv/ph,可满足实际体液样品ph检测需求。
实施例4:一体化微电极对aa测定
利用chi660d电化学工作站对修饰后一体化微电极在不同的浓度的aa进行cv测定,扫速:0.1vs-1。实验结果如图6所示,随着aa浓度加入,该一体化微电极对aa的cv响应曲线在0v左右出现的一个新的氧化峰,并且该氧化峰的峰电流密度(jaa)随着aa浓度的增加而逐渐增大,与此同时,ph识别分子nb的氧化还原峰保持不变,参比分子abts的氧化峰电流jabts也保持不变(扣背景),并且峰电流比值(jaa-j0)/jabts在20μm至4.0mm的范围内具有良好的线性关系,线性方程为(jaa-j0)/jabts=0.1332+0.4648caa(mm)。检测限为0.8μm。
实施例5:一体化微电极的选择性、稳定性、重现性
利用chi660d电化学工作站对本发明一体化微电极进行干扰测定,在ph=7.4的0.1mpbs溶液中加入其它生物活性物质(如aa、da、ua、atp、glucose、sa、h2o2、cys、gsh),对ph测定所引起峰电位变化和对aa测定所引起的峰电流变化均无变化(图7)。表明本发明制备一体化微电极对ph和aa检测具有较高的选择性。对本发明一体化微电极在ph=7.4的0.1mpbs溶液连续进行cv测定100圈,nb分子和abts分子的氧化还原峰电位和峰电流均无明显变化(图8),表明该一体化微电极具有良好的稳定性。此外,按照实施例1的制备方法制备三支一体化微电极并测定其cv响应。如图9,三支一体化微电极的nb分子和abts分子均具有良好的电化学活性,表明该电极具有较好的重现性。
实施例6:唾液样品中ph和aa同时测定
取正常人的唾液样品,无需处理,直接取50μl,将实施例1的一体化微电极直接植入唾液,连接导线,利用chi660d电化学工作站采用cv法在-0.7~0.72v电位窗口下直接测定(图10),得到ph识别分子与参比分子abts的电位差δepa,根据图5线性关系计算其ph值。记录在0v的峰电流引起峰电流变化与参比分子的abts产生电流比值,根据图6中的线性关系,计算唾液中aa的浓度。实现微量唾液ph和aa高准确及同时分析。
- 还没有人留言评论。精彩留言会获得点赞!