一种胶囊剂的囊材中辣椒总碱的含量测定方法与流程
本发明属于保健品技术领域,具体涉及一种胶囊剂的囊材中辣椒总碱的含量测定方法。
背景技术:
软胶囊是继片、针剂后发展起来的一种新剂型,属于胶囊剂的一种包装方式,常见于药品或保健食品。它是将液体药物或液果体药物经处理密封于软质囊材中而制成的一种胶囊剂。软质囊材是由胶囊用明胶、甘油或其他适宜的药用辅料单独或混合制成。
辣椒色素以辣椒果皮及其制品为原料,经萃取、过滤、浓缩、脱辣椒总碱等工艺制成。辣椒色素属于天然食品色素,广泛应用于食品、胶囊囊材、纺织品等领域。在胶囊囊材中辣椒色素的使用需要对其进行有效的控制,以满足质量要求。辣椒色素主要以辣椒碱作为其质量控制指标,但目前,尚未发现通过检测胶囊囊材中辣椒总碱的含量来控制辣椒色素的使用的文献报道。
因此,有必要研究一种胶囊剂的囊材中辣椒总碱的检测方法,以有效控制囊材中辣椒色素的使用。
技术实现要素:
本发明的目的在于提供一种胶囊剂的囊材中辣椒总碱的含量测定方法,该方法能够有效、准确的检测出胶囊剂的囊材中辣椒总碱的含量,有利于实现对胶囊剂的囊材中的辣椒色素进行有效的检测和控制。
本发明是通过以下技术方案实现:
一种胶囊剂的囊材中辣椒总碱的含量测定方法,包括以下步骤:
(1)对照品溶液制备:精密称取对照品降二氢辣椒碱、辣椒碱和二氢辣椒碱,加入适量无水乙醇制成对照品溶液,即得;
(2)供试液制备:精密称取胶囊剂样品,加入正己烷洗去胶囊内容物,得到胶囊皮;将胶囊皮挥发至无正己烷后,加入水超声至胶囊皮完全溶解,取出,加入四氢呋喃混匀,用无水乙醇定容,混匀后离心,收集上清液;精密移取上清液,通过c18固相萃取柱,用无水乙醇洗脱萃取柱,洗脱液合并;将洗脱液氮吹至近干,加入1%乙酸和乙腈混合制成的稀释液,涡旋溶解并定容,摇匀,经滤膜过滤,即得供试液;
(3)色谱条件:c18色谱柱;检测波长280nm;以乙腈为流动相a,以1%乙酸溶液为流动相b,梯度洗脱,洗脱程序如下表1所示;
(4)测定法:分别精密吸取对照品溶液与供试液各20μl,依上述色谱条件进行测定,采用外标法计算,即得。
优选的,步骤(2)中,所述超声的温度为40-70℃。
优选的,步骤(2)中,所述离心的转速为5000-10000r/min,离心的时间为2-5min。
优选的,步骤(2)中,所述氮吹的温度为40-60℃。
优选的,步骤(2)中,所述稀释液中,1%乙酸和乙腈的体积比为(3-7):(3-7),优选为1:1,接近初始流动相的比例,有利于色谱峰的峰型更好。
优选的,步骤(2)中,c18固相萃取柱的填料为500mg,柱体积为6ml,使用前用无水乙醇活化,以除去c18固相萃取柱自身的一些杂质。
优选的,步骤(3)中,柱温为25-35℃,流速为0.8-1.2ml/min。
本发明与现有技术相比,具有如下有益效果:
本发明提供了胶囊剂的囊材中辣椒总碱的含量测定方法,将胶囊皮经水溶解,四氢呋喃和无水乙醇提取,再经c18固相萃取柱净化后,用高效液相色谱仪分析,采用外标法定量即得。通过对辣椒总碱的含量测定方法进行线性、精密度、耐用性试验(稳定性)、专属性试验(空白)、检出限、定量限、准确度(回收率)试验,均符合gb/t27404-2008《实验室质量控制规范》的要求。本发明方法科学有效,能够有效、准确的检测出胶囊剂的囊材中辣椒总碱的含量,对胶囊剂的囊材中辣椒总碱的含量起到质量控制的目的。
附图说明
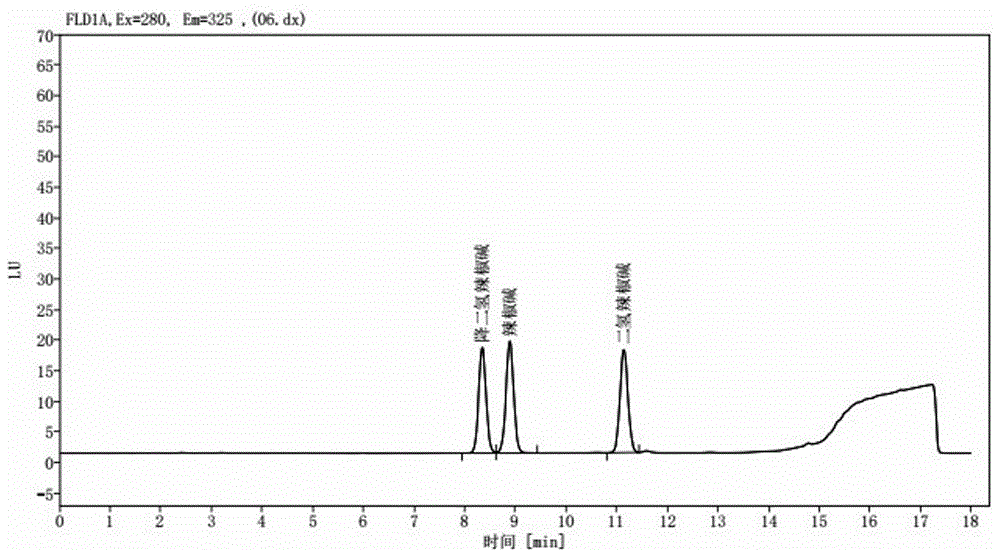
图1为本发明供试液的色谱图;
图2为流动相及洗脱条件的选择方法一的色谱图;
图3为流动相及洗脱条件的选择方法二的色谱图。
具体实施方式
下面通过具体实施方式来进一步说明本发明,以下实施例为本发明具体的实施方式,但本发明的实施方式并不受下述实施例的限制,其他的任何未背离本发明的精神实质与原理下所作的改变、修饰、替代、组合、简化,均应为等效的置换方式,都包含在本发明的保护范围之内。
一、仪器与试剂
对照品:降二氢辣椒碱(对照品来源:trc,批号:6-ush-145-3,纯度:97.65%);辣椒碱(对照品来源:中国食品药品检定研究院,批号:110839-201806,纯度:99%);二氢辣椒碱(对照品来源:anpel,批号:38980050,纯度:99.3%)。
仪器:waters2489高效液相系统,电子天平(北京赛多利斯科学仪器有限公司),离心机(常州市万丰仪器制造有限公司)。
试剂:无水乙醇(ar);正己烷(ar);乙腈(色谱纯);四氢呋喃(色谱纯);乙酸(色谱纯);一级用水。
二、实验方法
2.1对照品溶液的制备:
分别精密称取对照品,降二氢辣椒碱10.68mg,辣椒碱11.73mg,二氢辣椒碱11.27mg,置于50ml容量瓶中,加入无水乙醇溶解并定容至刻度,摇匀,即得对照品储备溶液(降二氢辣椒碱208.5804μg/ml、辣椒碱232.2540μg/ml、二氢辣椒碱223.8222μg/ml)。对照品储备溶液放在4℃的冰箱中避光储存备用。
精密移取5.00ml对照品储备溶液,置于50ml容量瓶中,加入无水乙醇定容至刻度,摇匀,即得对照品中间溶液(降二氢辣椒碱20.8580μg/ml、辣椒碱23.2254μg/ml、二氢辣椒碱22.3822μg/ml)。对照品中间溶液放在4℃的冰箱中避光储存备用。
精密移取1.00ml对照品中间溶液,置于50ml容量瓶中,加入稀释液定容至刻度,摇匀,即得对照品工作溶液(降二氢辣椒碱0.4171μg/ml、辣椒碱0.4645μg/ml、二氢辣椒碱0.4476μg/ml)。
2.2供试液的制备:
精密称取胶囊剂样品约1g,把胶囊剪开,置于50ml离心管中,加入10ml正己烷,洗去胶囊内容物,弃去正己烷,再加入正己烷重复洗2次;把胶囊皮置于通风橱挥发至无正己烷后,加入5ml水,60℃超声至胶囊皮完全溶解,取出,加入5ml四氢呋喃,混匀后,用无水乙醇定容至50ml,混匀后,8000r/min离心3min;精密移取5ml上清液,通过c18固相萃取柱,用10ml无水乙醇洗脱萃取柱,洗脱液合并到氮吹管;将洗脱液50℃氮吹至近干,加入1%乙酸和乙腈按体积比为1:1混合制成的稀释液涡旋溶解并定容至5ml,摇匀,经滤膜过滤,即得供试液。
2.3色谱条件:
色谱柱:phenomenex,kinetex,xb-c18,150×4.6mm,5μm;
检测波长280nm;柱温30℃,流速为1.0ml/min;
以乙腈为流动相a,以1%乙酸溶液为流动相b,梯度洗脱,洗脱程序如下表1所示:
表1梯度洗脱程序
2.4测定法:
分别精密吸取对照品溶液与供试液各20μl,依上述色谱条件进行测定。
2.5标准工作曲线绘制
对照品工作溶液分别进样0.4μl、1μl、10μl、20μl、40μl,在2.3条件下,进行分析测定,绘制降二氢辣椒碱、辣椒碱、二氢辣椒碱的外标法标准工作曲线。
2.6结果计算:
式中:xn—试样中降二氢辣椒碱(辣椒碱、二氢辣椒碱)的含量,%;
cn—试样溶液中降二氢辣椒碱(辣椒碱、二氢辣椒碱)的浓度,μg/ml;
m—试样的质量,g;
v—试样稀释的体积,ml;
k—单位转换系数,k=0.0001。
式中:x—试样中辣椒总碱的含量,%;
x1—试样中降二氢辣椒碱的含量,%;
x2—试样中辣椒碱的含量,%;
x3—试样中二氢辣椒碱的含量,%。
三、方法学考察:
3.1专属性试验(空白)
3.1.1试验方法
不加样品,按2.2试样制备方法处理空白溶液,按2.3色谱条件测定空白溶液,与降二氢辣椒碱、辣椒碱、二氢辣椒碱标准工作溶液的出峰时间对比。
3.1.2试验结果
空白溶液在降二氢辣椒碱、辣椒碱、二氢辣椒碱的出峰时间处均无吸收峰,表明空白对测定结果基本无干扰。
线性范围确认
3.2.1试验数据见表2:
表2线性关系数据
3.2.2线性试验结论
线性评价:降二氢辣椒碱、辣椒碱、二氢辣椒碱相关系数r分别为0.999998、0.999999、0.999999,所以用该方法测定降二氢辣椒碱在浓度为0.008343μg/ml至0.8343μg/ml,辣椒碱在浓度为0.009290μg/ml至0.9290μg/ml,二氢辣椒碱在浓度为0.008952μg/ml至0.8952μg/ml,之间呈现良好的线性,符合gb/t27404-2008《实验室质量控制规范》的要求【gb/t27404-2008要求相关系数r≥0.99】。
检出限和定量限
分析方法的检出限dl和定量限ql由信噪比(s/n)计算。dl定义为s/n=3时对应的待分析浓度,ql定义为s/n=10时对应的待分析浓度。
3.3.1检出限
当信噪比(s/n)为3时,降二氢辣椒碱检出限为0.007419μg/ml,辣椒碱检出限为0.008508μg/ml,二氢辣椒碱检出限为0.007877μg/ml;样品取样量1g,定容50ml时,方法的降二氢辣椒碱检出限为0.37μg/g,辣椒碱检出限为0.43μg/g,二氢辣椒碱检出限为0.40μg/g。
3.3.2定量限
当信噪比(s/n)为10时,降二氢辣椒碱定量限为0.01958μg/ml,辣椒碱定量限为0.02221μg/ml,二氢辣椒碱定量限为0.02100μg/ml;样品取样量1g,定容50ml时,方法的降二氢辣椒碱定量限为0.98μg/g,辣椒碱定量限为1.11μg/g,二氢辣椒碱定量限为1.05μg/g。
精密度试验
3.4.1试验方法
称取6份样品,按2.2试样制备方法处理样品;检测样品含量,计算其rsd(%)。试验数据见下表3:
表3精密度试验结果
3.4.2试验结论
样品降二氢辣椒碱x1含量的rsd为0.9%,辣椒碱x2含量的rsd为0.8%,二氢辣椒碱x3含量的rsd为0.9%,辣椒总碱x含量的rsd为0.7%,表明该方法有较好的精密度,符合gb/t27404-2008《实验室质量控制规范》的要求【gb/t27404-2008要求rsd(%)≤7.5%】。
耐用性试验
3.5.1稳定性试验
3.5.1.1试验方法:
将供试液分别在室温下放置0h、2h、4h、6h、8h、12h后,按2.3条件测定浓度(μg/ml),计算其rsd(%),试验数据见下表4:
表4稳定性试验结果
3.5.1.2试验结论
供试液分别在室温下放置0h、2h、4h、6h、8h、12h后,降二氢辣椒碱浓度的rsd为3.7%,辣椒碱浓度的rsd为3.8%,二氢辣椒碱浓度的rsd为4.1%,表明供试液在室温下12小时内的稳定性良好。
3.5.2不同品牌色谱柱试验
3.5.2.1试验方法:
使用不同品牌色谱柱按2.3条件测定对照品工作溶液,比较不同品牌色谱柱对降二氢辣椒碱、辣椒碱、二氢辣椒碱的分离效果。
3.5.2.3试验结论:
phenomenex,kinetexxb-c18和supelcodiscoveryhsc18均能较好分离降二氢辣椒碱、辣椒碱、二氢辣椒碱,都能满足检测要求。
准确度试验(回收率)
3.6.1试验方法
加标:精密称取约1g样品9份(已知样品的降二氢辣椒碱含量:0.000197%,辣椒碱含量:0.000219%,二氢辣椒碱含量:0.000215%),分成3组,每组3份,各组分别精密加入对照品中间溶液(降二氢辣椒碱20.8580μg/ml、辣椒碱23.2254μg/ml、二氢辣椒碱22.3822μg/ml)100μl、400μl、900μl。按2.2试样制备方法处理样品。
3.6.2试验数据如下表5-7所示:
表5回收率试验结果
测得加入量=加标样品测得量-样品测得量;
回收率(%)=测得加入量/理论加入量×100%。
3.6.3试验结论
降二氢辣椒碱平均回收率为:96.9%,rsd为2.7%;辣椒碱平均回收率为:96.7%,rsd为2.6%;二氢辣椒碱平均回收率为:97.0%,rsd为2.7%;符合gb/t27404-2008《实验室质量控制规范》的要求【gb/t27404-2008要求回收率为90~110%】。
四、供试液制备方法的考察
要实现对囊材中降二氢辣椒碱、辣椒碱和二氢辣椒碱3种成分的有效提取,准确测定其含量,供试液的制备方法尤为关键,本发明对供试液的制备方法进行了如下考察:
方法(1):精密称取胶囊剂样品约1g,把胶囊剪开,置于50ml离心管中,加入10ml正己烷,洗去胶囊内容物,弃去正己烷,再加入正己烷重复洗2次;把胶囊皮置于通风橱挥发至无正己烷后,加入5ml水,60℃超声至胶囊皮完全溶解,取出,用无水乙醇定容至50ml,混匀后,8000r/min离心3min;精密移取5ml上清液,通过c18固相萃取柱,并收集到氮吹管中,用10ml无水乙醇洗脱萃取柱,洗脱液合并到氮吹管;50℃氮吹至近干,加入1%乙酸和乙腈按体积比为1:1混合制成的稀释液涡旋溶解并定容至5ml,摇匀,经滤膜过滤,即得供试液。经测试,降二氢辣椒碱、辣椒碱和二氢辣椒碱的回收率分别为,65.6%、67.1%、63.8%,不符合gb/t27404-2008《实验室质量控制规范》的要求【gb/t27404-2008要求回收率为90~110%】。
方法(2):精密称取胶囊剂样品约1g,把胶囊剪开,置于50ml离心管中,加入10ml正己烷,洗去胶囊内容物,弃去正己烷,再加入正己烷重复洗2次;把胶囊皮置于通风橱挥发至无正己烷后,加入5ml水,60℃超声至胶囊皮完全溶解,取出,加入5ml二甲基亚砜,混匀后,用无水乙醇定容至50ml,混匀后,8000r/min离心3min;精密移取5ml上清液,通过c18固相萃取柱,并收集到氮吹管中,用10ml无水乙醇洗脱萃取柱,洗脱液合并到氮吹管;50℃氮吹至近干,加入1%乙酸和乙腈按体积比为1:1混合制成的涡旋溶解并定容至5ml,摇匀,经滤膜过滤,即得供试液。经测试,降二氢辣椒碱、辣椒碱和二氢辣椒碱的回收率分别为84.1%、80.5%、74.7%,不符合gb/t27404-2008《实验室质量控制规范》的要求【gb/t27404-2008要求回收率为90~110%】。
方法(3):将二甲基亚砜替换为n,n-二甲基甲酰胺,其余同方法(2)。经测试,降二氢辣椒碱、辣椒碱和二氢辣椒碱的回收率分别为76.3%、82.4%、72.7%,不符合gb/t27404-2008《实验室质量控制规范》的要求【gb/t27404-2008要求回收率为90~110%】。
方法(4):精密称取胶囊剂样品约1g,把胶囊剪开,置于50ml离心管中,加入10ml正己烷,洗去胶囊内容物,弃去正己烷,再加入正己烷重复洗2次;把胶囊皮置于通风橱挥发至无正己烷后,加入5ml水,60℃超声至胶囊皮完全溶解,取出,加入5ml四氢呋喃,混匀后,用无水乙醇定容至50ml,混匀后,8000r/min离心3min;精密移取5ml上清液,通过c18固相萃取柱,用10ml无水乙醇洗脱萃取柱,洗脱液合并到氮吹管;将洗脱液50℃氮吹至近干,加入1%乙酸和乙腈按体积比为1:1混合制成的稀释液涡旋溶解并定容至5ml,摇匀,经滤膜过滤,即得供试液。经测试,降二氢辣椒碱平均回收率为:96.9%,rsd为2.7%;辣椒碱平均回收率为:96.7%,rsd为2.6%;二氢辣椒碱平均回收率为:97.0%,rsd为2.7%;符合gb/t27404-2008《实验室质量控制规范》的要求【gb/t27404-2008要求回收率为90~110%】。
方法(5):用甲醇代替无水乙醇,其余同方法(4),经测试,降二氢辣椒碱、辣椒碱和二氢辣椒碱的回收率分别为84.7%、80.3%、76.9%,不符合gb/t27404-2008《实验室质量控制规范》的要求【gb/t27404-2008要求回收率为90~110%】。
因此,将方法(4)作为本发明供试液的制备方法,该方法通过提取溶剂的优化,将胶囊皮经水溶解,四氢呋喃和无水乙醇提取,并通过采用c18固相萃取柱进一步净化,能从胶囊皮中有效提取出降二氢辣椒碱、辣椒碱和二氢辣椒碱三种成分,保证了检测的准确性,且可适用于多种软胶囊产品。
五、色谱条件的优化
要实现同一色谱条件下同时测定囊材中降二氢辣椒碱、辣椒碱和二氢辣椒碱3种成分的含量测定,流动相及洗脱条件的选择是关键技术。
本发明流动相及洗脱条件的选择采用如下方法进行比较:
方法一:流动相采用乙腈-0.1%磷酸溶液,洗脱梯度同“方法三”,其hplc色谱图如图2所示,分离效果均不理想,降二氢辣椒碱和辣椒碱的峰达不到基线分离,影响准确定量。
方法二:流动相采用乙腈-1%乙酸溶液=40:60等度洗脱,其hplc色谱图如图3所示,洗脱时间长,色谱峰的峰宽较大,达不到理想的检测灵敏度。
方法三:以乙腈为流动相a,以1%乙酸溶液为流动相b,梯度洗脱,洗脱程序如表1所示,其hplc色谱图如图1所示,洗脱时间短,分离效果好,降二氢辣椒碱、辣椒碱、二氢辣椒碱均能达到基线分离,因此将方法三作为本发明的流动相及洗脱条件。
- 还没有人留言评论。精彩留言会获得点赞!