抑制荧光强度降低的成像试剂、试剂盒的制作方法
1.本发明涉及基因测序技术领域,具体涉及抑制荧光强度降低的成像试剂、试剂盒。
背景技术:
2.基因测序作为一种重要的实验技术,在生物学研究中有着广泛的应用。早在dna双螺旋结构被发现后不久就有人报道过dna测序技术,但是当时的操作流程复杂,没能形成规模。dna测序技术经历sanger法为代表的一代测序技术向边合成边测序二代测序技术再向纳米孔等单分子测序技术为代表的三代测序技术的发展,其中边合成边测序的二代测序技术包括形成阵列结构的模板簇结构后,用不同颜色的荧光标记四种不同的dntp,当dna聚合酶合成互补链时,每添加一种dntp就会释放出不同的荧光,根据捕捉的荧光信号并经过特定的计算机软件处理,从而获得待测dna的序列信息。
3.边合成边测序的检测方法在阵列情况下进行反复的荧光检测步骤会引起核酸损伤造成荧光强度损失,荧光分子在吸收激发光后的能量跃迁,以及在由激发态重新转变为基态反应过程,通常会伴随产生氧自由基,形成活性氧簇分子,在氧自由基或活性氧簇分子的作用下,鸟嘌呤转化为8-氧代-鸟嘌呤,或者引起脱碱基位点和胸腺嘧啶和胞嘧啶的均二聚作用和易二聚作用,最终导致核酸损伤或降解。因此,为了降低荧光检测过程中引起的核酸损伤造成的荧光强度损失,通常会选择在成像试剂中添加抗氧化剂,去除氧自由基,避免活性氧簇分子的形成,例如专利wo2006064199中公开了添加使用抗坏血酸盐;专利cn103403188b中公开了添加使用没食子酸等多酚类化合物。这些在先公开的现有技术中通过在成像试剂中添加使用抗氧化剂组分虽然在一定程度上减少了测序过程中的荧光强度衰减,但是随着测序读长的增长仍然会存在荧光强度的损失,导致长读长测序的准确性降低,因此如何进一步优化成像试剂的配方组成,进一步提高长读长测序的准确性成为了目前亟待解决的技术问题。
技术实现要素:
4.为了克服现有技术的缺陷,本发明的目的之一是提供一种抑制荧光强度降低的成像试剂,应用于基于荧光的多循环核酸测序反应,通过多种抗氧化剂的复配,发挥协同增效作用,抑制荧光强度随着测序读长延长的降低,提高测序准确性。
5.同时,本发明还在于提供一种试剂盒,包括本发明提供的成像试剂,应用于核酸测序,提高长读长测序的准确性。
6.为了实现上述目的,本发明采用的技术方案如下:
7.一种抑制荧光强度降低的成像试剂,包括3,4-二羟基苯甲酸乙酯、3,4-二羟基苯甲酸和抗坏血酸钠。
8.可选的,上述成像试剂中3,4-二羟基苯甲酸乙酯、3,4-二羟基苯甲酸和抗坏血酸钠的浓度配比为1:1:3。进一步的,上述成像试剂还包括tris缓冲剂。
9.本发明成像试剂中通过3,4-二羟基苯甲酸乙酯、3,4-二羟基苯甲酸和抗坏血酸钠
复配协同增效,减少荧光分子成像过程中自由基和活性氧簇的产生,降低由自由基和/或活性氧簇分子导致的鸟嘌呤氧化,或者脱碱基位点和胸腺嘧啶和胞嘧啶的均二聚作用、易二聚作用等,减少核酸损伤,降低测序过程中荧光强度的降低,在长读长测序过程中维持荧光强度在小幅度范围内浮动,降低定相和预定相,提高长读长测序的准确性。
10.作为优选的,上述成像试剂的具体配方组成为90~110mm tris,750~850mm nacl,15~25mm 3,4-二羟基苯甲酸乙酯,15~25mm 3,4-二羟基苯甲酸,45~65mm抗坏血酸钠,0.1%-0.2%3-[(3-胆酰胺基丙基)二甲基铵基]-1-丙磺酸盐,余量为水,ph=8.0。
[0011]
作为更进一步优选的,在本发明的一个实施例中,上述成像试剂的配方组成为:100mm tris,800mm nacl,20mm 3,4-二羟基苯甲酸乙酯,20mm 3,4-二羟基苯甲酸,60mm抗坏血酸钠,0.1%3-[(3-胆酰胺基丙基)二甲基铵基]-1-丙磺酸盐,余量为水,ph=8.0。
[0012]
一种核酸测序用试剂盒,包括延伸试剂、切割试剂、成像试剂和洗涤剂;其中延伸试剂中包括修饰核苷酸,修饰核苷酸分子上连接有可逆阻断部分;其中切割试剂包括作用在可逆阻断部分的组分,使可逆阻断部分脱离修饰核苷酸分子;所述成像试剂为上述成像试剂。
[0013]
可选的,所述修饰核苷酸分子上通过可切割接头连接有标记分子;所述可切割接头包含一个或多个可裂解基团;所述可裂解基团包括二硫键、和/或叠氮化物;所述切割试剂还包括作用在可裂解基团的组分使标记分子脱离修饰核苷酸分子;所述可逆阻断部分为甲基叠氮。作为进一步优选的,所述标记分子为荧光分子。
[0014]
可选的,所述洗涤剂中包括抗氧化剂和/或切割剂清除剂。
[0015]
可选的,所述可裂解基团为叠氮化物;所述切割试剂包括三-(羟丙基)膦;所述洗涤剂中包括胱氨酸,硫辛酸,3,3
′‑
二硫代二丙酸或聚乙二醇化的叠氮化物。
[0016]
可选的,所述洗涤剂中还包括没食子酸和/或抗坏血酸钠。
[0017]
在本发明的一个实施例中,采用本发明的试剂盒进行核酸测序方法包括:1)提供阵列的核酸模板分子;2)加入测序引物与对应的核酸模板分子杂交;3)加入延伸试剂,在延伸试剂中聚合酶的作用下,修饰核苷酸分子掺入测序引物;4)然后加入洗涤剂,去除未反应的延伸试剂;5)之后再加入成像试剂,在激发光的作用下,修饰核苷酸分子上通过可切割接头连接的荧光分子发光,采集阵列的核酸模板分子的荧光分子发光图像,根据图像信息判断对应每个模板分子掺入的修饰核苷酸的类型;本发明采用的成像试剂中包括3,4-二羟基苯甲酸乙酯、3,4-二羟基苯甲酸和抗坏血酸钠,三种组分协同增效作用,减小测序过程中核酸分子的光诱导损伤;6)然后再加入洗涤剂,替换冲洗掉成像试剂,之后再加入切割试剂,去除掺入测序引物的修饰核苷酸分子上的可逆阻断部分以及标记分子;7)之后加入洗涤剂,冲洗替换未反应的切割试剂;该步骤的洗涤剂可以通过加入没食子酸和/或抗坏血酸等抗氧化剂,消除反应体系中产生的氧自由基,同时加入切割剂清除剂,其中切割剂清除剂是抑制在步骤6)中使用或由其产生的反应性化合物与测序过程中使用或由测序过程产生的多核苷酸,测序过程中使用的酶或在测序过程中使用的其他试剂或化合物的相互作用的化合物,比如胱氨酸,硫辛酸,3,3
′‑
二硫代二丙酸或聚乙二醇化的叠氮化物,能够氧化残留的切割试剂,消除残留切割试剂对下一轮核苷酸的掺入产生影响;8)之后再返回至步骤3)循环测序。
附图说明
[0018]
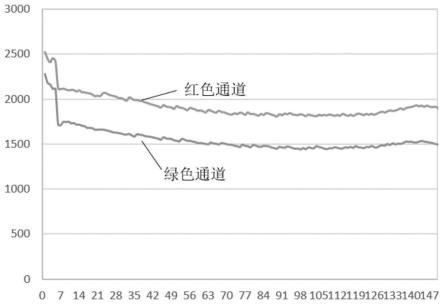
图1为采用illumina nextseq500配套试剂运行测序过程中荧光强度变化趋势图;
[0019]
图2为采用本发明实施例1提供的成像试剂运行测序过程中荧光强度变化趋势图;
[0020]
图3为采用本发明对比例1提供的成像试剂运行测序过程中荧光强度变化趋势图;
[0021]
图4为采用本发明对比例2提供的成像试剂运行测序过程中荧光强度变化趋势图;
[0022]
图5为采用本发明对比例3提供的成像试剂运行测序过程中荧光强度变化趋势图;
[0023]
图6为采用本发明对比例4提供的成像试剂运行测序过程中荧光强度变化趋势图;
[0024]
图7为采用本发明对比例5提供的成像试剂运行测序过程中荧光强度变化趋势图;
[0025]
图8采用本发明对比例6提供的成像试剂运行测序过程中荧光强度变化趋势图。
具体实施方式
[0026]
下面,结合具体实施方式,对本发明做进一步说明,但实施例并不对本发明做任何形式的限定。除非特别说明,本发明采用的试剂、方法和设备为本技术领域常规试剂、方法和设备。除非特别说明,以下实施例所用试剂和材料均为市购。
[0027]
实施例1
[0028]
本实施例提供一种抑制荧光强度降低的成像试剂,其配方组成为100mm tris,800mm nacl,20mm 3,4-二羟基苯甲酸乙酯,20mm 3,4-二羟基苯甲酸,60mm抗坏血酸钠,0.1wt%3-[(3-胆酰胺基丙基)二甲基铵基]-1-丙磺酸盐,余量为水,ph=8.0。
[0029]
其配制方法包括:
[0030]
1)分别称取3.0285g tris、11.688g nacl、2.9718g抗坏血酸钠、0.911g 3,4-二羟基苯甲酸乙酯、0.7705g 3,4-二羟基苯甲酸、0.25g 3-[(3-胆酰胺基丙基)二甲基铵基]-1-丙磺酸盐于250ml烧杯中;
[0031]
2)加200ml的超纯水于烧杯中,放入转子,将烧杯置于磁力搅拌器上让其溶解;
[0032]
3)待溶解后,使用浓盐酸调节ph为8.0;
[0033]
4)将溶液倒入量筒中定容至250ml,将定容完成的试剂进行过滤,-20℃保存。
[0034]
实施例2
[0035]
本实施例提供一种抑制荧光强度降低的成像试剂,其配方组成为90mm tris,750mm nacl,15mm 3,4-二羟基苯甲酸乙酯,15mm 3,4-二羟基苯甲酸,45mm抗坏血酸钠,0.1wt%3-[(3-胆酰胺基丙基)二甲基铵基]-1-丙磺酸盐,余量为水,ph=8.0。其配制方法过程同实施例1。
[0036]
实施例3
[0037]
本实施例提供一种抑制荧光强度降低的成像试剂,其配方组成为110mm tris,850mm nacl,25mm 3,4-二羟基苯甲酸乙酯,25mm3,4-二羟基苯甲酸,65mm抗坏血酸钠,0.2wt%3-[(3-胆酰胺基丙基)二甲基铵基]-1-丙磺酸盐,余量为水,ph=8.0。其配制方法过程同实施例1。
[0038]
对比例1
[0039]
本对比例提供一种成像试剂,其配方组成为100mm tris,800mm nacl,100mm 3,4-二羟基苯甲酸乙酯,0.1wt%3-[(3-胆酰胺基丙基)二甲基铵基]-1-丙磺酸盐,余量为水,ph=8.0。其配制方法过程同实施例1。
[0040]
对比例2
[0041]
本对比例提供一种成像试剂,其配方组成为100mm tris,800mm nacl,100mm 3,4-二羟基苯甲酸,0.1wt%3-[(3-胆酰胺基丙基)二甲基铵基]-1-丙磺酸盐,余量为水,ph=8.0。其配制方法过程同实施例1。
[0042]
对比例3
[0043]
本对比例提供一种成像试剂,其配方组成为100mm tris,800mm nacl,100mm抗坏血酸钠,0.1wt%3-[(3-胆酰胺基丙基)二甲基铵基]-1-丙磺酸盐,余量为水,ph=8.0。其配制方法过程同实施例1。
[0044]
对比例4
[0045]
本对比例提供一种成像试剂,其配方组成为100mm tris,800mm nacl,50mm 3,4-二羟基苯甲酸乙酯,50mm 3,4-二羟基苯甲酸,0.1wt%3-[(3-胆酰胺基丙基)二甲基铵基]-1-丙磺酸盐,余量为水,ph=8.0。其配制方法过程同实施例1。
[0046]
对比例5
[0047]
本对比例提供一种成像试剂,其配方组成为100mm tris,800mm nacl,60mm 3,4-二羟基苯甲酸乙酯,20mm 3,4-二羟基苯甲酸,20mm抗坏血酸钠,0.1wt%3-[(3-胆酰胺基丙基)二甲基铵基]-1-丙磺酸盐,余量为水,ph=8.0。其配制方法过程同实施例1。
[0048]
对比例6
[0049]
本对比例提供一种成像试剂,其配方组成为100mm tris,800mm nacl,20mm 3,4-二羟基苯甲酸乙酯,60mm 3,4-二羟基苯甲酸,20mm抗坏血酸钠,0.1wt%3-[(3-胆酰胺基丙基)二甲基铵基]-1-丙磺酸盐,余量为水,ph=8.0。其配制方法过程同实施例1。
[0050]
试验例
[0051]
试验方法:本发明使用illumina nextseq500测序仪v2.1运行测试,在边合成边测序的技术原理下,对本发明实施例1成像试剂和对比例成像试剂对测序反应过程中荧光信号的影响、以及对测序读长和准确性的影响进行对比试验分析,具体的测试包括150次循环和利用phix基因组的288个小区(title);
[0052]
试验分组:试验分为8组进行,其中第一组采用illumina nextseq500测序仪的配套试剂;第二组采用实施例1提供的成像试剂替换illumina nextseq500测序仪配套试剂中的成像试剂,其他试剂采用illumina nextseq500测序仪配套试剂;第三组采用对比例1提供的成像试剂替换illumina nextseq500测序仪配套试剂中的成像试剂,其他试剂采用illumina nextseq500测序仪配套试剂;第四组采用对比例2提供的成像试剂替换illumina nextseq500测序仪配套试剂中的成像试剂,其他试剂采用illumina nextseq500测序仪配套试剂;第五组采用对比例3提供的成像试剂替换illumina nextseq500测序仪配套试剂中的成像试剂,其他试剂采用illumina nextseq500测序仪配套试剂;第六组采用对比例4提供的成像试剂替换illumina nextseq500测序仪配套试剂中的成像试剂,其他试剂采用illumina nextseq500测序仪配套试剂;第七组采用对比例5提供的成像试剂替换illumina nextseq500测序仪配套试剂中的成像试剂,其他试剂采用illumina nextseq500测序仪配套试剂;第八组采用对比例6提供的成像试剂替换illumina nextseq500测序仪配套试剂中的成像试剂,其他试剂采用illumina nextseq500测序仪配套试剂。
[0053]
试验结果:
[0054]
1、各组单端循环150次的测序结果如下表1所示:
[0055]
表1
[0056][0057]
2、各组单端循环150次测序过程中荧光强度值变化趋势如图1至图8所示,其中图1显示市售试剂在测序过程中荧光强度变化趋势图;图2显示本发明提供的由3,4-二羟基苯甲酸乙酯、3,4-二羟基苯甲酸和抗坏血酸钠复配组成的成像试剂应用在测序过程中荧光强度变化趋势图;图3显示仅由3,4-二羟基苯甲酸乙酯组成的成像试剂应用在测序过程中荧光强度变化趋势图;图4显示仅由3,4-二羟基苯甲酸组成的成像试剂应用在测序过程中荧光强度变化趋势图;图5显示仅由抗坏血酸钠组成的成像试剂应用在测序过程中荧光强度变化趋势图;图6显示由3,4-二羟基苯甲酸乙酯和3,4-二羟基苯甲酸组成的成像试剂应用在测序过程中荧光强度变化趋势图;图7和图8均显示调整3,4-二羟基苯甲酸乙酯、3,4-二羟基苯甲酸和抗坏血酸钠复配比例组成的成像试剂应用在测序过程中荧光强度变化趋势图。
[0058]
由图1~8和表1所示的对比试验结果可知,本发明采用3,4-二羟基苯甲酸乙酯、3,4-二羟基苯甲酸和抗坏血酸钠复配组成的成像试剂应用在测序反应,在抑制荧光强度衰减方面,能够达到市售illumina nextseq500配套成像试剂同等的效果,在整个测序反应过程中能够维持荧光强度的整体平稳,不出现大幅度的衰减,而且由表1所示的数据也可得知,采用本发明3,4-二羟基苯甲酸乙酯、3,4-二羟基苯甲酸和抗坏血酸钠复配的成像试剂在定相值、q30和错误率等数据方面达到市售产品同等的水平,能够替代市售产品。
[0059]
单独的3,4-二羟基苯甲酸乙酯、3,4-二羟基苯甲酸作为成像试剂应用在测序反应,不能抑制荧光强度的衰减,测序过程中出现大量的定相错误,q30低于30,测序的错误率超过40,不能作为测序反应的成像试剂;单独的抗坏血酸、或者3,4-二羟基苯甲酸乙酯和3,4-二羟基苯甲酸复配组成的成像试剂,虽然相比3,4-二羟基苯甲酸乙酯、3,4-二羟基苯甲酸,作为成像试剂应用在测序反应,荧光强度衰减幅度有所降低,但是仍然不能在整个测序反应过程中维持荧光强度的整体平稳,表1所示的数据也显示单独的抗坏血酸、或者3,4-二羟基苯甲酸乙酯和3,4-二羟基苯甲酸复配组成的成像试剂的定相值、q30和错误率等方面
均不能达到本发明成像试剂的水平,由此可见3,4-二羟基苯甲酸乙酯、3,4-二羟基苯甲酸和抗坏血酸钠复配使用能够产生协同增效作用,作为成像试剂应用在测序反应中能够抑制荧光损伤,提高测序准确性。
[0060]
最后应说明的是:以上实施例仅用以说明本发明的技术方案,而非对其限制;尽管参照前述实施例对本发明进行了详细的说明,本领域的普通技术人员应当理解:其依然可以对前述各实施例所记载的技术方案进行修改,或者对其中部分技术特征进行等同替换;而这些修改或者替换,并不使相应技术方案的本质脱离本发明各实施例技术方案的精神和范围。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1