一种快速检测大肠杆菌O157:H7的石墨烯量子点免疫层析试纸条的制作方法
本发明涉及一种检测大肠杆菌o157:h7的试纸条。
背景技术:
目前食品工业的微生物污染问题是普遍性问题,特别是致病菌污染造成的急性中毒事件,对食品安全造成巨大威胁。如何快速准确的检测食品中的致病菌一直是一个难题,所以研发快速的微生物检测方法迫在眉睫。目前常用的用胶体金标记抗体检测微生物的快速检测的方法具有一定代表性,但是这种方法也局限性,如灵敏度较低,需要对样品进行培养才能检测到样品中的待测物,并且胶体金含有金元素,对环境具有一定的污染,需要对检测试剂进行一定的回收。
石墨烯量子点(简称gqds)是一种新型的准零维结构的纳米材料。作为石墨烯家族的新成员,gqds不同于常规碳材料,兼具了量子点的独特光学性质和石墨烯的特殊结构,gqds具有良好的水溶性(其粒径约为10nm,厚度为0.5nm~1nm),表面含有丰富的羟基、羰基、羧基等基团,其元素组成主要为碳,不含高毒性金属元素,无细胞毒性。同时,gqds具有更高的光稳定性和耐光漂白性,带隙宽度范围可调,荧光波长范围满足了各种技术对材料能隙和特征波长的要求。对gqds表面进行修饰能够在一定程度上改变其荧光性能、生物相容性以及电化学特性。
利用石墨烯量子点以上特性,并将其应用于卫生检验检测领域,如直接应用于重金属、农药残留检测或构建荧光探针应用于重金属、农药残留检测、微生物检测,开发出具有一定灵敏度和选择性的卫生检验检测新方法,是顺应新材料发展应用的潮流,符合“健康中国2030”战略,为地区的人民健康和经济发展保驾护航。
技术实现要素:
本发明是要解决现有的用胶体金标记抗体检测微生物的快速检测的方法灵敏度较低,需要对样品进行培养,胶体金含有金元素,对环境有污染,需要对检测试剂进行回收的技术问题,而提供一种快速检测大肠杆菌o157:h7的石墨烯量子点免疫层析试纸条。
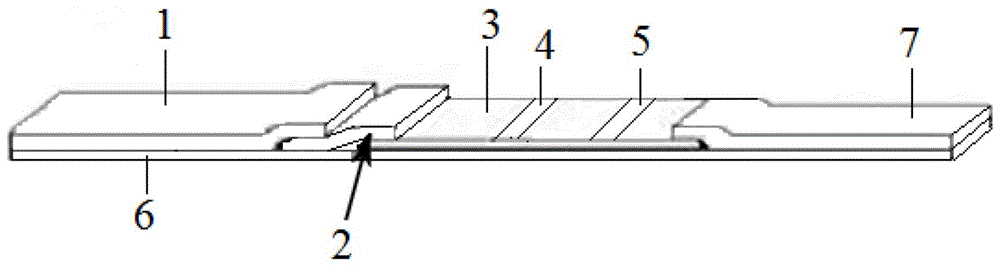
本发明的快速检测大肠杆菌o157:h7的石墨烯量子点免疫层析试纸条是由样品垫1、量子点标结合垫2、包被抗体的硝酸素纤维膜3、检测线t线4;质控线c线5、底板6和吸水纸7组成;所述的样品垫1、量子点标结合垫2、包被抗体的硝酸素纤维膜3和吸水纸7依次粘贴在底板6上;
所述的量子点标结合垫2的制备方法为:
一、石墨烯量子点制备:
1、使用pan基碳纤维作为碳源,经过500℃~550℃高温处理1h~1.5h除掉pan基碳纤维表面的上浆剂,然后用不锈钢夹子固定78束~80束除掉pan基碳纤维表面上浆剂的碳纤维作为阳极;
2、在恒定20v~25v的电压下,1mol/l的碳酸铵水溶液作为电解液,钛网作为阴极,进行电化学反应12h~13h;
此步骤中的现象为:随着电化学氧化剥离过程的进行,pan基碳纤维的长度逐渐减少,电解液的颜色由无色变为金黄色(10s),黄褐色(20s),最后变为完全的黑色(1h后)。由于电解过程中伴随电解质的分解,产生大量气泡,并带有刺激性的氨气气味,电解电流由初始的7.45a降低到1.65a;
3、将步骤2中经过电化学反应后的电解液在100℃加热分解4h~4.5h除去电解质中的碳酸铵;
4、使用0.1μm的滤膜抽滤,使用透析袋将滤液透析三天,得到gqds溶液;
二、向1ml的步骤一制备的gqds溶液中依次加入浓度为100mg/ml的1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐水溶液和100mg/ml的n-羟基琥珀酰亚胺水溶液各5μl,室温静置2h~2.5h,加入10μg大肠杆菌o157:h7菌壁蛋白单克隆抗体,室温静置4h,在4℃离心浓缩,弃上清液,加入400μl的重悬液混合均匀,均匀喷涂于结合垫上,喷涂浓度为10μl/cm2,37℃干燥,通风,得到量子点标结合垫2;
所述的重悬液按质量分数组成为:3%的蛋白保护剂海藻糖、0.5%的牛血清白蛋白、1%的稳定剂peg20000、1%的助悬剂pvp,其余为水;
所述的包被抗体的硝酸素纤维膜3的制备方法为:将包被液包被在硝酸素纤维膜上,包被量为1μl/cm,37℃干燥30min,得到包被抗体的硝酸素纤维膜3;
所述的包被液为将大肠杆菌o157:h7菌壁蛋白单克隆抗体溶解在0.01mol/l磷酸盐缓冲液中组成的混合液,其中大肠杆菌o157:h7菌壁蛋白单克隆抗体的浓度为1mg/ml;
所述的检测线t线4和质控线c线5的制备方法为:将大肠杆菌o157:h7活菌单克隆抗体用浓度为0.01mol/l的pbs溶液稀释到0.8mg/ml,二抗稀释到0.2mg/ml,混匀,摇匀,静置,取100μl点样在硝酸素纤维膜3分别为检测线和质控线,在37℃干燥。
本发明的快速检测大肠杆菌o157:h7的石墨烯量子点免疫层析试纸条的使用方法如下:
(1)样品的预处理:无菌吸取25ml液体样本或25g固体样本,加入到225ml的生理盐水中,以接种1ml10cfu/ml和100cfu/ml出血性大肠杆菌o157:h7为阳性对照,以生理盐水为空白对照;
(2)试纸条检测:吸取75μl样品、阳性对照液、生理盐水,加入到样品垫1上进行检测,反应15min后,先肉眼观察试纸条,再将试纸条放入荧光层析试纸条检测仪中的检测窗口,使用荧光层析检测仪进行读值,并判定结果;
(3)结果判定:
检测时间为10min,肉眼可见检测灵敏度为100cfu/ml,阳性反应为检测线t线4和质控线c线5位置层析试纸条检测仪皆出现肉眼可见的黑色条带(如图3所示);阴性反应只在质控线c线5出现黑色条带(如图2所示)。
荧光检测灵敏度为10cfu/ml,阳性反应为在激发波长450nm,检测波长650nm下,荧光检测方法中,结果的判定条件:检测线t线4有荧光信号为阳性,没有信号为阴性。
本发明根据gqds的结构特性,将其替代胶体金应用于标记抗原抗体,并制作免疫层析试纸条用于微生物检测。本发明的快速检测大肠杆菌o157:h7的石墨烯量子点免疫层析试纸条的结构为现有的结构,其特点在于量子点标结合垫2和包被抗体的硝酸素纤维膜3的组成。
本发明采用自上而下的电化学氧化剥离方法制备石墨烯量子点gqds,操作相对简便,对设备及反应条件要求不高,且电化学制备工艺容易重复,易于扩大化生产;所制备的gqds表面含有大量含氧官能团,尺寸均匀,反应活性较高,方便后续进一步的表面修饰与功能化。
本发明采用石墨烯量子点标记蛋白的原理:免疫抗原、抗体均属于蛋白,具有一定的吸附性,石墨烯量子点也具备一定的物理吸附能力,在一定的条件下,石墨烯量子点与蛋白可以结合成具有一定蛋白活性的偶连物,偶连效果与反应条件有关,比如ph,浓度,温度,蛋白活性等。
本发明采用新型纳米材料石墨烯量子点作为突破点,经过表面修饰,连接具有生物活性蛋白-抗体,可以指示抗原抗体的结合反应情况,利用双抗夹心法检测大肠杆菌o157:h7特异性菌壁蛋白,反应时间10min,以此来判断样品中是否存在大肠杆菌o157:h7,检测灵敏度为100cfu/ml(肉眼可见),如采用荧光检测器检测,检测灵敏度为10cfu/ml。具有定量半定量、快速、准确率高、特异性强、操作简便等特点。
本发明阐述了一种快速检测大肠杆菌o157:h7试纸条的制备方法,由于其核心材料石墨烯量子点的理化特性,本发明的石墨烯量子点免疫层析试纸条有以下四个优点:
一、所用的石墨烯量子点主要组成元素为碳元素,不含金属元素,低生物毒性;
二、由于其在微量检测时可以用荧光激发430nm,然后检测发射光650nm,大肠杆菌o157:h7灵敏度在10cfu/ml(荧光检测);
三、在样品中大肠杆菌o157:h7浓度在100cfu/ml时,t线展示出一条肉眼可见的黑色条带,较大程度上提高了微生物检测的灵敏度,且不需要辅助仪器设备既能定性;
四、本发明的试纸条不需要对样品进行增菌培养,大大的缩短了检测时间和检测过程,同时简化了操作过程,与同类方法对比较大程度上提高了微生物检测的灵敏度。
附图说明
图1为具体实施方式一中快速检测大肠杆菌o157:h7的石墨烯量子点免疫层析试纸条的结构示意图;
图2为试验一的快速检测大肠杆菌o157:h7的石墨烯量子点免疫层析试纸条阴性反应时肉眼可见的示意图;
图3为试验一的快速检测大肠杆菌o157:h7的石墨烯量子点免疫层析试纸条阳性反应时肉眼可见的示意图;
图4为试验一的快速检测大肠杆菌o157:h7的石墨烯量子点免疫层析试纸条无效时肉眼可见的示意图。
具体实施方式
具体实施方式一:本实施方式为一种快速检测大肠杆菌o157:h7的石墨烯量子点免疫层析试纸条,如图1所示,具体是由样品垫1、量子点标结合垫2、包被抗体的硝酸素纤维膜3、检测线t线4、质控线c线5、底板6和吸水纸7组成;所述的样品垫1、量子点标结合垫2、包被抗体的硝酸素纤维膜3和吸水纸7依次粘贴在底板6上;
所述的量子点标结合垫2的制备方法为:
一、石墨烯量子点制备:
1、使用pan基碳纤维作为碳源,经过500℃~550℃高温处理1h~1.5h除掉pan基碳纤维表面的上浆剂,然后用不锈钢夹子固定78束~80束除掉pan基碳纤维表面上浆剂的碳纤维作为阳极;
2、在恒定20v~25v的电压下,1mol/l的碳酸铵水溶液作为电解液,钛网作为阴极,进行电化学反应12h~13h;
3、将步骤2中经过电化学反应后的电解液在100℃加热分解4h~4.5h除去电解质中的碳酸铵;
4、使用0.1μm的滤膜抽滤,使用透析袋将滤液透析三天,得到gqds溶液;
二、向1ml的步骤一制备的gqds溶液中依次加入浓度为100mg/ml的1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐水溶液和100mg/ml的n-羟基琥珀酰亚胺水溶液各5μl,室温静置2h~2.5h,加入10μg大肠杆菌o157:h7菌壁蛋白单克隆抗体,室温静置4h,在4℃离心浓缩,弃上清液,加入400μl的重悬液混合均匀,均匀喷涂于结合垫上,喷涂浓度为10μl/cm2,37℃干燥,通风,得到量子点标结合垫2;
所述的重悬液按质量分数组成为:3%的蛋白保护剂海藻糖、0.5%的牛血清白蛋白、1%的稳定剂peg20000、1%的助悬剂pvp,其余为水;
所述的包被抗体的硝酸素纤维膜3的制备方法为:将包被液包被在硝酸素纤维膜上,包被量为1μl/cm,37℃干燥30min,得到包被抗体的硝酸素纤维膜3;
所述的包被液为将大肠杆菌o157:h7菌壁蛋白单克隆抗体溶解在0.01mol/l磷酸盐缓冲液中组成的混合液,其中大肠杆菌o157:h7菌壁蛋白单克隆抗体的浓度为1mg/ml;
所述的检测线t线4和质控线c线5的制备方法为:将大肠杆菌o157:h7活菌单克隆抗体用浓度为0.01mol/l的pbs溶液稀释到0.8mg/ml,二抗稀释到0.2mg/ml,混匀,摇匀,静置,取100μl点样在硝酸素纤维膜3分别为检测线和质控线,在37℃干燥。
具体实施方式二:本实施方式与具体实施方式一不同的是:所述的石墨烯量子点制备中的1、使用pan基碳纤维作为碳源,经过500℃高温处理1h除掉pan基碳纤维表面的上浆剂,然后用不锈钢夹子固定78束除掉pan基碳纤维表面上浆剂的碳纤维作为阳极。其他与具体实施方式一相同。
具体实施方式三:本实施方式与具体实施方式一或二不同的是:石墨烯量子点制备中的2、在恒定20v的电压下,1mol/l的碳酸铵水溶液作为电解液,钛网作为阴极,进行电化学反应12h。其他与具体实施方式一或二相同。
具体实施方式四:本实施方式与具体实施方式一至三之一不同的是:石墨烯量子点制备中的3、将步骤2中经过电化学反应后的电解液在100℃加热分解4h除去电解质中的碳酸铵。其他与具体实施方式一至三之一相同。
具体实施方式五:本实施方式与具体实施方式四不同的是:石墨烯量子点制备中的4张所述的透析袋的截留率为2000da~8000da。其他与具体实施方式四相同。
用以下试验对本发明进行验证:
试验一:本试验为一种快速检测大肠杆菌o157:h7的石墨烯量子点免疫层析试纸条,如图1所示,具体是由样品垫1、量子点标结合垫2、包被抗体的硝酸素纤维膜3、检测线t线4、质控线c线5、底板6和吸水纸7组成;所述的样品垫1、量子点标结合垫2、包被抗体的硝酸素纤维膜3和吸水纸7依次粘贴在底板6上;
所述的量子点标结合垫2的制备方法为:
一、石墨烯量子点制备:
1、使用pan基碳纤维作为碳源,经过500℃高温处理1h除掉pan基碳纤维表面的上浆剂,然后用不锈钢夹子固定78束除掉pan基碳纤维表面上浆剂的碳纤维作为阳极;
2、在恒定20v的电压下,1mol/l的碳酸铵水溶液作为电解液,钛网作为阴极,进行电化学反应12h;
3、将步骤2中经过电化学反应后的电解液在100℃加热分解4h除去电解质中的碳酸铵;
4、使用0.1μm的滤膜抽滤,使用透析袋将滤液透析三天,得到gqds溶液;
二、向1ml的步骤一制备的gqds溶液中依次加入浓度为100mg/ml的1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐水溶液和100mg/ml的n-羟基琥珀酰亚胺水溶液各5μl,室温静置2h,加入10μg大肠杆菌o157:h7菌壁蛋白单克隆抗体,室温静置4h,在4℃离心浓缩,弃上清液,加入400μl的重悬液混合均匀,均匀喷涂于结合垫上,喷涂浓度为10μl/cm2,37℃干燥,通风,得到量子点标结合垫2;
所述的重悬液按质量分数组成为:3%的蛋白保护剂海藻糖、0.5%的牛血清白蛋白、1%的稳定剂peg20000、1%的助悬剂pvp,其余为水;
所述的包被抗体的硝酸素纤维膜3的制备方法为:将包被液包被在硝酸素纤维膜上,包被量为1μl/cm,37℃干燥30min,得到包被抗体的硝酸素纤维膜3;
所述的包被液为将大肠杆菌o157:h7菌壁蛋白单克隆抗体溶解在0.01mol/l磷酸盐缓冲液中组成的混合液,其中大肠杆菌o157:h7菌壁蛋白单克隆抗体的浓度为1mg/ml;
所述的检测线t线4和质控线c线5的制备方法为:将大肠杆菌o157:h7活菌单克隆抗体用浓度为0.01mol/l的pbs溶液稀释到0.8mg/ml,二抗稀释到0.2mg/ml,混匀,摇匀,静置,取100μl点样在硝酸素纤维膜3分别为检测线4和质控线5,在37℃干燥。
试纸条的组装:首先将样品垫1和量子点标结合垫2经剪裁后通过浸泡处理液进行水化和封闭处理,浸泡30min,在37℃烘干2h,处理液为含有质量浓度为0.3%的吐温20、2%的海藻糖、10%的蔗糖,其余为ph值为7.2浓度为0.01mol/l的pbs溶液;
将30cm×2.4cm的nc膜3、30cm×2cm吸水纸7(国产特种纸)、30cm×0.8cm的量子点标结合垫2(国产聚酯纤维纸)、30.0cm×2.0cm样品垫1(国产玻璃纤维纸)按图1方式依次粘贴在pvc胶板6(国产带胶所料版)上,即成石墨烯量子点标记抗体试纸条。
本试验的快速检测大肠杆菌o157:h7的石墨烯量子点免疫层析试纸条的使用方法如下:
(1)样品的预处理:无菌吸取25ml液体样本或25g固体样本,加入到225ml的生理盐水中,以接种1ml样品终浓度为10cfu/ml和100cfu/ml出血性大肠杆菌o157:h7为阳性对照,以生理盐水为空白对照;
(2)试纸条检测:吸取75μl样品、阳性对照液、生理盐水,加入到样品垫1上进行检测,反应15min后,先肉眼观察试纸条,再将试纸条放入荧光层析试纸条检测仪中的检测窗口,使用荧光层析检测仪进行读值,并判定结果;
(3)结果判定:
检测时间为10min,肉眼可见检测灵敏度为100cfu/ml,阳性反应为检测线t线4和质控线c线5位置层析试纸条检测仪皆出现肉眼可见的黑色条带(如图3所示);阴性反应只在质控线c线5出现黑色条带(如图2所示);只在检测线t线4出现黑色条带为无效。
荧光检测灵敏度为10cfu/ml,阳性反应为在激发波长450nm,检测波长650nm下,荧光检测方法中,结果的判定条件:检测线t线4有荧光信号为阳性,没有信号为阴性。
本试验根据gqds的结构特性,将其替代胶体金应用于标记抗原抗体,并制作免疫层析试纸条用于微生物检测。本发明的快速检测大肠杆菌o157:h7的石墨烯量子点免疫层析试纸条的结构为现有的结构,其特点在于量子点标结合垫2和包被抗体的硝酸素纤维膜3的组成。
本试验采用自上而下的电化学氧化剥离方法制备石墨烯量子点gqds,操作相对简便,对设备及反应条件要求不高,且电化学制备工艺容易重复,易于扩大化生产;所制备的gqds表面含有大量含氧官能团,尺寸均匀,反应活性较高,方便后续进一步的表面修饰与功能化。
本试验采用石墨烯量子点标记蛋白的原理:免疫抗原、抗体均属于蛋白,具有一定的吸附性,石墨烯量子点也具备一定的物理吸附能力,在一定的条件下,石墨烯量子点与蛋白可以结合成具有一定蛋白活性的偶连物,偶连效果与反应条件有关,比如ph,浓度,温度,蛋白活性等。
本试验采用新型纳米材料石墨烯量子点作为突破点,经过表面修饰,连接具有生物活性蛋白-抗体,可以指示抗原抗体的结合反应情况,利用双抗夹心法检测大肠杆菌o157:h7特异性菌壁蛋白,反应时间10min,以此来判断样品中是否存在大肠杆菌o157:h7,检测灵敏度为100cfu/ml(肉眼可见),如采用荧光检测器检测,检测灵敏度为10cfu/ml。具有定量半定量、快速、准确率高、特异性强、操作简便等特点。
本试验阐述了一种快速检测大肠杆菌o157:h7试纸条的制备方法,由于其核心材料石墨烯量子点的理化特性,本发明的石墨烯量子点免疫层析试纸条有以下四个优点:
一、所用的石墨烯量子点主要组成元素为碳元素,不含金属元素,低生物毒性;
二、由于其在微量检测时可以用荧光激发430nm,然后检测发射光650nm,大肠杆菌o157:h7灵敏度在10cfu/ml(荧光检测);
三、在样品中大肠杆菌o157:h7浓度在100cfu/ml时,t线展示出一条肉眼可见的黑色条带,较大程度上提高了微生物检测的灵敏度,且不需要辅助仪器设备既能定性;
四、本试验的试纸条不需要对样品进行增菌培养,大大的缩短了检测时间和检测过程,同时简化了操作过程,与同类方法对比较大程度上提高了微生物检测的灵敏度。
- 还没有人留言评论。精彩留言会获得点赞!