用于快速筛查膀胱癌标志物的生物芯片及制备方法和应用
1.本发明涉及分析检测领域,具体涉及一种用于快速筛查膀胱癌标志物的生物芯片及制备方法和应用。
背景技术:
2.膀胱癌是泌尿系统中最常见的恶性肿瘤,发病率高,且术后易复发。目前膀胱癌的临床诊断主要是膀胱镜检查,但膀胱镜检查侵入性高,分辨率低,检查过程易引起尿道疼痛和血尿,因此很难用于膀胱癌的早期筛查。作为储尿器官,膀胱的早期癌变会对患者的尿液成分产生直接影响。目前,研究人员已经在尿液中发现了多种类型的膀胱癌生物标志物,包括dna、rna、蛋白质和肿瘤细胞。然而,这些标志物在尿液中的浓度极低,且尿液成分复杂易产生干扰信号,极大地限制了检测方法的选择性和灵敏度。鉴于此,开发一种高性能的生物传感器来实现高灵敏、选择性的检测膀胱癌患者尿液中的微量生物标志物,对于膀胱癌的早期筛查、术后监测和个人健康管理具有重大意义。
3.目前膀胱癌的临床诊断技术主要包括膀胱镜、尿脱落细胞学、影像学检查等。目前,膀胱镜检查是膀胱癌临床诊断的金标准方法,但是这种技术受癌变体积、位置以及环境限制而导致分辨率较低,并且膀胱癌检查侵入性强,患者会出现尿道疼痛和血尿等问题,不适合用于膀胱癌的早期筛查和诊断。尿脱落细胞学检查、影像学检查虽然不具有侵入性,但是诊断效率低,也不适合用于膀胱癌的早期筛查和诊断。因此,目前在膀胱癌疾病的快速诊断、早期筛查方面依然是一个严峻的挑战。
4.膀胱癌主要分为非肌层浸润型膀胱癌和肌层浸润型膀胱癌。约70%的患者早期初诊时为非肌层浸润型膀胱癌,治疗效果好。肌层浸润性膀胱癌,需要手术切除大部分的膀胱组织,治疗效果差且术后易复发,因此膀胱癌的早期筛查至关重要。目前,已经有多种类型的膀胱癌生物标志物(dna、rna、蛋白质和肿瘤细胞)被用于膀胱癌的早期筛查。其中,microrna(mirnas)作为dna转录后调控基因表达的非编码rna,在细胞的转移、发育、增殖、凋亡和癌变过程中发挥着至关重要的作用。膀胱组织癌变时,mirna会通过膀胱癌细胞的代谢排出到尿液中。因此,开发一款高灵敏度的生物传感器来定量检测人体尿液中的mirna是实现膀胱癌早期无创诊断的有效策略,对于膀胱癌的早期筛查和术后监测至关重要。
技术实现要素:
5.针对现有技术的不足,本发明的目的是提供一种用于快速筛查膀胱癌标志物的生物芯片及制备方法和应用。
6.为实现上述目的,本发明提供的技术方案如下:
7.第一方面,本发明提供一种用于快速筛查膀胱癌标志物的生物芯片的制备方法,其特征在于:采用磁控溅射法在硅衬底上制备了铟镓锌氧化物即igzo薄膜,将制备得到的igzo传感区域进行选择性修饰,得到探针dna修饰的igzo传感器件,包含如下步骤:
8.s1、金属源漏电极制备
9.(s1.1)选取具有300nm氧化硅层的p型硅片作为衬底,在其表面旋涂一层正性光刻胶az521,在110℃加热板上加热5min,然后使用紫外光刻机在掩膜版图形的保护下刻出电极沟道,在zx
‑
238显影液中显影50s,用去离子水冲洗硅片去除残留的显影液。
10.(s1.2)使用热蒸镀仪蒸发生长cr/au电极,其中,cr层在下,厚度为10nm,au层在上,厚度为50nm。金属cr能够增加硅片氧化层与金属au之间的结合力,将沉积完电极的硅片泡在丙酮溶液中来剥离光刻胶,最后使用去离子水冲洗并用氮气吹干,获得源漏电极沉积的硅片。
11.s2、igzo沟道层制备
12.使用陶瓷靶(in2o3:ga2o3:zno=1:1:1)通过磁控溅射法在图案化的电极中间沉积igzo沟道层(15
‑
20nm),溅射过程中气体氛围为氩气,气体总压强为0.65pa,射频电源功率为50w,衬底温度为150℃,溅射时间为20min,最后得到igzo晶体管器件。
13.s3、器件电极钝化和传感区域曝光处理
14.(s3.1)在制备好的igzo晶体管器件表面旋涂聚甲基丙烯酸甲酯(pmma)来钝化源漏电极。旋涂参数:预旋涂转速为500rpm,旋涂时间为5s,正式旋涂转速为4000rpm,旋涂时间为40s,每次旋涂完的器件置于150℃加热板上热烘5min,达到固化pmma的目的。
15.(s3.2)由于旋涂过程中igzo沟道层也被pmma覆盖,因此采用电子束曝光系统(ebl)对器件的传感区域进行图形化曝光,从而暴露出igzo传感区域。曝光结束后采用体积比为1:3的4
–
甲基
–2–
戊酮(mibk):异丙醇(ipa)混合溶液进行显影,使得曝光区域的pmma溶解,而未曝光区域的pmma不溶解,从而暴露出传感区域,而其他区域仍覆盖pmma实现钝化处理。
16.s4、储液槽制备
17.以质量比为10:1称取sylgard 184硅氧烷的预聚物和固化剂,将两者充分混合并搅拌均匀,然后置于真空箱中抽真空去除混合物中的气泡直至透明澄清。将混合物倒入预制的模具中成型,并将模具置于60℃加热板上加热1h,加快聚二甲基硅氧烷(pdms)槽的凝固,将凝固后的pdms槽进行脱模切割处理,从而制备出符合测试要求的储液槽。
18.s5、储液槽和器件的组装
19.将储液槽用氧等离子体处理3min,使得表面带含氧官能团。之后将晶体管器件和储液槽进行键合,含氧官能团可以保证储液槽与器件紧密接触,从而制备得到溶液栅igzo晶体管器件。
20.s6、igzo传感区域的选择性修饰
21.(s6.1)将暴露出传感区域的器件浸润到体积分数为5%的3
–
氨丙基三乙氧基硅烷(aptes)乙醇溶液中,在摇床中孵育1h(转速180r/min,温度25℃)。由于igzo的表面含有羟基基团(
–
oh),aptes会发生硅烷化结合羟基基团生成硅醇缩合物,从而使得igzo的表面含有氨基基团(
–
nh2)。
22.(s6.2)孵育结束后取出器件并用乙醇冲洗,去除残余的aptes,然后将器件置于110℃烘箱中30min,使得igzo表面的硅烷化更加牢固。
23.(s6.3)将表面硅烷化的器件浸润到1mg/ml 4
‑
(n
‑
马来酰亚胺甲基)环己烷
‑1‑
羧酸磺酸基琥珀酰亚胺酯钠盐(sulfo
–
smcc)的pb缓冲液(0.01mol/l,ph=7.4)中,并在转速为180r/min,温度为25℃的摇床中孵育2h。孵育结束后将器件取出,用pb缓冲液洗掉残余的
sulfo
–
smcc,氮气吹干。sulfo
–
smcc在ph=7.4的条件下,能够与器件表面的氨基基团(
–
nh2)反应形成稳定的酰胺键,同时另外一端也能与带巯基的dna反应,形成稳定的硫醚键。
24.(s6.4)在修饰sulfo
–
smcc的igzo传感区域滴加一定浓度的探针dna溶液(cdna),将器件置于4℃冰箱中孵育12h,孵育结束后,用pb缓冲液冲洗掉未结合的探针分子,并用氮气吹干。在孵育过程中sulfo
–
smcc和5’端修饰巯基(
–
sh)的cdna之间形成稳定的硫醚键,从而将探针成功的固定在igzo表面,得到探针dna修饰的igzo传感器件(cdna/igzo tft)。
25.第二方面,本发明提供一种纳米生物芯片,其特征在于:采用上述的方法制得而成。
26.第三方面,本发明提供一种如上述的纳米生物芯片在快速筛查膀胱癌病人尿液中核酸标志物中的应用。
27.作为优选方案,将所得的纳米生物芯片用于筛查尿液中核酸标志物的检测,用一定体积(一系列浓度梯度为10
–
16
~10
–9m)的已知浓度的rna溶液与cdna探针修饰的igzo传感器进行孵育,孵育过程中,igzo表面固定的dna探针可以依据碱基互补配对原则快速结合rna,这一结合过程会影响igzo表面的电荷数量,从而影响igzo的载流子密度,进而引起传感器电学信号的变化。igzo为n型半导体,其内部多数载流子为电子,在传感过程中,探针cdna带负电,因而会降低igzo沟道的载流子浓度,使得沟道电流i
d
减小。在检测目标物rna时,由于检测的rna也带负电,在孵育过程中,碱基互补配对的单链dna和rna发生杂交,导致igzo薄膜表面负电量增加,进一步降低沟道的载流子浓度,沟道电流i
d
进一步减小。通过测试已知浓度梯度的rna溶液,得到一系列rna浓度和电学信号对应变化的标准曲线,实现将浓度信号转化为电学信号的目的。在测试膀胱癌病人样本时,可以直接通过观察电学信号的变化来对应此标准曲线,从而计算得出膀胱癌患者尿液样本中的rna标志物含量。
28.本发明的优点和有益效果如下:
29.1、本发明中所构建的igzo传感器件具有良好的电学特性和稳定性,具有易于集成和微型化的特点。
30.2、本发明中构建的尿液中膀胱癌标志物检测方法,是基于纳米生物芯片优异的传感性能,具有非常高的灵敏度、高的信号响应速度以良好的特异性和选择性,检测的准确性高并且快速。
31.3、本发明中所构建的尿液中膀胱癌标志物检测方法,能够实现未知尿液样本的快速检测,适用于膀胱癌的早期筛查。
附图说明
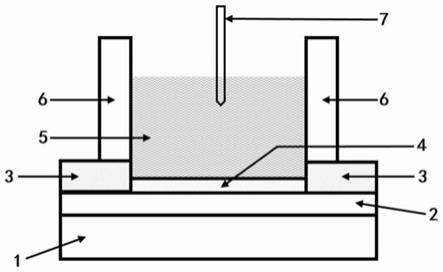
32.图1为本发明实施例1制得的纳米生物芯片构造图。
33.图2为本发明实施例1制得的纳米生物芯片的制备流程示意图。
34.图3为本发明实施例2纳米生物芯片检测核酸标志物的原理示意图。
35.图4为本发明实施例2纳米生物芯片对核酸标志物的检测结果图。
36.图5为本发明应用例1中纳米生物芯片对实际尿液样本测试结果图。
37.图中:1、p型硅片,2、硅片表面的二氧化硅层(300nm),3、10nm cr/50nmau的金属源漏电极,4、有源层铟镓锌氧化物沟道(igzo),5、0.01mol/l的pb缓冲液,6、pdms储液槽,7、ag/agcl参比电极。
具体实施方式
38.下面将结合实施例1
‑
3及附图1
‑
5对本发明的技术方案做进一步详细的阐述。
39.实施例1:纳米生物芯片的制备
40.s1、金属源漏电极制备
41.s1.1)选取具有300nm氧化硅层的p型硅片作为衬底,在其表面旋涂一层正性光刻胶az521,在110℃加热板上加热5min,然后使用紫外光刻机在掩膜版图形的保护下刻出电极沟道,在zx
‑
238显影液中显影50s,用去离子水冲洗硅片去除残留的显影液。
42.s1.2)使用热蒸镀仪蒸发生长cr/au电极,其中,cr层在下,厚度为10nm,au层在上,厚度为50nm。金属cr能够增加硅片氧化层与金属au之间的结合力,将沉积完电极的硅片泡在丙酮溶液中来剥离光刻胶,最后使用去离子水冲洗并用氮气吹干,获得源漏电极沉积的硅片。
43.s2、igzo沟道层制备
44.使用陶瓷靶(in2o3:ga2o3:zno=1:1:1)通过磁控溅射法在图案化的电极中间沉积igzo沟道层(15
‑
20nm),溅射过程中气体氛围为氩气,气体总压强为0.65pa,射频电源功率为50w,衬底温度为150℃,溅射时间为20min,最后得到igzo晶体管器件。
45.s3、器件电极钝化和传感区域曝光处理
46.s3.1)在制备好的igzo晶体管器件表面旋涂聚甲基丙烯酸甲酯(pmma)来钝化源漏电极。旋涂参数:预旋涂转速为500rpm,旋涂时间为5s,正式旋涂转速为4000rpm,旋涂时间为40s,每次旋涂完的器件置于150℃加热板上热烘5min,达到固化pmma的目的。
47.s3.2)由于旋涂过程中igzo沟道层也被pmma覆盖,因此采用电子束曝光系统(ebl)对器件的传感区域进行图形化曝光,从而暴露出igzo传感区域。曝光结束后采用体积比为1:3的4
–
甲基
–2–
戊酮(mibk):异丙醇(ipa)混合溶液进行显影,使得曝光区域的pmma溶解,而未曝光区域的pmma不溶解,从而暴露出传感区域,而其他区域仍覆盖pmma实现钝化处理。
48.s4、储液槽制备
49.以质量比为10:1称取sylgard 184硅氧烷的预聚物和固化剂,将两者充分混合并搅拌均匀,然后置于真空箱中抽真空去除混合物中的气泡直至透明澄清。将混合物倒入预制的模具中成型,并将模具置于60℃加热板上加热1h,加快聚二甲基硅氧烷(pdms)槽的凝固,将凝固后的pdms槽进行脱模切割处理,从而制备出符合测试要求的储液槽。
50.s5、储液槽和器件的组装
51.将储液槽用氧等离子体处理3min,使得表面带含氧官能团。之后将晶体管器件和储液槽进行键合,含氧官能团可以保证储液槽与器件紧密接触,从而制备得到溶液栅igzo晶体管器件。
52.s6、igzo传感区域的选择性修饰
53.s6.1)将暴露出传感区域的器件浸润到体积分数为5%的3
–
氨丙基三乙氧基硅烷(aptes)乙醇溶液中,在摇床中孵育1h(转速180r/min,温度25℃)。由于igzo的表面含有羟基基团(
–
oh),aptes会发生硅烷化结合羟基基团生成硅醇缩合物,从而使得igzo的表面含有氨基基团(
–
nh2)。
54.s6.2)孵育结束后取出器件并用乙醇冲洗,去除残余的aptes,然后将器件置于110℃烘箱中30min,使得igzo表面的硅烷化更加牢固。
55.s6.3)将表面硅烷化的器件浸润到1mg/ml 4
‑
(n
‑
马来酰亚胺甲基)环己烷
‑1‑
羧酸磺酸基琥珀酰亚胺酯钠盐(sulfo
–
smcc)的pb缓冲液(0.01mol/l,ph=7.4)中,并在转速为180r/min,温度为25℃的摇床中孵育2h。孵育结束后将器件取出,用pb缓冲液洗掉残余的sulfo
–
smcc,氮气吹干。sulfo
–
smcc在ph=7.4的条件下,能够与器件表面的氨基基团(
–
nh2)反应形成稳定的酰胺键,同时另外一端也能与带巯基的dna反应,形成稳定的硫醚键。
56.s6.4)在修饰sulfo
–
smcc的igzo传感区域滴加一定浓度的探针dna溶液(cdna),将器件置于4℃冰箱中孵育12h,孵育结束后,用pb缓冲液冲洗掉未结合的探针分子,并用氮气吹干。在孵育过程中sulfo
–
smcc和5’端修饰巯基(
–
sh)的cdna之间形成稳定的硫醚键,从而将探针成功的固定在igzo表面,得到探针dna修饰的igzo传感器件(cdna/igzo tft)。
57.实施例2:cdna/igzo tft器件标准曲线的测定
58.将实施例1中制备的cdna/igzo tft器件对不同浓度梯度的rna溶液进行测试,保持源漏电极电压v
d
不变(v
d
=0.1v),通过改变栅极电压v
g
来获得器件对不同浓度梯度rna溶液电信号变化曲线。通过连续的改变rna溶液的浓度梯度,测得了器件对一系列浓度mirna的电信号变化曲线。从图4所示,随着rna浓度的不断增加,在cdna/igzo tft器件的表面将结合越来越多的rna分子,此时带负电的rna链施加的负栅效应就越来越大,导致器件沟道内载流子浓度逐渐降低,电流随之逐步降低。以电流变化δi/i
o
作为器件对不同浓度mirna的响应变化,我们获得了器件响应变化与mirna浓度之间的对应关系图,可以看出cdna/igzo tft器件对mirna的线性检测范围为10
–
16
~10
–
12
m。由cdna/igzo tft器件与mirna浓度之间的线性对应关系图,可以评估未知尿液样本中mirna的浓度。
59.实施例3:病人尿液中核酸标志物mirna的提取
60.1、取病人尿液样本0.5ml,加入1.5ml裂解缓冲液(lysis buffer),用移液枪吹打尿液样本以加快裂解尿液样本中的细胞。(lysis buffer和尿液样本的体积比始终保持3:1)
61.2、将样品剧烈震荡混匀,在15
‑
30℃下孵育5min以使核蛋白体完全分解。
62.3、在混合溶液中加入0.2ml氯仿,剧烈振荡15s并在室温下放置2min。
63.4、将混合溶液在4℃,12,000rpm下离心10min,样本将分为三层:下层为有机相,中间层和上层为无色的水相,其中rna存在于水相中。
64.5、吸取上清液并转移到新的离心管内,同时加入1.5倍体积的无水乙醇,涡旋均匀。
65.6、精确估计上清液体积,加入等体积的70%乙醇,涡旋使其充分混匀。
66.7、将混合溶液加入到一个吸附柱ra中,12,000rpm离心30
‑
60s,收集滤过物。将滤过物从收集管转移到一个新的离心管中,把吸附柱子放回空的收集管内,再加入剩下的混合物,离心,收集滤过物。合并两次滤过物,计算体积。
67.8、由于滤过物中含有mirna,因此精确估计滤过物体积,加入0.65倍体积的无水乙醇,涡旋使其充分混匀。
68.9、取一套新的mirna吸附柱ma,将上一步的混合物加入吸附柱ma中,并将吸附柱放入收集管内,12,000rpm离心30s,弃掉废液。
69.10、向吸附柱ma中加入700μl的wash solution 1进行漂洗,12,000rpm离心30s,弃掉废液。
70.11、向吸附柱ma中再加入500μl的wash solution 2/3继续漂洗,12,000rpm离心30s,弃掉废液。
71.12、将吸附柱ra放回空的收集管中,13,000rpm离心2min,尽量除去漂洗液,避免漂洗液中残留乙醇影响后续反应。
72.13、取出吸附柱ra,放入到一个rnase free离心管内,根据预期产量在吸附膜中间部位加入30
‑
50μlrnase free water,室温下放置1min,12,000rpm离心1min。
73.14、最终收集rnase free离心管内的溶液即为所提取的mirna目标物溶液。
74.应用例1:病人尿液中核酸标志物mirna
‑
21的检测
75.取膀胱癌患者和健康人的晨尿,根据上述提取mirna的步骤对尿液中的mirna进行提取,将提取完的健康人和膀胱癌病人尿液样本标号并同时稀释到igzo器件的线性工作范围区间内。如图5所示,igzo器件对膀胱癌病人的尿液样本的电学响应显著大于健康人的尿液样本,说明膀胱癌病人尿液样本中的mirna含量远远高于健康人尿液样本中的mirna含量。通过测试3组膀胱癌患者和健康人的尿液样本,结合前期测试的标准曲线,对膀胱癌病人和健康人尿液中的mirna含量进行了计算。如图5所示,膀胱癌患者尿液中的mirna含量明显高于健康人尿液样本中的mirna含量。此外,不同时期的膀胱癌病人尿液样本的mirna含量也不同,说明我们构建的高灵敏、选择性igzo传感器件有极大的潜力应用于临床样本的分期分型。上述研究结果表明我们开发的纳米生物芯片传感技术能够实现非侵入性的快速筛查膀胱癌患者尿液中的核酸标志物,对于实现膀胱癌的早期诊断具有重要作用。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1