免疫球蛋白检测及相关治疗的制作方法
1.本发明涉及用于检测免疫球蛋白m(igm)抗体、免疫球蛋白a(iga)抗体和免疫球蛋白e(ige)抗体的改进方法,以及由致病性抗体和抗体复合物介导的疾病和病症的新疗法。
背景技术:
2.由致病性内源性抗体介导的自身免疫疾病和其它病症提出复杂的治疗挑战。对于患有例如肾脏、肝脏或心脏衰竭的患者的最后选择方案通常是器官移植,但是人白细胞抗原(hla)致敏是器官移植的主要障碍。高度致敏的患者具有高水平的抗hla抗体,这些抗体可能靶向并且显著损害移植的器官。此类抗体的丰度直接影响找到能匹配的供体器官的可能性。例如,许多患有肾功能衰竭的高度致敏的患者将在长期透析中无限期地处于衰弱的疾病状态,这与高成本、低生活质量和增加的死亡率关联。免疫抑制药物可以减少由于急性排斥引起的早期移植物损失,但是它们在解决由于慢性排斥引起的移植物损失方面效果不佳,并且它们会增加严重并发症的风险,例如危及生命的感染和癌症。
3.致病性内源性抗体和免疫复合物也会引起广泛的自身免疫疾病和病症,其中患者具有识别自身抗原的抗体并且这些抗体介导炎症和组织损害。
4.自身免疫疾病和由致病性内源性介导的其它病症的诊断和治疗需要用于检测致病性内源性抗体的灵敏测定和用于减少抗体的有害影响的治疗方法。然而,抗体是复杂的分子并且目前用于检测它们的免疫测定可能不可靠且不够灵敏。用于检测igm抗体(例如抗hla igm抗体)的目前方法改编自用于检测igg抗体的方法(paantjens等人,pulm.med.,2011)。如果在检测igg的方法中疑似存在干扰问题,通常使用还原剂例如二硫苏糖醇(dtt)以破坏igm并且防止igm阻断igg(paantjens等人,pulm.med.,2011)。需要用于检测抗体的改进测定,特别是用于检测igm抗体和除igg之外的其它抗体类别的方法。还需要用于治疗具有致病性抗体的患者的新方法。
5.降解免疫球蛋白g的半胱氨酸蛋白酶imlifidase(ides)是作为肾移植中快速脱敏治疗的目前正在开发的igg内肽酶。imlifidase具有高度特异性并且切割人igg的所有亚类。已经提出imlifidase也切割病理性抗hla igm(zhang等人,2019,am j transplant,2019;19(增刊)3))。
技术实现要素:
6.本发明提供检测样品中的igm抗体、iga抗体或ige抗体的改进方法,包括在允许igg半胱氨酸蛋白酶活性发生的条件下使所述样品与igg半胱氨酸蛋白酶接触,以及使所述样品与适合用于检测igm抗体、iga抗体或ige抗体的试剂接触。
7.在优选的实施方案中,本发明的方法用于检测igm抗体。发明人在实施例中已经表明,igm抗体可以与igg形成免疫复合物,其干扰抗原特异性igm抗体的检测。这些复合物可以由igg半胱氨酸蛋白酶切割,因此使用igg半胱氨酸蛋白酶将对任何用于检测igm抗体的方法提供改进。
8.在某些实施方案中,本发明的方法用于检测iga抗体。已知iga抗体与igg以与igm抗体类似的方式形成免疫复合物。此类复合物可以对任何检测抗原特异性iga抗体的方法造成干扰,因此使用igg半胱氨酸蛋白酶将对任何用于检测iga抗体的方法提供改进,如在实施例中针对igm抗体所证明的那样。
9.在某些实施方案中,本发明的方法用于检测ige抗体。已知ige抗体与igg以与igm抗体类似的方式形成免疫复合物。此类复合物可以对任何检测抗原特异性ige抗体的方法造成干扰,因此使用igg半胱氨酸蛋白酶将对任何用于检测ige抗体的方法提供改进,如在实施例中针对igm抗体所证明的那样。
10.在优选的实施方案中,igg半胱氨酸蛋白酶是ides或idez多肽,例如具有与seq id no:2、4或5至少80%相同,例如至少85%、90%、95%或99%相同的序列的多肽。在实施例中证实,这些多肽对igg具有已确立的特异性,并且有效地根除igg干扰而不影响igm、iga或ige水平。
11.在某些实施方案中,适用于检测igm抗体、iga抗体或ige抗体的试剂是抗igm抗体、抗iga抗体或抗ige抗体。这类抗体易于获得。可以将抗体固定在固体基质,例如珠粒或板上,以帮助处理样品且增加通量。在某些实施方案中,将适用于检测igm抗体、iga抗体或ige抗体的试剂标记,以帮助检测。
12.本发明的方法对于检测针对特定抗原的igm抗体、iga抗体或ige抗体尤其有用。实施例证明由igg半胱氨酸蛋白酶切割的igm-igg免疫复合物可以在靶标特异性抗体的测定中提供假阳性结果。因此,在某些实施方案中,在允许分离与感兴趣的抗原特异性结合的抗体的条件下,将样品与感兴趣的抗原接触。感兴趣的抗原可以是例如人白细胞抗原(hla)、红细胞抗原或药物抗原。
13.本发明的方法对于分析患者样品如血清样品(例如来自已被诊断为需要器官移植的患者或被诊断患有选自表a的疾病的患者)特别有用。
14.本发明还提供了用于实施本发明方法的试剂盒,其包含igg半胱氨酸蛋白酶和用于检测igm抗体、iga抗体或ige抗体的试剂,并且任选地包含感兴趣的抗原,例如人白细胞抗原(hla)、红细胞抗原或药物抗原。
15.本发明还提供了治疗全部或部分由致病性igm抗体、致病性iga抗体或致病性ige抗体介导的疾病或病症的方法,其中该方法包括施用igg半胱氨酸蛋白酶。发明人在实施例中已经证明,igm抗体可以与可以被igg半胱氨酸蛋白酶切割的igg抗体形成免疫复合物。iga抗体和ige抗体可能会与igg抗体形成类似的复合物。预期这些免疫复合物会介导疾病过程,因此igg半胱氨酸蛋白酶将可用于治疗由致病性igm抗体、致病性iga抗体或致病性ige抗体介导的疾病或病症。本发明还提供了igg半胱氨酸蛋白酶,用于在治疗全部或部分由致病性igm抗体、致病性iga抗体或致病性ige抗体介导的疾病或病症的方法中使用。
16.本发明还提供了用于治疗对象中的全部或部分由致病性igg抗体介导的疾病或病症的方法,其中所述对象被确定为表现出抗igg igm抗体、抗igg iga抗体或抗igg ige抗体,其中方法包括施用igg半胱氨酸蛋白酶。发明人在实施例中已经证明,igm抗体可以与可以被igg半胱氨酸蛋白酶切割的igg抗体形成免疫复合物。iga抗体和ige抗体可能会与igg抗体形成类似的复合物。预期这些免疫复合物会扩大致病性igg抗体的效果,因此igg半胱氨酸蛋白酶在治疗具有抗igg igm抗体或抗igg iga抗体的患者时特别有效。在进一步优选
的实施方案中,本发明提供了igg半胱氨酸蛋白酶,用于在治疗对象中的全部或部分由致病性igg抗体介导的疾病或病症的方法中使用,其中所述对象被确定为表现出抗igg igm抗体、抗igg iga抗体或抗igg ige抗体。
17.本发明还提供了用于治疗对象中的全部或部分由igg抗体与igm抗体、iga抗体或ige抗体的复合物介导的疾病或病症的方法,其中方法包括施用igg半胱氨酸蛋白酶。发明人在实施例中已经证明,igm抗体可以与可以被igg半胱氨酸蛋白酶切割的igg抗体形成免疫复合物。iga抗体和ige抗体可能会与igg抗体形成类似的复合物。这些免疫复合物可以介导疾病过程,因此igg半胱氨酸蛋白酶将在治疗由igg抗体与igm抗体、iga抗体或ige抗体的复合物介导的疾病时有效。在进一步优选的实施方案中,本发明提供了igg半胱氨酸蛋白酶,用于在治疗对象中的全部或部分由igg抗体与igm抗体、iga抗体或ige抗体的复合物介导的疾病或病症的方法中使用。
附图说明
18.图1-示出igm及其二硫桥的示意图。
19.图2-与imlifidase孵育后未观察到人igm的切割。
20.图3-使用captureselect igg-ch1亲和介质在血清中成功进行了igg的纯化。
21.图4-imlifidase对hla i+ii抗体(igg,hi)的影响,mfi截止值》3000。
22.图5-hla i+ii抗体(igg,edta)相比于hla i+ii抗体(igm,edta)。
23.图6-在纯血清中以及igg耗尽后对抗hla igm抗体所示的影响的比较。
24.图7-测定的检测限—抗人igm(pe)。
25.图8-imlifidase不消化致敏患者的人igm。
26.图9-a)来自esrd致敏患者的血清样品在imlifidase后24小时相对于给药前(predose)的sab-hla i类和ii类特异性igm的相对强度(mfi)。每个点代表患者血清中的一种sab-hla珠粒。在任一样品中的阳性珠粒截断为500,分析中仅包括阳性珠粒。b)在24小时样品中增加的珠粒。c)在24小时样品中减少的珠粒。作为参考,图中包括来自给药前血清的iggsab-hla。各个hla珠粒通过线连接。各个患者用不同的点和线类型标记。
27.图10-在sds-page凝胶(4-20%)上分析纯化的人igm和igg的消化。将纯化的人igm(a)和igg(b)与宽范围浓度的imlifidase在37℃下孵育2小时。用dtt还原高分子量igm样品(a)并且在sds-page凝胶上分离。将igg样品(b)加热3分钟并且在sds-page凝胶上进行非还原性分离。
28.图11-将来自4名esrd患者的血清样品与高浓度的imlifidase孵育。通过sds-page凝胶(a)和蛋白质印迹(b)分析人igm的消化。
29.图12-igg耗尽之前和之后的血清样品的sds-page评估。
30.a)包括患者02-922、患者02-923、患者02-925和患者02-926的样品。
31.b)包括患者02-927、患者02-928和患者02-929的样品。
32.图13-分析来自esrd致敏患者的给药前和imlifidase后24小时的igg耗尽血清样品的sab-hla i类和ii类(igm)。图中的n是该特定患者的给药前血清中达到1000mfi阈值的单抗原珠的数量(来自对纯血清中igm的分析[图4]),分析中仅包括阳性珠粒。a)患者02-922。b)患者02-923。c)患者02-925。d)患者02-926。e)患者02-927。f)患者02-928。g)患者
02-929。
[0033]
图14-将一名esrd致敏患者(02-927)的给药前和imlifidase后24小时的血清样品与用6μg/ml和30μg/ml imlifidase孵育1小时的体外处理进行比较。分析血清样品的sab-hla i类和ii类(igg和igm)。
[0034]
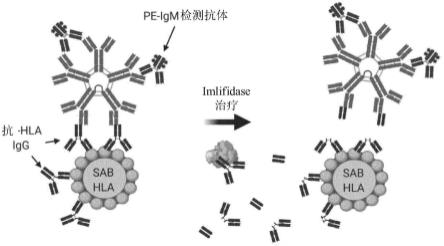
图15-我们提出的机制是igg-dsa复合的igm与sab-hla珠结合。igm检测抗体识别复合物中的igm,产生不真实的igm信号。在imlifidase处理后,这些igg-igm复合物将被切割,并且在sab hla测定中将记录到低得多但真实的igm信号。
[0035]
图16-分析来自esrd致敏患者的给药前和imlifidase后24小时的血清样品的sab-hla i类和ii类特异性igg。为清楚起见,分析中仅包括在给药前血清中达到3000mfi阈值的单抗原珠。n表示患者02-922(a)、02-923(b)、02-925(c)、02-926(d)、02-927(e)、02-928(f)和02-929(g)的阳性珠粒的数量。
[0036]
图17-针对igm在给药之前和之后之间变化量很少的珠粒。线和形状根据图例。
[0037]
序列的简要说明
[0038]
seq id no:1是ides的完整序列,包括n端甲硫氨酸和信号序列。它也可作为ncbi参考序列号wp_010922160.1获得。
[0039]
seq id no:2是ides的成熟序列,缺少n端甲硫氨酸和信号序列。它也可作为genbank登录号adf13949.1获得。
[0040]
seq id no:3是idez的完整序列,包括n端甲硫氨酸和信号序列。它也可作为ncbi参考序列号wp_014622780.1获得。
[0041]
seq id no:4是idez的成熟序列,缺少n端甲硫氨酸和信号序列。
[0042]
seq id no:5是杂合ides/z的序列。n端基于缺少n端甲硫氨酸和信号序列的idez。
[0043]
seq id no:6至25是用于在本发明方法中使用的示例性蛋白酶的序列。
[0044]
seq id no:26是ides多肽的序列。包含seq id no:2的序列,带有附加的n端甲硫氨酸和组氨酸标签(内部参考pcart124)。
[0045]
seq id no:27是idez多肽的序列。包含seq id no:4的序列,带有附加的n端甲硫氨酸和组氨酸标签(内部参考pcart144)。
[0046]
seq id no:28是ides/z多肽的序列。包含seq id no:5的序列,带有附加的n端甲硫氨酸和组氨酸标签(内部参考pcart145)。
[0047]
seq id no:29是连续序列pltpeqfrynn,其对应于seq id no:3的位置63-73。
[0048]
seq id no:30是连续序列ppanftqg,其对应于seq id no:1的位置58-65。
[0049]
seq id no:31是连续序列ddyqrnateayakevphqit,其对应于seq id no:3的位置35-54。
[0050]
seq id no:32是连续序列dsfsanqeirysevtpyhvt,其对应于seq id no:1的位置30-49。
[0051]
seq id no:33至55是编码上述蛋白酶的核苷酸序列。
[0052]
seq id no:56至69是用于在本发明方法中使用的示例性蛋白酶的序列。
[0053]
seq id no:70是连续序列nqtn,其对应于seq id no:1的位置336-339。
[0054]
seq id no:71是连续序列dsfsanqeir ysevtpyhvt,其对应于seq id no:1的位置30-49。
[0055]
seq id no:72至86是编码本文公开的多肽的核苷酸序列。seq id no:87是序列sfsanqeiry sevtpyhvt,其对应于seq id no:1的位置31-49。
[0056]
seq id no:88是序列dyqrnateay akevphqit,其对应于idez多肽(ncbi参考序列号wp_014622780.1)的位置36-54。
[0057]
seq id no:89是序列ddyqrnatea yakevphqit,其可以存在于本发明多肽的n端。
具体实施方式
[0058]
检测抗体的方法
[0059]
发明人在实施例中已经证明,igm抗体可以与igg抗体形成免疫复合物。在不存在与靶抗原反应的任何igm抗体的情况下,这些免疫复合物可以结合靶抗原和用于检测igm的试剂二者。因此,此类免疫复合物可能在用于检测igm抗体、特别是抗原特异性igm抗体的测定中产生假阳性结果。实施例还证明这些有问题的复合物可以被igg半胱氨酸蛋白酶切割。已知iga抗体和ige抗体以与igm类似的方式与igg形成复合物。因此,本发明提供了用于检测igm抗体、iga抗体和ige抗体的改进方法,包括在允许igg半胱氨酸蛋白酶活性发生的条件下使所述样品与igg半胱氨酸蛋白酶接触。
[0060]
发明人发现的干扰是不寻常的,因为它会导致不适当信号的增加,而不是阻断信号。发明人使用igg半胱氨酸蛋白酶开发的方案特别有效,因为它不会影响待检测的任何igm抗体、iga抗体或ige抗体。用于解决发明人所确定的干扰的其它技术,例如用抗igg抗体或用柱耗尽,可能会导致igm、iga和/或ige水平的减少。
[0061]
本发明提供了检测样品中的igm抗体、iga抗体或ige抗体的方法,包括:在允许igg半胱氨酸蛋白酶活性发生的条件下使所述样品与igg半胱氨酸蛋白酶接触;和使所述样品与适合用于检测igm抗体、iga抗体或ige抗体的试剂接触。
[0062]
各种免疫测定可用于检测igm抗体、iga抗体和ige抗体,并且可以适应于添加使样品与igg半胱氨酸蛋白酶接触的步骤。
[0063]
在某些实施方案中,本发明的方法用于固相测定例如elisa中,并且将用于检测抗体的试剂在板的孔中固定化。样品与igg半胱氨酸蛋白酶的接触可以在同一孔中进行。
[0064]
在某些实施方案中,本发明的方法用于固相测定例如多重珠测定中,并且将用于检测抗体的试剂在珠粒上固定化。可以将用于检测抗体和/或不同感兴趣的抗原的不同试剂在不同的珠粒上固定化。在某些实施方案中,将本发明的方法用于单抗原珠测定中。在某些实施方案中,本发明的方法使用平台。
[0065]
在某些实施方案中,本发明的方法用于固相测定,例如elisa或cap feia(immunocap)测试中,并且将感兴趣的靶抗原在固体基底固定化,例如孔或纤维素上。然后将样品与固定化抗原接触,与igg半胱氨酸蛋白酶接触,并且与用于检测感兴趣的抗体类别的试剂接触。
[0066]
在某些实施方案中,本发明的方法用于表面等离子共振测定中,并且将用于检测抗体的试剂在传感器芯片表面上固定化。
[0067]
在某些实施方案中,本发明的方法用于浊度测定中,并且样品与适于检测抗体的试剂的接触在溶液中进行。
[0068]
在某些实施方案中,本发明的方法用于生物层干涉测定中,并且将用于检测抗体
的试剂在生物传感器尖端上固定化。
[0069]
在优选的实施方案中,适用于检测igm抗体、iga抗体或ige抗体的试剂是抗igm抗体、抗iga抗体或抗ige抗体。此类抗体是熟知的并且可广泛获得。在某些实施方案中,适合用于检测igm抗体、iga抗体或ige抗体的试剂是标记的。标记可用于帮助检测。
[0070]
在优选的实施方案中,本发明的方法用于检测对感兴趣的靶标特异的igm抗体、iga抗体或ige抗体。如上所述,用于检测此类抗体的各种免疫测定是已知的并且可以适应于包括使样品与igg半胱氨酸蛋白酶接触的步骤。通常,可以通过在允许分离与感兴趣的抗原特异性结合的抗体的条件下使样品与感兴趣的抗原接触来检测靶标特异性抗体。在某些实施方案中,将感兴趣的抗原固定到固体基底或固相基质,例如珠粒或板。可以将抗原包被在固体基底上。在某些实施方案中,珠粒或板是聚苯乙烯。在某些实施方案中,珠粒是或顺磁性微球。在某些实施方案中,珠粒是标记的。多个珠粒可以是不同地标记的,以能够将不同珠粒区分并且在单个测定中检测多种不同的抗体。在某些实施方案中,本发明的方法包括使用流式细胞术分选珠粒。
[0071]
对于使用以igg半胱氨酸蛋白酶切割的步骤的任何免疫测定,确定适当的截止值是在本领域技术人员的正常能力范围内。通常,采用》1000mfi的截止值,在实例中采用》3000mfi。
[0072]
在某些实施方案中,本发明的方法利用多种感兴趣的抗原和/或用于检测igm抗体、iga抗体或ige抗体的多种试剂。此类多重测定允许在单次测定中检测针对多种不同抗原的抗体,并且此类测定将从通过使用igg半胱氨酸蛋白酶所提供的改进中受益。例如,在某些实施方案中,方法包括使样品与多种hla i类和/或hlaii类抗原(例如,至少2、3、4、5、6、7、8、9或10种抗原)接触。示例性的测定可以使用具有每个基因座hla-a、-b和-c的两个等位基因的珠粒;或hla-dr、-dq和-dp包被的珠粒,从而保持与在细胞表面观察到的相似的表达比率。或者,可以用单抗原的多个拷贝包被珠粒。
[0073]
因此,本发明提供了用于检测样品中的对感兴趣的抗原特异的igm抗体、iga抗体或ige抗体的方法,包括:在允许igg半胱氨酸蛋白酶活性发生的条件下使所述样品与igg半胱氨酸蛋白酶接触;使所述样品与感兴趣的抗原接触,所述感兴趣的抗原任选地固定在固体基底例如板或珠粒上;并且将所述样品与适合用于检测igm抗体、iga抗体或ige抗体的试剂接触。这种方法通常还会包括标准的洗涤步骤。使样品与igg半胱氨酸蛋白酶接触的步骤可以发生在样品与感兴趣的抗原接触之前或之后,但是会通常发生在样品与适合用于检测igm抗体、iga抗体或ige的试剂接触之前。
[0074]
在某些实施方案中,本发明的方法以elisa形式实施。在这样的测定中,测定板的孔通常会包被有抗体靶标。然后将igg蛋白酶添加到孔中,随后添加用于igm抗体、iga抗体或ige抗体以被检测的样品,这些抗体对包被孔的靶标具有特异性。允许蛋白酶和样品在适合于igg半胱氨酸蛋白酶活性的条件下相互作用。在合适的时间间隔后,洗涤测定板,并且在适合与靶标特异性抗体结合的条件下添加与igm抗体、iga抗体或ige抗体特异性结合的检测抗体。检测抗体将与已与每个孔中靶标结合的任何完整的靶标特异性抗体结合。洗涤后,孔中存在的检测抗体的量将与该孔结合的靶标特异性抗体的量成比例。检测抗体可以直接地或间接地与标记或其它报告系统(例如酶)缀合,如此可以确定每个孔中保留的检测抗体的量。
[0075]
含有或疑似含有igm抗体、iga抗体或ige抗体的任何合适的样品可以用于本发明的方法。在优选的实施方案中,样品是从患者获得的样品,例如血清样品。
[0076]
检测靶标特异性抗体
[0077]
在优选的实施方案中,本发明的方法检测对具体靶标或靶标组具有特异性的igm抗体、iga抗体或ige抗体的存在。如上所述,用于检测此类抗体的各种免疫测定是已知的,并且可以适应于包括使样品与igg半胱氨酸蛋白酶接触的步骤。一般而言,可以通过在允许分离与感兴趣的抗原特异性结合的抗体的条件下将样品与感兴趣的抗原接触来检测靶标特异性抗体。
[0078]
在优选的实施方案中,感兴趣的抗原是人抗原。针对此类人抗原的内源性抗体通常具有致病性,例如自身抗原可以引起自身免疫疾病,以及供体特异性抗原可以引起移植排斥。在优选的实施方案中,感兴趣的抗原是人白细胞抗原(hla)、红细胞抗原,或者是与自身免疫疾病关联的抗原,例如选自下表a的抗原。检测此类抗体是困难的并且需要特别的精确度,因为在诊断自身免疫疾病或确定患者是否可以接受来自特定供体的移植时临床医生通常需要准确且细致入微地评估患者的抗体特征。因此,本发明方法所实现的改进对于检测对这些hla、红细胞抗原或与自身免疫疾病关联的抗原具有特异性的igm抗体、iga抗体或ige抗体尤其有用。
[0079]
在进一步优选的实施方案中,将本发明方法用于在检测抗药物抗体中使用。在这样的实施方案中,感兴趣的抗原是药物,例如抗体或肽类药物,并且检测针对该药物的igm抗体、iga抗体或ige抗体。这种抗药物抗体可以降低药物的功效,因此它们的检测可用于确保可以根据需要调整治疗以保持功效。本发明方法尤其可用于检测抗药物抗体,因为需要很高的精确度以适当地调整治疗方案。
[0080]
治疗由致病性抗体和免疫复合物介导的疾病或病症的方法
[0081]
在优选的实施方案中,本发明提供了用于治疗对象中的全部或部分由致病性igm抗体、致病性iga抗体或致病性ige抗体介导的疾病或病症的方法,其中方法包括施用igg半胱氨酸蛋白酶。发明人在实施例中已经证明,igm抗体可以与可以被igg半胱氨酸蛋白酶切割的igg抗体形成免疫复合物。iga抗体和ige抗体可能会与igg抗体形成类似的复合物。预期这些免疫复合物介导疾病过程,因此igg半胱氨酸蛋白酶将可用于治疗由致病性igm抗体、致病性iga抗体或致病性ige抗体介导的疾病或病症。
[0082]
本发明还提供了igg半胱氨酸蛋白酶,用于在治疗由致病性igm抗体、致病性iga抗体或致病性ige抗体全部或部分介导的疾病或病症的方法中使用。本发明还提供了igg半胱氨酸蛋白酶在制备药物中的用途,该药物用于在治疗全部或部分由致病性igm抗体、致病性iga抗体或致病性ige抗体介导的疾病或病症的方法中使用。
[0083]
在某些实施方案中,全部或部分由致病性igm抗体、致病性iga抗体或致病性ige抗体介导的疾病或病症是选自表a的疾病。
[0084]
在某些实施方案中,待根据本发明被治疗的患有全部或部分由致病性igm抗体、致病性iga抗体或致病性ige抗体介导的疾病或病症的患者不表现出显著水平的抗自身igg抗体。在某些实施方案中,待根据本发明被治疗的患有全部或部分由致病性igm抗体、致病性iga抗体或致病性ige抗体介导的疾病或病症的患者表现出亚致病性的或正常范围内的抗自身igg抗体或其它igg抗体的水平。发明人在实施例中鉴定的免疫复合物可以在不存在抗
自身igg抗体的情况下介导疾病,并且因此igg半胱氨酸蛋白酶将可用于在不存在显著水平的抗自身igg抗体的情况下治疗此类疾病或病症。
[0085]
在进一步优选的实施方案中,本发明提供了用于治疗对象中的全部或部分由致病性igg抗体介导的疾病或病症的方法,其中所述对象被确定为表现出抗igg igm抗体、抗igg iga抗体或抗igg ige抗体,其中方法包括施用igg半胱氨酸蛋白酶。发明人在实施例中已经证明,igm抗体可以与可以被igg半胱氨酸蛋白酶切割的igg抗体形成免疫复合物。iga抗体和ige抗体可能会与igg抗体形成类似的复合物。预期这些免疫复合物会扩大致病性igg抗体的影响,因此igg半胱氨酸蛋白酶对治疗具有抗igg igm抗体、抗igg iga抗体或抗igg ige抗体的患者尤其有效。
[0086]
本发明还提供了igg半胱氨酸蛋白酶,用于在治疗对象中的全部或部分由致病性igg抗体介导的疾病或病症的方法中使用,其中所述对象被确定为表现出抗igg igm抗体、抗igg iga抗体或抗igg ige抗体。本发明还提供了igg半胱氨酸蛋白酶在制备药物中的用途,该药物用于在治疗对象中的全部或部分由致病性igg抗体介导的疾病或病症的方法中使用,其中所述对象被确定为表现出抗igg igm抗体、抗igg iga抗体或抗igg ige抗体。
[0087]
在进一步优选的实施方案中,本发明提供了用于治疗对象中的全部或部分由igg抗体与igm抗体、iga抗体或ige抗体的复合物介导的疾病或病症的方法,其中方法包括施用igg半胱氨酸蛋白酶。发明人在实施例中已经确定,igm抗体和igg抗体可以形成可以被igg半胱氨酸蛋白酶切割的复合物。预期iga抗体和ige抗体会形成类似的复合物。此类免疫复合物可以是致病性的并且在例如肾脏或血管中引起疾病。因此,在优选的这类实施方案中,本发明提供了用于治疗血管炎、肉芽肿性多血管炎(韦格纳肉芽肿)、iga肾病或系统性红斑狼疮的方法,包括施用igg半胱氨酸蛋白酶。iga肾病是由iga抗体在肾脏中的积聚引起的,并且这种积聚可能部分是由与实施例中所确定那些类似的iga与igg的复合物引起的。如实施例中所证明的,用igg半胱氨酸蛋白酶切割这种复合物可以减少或防止iga在肾脏中的积累,从而预防、治疗或减轻疾病的症状。血管炎、肉芽肿性多血管炎和系统性红斑狼疮可能是由可被根据本发明的igg半胱氨酸蛋白酶切割的自身抗体和免疫复合物引起的。igg与ige的复合物可以引起或加剧急性过敏反应或慢性炎症性过敏性疾病,因此在某些实施方案中,本发明提供了用于在治疗或预防急性过敏反应或慢性炎症性过敏性疾病的方法中使用的igg半胱氨酸蛋白酶。在某些此类实施方案中,待治疗的对象可以不表现出显著水平的、或任何的抗自身igg抗体或其它致病性igg抗体。相反,igg抗体与igm抗体、iga抗体或ige抗体的复合物本身就是致病性的。
[0088]
本发明还提供了igg半胱氨酸蛋白酶,用于在治疗对象中的全部或部分由igg抗体与igm抗体、iga抗体或ige抗体的复合物介导的疾病或病症的方法中使用。本发明还提供了igg半胱氨酸蛋白酶在制备药物中的用途,该药物用于在治疗对象中的全部或部分由igg抗体与igm抗体、iga抗体或ige抗体的复合物介导的疾病或病症的方法中使用。
[0089]
形成根据本发明可被切割且可被处理的免疫复合物的致病性igg抗体、igm抗体、iga抗体或ige抗体通常可以对靶向于全部或部分由抗体介导的自身免疫疾病或其它病症的抗原具有特异性。表a列出了这些疾病和相关抗原。本发明的蛋白酶可用于治疗这些疾病或病症中的任一种。该蛋白酶对于治疗或预防全部或部分由致病性igg抗体介导的自身免疫疾病尤其有效。此外,该蛋白酶对治疗具有抗igg igm抗体、抗igg iga抗体或抗igg ige
抗体的患者中的此类疾病尤其有效。该蛋白酶对于治疗或预防全部或部分由致病性igm抗体、iga抗体或ige抗体介导的自身免疫疾病也尤其有效。
[0090]
表a
[0091]
[0092]
[0093]
[0094][0095]
根据本发明的igg半胱氨酸蛋白酶也可以用于治疗或预防。在治疗性应用中,将蛋白酶以足够用于治愈、减轻或部分阻止病症或其一种或多种症状的量施用至已经患有障碍或病症的对象。这种治疗性治疗可以导致疾病症状的严重程度降低,或增加无症状期的频率或持续时间。足以实现这一点的量被定义为“治疗有效量”。在预防性应用中,将蛋白酶以足够用于预防或延缓症状发展的量施用于尚未表现出障碍或病症的症状的对象。这样的量被定义为“预防有效量”。对象可能已通过任何合适的方式被确定为具有发展出疾病或病症的风险。
[0096]
在本发明的方法中,蛋白酶可以与免疫抑制剂共同施用。在本发明的方法中,蛋白酶优选地通过静脉输注施用,但是可以通过任何合适的途径施用,包括例如皮内、皮下、经皮、肌内、动脉内、腹膜内、关节内、骨内或其它适当的给药途径。施用的蛋白酶的量可以在0.01mg/kg bw至2mg/kg bw之间、在0.05至1.5mg/kg bw之间、在0.1mg/kg bw至1mg/kg bw之间,优选地在0.15mg/kg bw至0.7mg/kg bw之间,最优选地在0.2mg/kg bw至0.3mg/kg bw之间,尤其是0.25mg/kg bw。可以将蛋白酶在多个时机施用于同一对象,条件是对象血清中的能够与该蛋白酶结合的抗药物抗体(ada)的量不超过由临床医生确定的阈值。对象血清中的能够与该蛋白酶结合的ada的量可以通过任何合适的方法来确定,例如药剂特异性cap feia(immunocap)测试或滴度测定。
[0097]
器官移植
[0098]
本发明的治疗性方法在上下文中可能特别有用于器官移植。器官可以选自肾脏、
肝脏、心脏、胰腺、肺或小肠。待治疗的对象可以优选地是致敏的或高度致敏的。“致敏(sensitized)”是指对象已经产生了针对人主要组织相容性(mhc)抗原(也称为人白细胞抗原(hla))的抗体。对象可以具有igm、iga或ige抗-hla抗体,或者对象可以具有igg抗-hla抗体和抗-igg igm、iga或ige抗体。抗hla抗体来源于同种异体致敏的b细胞,并且通常存在于先前已经因输血、既往移植或妊娠而致敏的患者中(jordan等人,2003)。
[0099]
潜在的移植接受者是否致敏可以通过任何合适的方法确定。例如,可以将群体反应性抗体(panel reactive antibody,pra)测试用于确定接受者是否是致敏的。pra评分》30%通常被认为意味着患者具有“高免疫风险”或是“致敏的”。或者,可以进行交叉匹配测试,其中将潜在移植供体的血液样品与预期接受者的血液样品混合。阳性交叉匹配意味着接受者具有对供体样品起反应的抗体,表明接受者是致敏的并且移植不应进行。交叉匹配测试通常在将要移植前作为最终检查进行。
[0100]
igg半胱氨酸蛋白酶
[0101]
发明人已经证明,在检测igm抗体、iga抗体或ige抗体的方法中使用igg半胱氨酸蛋白酶会导致提高的特异性和灵敏度,因为该蛋白酶能够切割可能干扰igm抗体、iga抗体和ige抗体检测的免疫复合物。用于本发明的igg半胱氨酸蛋白酶对igg具有特异性,并且对待检测的抗体没有显著的切割活性。因此,在某些实施方案中,蛋白酶切割igg而不切割igm。在某些实施方案中,蛋白酶切割igg而不切割iga。在某些实施方案中,蛋白酶切割igg而不切割ige。在某些实施例中,蛋白酶切割igg但不切割igm、iga或ige。
[0102]
在优选的实施方案中,用于在本发明方法中使用的蛋白酶是imlifidase(ides)(酿脓链球菌(s.pyogenes)的免疫球蛋白g-降解酶)。ides是由人病原体酿脓链球菌产生的细胞外半胱氨酸蛋白酶。ides最初是从血清型m1的a组链球菌菌株中分离出来的,但是现在已经在所有测试的a组链球菌菌株中鉴定出ides基因。ides具有极其高度的底物特异性,其唯一鉴定出的底物是igg。ides催化人igg所有亚类的重链下部铰链区的单一蛋白水解切割。ides还催化各种动物中一些igg亚类的重链的等效切割。ides通过两阶段机制有效地将igg切割为fc和f(ab')2片段。在第一阶段,igg的一条(第一)重链被切割以产生具有非共价结合的fc分子的单切割的igg(scigg)分子。scigg分子实际上是一种中间产物,它保留原始igg分子的剩余(第二)重链。在该机制的第二阶段,该第二重链被ides切割以释放f(ab')2片段和同源二聚体fc片段。这些是通常在生理条件下观察到的产物。在还原条件下,f(ab')2片段可以解离成两个fab片段,并且同源二聚体fc可以解离成其组成单体。seq id no:1是包含n端甲硫氨酸和信号序列的ides的完整序列。它也可作为ncbi参考序列号wp_010922160.1获得。seq id no:2是缺少n端甲硫氨酸和信号序列的ides的成熟序列。它也可作为genbank登录号adf13949.1获得。
[0103]
在替代的实施方案中,用于在本发明方法中使用的蛋白酶是idez,它是由马链球菌兽疫亚种(streptococcus equi ssp.zooepidemicu,一种主要发现于马中的细菌)产生的igg半胱氨酸蛋白酶。seq id no:3是包含n端甲硫氨酸和信号序列的idez的完整序列。它也可作为ncbi参考序列号wp_014622780.1获得。seq id no:4是缺少n端甲硫氨酸和信号序列的idez的成熟序列。
[0104]
在替代的实施方案中,用于在本发明方法中使用的蛋白酶是杂合ides/z,例如seq id no:5。该n端是基于缺少n端甲硫氨酸和信号序列的idez。
[0105]
在优选的实施方案中,用于在本发明中使用的蛋白酶可以包含seq id no:2、4或5或由seq id no:2、4或5组成。用于在本发明中使用的蛋白酶可以包含在n端的附加甲硫氨酸(m)残基和/或在c端的标签,以协助在标准细菌表达系统中表达和从标准细菌表达系统中分离。合适的标签包括组氨酸标签,其可以直接地连接到多肽的c端或通过任何合适的接头序列(例如3、4或5个甘氨酸残基)间接地连接。组氨酸标签通常由六个组氨酸残基组成,尽管它可以比这更长,通常多达7、8、9、10或20个氨基酸,或者更短,例如5、4、3、2或1个氨基酸。
[0106]
在进一步优选的实施方案中,用于在本发明中使用的蛋白酶可以包含以下、基本上由以下组成或由以下组成:seq id no:6至25中任一个的序列。这些序列代表具有增加的蛋白酶活性和/或降低的免疫原性的ides和idez多肽。seq id no:6至25中的每一个可以任选地包含在n端的附加甲硫氨酸和/或在c端的组氨酸标签。组氨酸标签优选地由六个组氨酸残基组成。组氨酸标签优选地通过3x甘氨酸或5x甘氨酸残基的接头连接到c端。
[0107]
在进一步优选的实施方案中,用于在本发明中使用的蛋白酶可以包含以下、基本上由以下组成或由以下组成:seq id no:56至69中任一个的序列。这些序列代表具有增加的蛋白酶活性和/或降低的免疫原性的ides多肽。seq id no:56至69中的每一个可以任选地包含在n端的附加甲硫氨酸和/或在c端的组氨酸标签。组氨酸标签优选地由六个组氨酸残基组成。组氨酸标签优选地通过3x甘氨酸或5x甘氨酸残基的接头连接到c端。
[0108]
在进一步优选的实施方案中,用于在本发明中使用的蛋白酶可以包含以下、基本上由以下组成或由以下组成:seq id no:6至25中任一个的序列,其任选地具有多达3个(例如1、2或3个)氨基酸取代。seq id no:6至25中的每一个及其变体可以任选地包含在n端的附加甲硫氨酸和/或在c端的组氨酸标签。
[0109]
在进一步优选的实施方案中,用于在本发明中使用的蛋白酶可以包含以下、基本上由以下组成或由以下组成:seq id no:56至69中任一个的序列,其任选地具有多达3个(例如1、2或3个)氨基酸取代。seq id no:56至69中的每一个及其变体可以任选地包含在n端的附加甲硫氨酸和/或在c端的组氨酸标签。
[0110]
本发明多肽的长度通常为至少100、150、200、250、260、270、280、290、300或310个氨基酸。本发明多肽的长度通常为不大于400、350、340、330、320或315个氨基酸。应当理解,上面列出的下限中的任一个都可以与上面列出的上限中的任一个组合以提供本发明多肽的长度范围。例如,多肽的长度可以为100至400个氨基酸、或250至350个氨基酸。该多肽的长度优选地为290至320个氨基酸,最优选地为300至315个氨基酸。
[0111]
本发明蛋白酶的一级结构(氨基酸序列)是基于ides、idez或ides/z的一级结构,特别是分别为seq id no:2、4或5的氨基酸序列。本发明蛋白酶的序列可以包含seq id no:2、4或5的氨基酸序列的变体,所述变体与seq id no:2、4或5的氨基酸序列至少80%相同。变体序列可以与seq id no:2、4或5的序列至少80%、至少85%,优选至少90%、至少95%、至少98%或至少99%相同。变体可以与seq id no:2、4或5的序列相同,除了包含在wo2016/128558或wo2016/128559中鉴定的一种或多种特定修饰之外。可以在seq id no:2、4或5所示的序列的至少50、至少100、至少200、至少300或更多连续氨基酸的区域上或更优选地在seq id no:4或5的全长上测量相对于seq id no:2、4或5序列的同一性。
[0112]
用于在本发明中使用的蛋白酶可以是包含seq id no:2、4或5的氨基酸序列的变
体的ides、idez或ides/z多肽,其中修饰(例如氨基酸添加、缺失或取代)是相对于seq id no:2、4或5的序列进行的。此类修饰优选地是保守氨基酸取代。保守取代是利用化学结构相似、化学性质相似或侧链体积相似的其它氨基酸替换氨基酸。引入的氨基酸可以具有其所取代的氨基酸相似的极性、亲水性、疏水性、碱性、酸性、中性或电荷。或者,保守取代可以引入芳香族或脂肪族的另一种氨基酸来代替先前存在的芳香族或脂肪族的氨基酸。保守氨基酸变化是本领域熟知的。
[0113]
igg半胱氨酸蛋白酶活性可以通过任何合适的方法来评估,例如通过将多肽与含有igg的样品孵育并且确定igg切割产物的存在。wo2016/128559中描述了合适的方法。合适的测定包括基于elisa的测定,例如在wo2016/128559中描述的那些。在这样的测定中,测定板的孔通常用抗体靶标例如牛血清白蛋白(bsa)包被。然后将待测试的多肽样品添加到孔中,随后添加靶标特异性抗体的样品,在该实例中该抗体是对bsa特异的。允许多肽和抗体在适合igg半胱氨酸蛋白酶活性的条件下相互作用。在合适的时间间隔后,将洗涤测定板,并且在适合与靶标特异性抗体结合的条件下添加特异性结合靶标特异性抗体的检测抗体。检测抗体将与每个孔中已与靶标结合的任何完整靶标特异性抗体结合。洗涤后,孔中存在的检测抗体的量将与结合到该孔的靶标特异性抗体的量成比例。检测抗体可以直接地或间接地与标记或另一种报告系统(例如酶)缀合,从而可以确定每个孔中剩余的检测抗体的量。孔中测试的多肽的效力越高,越少的完整靶标特异性抗体将保留,并且因此将存在更少的检测抗体。通常,给定测定板上的至少一个孔将包含ides,而不是待测试的多肽,因此可以将测试多肽的效力直接地与ides的效力进行比较。也可以包括idez和ides/z用于比较。
[0114]
其它测定可以通过直接地可视化和/或量化由测试多肽切割igg产生的igg片段来确定测试多肽的效力。这种类型的测定也在wo2016/128559中描述。这种测定通常将igg样品与滴定系列下不同浓度的测试多肽(或与作为对照的ides、idez和ides/z中的一种或多种)孵育。然后使用凝胶电泳,例如通过sds-page分离在每个浓度下孵育所产生的产物。然后整个igg和由切割igg产生的片段可以通过大小进行鉴定并且通过使用合适染料的染色强度进行量化。切割片段的数量越多,在给定浓度下测试多肽的效力越大。本发明的多肽通常在比idez和/或ides更低的浓度(滴定系列中的较低点)下会产生可检测量的切割片段。这种类型的测定还可以鉴定在切割igg分子的第一重链或第二重链方面更有效的测试多肽,因为也可以确定由每个切割事件产生的不同片段的量。本发明的多肽可以在切割igg分子的第一条链上比切割第二条链更有效,特别是在igg是igg2同种型时。本发明的多肽可以在切割igg1方面上比切割igg2更有效。
[0115]
多肽的产生
[0116]
如本文所公开的多肽可以通过任何合适的方式产生。例如,可以使用本领域已知的标准技术直接地合成多肽,例如fmoc固相化学、boc固相化学或通过液相肽合成。或者,可以通过用编码所述多肽的核酸分子或载体(vector)转化细胞、通常是细菌细胞来产生多肽。wo2016/128559中描述并例证了通过在细菌宿主细胞中表达来产生多肽。
[0117]
包含多肽的组合物和制剂
[0118]
本发明还提供了包含蛋白酶的组合物,用于在本发明的治疗方法中使用。例如,本发明提供了一种组合物,其包含一种或多种本发明的多肽和至少一种药学上可接受的载体(carrier)或稀释剂。载体需要在与组合物的其它成分相容且对被施用组合物的对象无害
的意义上是“可接受的”。通常,载体和最终组合物是无菌且无热原的。
[0119]
合适组合物的配制可以使用标准的药物制剂化学和方法进行,所有这些对于相当熟练的技术人员来说都是易于获得的。例如,药剂可以与一种或多种药学上可接受的赋形剂或载体组合。辅助物质(例如润湿剂或乳化剂)、ph缓冲物质、还原剂等可以存在于赋形剂或载体中。合适的还原剂包括半胱氨酸、硫代甘油、硫氧还原素(thioreducin)、谷胱甘肽等。赋形剂、载体和辅助物质通常是不会在接受组合物的个体中诱导免疫反应并且可以施用而没有过度毒性的药学上的药剂。药学上可接受的赋形剂包括但不限于液体如水、盐水、聚乙二醇、透明质酸、甘油、硫代甘油和乙醇。其中还可包含药学上可接受的盐,例如无机酸盐,例如盐酸盐、氢溴酸盐、磷酸盐、硫酸盐等;以及有机酸盐,例如乙酸盐、丙酸盐、丙二酸盐、苯甲酸盐等。药学上可接受的赋形剂、载体和辅助物质的深入讨论可在《雷氏药学大全》(remington's pharmaceutical sciences,mack pub.co.,nj 1991)中获得。
[0120]
此类组合物可以以适合于单次施用(bolus administration)或连续施用的形式制备、包装或出售。可注射的组合物可以以单位剂型(例如于含防腐剂的安瓿或多剂量容器中)制备、包装或出售。组合物包含但不限于混悬剂、溶液剂、油性或水性载体中的乳剂、糊剂和可植入的缓释或可生物降解的制剂。此类组合物还可包含一种或多种附加成分,包括但不限于混悬剂、稳定剂或分散剂。在用于肠胃外施用的组合物的一个实施方案中,活性成分是以干燥(例如,粉末或颗粒)形式提供,用于用合适的载体(例如,无菌无热原水)重构然后在肠胃外施用重构的组合物。组合物可以以无菌可注射的水性或油性混悬剂或溶液剂的形式制备、包装或出售。该混悬剂或溶液剂可以根据已知技术进行配制,并且可以包含除活性成分外的附加成分,例如本文所述的分散剂、润湿剂或混悬剂。此类无菌可注射制剂可以使用无毒的肠胃外可接受的稀释剂或溶剂(例如水或1,3-丁二醇)来制备。其它可接受的稀释剂和溶液剂包括但不限于林格氏溶液、等渗氯化钠溶液和不挥发油(例如合成的甘油单酯或甘油二酯)。
[0121]
其它可用的肠胃外施用的组合物包括包含微晶形式、脂质体制剂或作为生物可降解聚合物系统组分的活性成分的那些组合物。用于持续释放或植入的组合物可以包含药学上可接受的聚合物或疏水材料,例如乳液、离子交换树脂、微溶聚合物或微溶盐。组合物可以适合于通过任何合适途径施用,包括例如皮内、皮下、经皮、肌内、动脉内、腹膜内、关节内、骨内或其它适当的施用途径。优选的组合物适合于通过静脉内输注施用。
[0122]
试剂盒
[0123]
本发明还提供了用于实施本发明方法的试剂盒。本发明的试剂盒如上文所定义和所述的igg半胱氨酸蛋白酶和如上文所定义和所述的用于检测igm抗体、iga抗体或ige抗体的试剂。在某些实施方案中,试剂盒还包含感兴趣的抗原,例如人白细胞抗原(hla)、红细胞抗原或药物抗原。如上所述,可以将感兴趣的抗原固定例如包被在固体基底例如板或珠粒上。
[0124]
一般知识
[0125]
应当理解,所公开的产品和方法的不同应用可以针对本领域中的特定需要进行定制。还应理解,本文使用的术语是用于描述本发明的特定实施方案的目的,并不旨在限制。
[0126]
此外,如在本说明书和所附权利要求中使用的,单数形式“a”、“an”和“the”包括复数指称,除非该内容明确规定。因此,例如,提及“多肽(a polypeptide)”包括“多肽
(polypeptides)”等。
[0127]
除非明确禁止,本文公开的方法的步骤可以以任何适当的顺序执行,并且不应认为对列出步骤顺序的限制。
[0128]“多肽”在本文中以其最广泛的含义使用,是指两个或更多个亚基氨基酸的化合物、氨基酸类似物或其它肽模拟物。因此,术语“多肽”包括短肽序列以及更长的多肽和蛋白质。如本文所用,术语“氨基酸”是指天然和/或非天然或合成的氨基酸,包括d或l旋光异构体二者和氨基酸类似物和肽模拟物。
[0129]
术语“患者”和“对象”可互换使用,并且通常指的是人。除非另有说明,否则对igg的提及通常是指人igg。
[0130]
如上所述的氨基酸同一性可以使用任何合适的算法来计算。例如,pileup和blast算法可用于计算同一性或排列序列(例如识别等效序列或相应序列(通常以它们的默认设置),例如altschul sf(1993)j mol evol 36:290-300;altschul,s,f等人(1990)j mol biol 215:403-10中所述。执行blast分析的软件可通过国家生物技术信息中心(http://www.ncbi.nlm.nih.gov/)公开获得。该算法包括首先通过识别查询序列中长度w的短字段(word)来鉴定高评分序列对(hsp),这些短字段在与数据库序列中相同长度的字段对齐时匹配或满足一些正值阈值得分t。t被称为邻域字段得分阈值(altschul等人,同上)。这些初始邻域字段命中(word hit)充当启动搜索以查找包含它们的hsp的种子。字段命中沿着每个序列在两个方向上扩展,只要可以增加累积对齐分数。在以下情况下,字段命中在每个方向上的扩展都会停止:在累积对齐得分从其最大实现值下降数量x;由于一个或多个负得分残基对齐的累积,累积得分变为零或更低;或到达任一序列的末端。blast算法参数w、t和x确定对齐的灵敏度和速度。blast程序默认使用11的字段(w),blosum62得分矩阵(参见henikoff和henikoff(1992)proc.natl.acad.sci.usa 89:10915-10919)对齐(b)为50,期望(e)为10,m=5,n=4,以及两者链的比较。
[0131]
blast算法对两个序列之间的相似性进行统计分析;参见例如,karlin和altschul(1993)proc.natl.acad.sci.usa 90:5873-5787。blast算法提供的相似性的一种度量是最小和概率(p(n)),它提供对两个多核苷酸或氨基酸序列之间的匹配是偶然发生的概率的指示。例如,一种序列被认为与另一种序列相似,如果第一序列与第二序列相比的最小和概率小于约1,优选小于约0.1,更优选小于约0.01,且最优选小于约0.001。或者,uwgcg包提供bestfit程序,其可以用于计算同一性(例如在其默认设置上使用)(devereux等人(1984)nucleic acids research 12,387-395)。
[0132]
无论是上文或下文中的本文引用的所有出版物、专利和专利申请通过引用其整体并入本文。
[0133]
实施例1
[0134]
除非另有说明,否则所使用的方法是标准的生物化学和分子生物学技术。合适的方法教科书的实例包括sambrook等人,分子克隆(molecular cloning),a laboratory manual(1989)和ausubel等人,current protocols in molecular biology(1995),john wiley和sons,inc。
[0135]
介绍
[0136]
降解免疫球蛋白g的半胱氨酸蛋白酶imlifidase(ides)是一种igg内肽酶,目前正
在开发作为肾移植中的快速脱敏治疗。imlifidase具有高特异性并且切割人igg的所有亚类。由于其特定的蛋白酶活性,imlifidase有效地阻止igg的fc介导的效应功能,包括抗体依赖性细胞吞噬作用(adcp)、抗体依赖性细胞毒性(adcc)和补体依赖性细胞毒性(cdc)。
[0137]
本研究的目的是进一步评估imlifidase是否对igm抗体(abs)、尤其是对患有终末期肾病(esrd)的致敏患者中的igm抗体(abs)具有影响,并且确定imlifidase的新用途。
[0138]
材料和方法
[0139]
患有终末期肾病(esrd)的致敏患者的血清样品
[0140]
将纳入临床ii期试验(13-hmedides-02;nct02224820)的患有终末期肾病(esrd)的致敏患者的血清样品进行研究,该血清样品用0.12或0.25mg/kg的imlifidase处理。对给药前和imlifidase给药后24小时的研究样品进行研究。
[0141]
imlifidase的处理
[0142]
将imlifidase(p16-0041701)用于体外处理。
[0143]
sds-page和免疫印迹
[0144]
将imlifidase切割的纯化的人igm(#16-16-090713-m,athens research&technology)或来自esrd致敏患者的血清样品中的人igg和igm以tris-甘氨酸-sds缓冲液中的4-20% mini-protean tgx免染凝胶(bio-rad)在非还原条件下进行分离。将凝胶转移到0.45μm硝酸纤维素膜上并且在5%脱脂牛奶(nfm)中封闭,然后用在pbs-吐温中的pe-缀合的驴抗人igm(#igm-pec1,one lambda)孵育。
[0145]
洗涤膜并且以适合于pe的印迹设置进行分析。使用chemidoc mp系统(bio-rad)来采集信号。
[0146]
使用captureselect亲和介质纯化igg
[0147]
将captureselect
tm igg-ch1亲和介质(#194320005,赛默飞世尔科技)用于血清样品的纯化。captureselect
tm
亲和介质以单个步骤从复杂来源材料中纯化重组人fab片段和igg。亲和介质识别igg的全部四种亚类(igg1、igg2、igg3和igg4),与轻链类型(κ/λ)无关。以sds-page分析血清样品以igg的评估和纯化。
[0148]
用于i类和ii类的单抗原珠hla测定(one lambda/赛默飞世尔)
[0149]
对用0.12或0.25mg/kg imlifidase处理的来自esrd致敏患者的血清样品进行研究。研究了给药前和imlifidase给药后24小时的研究样品。所有血清样品均用edta预处理以克服前带效应。在luminex平台上使用商业单抗原珠(labscreen single antigen,#ls1a04,#ls2a01,one lambda)测试血清的hla i类和ii类抗hla抗体二者。首先将血清与labscreen珠粒孵育30分钟,用洗涤缓冲液洗涤3次。添加藻红蛋白(pe)-缀合的山羊抗人igg或pe-缀合的驴抗人igm并且孵育30分钟,洗涤两次。采用labscan 100分析仪以检测每个珠粒的pe荧光发射。将测试血清的反应模式与定义抗原阵列并指定hla特异性的指定批次工作表(lot-specific worksheet)进行比较。使用hlafusion软件(one lambda)解释结果并表示为平均荧光强度(mfi)。
[0150]
类风湿因子(rf)
[0151]
对esrd致敏患者的血清样品进行类风湿因子(igm-rf)的筛查(labmedicin临床免疫学和输血医学,隆德,瑞典)。
[0152]
免疫球蛋白(ig)类别和igg亚类
[0153]
测量来自两名健康志愿者的血清样品在用captureselect介质纯化前和纯化后的免疫球蛋白类别和igg亚类(labmedicin临床免疫学和输血医学,隆德,瑞典)。
[0154]
结果
[0155]
用imlifidase孵育后未观察到纯化人igm的切割
[0156]
通过在sds-page凝胶上分离测试项目来评估imlifidase切割纯化的人igm的能力。在加热前加入dtt以消化igm,以破坏二硫键(见图1)。在37℃下用高浓度(高达200μg/ml)imlifidase孵育2小时后未观察到纯化的人igm的消化(见图2)。
[0157]
采用captureselect亲和介质成功纯化血清中的igg
[0158]
采用captureselect igg-ch1亲和介质成功地纯化血清样品,并且与未处理的血清样品相比,在sds-page凝胶上未检测到完整的igg条带(参见图3)。
[0159]
imlifidase处理对具有igg特异性的循环抗hla抗体水平有很大影响
[0160]
先前已经发表了imlifase能够切割igg并因而切割供体特异性抗体(dsa),并且使与已故供体具有阳性交叉配型的患者能够接受移植而无需数周的移植前治疗(jordan等人,2017;lonze等人,2018;lorant等人,2018)。
[0161]
对给药前和imlifidase后24小时的来自esrd致敏患者的血清样品进行研究。在这项研究中还可以检测到imlifidase对抗hlaigg抗体的切割。在所有七名患者中均出现i类和ii类的循环抗hla抗体的水平明显降低(参见图4)。
[0162]
imlifidase处理对具有igm特异性的循环抗hla抗体水平没有影响
[0163]
2019年atc会议上提出了,所谓imlifidase能够切割igm并因而切割具有igm特异性的供体特异性抗体(dsa)的能(x.zhang,s.jordan,2019.anti-hla igmantibodies are reduced in highly-hla sensitized patients transplanted after imlifidase(ides)treatment)。
[0164]
对给药前和imlifidase后24小时的用imlifidase处理的来自esrd致敏患者的血清样品进行了研究。在7名患者中的2名患者(对象02-927和对象02-929)中检测到用imlifidase处理后循环抗hla igm抗体的减少(参见图5)。
[0165]
然而,在用captureselect介质纯化(igg耗尽)血清样品时,在用imlifidase处理后未观察到对循环抗hla igm抗体水平的影响(参见图6)。
[0166]
未检测到imlifidase对人igm的切割
[0167]
对纯化的人igm进行滴定(1250至4.8ng/孔)以查看该测定的检测限。在免染sds-page凝胶上分离出dtt还原的人igm。还原的重链位于75kda处,并且利用所使用的设置在低至39ng/孔处可见。转移到硝酸纤维素膜后,在硝酸纤维素膜上使用免染凝胶设置来检查蛋白质的重新定位。封闭膜,并且用pe-缀合的驴抗人igm(one lambda)显色。75kda重链在低至19ng/孔处可见。在最高igm浓度下在约200kda和50kda处也可见一些条带(参见图7)。
[0168]
来自4名致敏esrd患者(02-925、02-927、02-928和02-929)的血清分别用imlifidase和pbs体外处理。将血清样品和纯化的igm进行dtt处理并且在sds-page凝胶上分离,以及转移到硝酸纤维素膜上,封闭并用pe-缀合的驴抗人igm(one lambda)显色。75kda重链条带被清晰染色,并且在用或不用imlifidase处理下均看不出差异(参见图8)。
[0169]
类风湿因子(rf)的测量
[0170]
本次报告所调查的所有血清样品均被诊断为类风湿因子(igm-rf)阴性。
[0171]
captureselect介质纯化后的免疫球蛋白(ig)类别和igg亚类的测量
[0172]
测量在captureselect介质纯化前和纯化后的来自两名健康志愿者的血清样品的免疫球蛋白类别和igg亚类,以确定captureselect igg-ch1亲和介质的纯化是否会影响人血清中ig的组成。结果如表b所示:
[0173][0174]
结论
[0175]
在一些患者中用igg半胱氨酸蛋白酶处理后的抗hla igm信号降低。然而,在igg耗尽的血清中未观察到这种hla-igm信号降低。初始的高抗hla igm信号可能是labscreen hla珠表面上的与igg复合的igm的结果。因此,人igm没有被igg半胱氨酸蛋白酶切割,但是igg复合的igm会干扰用于检测igm的方法,并且可以产生假信号。在用igg半胱氨酸蛋白酶处理后的某些患者中观察到抗hla igm信号的降低,表明igg半胱氨酸蛋白酶能够切割有问题的复合物。
[0176]
zhang等人的摘要(2019,am j transplant.19(suppl 3))声称igg半胱氨酸蛋白酶imlifidase可以降低病理性抗hla igm,在这种情况下,imlifidase将不能用于检测任何抗原特异性igm并且也不能用于治疗由igg与igm的复合物介导的疾病。引人注目的是,现在的研究表明,igg半胱氨酸蛋白酶能够通过切割igg来降低由igg和igm组成的抗原复合物。数据还强调,如果希望确保在检测igm抗体的测定中获得真实的igm信号,则需要耗尽igg的方法,并且使用降解igg的半胱氨酸蛋白酶可以特别适合此目的。同样地,igg半胱氨酸蛋白酶可以对旨在降低由igg与其它ig同种型(例如igm、iga或ige)组成的抗体复合物的治疗有用。
[0177]
实施例2
[0178]
介绍
[0179]
本研究的目的是通过调查是否对esrd致敏患者中的人抗hla igm有任何影响,或
antigen,#ls1a04,批次010,#ls2a01批次012,one lambda,canoga park,ca)测试血清的hla i类和ii类抗hla抗体二者。首先将血清与labscreen珠粒孵育30分钟,然后用洗涤缓冲液洗涤珠粒三次。添加藻红蛋白(pe)-缀合的山羊抗人igg(#ls-ab2,one lambda,canoga park,ca)或pe-缀合的驴抗人igm(#igm-pec1,one lambda,canoga park,ca),并且孵育30分钟,洗涤两次。采用labscan 200分析仪以检测每个珠粒的pe荧光发射。将测试血清的反应模式与定义抗原阵列并指定hla特异性的指定批次工作表进行比较。使用hla fusion软件(版本4.3,one lambda)解释结果并且表示为原始数据的平均荧光强度(mfi)。
[0191]
单抗原珠hla测定的数据分析
[0192]
使用hlafusion 4.3软件(one lambda)中的基线公式来确定每种抗体特异性的平均荧光强度(mfi)值。将3,000的基线mfi阈值用于指定所有报告抗体(igg-pe和igm-pe)的阳性反应。将每个测试血清的基线原始mfi数据传输到microsoft office excel软件(microsoft)电子表格中以分析和比较不同测试条件。
[0193]
类风湿因子(rf)
[0194]
对esrd致敏患者的血清样品进行类风湿因子(igm-rf)的诊断(labmedicin临床免疫学和输血医学,瑞典隆德)。
[0195]
免疫球蛋白(ig)类和igg亚类的分析
[0196]
测量来自两名健康志愿者的血清样品在用captureselect
tm
介质纯化前和纯化后的免疫球蛋白类别和igg亚类(labmedicin临床免疫学和输血医学,隆德,瑞典)。
[0197]
结果
[0198]
imlifidase切割循环抗hla igg抗体
[0199]
对imlifidase处理前和imlifidase处理后24小时的esrd致敏患者(n=7)的血清样品进行研究。证实了imlifidase切割包括抗hla igg抗体在内的igg的能力(图16),如先前研究中确定的(jordan等人,2017;lonze等人,2018;lorant等人,2018;jordan等人,2020,schinstock,2020)。在所有测试患者中观察到循环抗hla igg水平明显降低(图16)。
[0200]
在使用纯血清时用imlifidase处理对抗hla igm sab测定的测定信号具有影响
[0201]
还分析了样品的sab-hla igm(图10)。在经测试的7名患者中的2名患者中,观察到在给药前和imlifidase处理后24小时之间抗hla igm信号的降低(图10e和10g;患者02-927和02-929)。对于患者02-927和02-929,在抗原mfi值上,分别具有平均约26倍(32个抗原)和15倍(7个抗原)的降低。所有这些抗原的共同特征是,对于iggsab-hla测定中的相同抗原,珠粒的相应给药前值的强度非常高(最低为11000mfi)。
[0202]
在患者02-923和02-925(图10b和10c)中,存在一些珠粒在给药后24小时的sab-hla igm测定中增加。对于患者02-923,在含有hla-a抗原和hla-b抗原(13个抗原)的珠粒上观察到增加,平均增加到给药前值的5倍。对于患者02-925,在含有hla-dq抗原(10个抗原)的珠粒上观察到增加,平均增加到给药前值的2倍。igg sab-hla测定珠粒中相同抗原的给药前值非常高(最低为22000mfi),这在珠粒的预期饱和度范围内(通常出现为》20000mfi)(mccaughan等人,2019)。因此,高水平igg的存在可能会对测定中低亲和力igm的可用结合位点的数量产生负面影响。当igg测定中的sab-hla珠粒含量低时,对于给药前和24小时样品之间的igm测定通常几乎没有差异(图17)。
[0203]
纯化的人igm不受imlifidase处理的影响
[0204]
采用sds-page来测试imlifidase是否具有切割纯化的人igm的能力。即使在高达200μg/ml的高浓度下,也没有观察到imlifidase对纯化的人igm的切割(图10a)。相比之下,经过相同处理的人igg在0.2μg/ml下已被切割为scigg,并且在2μg/ml下igg已被完全切割(图10b)。
[0205]
在经imlifidase处理的人血清中无igm切割
[0206]
研究在体外用高浓度imlifidase处理后的来自4名致敏esrd患者(02-925、02-927、02-928和02-929)的血清样品中人igm的切割。在imlifidase处理后,血清样品(和纯化的igm)被还原,在sds-page上分离(图11a),并且使用pe缀合的抗人igm进行蛋白质印迹(图11b)。完整人igm的完整75kda重链带被清晰染色,并且在用或不用imlifidase处理下都看不出强度差异,这清楚地表明血清中的igm在体外没有被imlifidase切割。
[0207]
采用captureselect
tm
亲和介质从血清纯化igg
[0208]
采用captureselect
tm
亲和介质成功地耗尽七名患者的所有血清样品中的igg。与未处理的血清样品相比,在凝胶上没有检测到igg(图4)。根据所使用的临床测定,用于本报告调查的所有血清样品均被诊断为类风湿因子(igm-rf)阴性(analysportalen瑞典隆德)。
[0209]
为了确定captureselect介质主要去除igg而没有去除其它免疫球蛋白,测量血清样品中的igg、iga和igm以及igg亚类。由于此分析需要的血清量,将健康志愿者而不是患者样品与凝胶结合用于作为原理证明(图12)。所有igg亚类均被耗尽为低于检测限。由于该步骤,其它免疫球蛋白类别被减少为其初始值的约50%。
[0210]
imlifidase处理对igg耗尽血清中的抗hla igm抗体没有影响
[0211]
在图1中观察到的给药前和给药后之间的影响在igg耗尽的样品中完全消除(图13)。与耗尽前相比,igg耗尽样品的抗hla igm信号通常较低(~80%)(比较图9和图13),可能是由于耗尽方案中洗涤造成的稀释。对于患者02-925,对于一些hla-dq抗原,在耗尽后观察到与耗尽前相似的模式,即24小时样品与给药前相比增加,但效果降低,增加46%而不是115%。对于患者02-927(图13),与24小时的样品相比,对于给药前的igg耗尽,仍有10种珠粒更高(平均3倍)。这些是在耗尽前具有最多减少的珠粒(图9c),对于这些珠粒,在igg耗尽之前和之后的平均mfi分别为15186和1023。在igg耗尽之前和之后,相同珠粒的24小时样品的mfi是相同的。对于02-929,观察到相同模式,但是珠粒更少。这些珠粒的减少仍然存在,这可能是因为这些igm抗体由于igm抗体对igg而不是对hla有亲和力而与igg共同耗尽。在sab-hla igg/igm测试之前,用imlifidase对血清样品进行体外处理产生与igg耗尽相当的结果(图14)。
[0212]
讨论
[0213]
实施例2中呈现的数据证实了实施例1中的结论。在此研究中评估了imlifidase活性针对igm的特异性。我们可以有信心地得出结论,imlifidase在体外即使在理想条件下在pbs缓冲系统中,也不具有可检测的对igm的活性。
[0214]
此处呈现的数据证明,在sab-hla igm测定中出现的imlifidase处理后igm信号的降低可能是由于因imlifidase处理引起的不真实结果。
[0215]
我们提出的机制是igg-dsa复合的igm与sab-hla珠粒结合(图15)。igm检测抗体识别了复合物中的igm,产生不真实的igm信号。在imlifidase处理后,这些igg-igm复合物将
被切割,sab hla测定中会记录到低得多但真实的igm信号。因此,这些数据证明imlifidase处理在检测igm抗体时的实用性。
[0216]
这种模型得到了我们观察的支持;
[0217]
首先,即使利用非常高浓度的imlifidase,在理想的条件下对人igm也检测不到酶活性;
[0218]
其次,可以明确地将一些患者中不真实结果的出现与igm以及存在特别高的igg dsa水平联系起来。这种结合看上去是假阳性igm信号产生的先决条件,并且在进行测试之前在体外用imlifidase处理给药前患者血清样品后该假阳性信号消失。
[0219]
第三,所有观察到的病例中,在igg耗尽后,给药前样品中的假阳性信号也消失了。此外,这种假阳性igm信号的减少主要出现在sab-igg测定中igg dsa信号水平尤其高的抗原珠上。
[0220]
有趣的是,在使用标准临床测定时,在患者中检测不到rf的存在。
[0221]
由我们的结果清楚的是,imlifidase的酶活性可以有效地溶解igm与igg的复合物。这可以对igg与igm的复合物形成导致自身免疫疾病的症状恶化的患者具有临床意义。
[0222]
有趣的是,与刚刚描述的假阳性信号相反,在某些患者中,尤其是在观察具有高igg信号的抗原珠时,我们还可以观察到imlifidase处理后igm信号的增加。这很可能解释为dsa igg的空间位阻降低,在imlifidase处理后血清ig水平降低后,使得dsa igm现在能够结合并且产生信号。
[0223]
因此,在高iggdsa浓度下,似乎存在在sab-hla igm测试中产生假阳性和假阴性igm dsa信号的风险。在最坏的情况下,这可能会危及医生做出正确临床决定的能力或导致基于不准确数据的决定。
[0224]
igm测定目前在临床决策中很少使用,但是igg sab hla中igg igm聚集体的存在可能以类似的方式潜在地错误增加igg dsa信号,并且结果可能导致这些患者不必要地长时间在等待名单上。
[0225]
一些hla中心实验室采用例如添加edta、热灭活、添加dtt(二硫苏糖醇)和连续稀释的方法来克服前带效应的问题,并且这些方法可以提高sab-hla测定的预测准确性。我们的结果表明,在运行sab-hla测试之前用imlifidase对测试样品体外处理或耗尽igg可以改善某些珠粒上的信号并且降低假阴性结果的风险,同时降低假阳性igm信号的风险。因此,在测试之前用imlifidase对样品进行体外处理可以是提高igm sab-hla测定的准确性和可靠性的潜在新方法。总之,我们已经观察到的imlifidase对igg/igm复合物的影响预计具有临床性用途和诊断性用途。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1