一种生物样品的处理方法与流程
1.本发明属于医药技术领域,涉及一种生物样品的处理方法,具体涉及一种含有小儿消积止咳口服液代表成分及其代谢产物的生物样品处理方法。
背景技术:
2.小儿消积止咳口服液/颗粒由鲁南厚普制药有限公司独家生产,清热肃肺,消积止咳。用于小儿饮食积滞、痰热壅肺所致的咳嗽、夜间加重、喉间痰鸣、腹胀、口臭。成份包括:炒山楂、槟榔、枳实、蜜枇杷叶、瓜蒌、炒莱菔子、炒葶苈子、桔梗、连翘、蝉蜕。方中山楂、槟榔,消食导滞,食积得消,则郁热痰浊无依、生热生痰无源。以枇杷叶、瓜蒌、桔梗、连翘清肺化痰,宣散肺气,痰热消,肺热清,肺气降,则咳嗽自止。葶苈子泻肺平喘,莱菔子消食化积兼降气化痰,蝉蜕清肺热、宣肺热,枳实行气消痰。桔梗除宣散肺气、祛痰止咳外,还能引导诸药直达病所。诸药合用,达到消积化痰,宣肺止咳的功效。
3.小儿消积止咳口服液的质量控制成分为枳实的主成分辛弗林,目前对于口服小儿消积止咳口服液后,辛弗林的体内代谢情况研究较少,特别在幼龄动物体内,还面临采样困难,样品量少的问题。
4.2020年11月26日,iarc在《柳叶刀-肿瘤学》发表了对槟榔主要活性成分—槟榔碱(arecoline)致癌性的主要评估结论,槟榔碱被定为2b类致癌物。鉴于小儿消积止咳口服液中含有槟榔这味药材,对其主要活性成分槟榔碱的吸收入血情况进行考察颇有必要。
5.药物在生物样品处理过程中的稳定性是样品处理过程中的关键。例如槟榔碱在血液中不稳定,2小时后血液内的槟榔碱浓度降低到原来的15%。如何保证在样品处理过程中待测成分保持稳定且不影响测定是急需解决的问题。
技术实现要素:
6.本发明的目的在于提供一种生物样品的处理及测定前预处理的方法,所述的生物样品中含有小儿消积止咳口服液和/或小儿消积止咳颗粒中的质量控制成分(辛弗林)和毒性成分(槟榔碱),以及辛弗林的ⅱ相代谢产物(葡萄糖醛酸结合型辛弗林)和槟榔碱的ⅰ相代谢产物(槟榔次碱)。
7.所述的生物样品包括但不限于血液、胆汁、脏器、尿液、粪便等。
8.本发明所述的生物样品的处理方法为:生物样品采集后用甲酸生理盐水或甲醇作为稳定剂;优选的,所述甲酸生理盐水为0.1%甲酸生理盐水。
9.在进行成分检测时,辛弗林的ⅱ相代谢产物将通过将生物样品酶解后测定总的辛弗林来实现,其他成分通过直接测定生物样品中的游离药物浓度来实现。
10.因此,本发明所述的生物样品的测定前预处理方式为:
11.(1)检测游离成分时,取上述加入稳定剂的生物样品,加入内标液和沉淀溶剂混合,取澄清液体分析;
12.和/或
13.(2)检测总药物浓度时,取上述加入稳定剂的生物样品,加入甲酸生理盐水和酶溶液,混合,温孵后加入内标液和沉淀溶剂,混合,取澄清溶液分析。
14.优选的,测定前处理方法中沉淀溶剂为乙腈;甲酸生理盐水为0.1%甲酸生理盐水。
15.具体的,本发明上述所述的生物样品的处理方法包括如下步骤:
16.1.生物样品处理:血液、胆汁、尿液等生物样品与等体积0.1%甲酸生理盐水或甲醇混合,脏器、粪便等组织取样后立即用相应体积的0.1%甲酸生理盐水或甲醇研磨,离心,取上层澄清液体作为待测液;
17.2.测定前预处理:
18.(1)检测游离成分时,取上述处理后的生物样品,加入内标液和乙腈沉淀液,涡旋混匀,离心,取上清液分析。
19.(2)检测总药物浓度时,取上述处理后的生物样品,加入0.1%甲酸生理盐水和酶溶液,混匀后,37℃温孵至少16h;加入内标液和乙腈沉淀液,涡旋,离心,取上清液进样分析。
20.与现有技术相比,本发明具有以下技术优势:
21.(1)生物样品采出后立即与等体积0.1%甲酸生理盐水混合,保证在样品处理过程中槟榔碱不降解,同时加入的甲酸生理盐水不影响辛弗林和槟榔次碱的测定。
22.(2)本发明采用乙腈为沉淀溶剂,操作简单,耗时较少,且可有效避免沉淀后基质效应较大的问题。
附图说明
23.图1为大鼠空白血浆样品色谱图。
24.图2为实施例2大鼠血浆样品色谱图。
25.注:通道i为总离子流图,通道ii为槟榔次碱色谱峰,通道ⅲ为槟榔碱色谱峰,通道ⅳ为氘代槟榔碱色谱峰,通道
ⅴ
为辛弗林色谱峰,通道ⅵ为[13c,2h3]-辛弗林色谱峰。
具体实施方式
[0026]
为了使本领域技术人员更清楚地了解本发明,申请人对本发明含有小儿消积止咳口服液或小儿消积止咳口服液代表性成分及其代谢产物的生物样品的处理方法进一步描述如下,其中考查的生物样品以大鼠血浆为例,其他生物样品,申请人同样进行了处理方法的摸索,在此不再一一赘述,但本领域技术人员应能知晓,所述的进一步阐述和举例并不以任何方式限定本发明的专利保护范围。
[0027]
实施例1溶液配制
[0028]
(1)内标溶液的配制
[0029]
[13c,2h3]辛弗林储备液的配制:取[13c,2h3]辛弗林标准品一支(1mg),加入1ml甲醇溶解,即配成1000μg/ml的[13c,2h3]辛弗林储备液。
[0030]
[13c,2h3]辛弗林工作液的配制:取[13c,2h3]辛弗林储备液,用80%乙腈水稀释成2000ng/ml浓度的内标工作液。
[0031]
d5-氢溴酸槟榔碱储备液的配制:取d5-氢溴酸槟榔碱标准品一支(5mg),用甲醇溶
解,并转移至10ml容量瓶中定容,即配成500μg/ml的d5-氢溴酸槟榔碱储备液。
[0032]
d5-氢溴酸槟榔碱工作液的配制:取槟榔碱内标储备液,用80%乙腈水稀释成2000ng/ml浓度的内标工作液。
[0033]
[13c,2h3]辛弗林作为游离辛弗林测定的内标,d5-氢溴酸槟榔碱作为槟榔碱和槟榔次碱测定的内标。
[0034]
(2)标准质控溶液的配制
[0035]
辛弗林质控储备液的配制:称取辛弗林标准品,约20mg置于20ml容量瓶中,加甲醇溶解并定容,配成浓度约为1000μg/ml的辛弗林质控储备液。
[0036]
辛弗林的质量计算公式:辛弗林的质量=m
×
99.5%(m为辛弗林标准品的称量量)。
[0037]
槟榔碱质控储备液的配制:称取氢溴酸槟榔碱标准品约30mg置于20ml容量瓶中,加甲醇溶解并定容,配成浓度约为1000μg/ml的槟榔碱质控储备液。
[0038]
槟榔碱的质量计算公式:槟榔碱的质量=m
×
155.19/236.12
×
99.8%(m为氢溴酸槟榔碱标准品的称量量)。
[0039]
槟榔次碱质控储备液的配制:称取槟榔次碱标准品约20mg置于20ml容量瓶中,加甲醇溶解并定容,配成浓度约为1000μg/ml的槟榔碱质控储备液。
[0040]
游离药物混合质控工作液的配制:分别取辛弗林、槟榔碱和槟榔次碱储备液,用80%乙腈做稀释溶媒,梯度稀释至900ng/ml,再把稀释后的标准系列溶液同梯度等比例混合,混合后的工作液浓度为300.0ng/ml。
[0041]
各储备液及工作液置4℃冰箱保存备用。
[0042]
实施例2待测血浆制备
[0043]
1.大鼠锁骨下静脉取空白血液,按照每45μl血液加入5μl工作液比例,加入实施例1制备的游离药物混合质控工作液,再用等体积0.1%甲酸生理盐水稀释血液。血液稀释后室温放置2h,4000g离心10min,取上层澄清血浆,作为待测血浆备用。
[0044]
2.取50μl待测血浆样品,加入5μl实施例1所制备的内标工作液和145μl乙腈沉淀液,涡旋,9600g离心10min,取上清液作为进样溶液。
[0045]
实施例3待测血浆制备
[0046]
1.大鼠锁骨下静脉取空白血液,按照每45μl血液加入5μl工作液比例,加入实施例1制备的游离药物混合质控工作液,再用等体积0.01%甲酸生理盐水稀释血液。血液稀释后室温放置2h,4000g离心10min,取上层澄清血浆,作为待测血浆备用。
[0047]
2.取50μl待测血浆样品,加入5μl实施例1所制备的内标工作液和145μl乙腈沉淀液,涡旋,9600g离心10min,取上清液作为进样溶液。
[0048]
实施例4待测血浆制备
[0049]
1.大鼠锁骨下静脉取空白血液,按照每45μl血液加入5μl工作液比例,加入实施例1制备的游离药物混合质控工作液,再用等体积1.0%甲酸生理盐水稀释血液。血液稀释后室温放置2h,4000g离心10min,取上层澄清血浆,作为待测血浆备用。
[0050]
2.取50μl待测血浆样品,加入5μl实施例1所制备的内标工作液和145μl乙腈沉淀液,涡旋,9600g离心10min,取上清液作为进样溶液。
[0051]
实施例5待测血浆制备
[0052]
1.大鼠锁骨下静脉取空白血液,按照每45μl血液加入5μl工作液比例,加入实施例1制备的游离药物混合质控工作液,再用等体积生理盐水稀释血液。血液稀释后室温放置2h,4000g离心10min,取上层澄清血浆,作为待测血浆备用。
[0053]
2.取50μl待测血浆样品,加入5μl实施例1所制备的内标工作液和145μl乙腈沉淀液,涡旋,9600g离心10min,取上清液作为进样溶液。
[0054]
实施例6小儿消积止咳口服液幼龄大鼠药代动力学预试验
[0055]
取以上实施例2-5所制备的进样溶液,采用超高效液相色谱法-电喷雾离子化串联质谱法即uplc-ms/ms法来检测其中游离辛弗林、槟榔碱、槟榔次碱的浓度。
[0056]
uplc-ms/ms分析条件
[0057]
1.液相色谱条件:
[0058]
色谱柱:hilic柱50mm
×
2.1mm,1.9μm;
[0059]
流动性:a:0.1%甲酸-5mm乙酸铵;b:乙腈,梯度洗脱。0~0.5min 90%b,0.5~2min 90%~50%b,2.0~4.0min 50%b,4.0~5.5min 50%~90%b,5.5~6.0 90%b;
[0060]
流速:200μl/min;
[0061]
柱温:35℃;
[0062]
样品盘温度:8℃;
[0063]
进样体积:3μl。
[0064]
2.质谱条件:各待测物的离子化采用电喷雾离子源,正离子模式。在srm扫描模式下,各待测物质子化的母离子为[m+h]
+
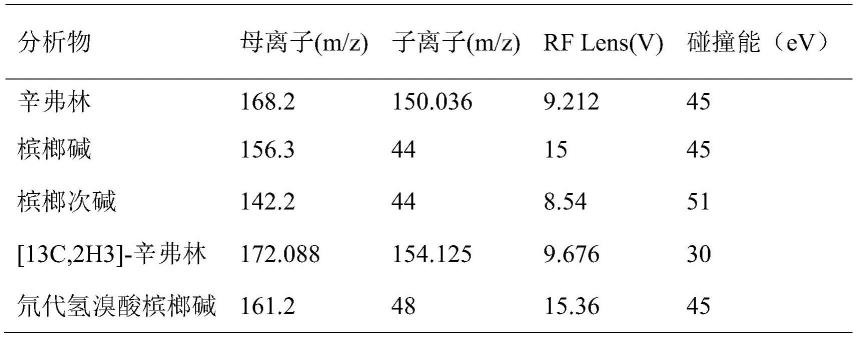
。所用的离子对和碰撞反应条件如下表:
[0065][0066]
离子源:h-esi;喷射电压:4100v;鞘气:35arb;辅助气:10arb;尾吹气:0arb;离子传输毛细管温度:325℃;气化温度:150℃。
[0067]
3.实验结果:
[0068]
实施例2待测血浆中,均可有效检出游离辛弗林、槟榔碱、槟榔次碱,实施例3-5中槟榔碱和槟榔次碱含量较实施例2明显减少,可见其在生物样品制备过程中发生了分解或转化;说明实施例2方法能有效保持槟榔碱和槟榔次碱的稳定还不影响辛弗林的检测。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1