一种全面控制壁虎配方颗粒质量的控制方法与流程
1.本发明涉及药物质量控制方法,特别涉及一种全面控制壁虎配方颗粒质量的控制方 法。
背景技术:
2.壁虎为壁虎科动物无蹼壁虎gekko swinhoana g
ü
enther的干燥全体。壁虎体内含有 多种活性成分,其中含有马蜂毒类似物及蛋白质、维生素、组胺类、核苷类和氨基酸等 (刘妍婕,吴小东,徐寒梅.壁虎药用价值的研究进展.药学进展[j],2015,39(12):915-919)。 其气微臭,味咸;具祛风定惊,散结解毒之功效;主治中风瘫痪,风痰惊痫,瘰疬恶疮 (江苏省食品药品监督管理局.江苏省中药材标准[s].江苏凤凰科学技术出版 社,2016:721-723.)。
[0003]
现代药理作用与临床应用研究表明,壁虎在抗肿瘤(陈建祥,张鸿未.放化疗联合 金龙胶囊治疗恶性肿瘤临床疗效观察[j].浙江医学,2007,29(7):650-652),治疗口 腔溃疡(刘顺勤,刘昌.壁虎粉治疗口腔溃疡疗效观察[j].中国中医药信息杂志,2000, 7(31):53-54)、乳腺增生(彭轶侠,杨普选,宋立夏.壁消散治疗乳腺增生病78例[j].陕 西中医,2001,22(12):722)、乳腺纤维瘤(张长富.乳舒胶囊治疗乳腺纤维瘤117例 [j].陕西中医,2001,22(9):522)、肺结核和淋巴结核(蒋卫健.守百胶囊治疗肺结 核79例临床观察[j].湖南中医杂志,2003,19(3):8)等方面都有较好的疗效。
[0004]
中药配方颗粒是由单味中药饮片经水提、浓缩、干燥、制粒而成,是饮片改革的一 种新形式,相比于传统饮片汤剂具有方便携带,使用简单的特性,能够满足现代快节奏 工作与生活的要求。近年来,中药配方颗粒快速发展,多个中药品种的配方颗粒国家标 准相继出台,为规范中药配方颗粒的生产,推动中药现代化做出了巨大贡献。壁虎配方 颗粒是壁虎饮片经过现代工艺提取、浓缩、干燥、制粒而成,保留了壁虎的临床效果, 同时兼顾了使用的便携性。
[0005]
关于壁虎的质量控制手段目前已有部分报道。包华音等人建立壁虎药材指纹图谱分 析方法,利用page法对药材进行电泳鉴别,将电泳凝胶经凝胶成像系统进行照相处理, 后利用genescope分析软件对电泳谱带进行分析,得到药材的page指纹图谱(包华音. 中药壁虎质量控制关键技术与质量评价体系研究[d].山东中医药大学,2012)。张永太等 人建立壁虎药材的质量标准,分别对壁虎进行薄层鉴别及水分、水溶性浸出物、醇溶性 浸出物、灰分、总多糖成分分析(张永太.中药壁虎质量标准研究[j].亚太传统医 药,2017,13(18):25-27)。田雨晴等人利用hplc方法建立了壁虎药材中核苷类成分的含 量测定方法(田雨晴,刘杨,张宁,等.hplc同时测定不同产地壁虎中8种核苷类成分含 量[j].中药材,2020,43(9):4)。已有的文献资料表明壁虎的质量控制研究主要是集中在 药材上,对于壁虎配方颗粒质量控制的研究较少,如上海市药品监督管理局发布的壁虎 配方颗粒的质量标准所示,建立了壁虎的薄层鉴别,特征图谱,浸出物,含量测定等方 法,使壁虎配方颗粒的质量控制有所依据。
为20℃~30℃;采用紫外检测器。
[0021]
进一步地,所述梯度洗脱如下:
[0022][0023]
进一步地,液相色谱条件为:壁虎配方颗粒特征图谱,供试品溶液色谱中呈现7个 特征峰,并与对照药材参照物色谱中的7个特征峰保留时间相对应,其中峰4、峰7应 与酪氨酸对照品、色氨酸对照品参照物峰保留时间相一致,与酪氨酸参照物相应的峰为 s峰,计算峰1、2、3、5、6与s峰的相对保留时间,其相对保留时间应在规定值的
±ꢀ
10%范围之内,规定值为:0.48(峰1)、0.56(峰2)、0.74(峰3)、1.37(峰5)、 1.50(峰6)。
[0024]
进一步地,薄层板为硅胶g,展开剂为正丁醇-冰醋酸-水(4∶1∶1),显色剂 为茚三酮试液。
[0025]
进一步地,该方法适用于壁虎药材、饮片及其炮制品、制剂中间体或制剂成品。
[0026]
本发明建立了一组快速、全面、专属性强的壁虎配方颗粒质量检测方法,该方法包 括一套薄层鉴别方法,一套液相方法同时进行特征图谱和酪氨酸、色氨酸的含量测定。 较发明较专利cn113960203a和上海公示的壁虎配方颗粒标准,其优势在于:
[0027]
(1)薄层鉴别方法使用对照药材作为参照,对应斑点数更多,符合中药整体质量 控制特性。
[0028]
(2)本发明采用一套色谱方法,实现了壁虎的定性和定量控制。以酪氨酸、色氨 酸为含量指标成分,以壁虎对照药材为参照,建立了含有7个特征峰的特征图谱,指认 了超过半数的特征峰,首次建立了符合壁虎整体性要求的多指标控制手段,相比于现有 方法,更加快捷、全面、有效,更有利于壁虎配方颗粒的质量控制。特征图谱规定了7 个特征峰,多于专利cn113960203a中的6个;指认了4个,超过特征峰的50%,同时 使用对照药材作为参照物,更能体现配方颗粒和药材的一致性。
[0029]
(3)含量测定指标为酪氨酸和色氨酸两个指标,含量较高,相比于喋呤-6-羧酸, 药效也更明确,同时双指标相比于单指标也更能有效控制壁虎配方颗粒的质量标准。本 发明所涉及方法考虑了中药的整体性,对壁虎原料、中间体以及配方颗粒的质量提供技 术控制手段,为其产业化及质量控制提供有力保障。
[0030]
(4)本发明采用超高液相色谱法和薄层色谱法,并对色谱条件进行合理优化,建 立壁虎配方颗粒的特征图谱、含量测定和薄层鉴别方法的有机组合,特征图谱和薄层鉴 别两个属于定性方法,含量测定属于定量方法,能够对主要有效成分进行定量分析,薄 层鉴别操作方便,设备简单,成本较低,可以通过优化展开剂分析不同极性成分,特征 图谱方法依赖于液相设备,人为干扰较少,检测灵敏度较高,主要适合分析中等极性和 低极性成分,两者互相补充.该组方法操作简便,检测时间成本低,为壁虎配方颗粒质量 控制提供新的分析手段。
[0031]
有益效果:本发明方法更加全面的,简单、快捷、有效的壁虎配方颗粒的质量控制 方法,从薄层鉴别,特征图谱,含量测定多个角度进行质量控制,为壁虎配方颗粒的产 业化
虎对照药材;
[0056]
图24不同梯度的分离效果;
[0057]
图25不同提取溶剂的提取效率对比图;
[0058]
图26不同提取方式的提取效率对比图;
[0059]
图27不同提取时间的提取效率对比图;
[0060]
图28不同提取体积的提取效率对比图;
[0061]
图29壁虎配方颗粒专属性试验;
[0062]
图30壁虎配方颗粒整体性试验;
[0063]
图31壁虎配方颗粒专属性试验;
[0064]
图32壁虎配方颗粒的tlc图谱(不同展开剂考察),其中,左:展开剂一;右: 展开剂二,1~2:供试品;s1~s2:对照药材;
[0065]
图33壁虎配方颗粒的tlc图谱(不同供试品制备方法),其中,左:供试品制备 方法一;右:供试品制备方法二,1~2:供试品;s1~s2:对照药材。
具体实施方式
[0066]
本实施例提供了一组全面控制壁虎配方颗粒质量的检测方法,具体内容如下:
[0067]
(1)薄层鉴别:取壁虎配方颗粒0.5g,研细,加水10ml,超声处理30分钟,滤过,滤液作 为供试品溶液。另取壁虎对照药材1g,加水20ml,加热回流30分钟,摇匀,滤过,滤液作为对 照药材溶液。吸取上述两种溶液各5μl,分别点于同一硅胶g薄层板上,以正丁醇-冰醋酸-水 (4∶1∶1)为展开剂,展开,取出,晾干,喷以茚三酮试液,在105℃加热至斑点显色清晰。
[0068]
(2)特征图谱、含量测定:
[0069]
色谱条件参数:以十八烷基硅烷键合硅胶为填充剂(柱长为100mm,内径为2.1mm,粒径为 1.8μm);以乙腈为流动相a,以0.08%磷酸溶液为流动相b,按下表中的规定进行梯度洗脱;流速 为每分钟0.3ml;柱温为25℃;检测波长为220nm。
[0070][0071]
参照物溶液的制备:取壁虎对照药材1g,置具塞锥形瓶中,加入50%甲醇25ml,密塞,超声 处理(功率250w,频率40khz)30分钟,滤过,取续滤液,作为对照药材参照物溶液。另取酪 氨酸对照品、色氨酸对照品适量,精密称定,加水制成每1ml分别含酪氨酸40μg、色氨酸15μg 的溶液,作为对照品参照物溶液。
[0072]
供试品溶液的制备:取壁虎配方颗粒约0.5g,精密称定,置具塞锥形瓶中,精密加入50%甲 醇25ml,密塞,称定重量,超声处理(功率250w,频率40khz)30分钟,放冷,再称定重量, 用50%甲醇补足减失的重量,摇匀,滤过,取续滤液,即得。
[0073]
测定法:分别精密吸取参照物溶液与供试品溶液各1μl,注入液相色谱仪,测定,即得。
[0074]
下面结合实施例对本发明提供的方法进行详细的说明,实施例所描述的具体的实验条件及其 结果仅用于说明本发明,而不应当也不会限制权利要求书中所详细描述的本发明。
[0075]
实施例一壁虎配方颗粒特征图谱方法的建立及其方法学研究
[0076]
1.仪器与试药
[0077]
agilent-1290超高效液相色谱仪,thermo超高效液相色谱仪;kq-250b超声清洗机(昆山超 声仪器有限公司);电子分析天平(梅特勒-托利多仪器(上海)有限公司;控温水浴锅(南通华 泰实验仪器有限公司);hy-4振荡器(金坛市科兴仪器厂);纯水系统(millipore公司);tgl-16c 型离心机(上海安亭科学仪器厂);乙腈(色谱纯,thermo fisher公司);甲醇(色谱纯,thermofisher公司);水为超纯水;其它试剂均为分析纯。
[0078]
壁虎对照药材购自上海鸿永生物科技有限公司,编号220041-202104。
[0079]
酪氨酸(140609-201914)、色氨酸(140686-201303)对照品购自中国食品药品检定研究院.。
[0080]
壁虎配方颗粒由江阴天江药业有限公司提供。
[0081]
2.检测波长的确定
[0082]
取本品适量,研细,取约0.5g,置具塞锥形瓶中,精密加入50%甲醇25ml,密塞,称定重量, 超声处理(功率250w,频率40khz)15分钟,放冷,再称定重量,用50%甲醇补足减失的重量, 摇匀,滤过,取续滤液,即得。采集样品在220nm,254nm和300nm下的色谱图,如图7所示。
[0083]
结果表明,在220nm波长下峰的个数最多,保留的信息也最多,同时参照壁虎标准汤剂特征 图谱,选用220nm作为检测波长。
[0084]
3.色谱条件的优化
[0085]
方法1:以十八烷基硅烷键合硅胶为填充剂(柱长为100mm,内径为2.1mm,粒径为1.8μm); 以乙腈为流动相a,以水为流动相b,按下表规定进行梯度洗脱;流速为每分钟0.3ml;柱温为25℃; 检测波长为220nm。
[0086][0087]
方法2:以十八烷基硅烷键合硅胶为填充剂(柱长为100mm,内径为2.1mm,粒径为1.8μm); 以乙腈为流动相a,以水为流动相b,按下表规定进行梯度洗脱;流速为每分钟0.3ml;柱温为25℃; 检测波长为220nm。
[0088][0089]
[0090]
方法3:以十八烷基硅烷键合硅胶为填充剂(柱长为100mm,内径为2.1mm,粒径为1.8μm); 以乙腈为流动相a,以0.08%磷酸溶液为流动相b,按下表规定进行梯度洗脱;流速为每分钟0.3ml; 柱温为25℃;检测波长为220nm。
[0091][0092]
结果表明(上表、图24),方法3的分离效果最好,峰形对称,保留时间适中,因此,本方 法选择方法3进行后续研究。
[0093]
4.供试品溶液的制备
[0094]
4.1不同提取溶剂的考察
[0095]
取本品适量,研细,取约0.5g,平行5组,精密称定,置具塞锥形瓶中,精密加入水、30% 甲醇、50%甲醇、70%甲醇、甲醇各25ml,密塞,称定重量,分别超声处理(功率250w,频率 40khz)15分钟,放冷,再称定重量,用相应溶剂补足减失的重量,摇匀,滤过,取续滤液,即 得。分别精密吸取各供试液1μl,注入液相色谱仪,按上述色谱条件测定,计算特征峰峰面积/称 样量的比值,结果见表1、图10、25。
[0096]
表1不同提取溶剂的提取效率比较(峰面积/称样量)
[0097][0098]
由上表可以看出:不同浓度甲醇作为提取溶剂,提取效率比较接近,同时考虑到70%及以上 浓度甲醇溶剂化效应较明显,水作为溶剂提取溶液不澄清,过滤较难,因此综合考虑,确定提取 溶剂为50%甲醇。
[0099]
4.2不同提取方法的考察
[0100]
取本品适量,研细,取约0.5g,平行3组,精密称定,置具塞锥形瓶中,精密加入50%甲醇 25ml,密塞,称定重量,分别进行超声处理(功率250w,频率40khz)、振摇提取、加热回流 30分钟,放冷,再称定重量,用50%甲醇补足减失的重量,摇匀,过滤,取续滤液,即得。分
别 精密吸取各供试液1μl,注入液相色谱仪,按上述色谱条件测定,计算特征峰峰面积/称样量,结 果见表2、图11、图27。
[0101]
表2不同提取方式的提取效率比较(峰面积/称样量)
[0102][0103]
由上表可以看出:超声提取和回流提取的提取效率接近,考虑到操作的简便性,因此确定提 取方法为超声处理。
[0104]
4.3不同提取时间的考察
[0105]
取本品适量,研细,取约0.5g,平行4组,精密称定,置具塞锥形瓶中,精密加入50%甲醇 25ml,密塞,称定重量,分别进行超声处理(功率250w,频率40khz)10分钟、15分钟、30分 钟和45分钟,放冷,再称定重量,用50%甲醇补足减失的重量,摇匀,过滤,取续滤液,即得。 分别精密吸取各供试液1μl,注入液相色谱仪,按上述色谱条件测定,计算特征峰峰面积/称样量, 结果见表3、图11、图27。
[0106]
表3不同提取时间的提取效率比较(峰面积/称样量)
[0107][0108]
由上表可以看出:超声处理不同时间,壁虎配方颗粒中特征峰峰面积/称样量差别较小,超声 处理15分钟提取时已较为充分,为确保提取效率,确定提取时间为30分钟。
[0109]
4.4不同提取体积的考察
[0110]
取本品适量,研细,取约0.5g,平行3组,精密称定,置具塞锥形瓶中,精密加入50%甲醇 10ml、25ml、50ml,密塞,称定重量,分别超声处理(功率250w,频率40khz)30分钟,放冷, 再称定重量,用50%甲醇补足减失的重量,摇匀,滤过,取续滤液,即得。分别精密吸取各供试 液1μl,注入液相色谱仪,按上述色谱条件测定,计算特征峰峰面积/称样量*提取体积/25,结果见 表4、图12、图28。
[0111]
表4不同提取体积的提取效率比较(峰面积/称样量*提取体积/25)
[0112][0113]
由上表看出:当提取体积为10ml时,提取不充分,提取体积25ml时,壁虎配方颗粒中特征 峰峰面积/称样量*提取体积/25的值较大,因此确定提取体积为25ml。
[0114]
4.5供试品溶液制备方法的确定
[0115]
根据上述研究结果,确定壁虎配方颗粒特征图谱的供试品溶液制备方法为:
[0116]
取壁虎配方颗粒,研细,取约0.5g,精密称定,置具塞锥形瓶中,精密加入50%甲醇25ml,密塞, 称定重量,超声处理(功率250w,频率40khz)30分钟,放冷,再称定重量,用50%甲醇补足 减失的重量,摇匀,滤过,取续滤液,即得。
[0117]
5.特征图谱方法学研究
[0118]
5.1专属性考察
[0119]
取壁虎配方颗粒供试品溶液、缺壁虎的阴性溶液注入液相色谱仪,结果见下图29。
[0120]
实验结果表明:阴性溶液在供试品溶液色谱图中各特征峰的保留时间处没有色谱峰,说明溶 剂对壁虎配方颗粒的测定无干扰,以本法测定壁虎配方颗粒具有专属性。
[0121]
5.2整体性考察
[0122]
在确定的色谱条件上,延长洗脱时间,考察在既定的色谱条件系统下,是否会残留杂质峰对 后续样品造成影响,结果见下图30。
[0123]
由实验结果可知,延长洗脱时间,无杂质峰,表明该色谱条件基本满足了信息量最大的原则, 对后续样品的分析亦无影响。
[0124]
5.3精密度考察
[0125]
取同一批号样品,按供试品溶液制备方法制备成供试液,连续进样6次,每次1μl,记录其特 征峰保留时间,按照正文要求计算相对保留时间,结果见表5。
[0126]
表5精密度实验结果(相对保留时间)
[0127][0128]
结果表明,各特征峰的相对保留时间的rsd均小于1%,精密度良好。
[0129]
5.4中间精密度考察
[0130]
取同一批号样品,按供试品溶液制备方法制备成供试液,由两个实验员a、b分别按照正文 项下的要求处理3份,分别在agilent、thermo仪器上进样1μl,记录其特征峰保留时间,按照正 文要求计算相对保留时间,结果表6。
[0131]
表6中间精密度考察(相对保留时间)
[0132][0133][0134]
结果表明:样品的特征峰相对保留时间的rsd小于8%,说明不同仪器对相对保留时间有一 定影响,但都在规定的范围内,中间精密度试验良好。
[0135]
5.5稳定性考察
[0136]
取同一批号样品,按供试品溶液制备方法制备成供试液,分别于0、2、4、6、8、12、18、 24小时进样1μl,记录其特征峰保留时间,按照正文要求计算相对保留时间,结果表7。
[0137]
表7稳定性考察(相对保留时间)
[0138][0139]
结果表明,各特征峰的相对保留时间的rsd均小于1%,供试液在24小时内稳定性良好。
[0140]
5.6重复性考察
[0141]
取同一批号样品,平行6组,按供试品溶液制备方法制备成供试液,分别进样1μl,记录其特 征峰保留时间,按照正文要求计算相对保留时间,结果表8。
[0142]
表8重复性试验(相对保留时间)
[0143][0144][0145]
结果表明,方法的重复性试验良好。
[0146]
5.7耐用性考察
[0147]
(1)色谱柱考察
[0148]
取同一批号样品,按正文供试品溶液的制备方法制备供试品溶液,分别采用acclaimtm rslc120 c18(thermo,2.1mm
×
100mm,2.2μm);t3
(agilent,2.1mm
×
100mm,1.6μm);acquityhsst3(waters,2.1
×
100mm,1.8μm)三种色谱柱,分别进样1μl,记录相应色谱图,结果见图14。
[0149]
结果表明:acquityhsst3色谱柱的分离较好,峰形对称,保留时间适中,acclaim
tm
rslc120c18色谱柱和t3色谱柱存在分离度不佳或峰形不佳的现象,由于3种色谱柱色谱图差异较大,因此,壁虎配方颗粒特征图谱检测推荐使用色谱柱为acquityhsst3(waters,2.1
×
100mm,1.8μm)。
[0150]
(2)柱温考察
[0151]
取同一批号样品,按正文供试品溶液的制备方法制备供试品溶液,考察20℃、25℃、30℃三个温度,分别进样1μl,记录其特征峰保留时间,按照正文要求计算相对保留时间,结果见图15、表9柱温考察(相对保留时间)表9。
[0152]
表9柱温考察(相对保留时间)
[0153][0154]
结果表明,柱温在20℃~30℃区间对样品的测定结果比较稳定且均符合方法规定的保留时间要求,耐用性良好
[0155]
(3)流速考察
[0156]
取同一批号样品,按正文供试品溶液的制备方法制备供试品溶液,考察每分钟0.25ml、0.30ml、0.35ml三个流速,分别进样1μl,记录其特征峰保留时间,按照正文要求计算相对保留时间,结果见图15、表10。
[0157]
表10流速考察(相对保留时间)
[0158][0159]
结果表明,流速在0.25ml/min~0.35ml/min区间对样品的测定结果比较稳定且均符合方法规定的保留时间要求,耐用性良好。
[0160]
6.样品测定
[0161]
取3批壁虎配方颗粒样品、17批壁虎药材和饮片,按照正文项下操作,测定结果见下表。
[0162]
表11样品测定结果(相对保留时间)
[0163][0164]
表12 17批壁虎药材样品测定结果(相对保留时间)
[0165][0166][0167]
表13 17批壁虎饮片样品测定结果(相对保留时间)
[0168][0169]
5.1实施例二壁虎配方颗粒含量测定方法的建立及其方法学研究
[0170]
1仪器与试剂
[0171]
thermo超高效液相色谱仪;agilent-1290超高效液相色谱仪;kq-250b超声清洗机(昆山超 声仪器有限公司);电子分析天平(梅特勒-托利多仪器(上海)有限公司);控温水浴锅(南通 华泰实验仪器有限公司);hy-4振荡器(金坛市科兴仪器厂);纯水系统(millipore公司);as165w 型离心机(亚速旺(上海)商贸有限公司);乙腈(色谱纯,thermo fisher公司);甲醇(色谱 纯,thermo fisher公司);磷酸(色谱纯,aladdin公司);水为超纯水;其它试剂均为分析纯。
[0172]
酪氨酸(140609-201914)、色氨酸(140686-201303)对照品均购自中国食品药品检定研究院;
[0173]
壁虎配方颗粒由江阴天江药业有限公司提供。
[0174]
2对照品来源及纯度检查
[0175]
酪氨酸购于中国食品药品检定研究院,编号为140609-201914,供含量测定用,含量以99.9% 计,使用前无须处理。
[0176]
色氨酸购于中国食品药品检定研究院,编号为140686-201303,供含量测定用,含量以99.9% 计,使用前无须处理。
[0177]
3检测波长的确定
[0178]
实验对酪氨酸、色氨酸对照品溶液进行全波长扫描,记录其紫外吸收图,见图8、图9。
[0179]
结果可知,酪氨酸、色氨酸均在220nm左右波长处有较大吸收,因此选择220nm作为
含量测 定的检测波长。
[0180]
4色谱条件的确定
[0181]
参照壁虎特征图谱测定方法,建立了壁虎配方颗粒中酪氨酸、色氨酸的含量测定方法,色谱 条件如下:
[0182]
以十八烷基硅烷键合硅胶为填充剂(柱长为100mm,内径为2.1mm,粒径为1.8μm);以乙 腈为流动相a,以0.08%磷酸溶液为流动相b,按下表中的规定进行梯度洗脱;流速为每分钟0.3ml; 柱温为25℃;检测波长为220nm。
[0183][0184]
5供试品溶液的制备
[0185]
5.1不同提取溶剂的考察
[0186]
取壁虎配方颗粒适量,研细,取约0.5g,平行5组,每组平行2份,精密称定,置具塞锥形 瓶中,精密加入水、30%甲醇、50%甲醇、70%甲醇、甲醇各25ml,密塞,称定重量,分别超声 处理(功率250w,频率40khz)30分钟,放冷,再称定重量,用相应溶剂补足减失的重量,摇 匀,滤过,取续滤液,即得。分别精密吸取各供试液1μl,注入液相色谱仪,计算酪氨酸、色氨酸 含量,结果见图9、表14、表15。
[0187]
表14不同提取溶剂的比较-酪氨酸
[0188][0189]
表15不同提取溶剂的比较-色氨酸
[0190][0191]
结果可知:水、30%甲醇、50%甲醇、70%甲醇提取结果较接近,但考虑到高浓度有机相容易 产生溶剂化效应,水提取溶液不澄清,因此确定提取溶剂为50%甲醇。
[0192]
5.2不同提取方法的考察
[0193]
取壁虎配方颗粒适量,研细,取约0.5g,平行3组,每组平行2份,精密称定,置具塞锥形 瓶中,精密加入50%甲醇25ml,密塞,称定重量,分别进行超声处理(功率250w,频率40khz)、 振摇提取、加热回流30分钟,放冷,再称定重量,用50%甲醇补足减失的重量,摇匀,滤过,取 续滤液,即得。分别精密吸取各供试液1μl,注入液相色谱仪,计算酪氨酸、色氨酸含量,结果见 图10、表16、表17。
[0194]
表16不同提取方法的比较-酪氨酸
[0195][0196]
表17不同提取方法的比较-色氨酸
[0197]
[0198][0199]
结果可知:超声、振摇、加热回流提取效率相当,考虑到操作的方便,因此确定提取方法为 超声处理。
[0200]
5.3不同提取时间的考察
[0201]
取壁虎配方颗粒适量,研细,取约0.5g,平行4组,每组平行2份,精密称定,置具塞锥形 瓶中,精密加入50%甲醇25ml,密塞,称定重量,分别进行超声处理(功率250w,频率40khz) 10分钟、15分钟、30分钟和45分钟,放冷,再称定重量,用50%甲醇补足减失的重量,摇匀, 滤过,取续滤液,即得。分别精密吸取各供试液1μl,注入液相色谱仪,计算酪氨酸、色氨酸含量, 结果见图11、表18、表19。
[0202]
表18不同提取时间的比较-酪氨酸
[0203][0204]
表19不同提取时间的比较-色氨酸
[0205][0206]
结果可知:不同的提取时间对于酪氨酸、色氨酸的含量无明显影响,从提取完全和节省时间 的角度考虑,因此确定提取时间为30分钟。
[0207]
5.4不同提取体积的考察
[0208]
取壁虎配方颗粒适量,研细,取约0.5g,平行3组,每组平行2份,精密称定,置具塞锥形 瓶中,精密加入50%甲醇10ml、25ml、50ml,密塞,称定重量,分别超声处理(功率250w,频 率40khz)30分钟,放冷,再称定重量,用50%甲醇补足减失的重量,摇匀,滤过,取续滤液, 即得。分别精密吸取各供试液1μl,注入液相色谱仪,计算酪氨酸、色氨酸含量,结果见 表20、表21。
[0209]
表20不同提取体积的比较-酪氨酸
[0210]
[0211][0212]
表21不同提取体积的比较-色氨酸
[0213][0214]
结果可知:当提取体积为10ml时,提取不充分,当提取体积为25ml、50ml时,提取效
率相 当,从充分提取与节省溶剂的角度综合考虑,确定提取体积为25ml。
[0215]
经过考察,最终确定壁虎颗粒含量测定的供试品制备方法为:
[0216]
取壁虎配方颗粒适量,研细,取约0.5g,精密称定,置具塞锥形瓶中,精密加入50%甲醇25ml, 密塞,称定重量,超声处理(功率250w,频率40khz)30分钟,放冷,再称定重量,用50%甲 醇补足减失的重量,摇匀,滤过,取续滤液,即得。
[0217]
6方法学验证
[0218]
6.1线性
[0219]
分别精密吸取酪氨酸、色氨酸对照品混合溶液(浓度41.50μg/ml、13.19μg/ml)0.1μl、0.2μl、 0.5μl、1.0μl、1.5μl、2.0μl注入液相色谱仪,按上述色谱条件测定,以峰面积积分值为纵坐标,进 样量(μg)为横坐标,绘制标准曲线,求得色氨酸、酪氨酸回归方程,结果见表22、表23、图 16、图17。
[0220]
表22回归方程
[0221][0222]
表23色氨酸对照品进样重与峰面积关系
[0223][0224]
结果表明:酪氨酸进样量在0.0041500μg~0.0830000μg范围内,色氨酸进样量在0.00131900μg~ 0.0263800μg范围内,进样量与峰面积值呈良好的线性关系。
[0225]
6.2精密度试验
[0226]
6.2.1仪器精密度试验
[0227]
精密吸取供试品溶液,注入液相色谱仪,按上述色谱条件测定,连续进样6次,记录其峰面 积,计算相对标准偏差,结果见下表。
[0228]
表24仪器精密度试验
[0229][0230]
结果表明:仪器精密度试验良好(rsd%≤2.0%)。
[0231]
6.2.2重复性试验
[0232]
取壁虎配方颗粒适量,研细,取约0.5g,精密称定,平行6份,分别按方法供试品溶液制备 方法制成供试品溶液,分别进样1μl,测定色氨酸、酪氨酸的峰面积,计算其含量及rsd,结果 见表25。
[0233]
表25样品的重复性试验结果-酪氨酸
[0234][0235][0236]
表26样品的重复性试验结果-色氨酸
[0237][0238]
结果表明:重复性试验良好(rsd%≤2.0%)。
[0239]
6.2.3中间精密度试验
[0240]
取壁虎配方颗粒适量,研细,取约0.5g,由两个实验员a、b分别按照上述要求处理3份, 分别在thermo-uplc、agilent-uplc上进样1μl,测定色氨酸、酪氨酸峰面积值并计算其含量及 rsd,结果见表27。
[0241]
表27中间精密度试验-酪氨酸
[0242][0243]
[0244]
表28中间精密度试验-色氨酸
[0245][0246]
结果表明:中间精密度良好。
[0247]
6.3准确度试验
[0248]
取三组已知含量的样品(酪氨酸含量2.16mg/g,色氨酸含量0.85mg/g)适量,研细,取约0.25g, 平行3份,精密称定,分别加入0.25g样品所含各成分的50%、100%、150%的对照品。按上述供 试品溶液制备方法制成加样回收供试品溶液,分别进样1μl,以下列公式计算回收率,平均回收率, rsd,结果见表29,表30。
[0249][0250]
表29酪氨酸准确度结果
[0251]
[0252][0253]
表30色氨酸准确度结果
[0254]
[0255][0256]
结果表明:酪氨酸回收率在99.14%~104.61%之间,色氨酸回收率在98.09%~100.58%之间, 准确度试验结果良好。
[0257]
6.4专属性试验
[0258]
壁虎配方颗粒中所添加的辅料为乳糖和二氧化硅及硬脂酸镁。本次实验考察缺壁虎的阴性样 品对壁虎配方颗粒含量测定的影响。取缺壁虎的阴性样品按供试品制备方法制备阴性样品溶液。
[0259]
取壁虎配方颗粒供试品溶液、阴性对照溶液与酪氨酸、色氨酸对照品溶液注入液相色谱仪。
[0260]
实验结果表明(图1):阴性色谱图中在与对照品相应的保留时间处没有色谱峰,说明辅料 及溶剂对酪氨酸、色氨酸的测定无干扰,以本法测定壁虎配方颗粒中酪氨酸、色氨酸的含量具有 专属性。
[0261]
6.5整体性试验
[0262]
在确定的色谱条件上,保持乙腈比例最高时的洗脱梯度,洗脱时间延长一倍,考察在既定的 色谱条件系统下,是否会残留杂质峰对后续样品造成影响,结果见图31。
[0263]
由实验结果可知,延长洗脱时间一倍,无杂质峰,表明该色谱条件基本满足了信息量最大的 原则,对后续样品的分析亦无影响。
[0264]
6.6耐用性试验
[0265]
6.6.1稳定性试验
[0266]
取壁虎配方颗粒,按上述供试品溶液的制备方法制备供试品溶液,分别于0、2、4、6、8、 12、18、24小时进样1μl,测定峰面积值,计算其rsd。
[0267]
表31稳定性试验测定结果
[0268]
[0269][0270]
结果表明:样品供试液在24小时内稳定性良好。
[0271]
6.6.2不同流速考察
[0272]
取壁虎配方颗粒,按上述供试品溶液的制备方法制备供试品溶液,考察0.25ml/min、 0.30ml/min、0.35ml/min流速下酪氨酸、色氨酸含量,结果见图16、表32、表33。
[0273]
表32不同流速考察
[0274][0275]
表33不同流速考察
[0276][0277]
结果表明:三种流速下,酪氨酸、色氨酸色谱峰的分离度均较好,含量相近,耐用性较好。
[0278]
6.6.3不同柱温的考察
[0279]
取壁虎配方颗粒,按上述供试品溶液的制备方法制备供试品溶液,考察20℃、25
℃、30℃三 个温度下酪氨酸、色氨酸含量,结果见图15、表34、表35。
[0280]
表34不同柱温的考察-酪氨酸
[0281][0282]
表35不同柱温的考察-色氨酸
[0283][0284]
结果表明:三种柱温下,酪氨酸、色氨酸色谱峰的分离度均较好,含量相近,耐用性较好。
[0285]
6.6.4色谱柱考察
[0286]
取壁虎配方颗粒,按上述供试品溶液的制备方法制备供试品溶液,分别考察acclaimtm rslc120 c18(thermo,2.1mm
×
100mm,2.2μm);t3(waters,2.1mm
×
100mm, 1.6μm);acquityhss t3(waters,2.1
×
100mm,1.8μm)3种不同色谱柱条件下壁虎 配方颗粒中酪氨酸、色氨酸的含量,结果见图14、表36、表37。
[0287]
表36不同色谱柱的比较-酪氨酸
[0288][0289]
表37不同色谱柱的比较-色氨酸
[0290]
[0291][0292]
结果表明:不同色谱柱对酪氨酸、色氨酸含量测定影响不大,考虑到壁虎含量测定和特征图 谱使用同一方法,因此,壁虎配方颗粒含量测定推荐使用色谱柱为acquityhss t3 (waters,2.1
×
100mm,1.8μm).
[0293]
7.样品测定
[0294]
取3批壁虎配方颗粒,17批壁虎药材和饮片,按上述供试品溶液的制备方法制备供试品溶液 供试液,测定样品中酪氨酸、色氨酸的含量,实验结果见表38,表39,表40。
[0295]
表38壁虎配方颗粒中酪氨酸、色氨酸的含量测定
[0296][0297]
表39壁虎药材中酪氨酸、色氨酸的含量测定
[0298][0299]
表40壁虎饮片中酪氨酸、色氨酸的含量测定
[0300]
[0301][0302]
5.3实施例三壁虎配方颗粒薄层鉴别方法的建立及其方法学研究
[0303]
1仪器与试药
[0304]
仪器:薄层自动成像仪(camag tlc visualizer)、me204e万分之一天平(梅特勒-托 利多)、万分之一天平(梅特勒-托利多)、kq-250e型超声清洗器(昆山超声电子有限公司)、 电子调温电炉(江阴市保利科研器械有限公司)、gkc114控温水浴锅(南通华泰实验仪器有限 公司)。
[0305]
试药:甲醇(国药集团化学试剂有限公司)、无水乙醇(国药集团化学试剂有限公司)、正 丁醇(国药集团化学试剂有限公司)、冰醋酸(国药集团化学试剂有限公司);硅胶g薄层板(青 岛海洋化工厂、青岛康业鑫药用硅胶干燥剂有限公司、烟台市化学工业研究所)。
[0306]
壁虎对照药材(批号:220041-202104)购于上海鸿永生物科技有限公司。
[0307]
壁虎配方颗粒由江阴天江药业有限公司提供。
[0308]
2薄层鉴别条件
[0309]
展开剂一:采用硅胶g薄层板,以正丁醇-冰醋酸-水(4∶1∶1)为展开剂,展开,取出, 晾干,喷以茚三酮试液,在105℃加热至斑点显色清晰。
[0310]
展开剂二:采用硅胶g薄层板,以无水乙醇-水(6∶1)为展开剂,展开,取出,晾干,喷 以茚三酮试液,在105℃加热至斑点显色清晰。
[0311]
3溶液的制备
[0312]
3.1供试品溶液的制备
[0313]
方法一:取本品0.5g,研细,加水10ml,超声处理30分钟,作为供试品溶液。
[0314]
方法二:取本品0.5g,研细,加30%甲醇10ml,超声处理30分钟,作为供试品溶液。
[0315]
3.2对照药材溶液的制备
[0316]
方法一:取壁虎对照药材1g,加水20ml,加热回流30分钟,滤过,滤液作为对照药材溶液。
[0317]
方法二:取壁虎对照药材1g,加30%甲醇20ml,加热回流30分钟,滤过,滤液作为对照药 材溶液。
[0318]
3.3阴性对照溶液的制备
[0319]
取壁虎颗粒的阴性样品0.5g,同“3.1方法一”制成阴性对照溶液。
[0320]
4薄层鉴别方法的确定
[0321]
4.1不同展开剂的考察
[0322]
取壁虎配方颗粒按供试品溶液的制备方法一制成供试品溶液,另取壁虎对照药材按对照药材 溶液的制备方法一制成对照药材溶液,分别点样于硅胶g薄层板上,按上述两种展开剂,分别展 开,取出,晾干,喷以茚三酮试液,在105℃加热至斑点显色清晰。结果如下图32。
[0323]
由图可见,采用展开剂一,斑点清晰且分离效果较好;而展开剂二的色谱斑点拖尾。经过综 合考虑,选择展开剂一作为壁虎配方颗粒的薄层色谱的展开剂。
[0324]
4.2供试品溶液和对照药材溶液制备方法的考察
[0325]
取壁虎配方颗粒按上述两种供试品溶液的制备方法制成供试品溶液,另取壁虎对照药材按上 述两种对照药材溶液的制备方法制成相应的对照药材溶液,分别点样于硅胶g薄层板上,按上述 确定的薄层色谱展开剂展开,取出,晾干,喷以茚三酮试液,在105℃加热至斑点显色清晰。结 果如下图33。
[0326]
由图可见,两种供试品处理方法的供试品溶液,斑点均较清晰,同时考虑到溶剂的安全性问 题,所以选择方法一作为供试品的制备方法,同时采用方法一制备的对照药材溶液,色谱斑点也 较为清晰,且与供试品色谱主斑点一一对应,所以选择方法一作为该薄层鉴别的对照药材处理方 法。
[0327]
4.3不同点样量的考察
[0328]
取壁虎配方颗粒和壁虎对照药材,分别按确定的制备方法制成供试品溶液和对照药材溶液, 按正文薄层色谱条件,分别以不同点样量点样于同一硅胶g薄层板上,以正丁醇一冰醋酸一水(4 ∶1∶1)为展开剂,展开,取出,晾干,喷以茚三酮试液,在105℃加热至斑点显色清晰,置日 光下检视。结果见图19。
[0329]
由图可见,当供试品溶液点样量为1~8μl、对照药材溶液点样量为3~8μl,供试品色谱中与对 照药材色谱相应位置上荧光斑点清晰对应,无其他干扰,因此考虑到不同批次的样品之间的差异, 因此选择供试品溶液与对照药材溶液的的点样量均为5μl。
[0330]
5薄层鉴别方法的确定
[0331]
根据上述研究结果,确定壁虎配方颗粒的薄层鉴别方法为:
[0332]
取本品0.5g,研细,加水10ml,超声处理30分钟,滤过,滤液作为供试品溶液。另取壁虎 对照药材1g,加水20ml,加热回流30分钟,摇匀,滤过,滤液作为对照药材溶液。吸取上述两 种溶液各5ul,分别点于同一硅胶g薄层板上,以正丁醇-冰醋酸-水(4∶1∶1)为展开剂,展 开,取出,晾干,喷以茚三酮试液,在105℃加热至斑点显色清晰。供试品色谱中,在与对照药 材色谱相应的位置上,显相同颜色的斑点。
[0333]
6方法学验证
[0334]
6.1样品的专属性实验
[0335]
取壁虎配方颗粒供试品溶液、对照药材溶液、阴性对照溶液,分别点样于同一硅胶g薄层板 上,以正丁醇-冰醋酸-水(4∶1∶1)为展开剂,展开,取出,晾干,喷以茚三酮试液,在105℃ 加热至斑点显色清晰,置日光下检视。结果见。
[0336]
由图可见,壁虎配方颗粒供试品色谱与对照药材色谱在相应位置上显相同颜色的斑点,且阴 性对照无干扰,说明该薄层鉴别方法专属性好。
[0337]
6.2耐用性试验
[0338]
6.2.1不同温度的考察
[0339]
取供试品溶液、对照药材溶液,分别在常温、低温和高温条件下,在同一硅胶g薄层板上, 以正丁醇-冰醋酸-水(4∶1∶1)为展开剂,展开,取出,晾干,喷以茚三酮试液,在105℃加 热至斑点显色清晰,置日光下检视。结果见图21。
[0340]
由图可见,不同温度条件下,壁虎配方颗粒供试品色谱与对照药材色谱的相应位置上显相同 颜色的斑点,且分离效果都较好。实验结果表明,温度对壁虎配方颗粒薄层鉴别无影响,说明该 薄层鉴别方法对不同温度的耐用性好。
[0341]
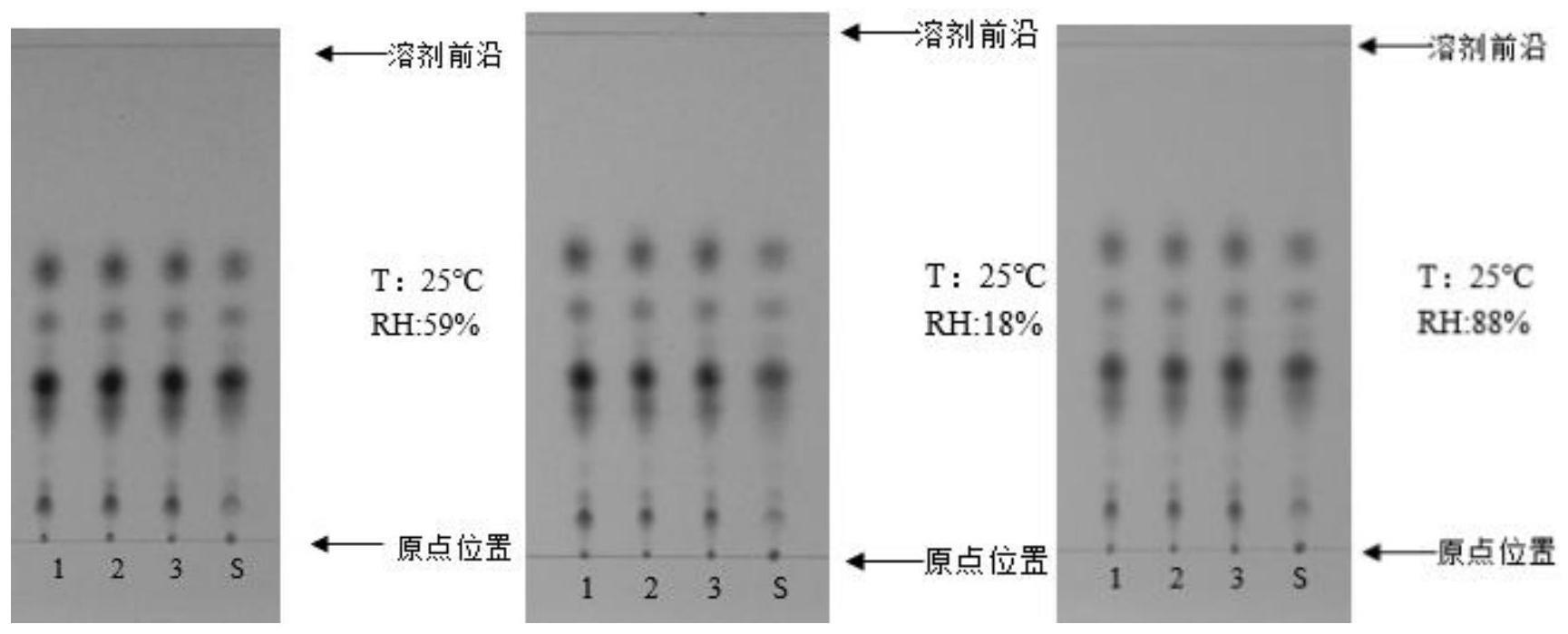
6.2.2不同湿度的考察
[0342]
取供试品溶液、对照药材溶液,分别在不同湿度条件下,于同一硅胶g薄层板上,以正丁醇
ꢀ‑
冰醋酸-水(4∶1∶1)为展开剂,展开,取出,晾干,喷以茚三酮试液,在105℃加热至斑点 显色清晰,置日光下检视。结果见图22。
[0343]
由图可见,不同湿度条件下,壁虎配方颗粒供试品色谱与对照药材色谱在相应位置上显相同 颜色的斑点,且均达到基本分离。实验结果表明,湿度对壁虎方颗粒薄层鉴别无影响,说明该薄 层鉴别方法对不同湿度的耐用性好。
[0344]
6.2.3不同品牌薄层板的考察
[0345]
取供试品溶液、对照药材溶液,在不同品牌硅胶g薄层板上分别点样,以正丁醇-冰醋酸
‑ꢀ
水(4∶1∶1)为展开剂,展开,取出,晾干,喷以茚三酮试液,在105℃加热至斑点显色清晰, 置日光下检视。结果见图23。
[0346]
由图可见,不同品牌硅胶g板中,壁虎配方颗粒供试品色谱与对照药材色谱的相应位置上显 相同颜色的斑点,且斑点分离度均较好。实验结果表明,不同品牌硅胶g板对壁虎配方颗粒薄层 鉴别结果无影响,说明该薄层鉴别方法对不同薄层板的耐用性好。
[0347]
7样品检测
[0348]
根据上述确定的薄层色谱条件,取不同批次的壁虎配方颗粒,按供试品溶液的制备方法,制 成供试品溶液,分别点样于同一硅胶g薄层板上,以正丁醇-冰醋酸-水(4∶1∶1)为展开剂, 展开,取出,晾干,喷以茚三酮试液,在105℃加热至斑点显色清晰,置日光下检视。结果见图24。
[0349]
由图可见,壁虎配方颗粒色谱与对照药材色谱在相应的位置上显相同颜色的斑点。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1