EDA-A2蛋白作为结直肠癌血清生物标志物的应用
eda-a2蛋白作为结直肠癌血清生物标志物的应用
技术领域
1.本技术涉及一种eda-a2蛋白作为结直肠癌血清生物标志物的应用。
背景技术:
2.目前,结直肠癌筛查的方式主要为肠镜、ct检查、磁共振检查等。其中肠镜是临床上常用的结直肠癌筛查方式,通过肠镜可以明确了解结直肠肠壁的情况,同时配合对病变部位进行的病理活检可以明确诊断。但是肠镜检查需要专业的仪器设备和专门的操作人员,且费用贵,检查前要求多。而ct检查存在射线,磁共振检查价格较高,且对于早期体积较小的肿瘤容易漏诊,因此,ct和磁共振检查不适用于反复检查和人群普查。此外,还有一些其他筛查结直肠癌的方法,如癌胚抗原(cea)、ca199、ca724、ca125等,但由于其假阳性率高、灵敏度低,目前仍需进一步研究。
3.血清肿瘤标志物是指伴随肿瘤出现,含量增加的糖类抗原、激素、受体、酶或代谢产物形式的蛋白质、癌基因、抑癌基因及其相关产物。这些成分由肿瘤细胞产生和分泌到血清中而被检测到,能在一定程度上反映体内肿瘤的存在。这些标志物可以用于癌症的筛查、诊断和预后监测。临床上用于结直肠癌诊断的生物标志物缺乏,尤其是非侵入性的生物标志物的发现意义重大。
技术实现要素:
4.本技术的目的在于提供一种eda-a2蛋白作为结直肠癌血清生物标志物的应用。
5.本技术的目的是通过以下技术方案实现的:
6.一种eda-a2蛋白作为结直肠癌血清生物标志物用于非诊断目的的结直肠癌判断。
7.一种结直肠癌血清生物标志物,包括eda-a2蛋白。
8.上述eda-a2蛋白为人的eda-a2蛋白。
9.一种结直肠癌血清生物标志物试剂盒,用于检测上述的结直肠癌血清生物标志物,包括eda-a2蛋白的免疫球蛋白g抗体。
10.上述结直肠癌血清生物标志物试剂盒,还包括定量芯片、样品稀释液、20
×
洗液i、20
×
洗液ii、标准品混合物、cy3-链霉亲和素、玻片清洗和干燥器、密封条。
11.一种如权利上述的结直肠癌血清生物标志物的检测方法,包括以下步骤:
12.a)获取血清样本;
13.b)检测血清样本
14.b1)定量芯片干燥
15.将定量芯片从盒子中取出来,在室温放置20-30min后,将包装袋打开,揭开密封条,然后将定量芯片放在干燥器或者室温干燥1-2小时;
16.b2)标准品的配置
17.b21)添加500μl的样品稀释液到标准品混合物的小管中,重新溶解标准品混合物。打开小管前,先快速的离心,轻轻的上下吹打溶解粉末,标记这个小管为std 1;
18.b22)分别标记6个干净的离心管为std2、std3、std4、std5、std6、std7,添加200μl的样品稀释液到每个离心管中;
19.b23)从标记为std 1的离心管中抽取100μl样品稀释液加入到标记为std2的离心管中轻轻混合,然后从标记为std 2的离心管中抽取100μl样品稀释液加入到标记为std 3的离心管中,依次类推,如此梯度稀释至标记为std7的离心管中,得到标准液;
20.b24)从标记为std7的离心管中抽取100μl的标准液到另一个新的离心管中,标记为cntrl,作为阴性对照;
21.b3)定量芯片的操作流程
22.b31)在定量芯片的每个孔中加入100μl的样品稀释液,室温摇床上孵育1h,封闭定量芯片;
23.b32)、抽去每个孔中的样品稀释液,从标记为cntrl的离心管中取80μl的标准液与血清样本一起添加到孔中,4℃过夜孵育;
24.b33)清洗定量芯片,首先用1
×
洗液i进行清洗,每孔250μl的1
×
洗液i,清洗10次,每次震荡10s,震荡强度选择高,用去离子水稀释20
×
洗液i,然后换用1
×
洗液ii对通道进行清洗,每孔250μl的1
×
洗液ii,清洗6次,每次震荡10s,震荡强度选择高,用去离子水稀释20
×
洗液ii;
25.b34)eda-a2蛋白的免疫球蛋白g抗体的孵育,离心装有eda-a2蛋白的免疫球蛋白g抗体的小管,然后加入1.4ml的样品稀释液,混合均匀后再次快速离心,然后添加80μl的eda-a2蛋白的免疫球蛋白g抗体到每个孔中,rt摇床上孵育2小时;
26.b35)清洗,同步骤b33);
27.b36)cy3-链霉亲和素的孵育,离心装有cy3-链霉亲和素的小管,然后加入1.4ml的样品稀释液,混合均匀后再次快速离心,添加80μl的cy3-链霉亲和素到每个孔中,用铝箔纸包住定量芯片避光孵育,rt摇床上孵育1个小时;
28.b37)清洗,同步骤b33);
29.b38)荧光检测,采用激光扫描仪扫描信号,采用cy3或者绿色通道;
30.b39)采用qah-cust的数据分析软件来进行数据分析,获得每例血清样本中eda-a2蛋白的含量。
31.本技术的可选方案既可以作为独立的方案,也可以相互组合。本技术的任意一个方案中的结构,既可以作为独立的技术方案,也可以与其他技术方案相互组合。
32.本技术的有益之处在于:提供了一种eda-a2蛋白作为结直肠癌血清生物标志物的应用,用于非诊断目的的结直肠癌判断中,提高了结直肠癌血清筛查的灵敏度和特异度。
附图说明
33.图1为本技术实施例1中各类样本中eda-a2蛋白含量及差异性;
34.图2为本技术实施例1中健康-晚期结直肠癌患者eda-a2蛋白的roc曲线。
具体实施方式
35.本技术所用的术语“roc曲线”或“roc图”是指展示二元分类器系统的性能随着其辨别阈值的变化的图形曲线。通过在各种阈值设置下绘制真阳性率对假阳性率的曲线来创
建该曲线。真阳性率也被称为灵敏度。假阳性率计算为1-特异性。因此,roc曲线是一系列截断值范围内的真阳性率对假阳性率(灵敏度vs(1-特异性))的图形显示以及选择最佳截断值进行临床使用的方式。将准确度表示为roc曲线下面积(auc),为比较测试性能提供了有用的参数。接近1的auc表示该测试高度灵敏并且具有高度特异性,而auc接近0.5则表明该测试既不灵敏也不具有特异性。
36.当涉及测试样品与对照样品或参考样品之间的差异时,术语“统计学差异”或“统计学意义”涉及在使用适当的统计分析时,各组相同的概率小于5%(例如p《0.05)的情况。换句话说,在完全随机基础上获得相同结果的概率在100次尝试中少于5次。本领域技术人员知道如何选择适当的统计分析。典型地,基于所研究的变量是否具有正态分布(例如通过用kolmogorov-smirnov检验)和是否存在同方差性(例如用levene检验)来确定适当的统计分析。优选地,在存在正态分布和同方差性的情况下,使用参数模型比如t检验或anova检验;并且在这两个要求中的至少一个要求未达到的情况下,通常使用非参数模型,比如mannwhitney u检验或kruskal-wallis检验。
37.本技术中的eda-a2(又称ectodysplasin a,eda)基因编码的蛋白质是一种ii型膜蛋白,可以被弗林蛋白酶切割以产生分泌形式。编码的蛋白质属于肿瘤坏死因子家族,作为同源三聚体,可能在外胚层器官发育过程中参与细胞间信号传导。该基因的缺陷是导致外胚层发育不良、无汗性的原因,也称为x连锁少汗性外胚层发育不良。已经为该基因发现了编码许多不同同种型的几种转录变体。
38.下面参照附图,对本技术的优选方式详细地进行说明,为了使本技术领域的人员更好的理解本技术方案,下面将结合本技术实施例中的附图,对本技术中实施例中的技术方案进行清楚、完整的描述。以下实施例仅用于说明本发明而不用于限制本发明的范围。实施例中未注明具体条件的实验方法,通常按照常规条件,或按照制造厂商所建议的条件。
39.实施例1:
40.一、获取血清样本
41.通过招募的方式,获得总合计71例受试者血清样本,其中健康人(hc)39例,结直肠癌(ccr)32例
42.二、血清检测
43.本实施例中,使用qah-cust试剂盒对每例受试者的血清样本进行检测,以获得每例血清样本中的eda-a2蛋白含量,该qah-cust试剂盒包括定量芯片(quantibodyarxax glass chip)、样品稀释液(sample diluent)、20
×
洗液i(20x wash buffer i)、20
×
洗液ii(20x wash buffer ii)、标准品混合物(lyophilized cytokine standard mix*)、eda-a2蛋白的免疫球蛋白g抗体(detection antibody)、cy3-链霉亲和素(cy3equivalent dye-conjugated streptavidin)、玻片清洗和干燥器(slide washer/dryer)、密封条(adhesive device sealer);具体的检测方法包括如下步骤:
44.s1、定量芯片干燥
45.将定量芯片从盒子中取出来,在室温放置20-30min后,将包装袋打开,揭开密封条,然后将定量芯片放在干燥器或者室温干燥1-2小时。
46.s2、标准品的配置
47.s21、添加500μl的样品稀释液到标准品混合物的小管中,重新溶解标准品混合物。
打开小管前,先快速的离心,轻轻的上下吹打溶解粉末,标记这个小管为std 1。
48.s22、分别标记6个干净的离心管为std2、std3、std4、std5、std6、std7,添加200μl的样品稀释液到每个离心管中。
49.s23、从标记为std 1的离心管中抽取100μl样品稀释液加入到标记为std2的离心管中轻轻混合,然后从标记为std 2的离心管中抽取100μl样品稀释液加入到标记为std 3的离心管中,依次类推,如此梯度稀释至标记为std7的离心管中,得到标准液。
50.s24、从标记为std7的离心管中抽取100μl的标准液到另一个新的离心管中,标记为cntrl,作为阴性对照。
51.s3、定量芯片的操作流程
52.s31、在定量芯片的每个孔中加入100μl的样品稀释液,室温摇床上孵育1h,封闭定量芯片。
53.s32、抽去每个孔中的样品稀释液,从标记为cntrl的离心管中取80μl的标准液与血清样本(样本2倍稀释上样)一起添加到孔中,4℃过夜孵育。
54.s33、清洗定量芯片(玻片),本实施例中使用thermo scientific wellwash versa芯片洗板机,分为两步,首先用1
×
洗液i进行清洗,每孔250μl的1
×
洗液i,清洗10次,每次震荡10s,震荡强度选择高,用去离子水稀释20
×
洗液i。然后换用1
×
洗液ii对通道进行清洗,每孔250μl的1
×
洗液ii,清洗6次,每次震荡10s,震荡强度选择高,用去离子水稀释20
×
洗液ii。
55.s34、eda-a2蛋白的免疫球蛋白g抗体的孵育
56.离心装有eda-a2蛋白的免疫球蛋白g抗体的小管,然后加入1.4ml的样品稀释液,混合均匀后再次快速离心,然后添加80μl的eda-a2蛋白的免疫球蛋白g抗体到每个孔中,rt摇床上孵育2小时。
57.s35、清洗,同步骤s33。
58.s36、cy3-链霉亲和素的孵育
59.离心装有cy3-链霉亲和素的小管,然后加入1.4ml的样品稀释液,混合均匀后再次快速离心,添加80μl的cy3-链霉亲和素到每个孔中,用铝箔纸包住定量芯片(玻片)避光孵育,rt摇床上孵育1个小时。
60.s37、清洗,同步骤s33。
61.s38、荧光检测
62.采用激光扫描仪扫描信号,采用cy3或者绿色通道(激发频率=532nm)
63.本实施例中采用的是innoscan 300,仪器型号:innoscan 300microarray scanner;厂家:innopsys;产地:parcd'activit
é
sactivestre;31 390carbonne
–
france;扫描参数:wavelengh:532nm;resolution:10μm。
64.s39、采用qah-cust的数据分析软件来进行数据分析,获得每例血清样本中eda-a2蛋白的含量。
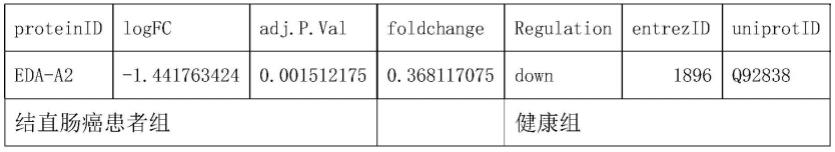
65.三、实验结果
66.foldchange(fc):表达差异倍数,即两组结果比值;
67.logfc:表达差异倍数,以2为底;
68.regulation:up上调;down下调;
69.entrezid uniprotid:蛋白编号;具体数据如表1所示,
70.表1
[0071][0072]
[0073][0074]
如图1所示,结直肠癌组中eda-a2蛋白的水平升高,并与其他组别之间有统计学意义(其中,图1中健康组与结直肠癌组之间的“**”表示统计学差异p值小于0.01),进一步对数据进行分析,roc曲线(receiver operating characteristic curve,受试者工作特征曲线)所获得结果如图2所示,结直肠癌患者的eda-a2蛋白的auc(area under roc curve,auc值为roc曲线所覆盖的区域面积,auc越大,区分两组效果越好)值为0.708。
[0075]
本技术的任意实施例既可以作为独立的技术方案,也可以跟其他实施例相互组合。本技术说明书中提到的所有专利和出版物都表示这些是本领域的公开技术,本技术可以使用。这里所引用的所有专利和出版物都被同样列在参考文献中,跟每一个出版物具体的单独被参考引用一样。这里的本技术可以在缺乏任何一种元素或多种元素,一种限制或多种限制的情况下实现,这里这种限制没有特别说明。这里采用的术语和表达方式所为描述方式,而不受其限制,这里也没有任何意图来指明此书描述的这些术语和解释排除了任何等同的特征,但是可以知道,可以在本技术和权利要求的范围内做任何合适的改变或修改。可以理解,本技术所描述的实施例子都是一些在一些实施例中实施例子和特点,任何本领域的一般技术人员都可以根据本技术描述的精髓下做一些更改和变化,这些更改和变化也被认为属于本技术的范围和独立权利要求以及附属权利要求所限制的范围内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1