光学超振激发和阵列探测接收的超分辨显微方法及系统与流程
1.本发明属于光学显微成像技术领域,尤其涉及一种集成光学超振激发和阵列探测接收的超分辨显微方法及系统。
背景技术:
2.细胞是地球上所有生物的最小单位,具有非常精巧、复杂的功能单元。通过显微成像技术解析细胞的精细结构和运作机理,这对促进细胞生物学、肿瘤细胞学等发展具有非常重要的作用。超分辨显微技术可以突破衍射极限的约束,为人们在分子水平探索细胞的生命信息提供新的机会。特别是,为了在分子水平研究活细胞的内部结构和功能,急需发展具备长时程、多色、快速、三维和超分辨性能的超分辨显微成像技术。
3.然而,现有基于荧光非线性效应的超分辨显微技术(受激辐射损耗显微技术sted/单分子定位显微技术smlm)在活细胞成像中还存在不少的挑战,如强光照明容易诱发光毒性和光漂白,导致分辨率下降、细胞死亡等;需要控制荧光染料反复“开关”获得足够的光子数,导致成像速度偏慢;具有“开关”特性的特殊荧光染料不易穿透细胞膜,难以标识细胞内部目标;特殊荧光染料的标记方式影响空间分辨率等。
4.此外,基于结构光照明的超分辨显微技术(sim),利用混频效应可以获得两倍空间分辨率的提升(约100nm),仅需要较低光强照明,能够兼容标准样品制作,利用常规荧光染料就可以实现快速、多色、长时程等活细胞成像。但是,偏低的空间分辨率限制sim在活细胞成像的应用范围。非线性sim尽管利用荧光饱和激发或者具有“开关”特性的荧光染料,可以获得更高的空间分辨率,但是又存在上述基于荧光非线性效应的超分辨显微技术局限。
5.另外,光学超振理论上可以在远场获得无限小的超衍射极限焦斑,是一种非常有发展潜力的超分辨显微手段。目前,基于光学超振显微成像的模式主要分两种:(1)利用光学超振透镜实现超分辨成像;(2)利用超衍射光斑实现超分辨成像。对于模式(1),光学超振透镜可以简化显微成像系统的结构,但是往往面临复杂结构的优化设计和微纳结构加工的高精度要求。对于模式(2),光学超振焦斑可以通过光束调控灵活获取或控制,容易兼容其它显微成像方法和显微光路系统。然而,光学超振中心焦斑的压缩会导致中心焦斑光强减小而边带与旁瓣的光强增大,容易在显微成像系统引入大的背景噪声。可见,仅单一控制光学超振中心焦斑尺度实现超分辨成像的方法制约光学超振在活细胞超分辨显微成像的实际应用。
6.总之,不管是利用荧光非线性效应或者结构光照明的荧光超分辨显微技术,还是利用光学超振中心焦斑调控实现远场超分辨成像,现有方法在长时程、多色、快速、三维和超分辨的活细胞成像中还存在很多约束。
技术实现要素:
7.本发明的目的在于针对现有技术的不足,提供一种集成光学超振激发和阵列探测接收的超分辨显微方法及系统,本发明通过基于荧光线性效应的光场调控和混频接收获取
超分辨显微图像,解决强光照、特殊荧光染料标识、背景噪声强等问题,可以更加适合活细胞长时程、多色、快速和超分辨显微成像。
8.本发明的目的是通过以下技术方案来实现的:一种集成光学超振激发和阵列探测接收的超分辨显微方法,包括以下步骤:
9.1)光源模块发出的激发光经波长选择模块进行滤波和传输;输出光束进入光束控制模块,由光束控制模块调控光束的振幅、相位和偏振参数;经调控的输出光束经显微成像模块在测试样品内部形成艾利斑大小的光学超振,由中心焦斑和旁瓣环带构成;光学超振调制激发的荧光信号由显微成像模块接收经二色镜进入光束转换模块;荧光信号经过滤光和光束转换后耦合进入阵列探测器输入端的光纤阵列;阵列探测器各通道采集的光信号被转换成电信号,输入计算机处理;测试样品固定在三维扫描平台,实现样品的横向大范围移动和轴向高精度一维移动;结合光束二维扫描和样品的三维移动,以及波长、针孔和滤光片选择,系统获得样品内被调制激发荧光信号的数据阵列组。
10.2)选择同一探测时刻阵列探测器获取的数据归为一组,将各探测通道在同一扫描位置获取的数据根据光纤阵列输入端的排布结构和各光纤相对探测光路部分光轴的空间位置进行处理,通过平移和叠加获得中心焦斑调制激发对应的扫描点荧光信号;根据扫描点的时序和空间位置获得中心焦斑调制激发对应的初始测量图像,再利用反卷积算法获得中心焦斑调制激发对应的超分辨显微图形。
11.3)选择同一探测位置阵列探测器获取的数据归为一组,将各探测通道在不同时刻获取的图像数据根据光纤阵列输入端的排布结构和各光纤相对探测光路部分光轴的空间位置进行处理,通过滤波和叠加获得旁瓣环带焦斑调制激发对应的初始测量图像,再利用反卷积算法获得旁瓣环带焦斑调制激发对应的超分辨显微图形。
12.4)利用步骤2)和步骤3)获得的超分辨图像进行权重叠加,获得光学超振调制激发的初始测量图像,利用反卷积算法缝合中心焦斑和旁瓣环带调制激发对应的不同频带超分辨图像,最后重构出光学超振调制激发获得的超分辨图像。
13.作为优选,步骤1)中,通过光束参数(振幅、相位和偏振)调制获得以下光学超振:中心焦斑和旁瓣环带的半高全宽都小于衍射极限,而且两者的光强峰值基本相等;在衍射极限范围内包含一个中心圆焦斑和至少一个环带光斑;中心焦斑和环带构成双模式调制照明模式。
14.一种集成光学超振激发和阵列探测接收的超分辨显微系统,包括:
15.光源模块,提供不同荧光染料激发所需要的激发光。
16.波长选择模块,根据不同的荧光染料依次或者分时选择不同的激发波长。
17.光束调控模块,将激发光束准直成平行光束,并控制光束的振幅、相位和偏振分布。
18.二色镜,分路传输激发光束和荧光信号光束。
19.显微成像模块,实现光学超振二维快速扫描调制激发和荧光信号接收;包括二维振镜扫描装置、扫描透镜、镜筒透镜和显微物镜。
20.样品台,固定和移动被测样品。
21.光场转换模块,过滤背景杂散光,并控制荧光信号耦合进入光纤阵列。
22.阵列探测器,将光纤阵列输出的荧光信号转换成电信号。
23.计算机,采集和处理多通道样品信息,显示重构的超分辨图像,并发出扫描样品的控制信号,以及波长、针孔和滤光片选择的控制信号。
24.作为优选,光源模块为多个半导体激光器组合、白光激光器或超连续激光器之一。
25.作为优选,波长选择模块由aotf(声光可调谐滤波器)根据荧光染料选择所需激发波长,单模保偏光纤与aotf相连提供照明光束的输入和输出。
26.作为优选,光束调制模块包含准直透镜、1/2波片、振幅、相位和偏振调制器。
27.作为优选,光场转换模块包含准直透镜、滤光片转轮、针孔转轮和双透镜组成的光束转换透镜组。
28.与现有技术相比,本发明的有益效果是:
29.1)通过光学超振双模式调制激发超分辨信息,可以避免基于荧光非线性效应或者基于光学超振单一中心焦斑激发实现超分辨存在的局限性,能够兼容普通荧光染料标记的标准样品制作方法,更容易实现多色活细胞成像;
30.2)通过阵列探测器的并行探测模式,可以获得更多的中心焦斑和旁瓣环带调制激发的混频信号,同时提高系统测量的信噪比,有助于实现低强度光学超振调制激发,更容易实现长时程活细胞成像。
31.3)通过算法解调激发和探测端被时空调制的荧光信号,可以将荧光激发光场数字分解成中心焦斑和旁瓣环带两部分,更容易解调混叠的超高空间频率信息重构出超分辨图像。
附图说明
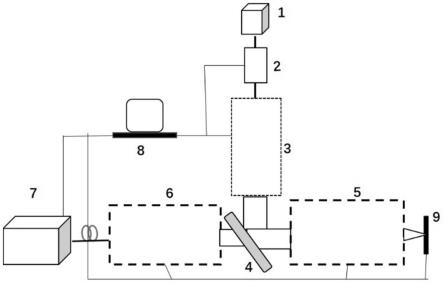
32.图1为本发明系统的结构图;
33.图2为本发明的光路结构;
34.图3为本发明方法的信号处理流程图;
35.图中,1、光源模块;2、波长选择模块;3、光束调控模块;4、二色镜;5、显微成像模块;6、光场转换模块;7、阵列探测器;8、计算机;9、样品台、10、单模保偏光纤;11、aotf;12、单模保偏光纤;13、准直透镜;14、1/2波片;15、振幅、相位和偏振调制器;16、二维振镜扫描装置;17、扫描透镜;18、镜筒透镜;19、显微物镜;20、滤光片转轮;21、会聚透镜;22、针孔转轮;23、透镜;24、透镜;25、光纤阵列;26、样品。
具体实施方式
36.下面结合附图对本发明进一步说明。
37.参考图1,本实施例的一种集成化光学超振激发和阵列探测接收的超分辨显微系统包括光源模块1、波长选择模块2、光束调制模块3、二色镜4、显微成像模块5、光束转换模块6、阵列探测器7、计算机8、样品台9。其中,波长选择模块2包括单模保偏光纤10、aotf 11、单模保偏光纤12。光束调制模块3内部包含准直透镜13、1/2波片14、振幅、相位和偏振调制器15。显微成像模块5包括二维振镜扫描装置16、扫描透镜17、镜筒透镜18和显微物镜19。光束转换模块6包括滤光片转轮20、会聚透镜21、针孔转轮22、光束转换透镜组;光束转换透镜组由透镜23和透镜24构成远心光学系统。
38.其中,如图2所示,光源模块1为多个不同中心波长半导体激光器组合、白光激光器
或超连续光源之一。光源模块1发出的激发光耦合进入波长选择模块2输入端的单模保偏光纤10,通过aotf 11根据荧光染料类型滤波选择相应的分时或者依次不同的激发光波长,提供获取多色荧光染料标记活细胞显微图像的激发光源;选择的激发光波由波长选择模块2输出端的单模保偏光纤12导入光光束调制模块3。准直透镜13将输入光束准直成平行光束;1/2波片14控制入射线偏振平行光束的振动方向,控制光束参数调控的效率;振幅、相位和偏振调制器15分别由计算机控制光束的相位、振幅和偏振分布;具体控制参数由光场调控构造光学超振的矢量衍射理论确定,使光学超振由中心焦斑和旁瓣环带组成。经过光束参数调制的平行光束通过二色镜4导入显微成像模块5。二维振镜扫描装置16控制光学超振在样品内二维快速扫描;扫描透镜17和镜筒透镜18构成远心光学系统,控制扫描光束无像差进入无限远共轭距的显微物镜19;显微物镜19将扫描平行光束转化成扫描的光学超振光斑。光学超振的中心焦斑和旁瓣环带双模式调制激发产生荧光信号,后向散射的荧光信号由显微成像模块5接收;荧光信号经二色镜4导入光束转换模块6。滤光片转轮20根据激发光选择时序通过马达控制选择过滤目标荧光信号以外的背景杂散光;会聚透镜21聚焦荧光信号;针孔转轮22过滤个性化光学超振荡边带激发的背景荧光信号,并控制可探测荧光信号的强度;光束转换透镜组控制荧光信号耦合进入阵列探测器7输入端的光纤阵列25;阵列探测器7各个信号通道将接收的荧光信号转换成电信号,电信号通过放大、调理后输入计算机8。
39.计算机8采集、处理和显示系统测量的电信号,并发出波长选择、光束扫描、样品台移动、滤光片转轮、针孔转轮的控制信号;通过二维光束扫描和样品26的一维或三维移动,阵列探测器获取被测样品的二维或三维信息对应的数据阵列。
40.在光学超振荡一个艾利斑大小的照明区域内,相邻的荧光染料标记点可能被同时激发,阵列探测器7实际接收到的是不同荧光标记位置产生的混频信号,利用算法根据分时调制(相对同一标记位置)成像特征,区分出这些来自不同空间位置点(相对同一测量时间)的混频信息。其中,中心焦斑调制激发类似高斯光斑照明+阵列探测器技术,而旁瓣环带调制照明类似多焦点并行结构照明和阵列探测器接收,通过richardson-lucy(rl)反卷积算法,重构出两种调制激发模型下分别对应的显微图像。鉴于两种模式调制激发加载的信号频谱范围不一致,将通过rl多维反卷积方法缝合两个频带信息,最后重构出光学超振调制激发所获得的超分辨图像。
41.参见图3,本实施例的一种集成化光学超振激发和阵列探测接收的超分辨显微方法,包括以下过程:
42.1)根据扫描成像时间和阵列探测器对应信号通道在探测系统光路中的空间位置,将阵列探测器测量的数值阵列分成两类:同一探测时间,所有信号通道测量数据归为中心焦斑调制激发获取的信息;同一探测位置,所有信号通道测量数据归为旁瓣环带调制激发获取的信息。
43.2)对于中心焦斑调制激发情况,将光纤阵列中位于探测系统光路光轴上的光纤作为中心探测通道,将其他探测通道在每个扫描位置获得的信号,向中心探测通道平移后求和,得到该扫描位置点对应的样品信息,根据扫描时序得到初始图像
44.3)对于旁瓣环带调制照明情况,将阵列探测各个通道获得的显微图像,滤波、求
和、归一化,得到样品的初始图像
45.4)根据下式描述的盲反卷积方法,进行图像重构:
[0046][0047]
其中,f和f-1
分别表示傅里叶和傅里叶逆运算;*表示复共轭;k是迭代次数;显微成像系统光学传递函数otf可以通过共聚焦显微成像理论获取。当低于设定的阈值时迭代停止,可以分别获得旁瓣环带调制和中心焦斑调制照明对应的重构图像和
[0048]
5)利用以下多维rl反卷积方法,缝合中心焦斑和旁瓣环带调制激发对应的重构图像。
[0049]
由下式获得最初估算物体
[0050][0051]
式中,max()表示求取图像光强的最大值。
[0052]
再按照以下步骤依次代入i
obj-c
和i
obj-s
,迭代进行超分辨图像的重构:
[0053][0054]
当低于设定的阈值时迭代停止,将获得重构的超分辨图像
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1