强毒性淀粉样蛋白寡聚体的诊断用途的制作方法
本发明涉及强毒性淀粉样蛋白寡聚体的诊断用途。具体而言,本发明涉及新的强毒性淀粉样蛋白寡聚体aβo*3f作为靶标用于诊断早期和中晚期阿尔茨海默病(ad)及ad源性轻度认知障碍(mci)的用途。
背景技术:
1、阿尔茨海默病(alzheimer’s disease,ad,俗称老年性痴呆)是一种慢性神经退行性疾病,目前全球大约有5000万ad患者,迄今为止,没有任何特异性的有效治疗药物和手段,已给人类带来沉重负担。ad的发展时程较长,起初患者无明显临床症状,逐步发展为记忆减退、性格行为发生变化,后期ad患者脑内的神经元广泛死亡,大脑显著萎缩,治疗药物难以起效。近几年的临床试验表明,对于早期发现、早期有预警的ad患者进行早期干预,可延缓ad的发展,而要实现对ad患者的早期治疗和干预,首先应及时准确地鉴别诊断出ad患者,但目前尚无理想的早期诊断方法和技术应用于临床。研究表明,诱发ad发生发展的β淀粉样蛋白(aβ)变化早在临床症状出现15~20年之前就已经出现。
2、ad的病理特征为脑内aβ聚集形成的老年斑和tau蛋白聚集形成的神经纤维缠结。aβ可聚集成寡聚体、前纤维和成熟的纤维。aβ寡聚体是最具神经毒性的聚集体形式,报道较多的为aβ二聚体、三聚体、addl等形式。aβ寡聚体按照分子量大小可分为低分子量和高分子量两种类型,并且高分子量寡聚体具有更大的神经细胞毒性。aβ二聚体是最小的aβ寡聚体,一般认为aβ二聚体可能是aβ寡聚体的基本组成单元。aβ二聚体在ad患者和ad转基因小鼠的大脑中含量升高,且在sds和强变性剂中稳定,具有一定的神经毒性。除aβ二聚体外,aβ三聚体也被认为是多种aβ寡聚体如六聚体和十二聚体的聚集单元,aβ三聚体在ad患者和ad转基因小鼠大脑中出现较早,但aβ三聚体与aβ斑块沉积之间没有显著相关性,且其毒性目前还存在争议。另外,aβ寡聚体还能够通过进一步聚集形成直径约为12nm的球形低聚物(aspd)和直径为5-6nm的可扩散寡聚体(addl)。此两种形式的聚合物均被认为是具有独特构象且具有神经毒性的aβ寡聚体。目前,尽管已有多种aβ寡聚体形式被发现,然而具体哪种或哪些aβ寡聚体毒性最大,且对ad的发生发展起到主要作用尚未可知。而且,特异检测寡聚体,特别是毒性寡聚体的方法十分有限,获得特异结合毒性淀粉样蛋白寡聚体的抗体尤其困难,这严重限制了针对aβ寡聚体的临床检测和治疗制剂的开发。
3、大量研究表明,神经退行性疾病的严重程度与患者脑内的淀粉样蛋白寡聚体水平密切相关,aβ寡聚体通过引起功能性神经元死亡、认知损伤和痴呆,在ad的发生和发展中发挥关键作用,但aβ寡聚体种类繁多,可通过多种作用机制影响中枢神经的功能,各种aβ寡聚体间毒性各异,在大小、构象、聚集方式、毒性以及在脑内出现的时间上也存在很大的差异。尽管许多研究表明一些aβ寡聚体,如二聚体、三聚体、addl等能够发挥神经毒性作用,但当前对于真正能够起到关键致病作用的aβ寡聚体的形式了解还不够深入。因此,确定与ad发生发展关系密切的关键毒性寡聚体,可为ad的早期预警和早期诊断提供理想标志物,也可为ad的治疗提供理想靶标。
4、除影像检测外,特异性生物标志物是ad临床诊断和检测的基础。目前,业界比较认可的ad诊断标志物主要为脑脊液(csf)中aβ42、aβ40、总的tau蛋白(t-tau)和磷酸化的tau蛋白(p-tau)等。其他标志蛋白也时有报道,如sappα、sappβ、bace1、aβ寡聚物、总aβ、轴突和突触类标记物等。这些csf标记物具有较高的诊断准确性,联合ad其他诊断指标,可使ad的诊断敏感度和特异性达到85-90%。与csf相比,血液易于获取,侵袭性小,是临床检测的理想样本来源。目前,已有多项研究开始联合应用外周血蛋白、脂质和代谢物等的含量来区分ad患者和正常人群,如外周血细胞膜上的aβ42二聚体含量、可解聚aβ42纤维的血浆凝溶胶蛋白(gsn)及gsn的主要降解酶mmp3含量等。最近,检测外周血中的特异性成分如tau181、tau217、aβ含量也成为研究的热点。
5、主流的ad生化检测方法主要集中在对csf中aβ以及tau蛋白标志物的测定上。大量研究表明,在正常人发展成为早期认知障碍(mci)及ad患者的过程中,csf中aβ42单体水平逐渐降低,aβ42寡聚体和t-tau水平逐渐升高,而p-tau与aβ42比值变化更加明显。但是,获取csf样本需要做腰椎穿刺,损伤较大,mci患者和轻度ad患者往往难以接受。此外,由于csf样本前处理和检测方法不统一,导致不同厂家、不同实验室的检测结果差别巨大,严重限制了该类方法的临床推广应用。相比csf而言,基于血液的检测成本较低、依从性高。但是,血液中可用于ad诊断检测的标记物含量低、种类少,并且受外周组织和器官的影响大,阻碍了ad诊断方法的研发。目前,国际上最前沿的方法是通过液质联用(lc-ms)以及单分子免疫分析技术(simoa)检测血液中aβ42与aβ40的比值,以及p-tau181、p-tau217等蛋白的含量。血液里的这些指标虽然具有一定的诊断意义,但特异性差,单一指标不能很好地区分目标人群,其原因在于对aβ或磷酸化tau蛋白的检测是对其总量的检测,其中包含有它们的单体及其多种多样的毒性各异的聚集物。单体和许多类型的寡聚体细胞毒性小,但它们的含量高,对aβ总体水平数值贡献大,严重干扰了毒性大、具有关键致病作用的淀粉样蛋白寡聚体的检测,而只有毒性大的寡聚体才与ad发生发展直接相关,它的出现和水平高低直接精准关联着患者脑部病理变化,对该类寡聚体的特异检测才更有价值和意义。
6、因此,本领域仍然存在对血液中特定aβ寡聚体含量进行高灵敏度和高特异性检测用以诊断ad的迫切需求。
技术实现思路
1、本发明的一个方面涉及一种诊断受试者是否患有早期和中晚期ad或ad源性mci或处于患有ad的风险中的方法,所述方法包括如下步骤:
2、a)任选地,提供来自受试者的待检测样品,
3、b)使检测所述受试者样品中aβo*3f的存在和/或水平的试剂与受试者样品接触,
4、c)检测所述受试者样品中aβo*3f的存在和/或水平,
5、其中,所述受试者样品中aβo*3f的存在和/或水平指示了所述受试者患有ad或ad源性mci,其中所述aβo*3f是与3f抗体特异性结合的aβ寡聚体,基于分子排阻色谱(sec)分析,其分子量约588kda,所述3f抗体的轻重链cdr序列分别如seq id no:17-22所示。
6、在一些实施方案中,所述受试者为疑似患有ad或ad源性mci的患者,优选地,所述受试者为人、非人灵长类动物、猫或犬。
7、在一些实施方案中,所述诊断方法还包括临床神经心理学和神经影像学评估步骤,优选地,神经影像学是aβ-pet扫描成像和/或tau-pet。更优选地,神经影像学是3f-pet扫描成像,即基于3f的免疫pet成像,用于识别和检测受试者脑中aβo*3f的存在和/或水平。
8、在一些实施方案中,所述诊断方法还包括检测所述受试者样品中tau水平的变化,优选地,所述tau水平为tau总水平或者磷酸化tau水平。
9、本发明的第二方面涉及一种诊断受试者是否患有早期和中晚期ad或ad源性mci或处于患有ad的风险中的试剂盒,其包含检测受试者样品中aβo*3f的存在和/或水平的试剂,其中所述aβo*3f是与3f抗体特异性结合的aβ寡聚体,基于分子排阻色谱分析,其分子量约588kda,所述3f抗体的轻重链cdr序列分别如seq id no:17-22所示。
10、在一些实施方案中,受试者样品是进行所述诊断时从受试者现场获取的样品。在一些实施方案中,受试者样品是受试者在先前的诊断程序中获取的样品。
11、在一些实施方案中,所述分子排阻色谱分析利用superdex 200 10/300gl分子筛色谱柱进行。
12、在一些实施方案中,aβo*3f存在于获自受试者的脑脊液样品中。在一些实施方案中,利用免疫沉淀和分子排阻色谱分析受试者的脑脊液样品并测得aβo*3f的分子量。
13、在一些实施方案中,所述方法或试剂盒涉及或包括aβo*3f的富集试剂,所述aβo*3f的富集试剂包括特异性结合aβo*3f的结合剂,优选地,特异性结合aβo*3f的结合剂是特异性结合aβo*3f的抗体,优选地,所述抗体是单克隆抗体、多克隆抗体或其抗原结合片段,更优选地,所述抗原结合片段选自scfv、f(ab')2、fab2、fab、fab’、fv、fd、dab、骆驼抗体、纳米抗体、双抗体或双特异性抗体。通过所述aβo*3f的富集试剂,受试者样品中的aβo*3f可以被有效富集,以用于后续程序。
14、在一些实施方案中,检测aβo*3f的存在和/或水平的试剂包括特异性结合aβo*3f或aβ聚集物的第一结合剂,优选地,特异性结合aβo*3f或aβ聚集物的第一结合剂是特异性结合aβo*3f或aβ聚集物的抗体,优选地,所述抗体是单克隆抗体、多克隆抗体或其抗原结合片段,更优选地,所述抗原结合片段选自scfv、f(ab')2、fab2、fab、fab’、fv、fd、dab、骆驼抗体、纳米抗体、双抗体或双特异性抗体。在一些实施方案中,特异性结合aβo*3f或aβ聚集物的第一结合剂是特异性结合aβo*3f或aβ聚集物的scfv或全长抗体。
15、在一些实施方案中,所述第一结合剂与允许其检测的检测剂连接。
16、在一些实施方案中,检测aβo*3f的存在和/或水平的试剂还包括第二结合剂,所述第二结合剂与所述第一结合剂特异性结合,优选地,所述第二结合剂是特异性结合所述第一结合剂的抗体,优选地,所述特异性结合所述第一结合剂的抗体是单克隆抗体、多克隆抗体或其抗原结合片段,更优选地,所述抗原结合片段选自scfv、f(ab')2、fab2、fab、fab’、fv、fd、dab、骆驼抗体、纳米抗体、双抗体或双特异性抗体,优选地,所述特异性结合所述第一结合剂的抗体与允许其检测的检测剂连接。在一些实施方案中,所述特异性结合所述第一结合剂的抗体是全长抗体。
17、在一些实施方案中,所述检测剂选自化学发光标记、电化学发光标记、发色团、荧光标记、荧光素型标记、伞形酮、丽丝胺、花菁、德克萨斯红、bodipy(英杰公司)或其类似物、顺磁性标记、放射性标记、生物素、链霉亲和素/生物素、亲和素/生物素、半抗原、地高辛、金属络合物、金属、酶、胶体金或其组合。在一些实施方案中,所述检测剂选自化学发光标记、电化学发光标记、发色团、荧光标记、放射性标记、酶、或其组合。在一些实施方案中,所述检测剂是化学发光标记或电化学发光标记。
18、在一些实施方案中,所述检测选自化学发光测定、电化学发光测定、酶联免疫吸附测定、免疫荧光测定、免疫组织化学测定、免疫色谱测定、放射免疫测定、单分子免疫分析技术(simoa)、流式细胞术、细胞分选术、免疫沉淀测定、免疫扩散测定、斑点印迹测定、western印迹、蛋白质芯片、正电子发射断层术和/或单光子发射计算机断层术,优选地,所述试剂盒包括实施选自化学发光测定、电化学发光测定、酶联免疫吸附测定、免疫荧光测定、免疫组织化学测定、免疫色谱测定、放射免疫测定、单分子免疫分析技术、流式细胞术、细胞分选术、免疫沉淀测定、免疫扩散测定、斑点印迹测定、western印迹和/或蛋白质芯片的检测所需的试剂、材料、容器和/或装置,优选地,所述酶联免疫吸附测定选自直接酶联免疫吸附测定、间接酶联免疫吸附测定、直接夹心酶联免疫吸附测定以及间接夹心酶联免疫吸附分析。
19、在一些实施方案中,所述受试者样品选自受试者的细胞、组织、器官和/或体液,优选地,所述体液选自全血、血浆、血清、脑脊液、淋巴液、唾液、滑液、支气管肺泡灌洗液、痰、腹水、尿液、羊水、腹膜液、心包液、精液和/或阴道分泌物,优选地,所述体液选自全血、血浆、血清和/或脑脊液。
20、在一些实施方案中,所述特异性结合aβo*3f的富集试剂或第一结合剂被附着至固体支持物上。
21、在一些实施方案中,所述方法还包括检测对照样品的步骤,和/或所述试剂盒还含有对照样品,所述对照样品来自健康受试者或未患有ad和ad源性mci的受试者。
22、在一些实施方案中,所述特异性结合aβo*3f的抗体为针对aβo*3f进行免疫所获得多克隆抗体和/或单克隆抗体或其抗原结合片段,优选地,所述抗体为人抗体、人源化抗体、嵌合抗体、小鼠抗体、大鼠抗体、兔抗体、山羊抗体、马抗体、绵羊抗体或非人灵长类动物抗体。
23、在一些实施方案中,基于msd电化学发光方法,健康人群的脑脊液中aβo*3f的浓度为aβ42o*3f:80.44±20.88pg/ml、aβ40o*3f:24.35±5.08pg/ml;和/或血浆中aβo*3f的浓度为aβ42o*3f:71.63±36.8pg/ml、aβ40o*3f:2.24±0.92pg/ml;mci人群的血浆中aβo*3f的浓度为aβ42o*3f:112.93±25.02pg/ml、aβ40o*3f:4.64±1.43pg/ml;ad患者人群的脑脊液中aβo*3f的浓度为aβ42o*3f:264.8±42.26pg/ml、aβ40o*3f:85.74±10.62pg/ml,和/或血浆中aβo*3f的浓度为aβ42o*3f:159.44±36.8pg/ml、aβ40o*3f:14.0±5.59pg/ml;或
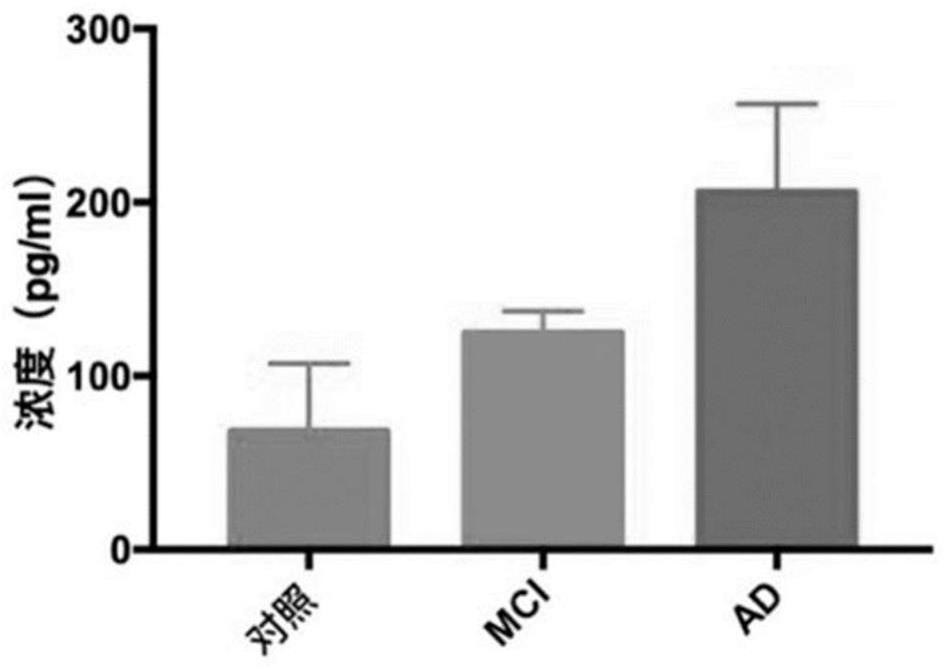
24、基于化学发光方法,健康人群的血浆中aβ42o*3f的浓度为68.02±39.17pg/ml;mci人群的血浆中aβ42o*3f的浓度为124.5±12.57pg/ml;ad患者人群的血浆中aβ42o*3f的浓度为205.75±50.96pg/ml。在一些实施方案中,所述msd电化学发光方法如说明书实施例7所述进行。在一些实施方案中,所述化学发光方法如说明书实施例8所述进行。
25、在一些实施方案中,基于msd电化学发光方法和化学发光方法,所述检测的灵敏度低至0.5pg/ml。
26、在一些实施方案中,特异性结合aβo*3f的抗体是特异性针对aβo*3f的不同表位的多种抗体,例如分别特异性针对aβo*3f的2个、3个、4个、5个或更多个不同表位的2种、3种、4种、5种或更多种抗体。
27、在一些实施方案中,从样本中富集aβo*3f的步骤利用特异性结合aβo*3f的抗体的免疫沉淀法进行。
28、换言之,在前期研究中,本发明人利用噬菌体显示技术在国际上率先筛选出了特异结合aβ寡聚体的全人源单链抗体w20(参见cn101463082a),3f抗体(氨基酸序列如seq idno.23所示)是w20抗体的改进形式,其相对于w20抗体,与aβ寡聚体的亲和力显著提高,能够更显著地抑制aβ的聚集和aβ寡聚体诱导的神经细胞毒性,更有效地改善ad模型小鼠的认知和记忆功能,降低小鼠脑内的病理变化。更有意义的是,该抗体特异识别的aβ寡聚体为超强毒性寡聚体,是aβ寡聚体混合物中最主要的毒性成分,具有强烈的致病作用,在ad的发生和发展中起着关键作用,3f识别的强毒性寡聚体存在于ad患者和ad源性mci患者的csf、血液和/或脑组织中,且其水平在ad患者、mci患者和健康老年人三类人群的csf、血液和/或脑组织呈现极显著差别,因此可精确区分出ad患者、mci患者和健康老年人群。该种毒性寡聚体也存在于ad转基因小鼠中,并与ad转基因小鼠的发病直接相关。本发明中将3f识别的强毒性aβ寡聚体称为aβo*3f,可采用免疫沉淀(使用3f抗体)从aβ寡聚体混合物中分离而来,其典型特征为aβ高分子量寡聚体,基于分子排阻色谱(sec)分析,其分子量大小约为588kda,直径约为10nm,对神经元有强毒性作用,其毒性比aβ寡聚体混合物毒性高200倍以上。aβo*3f可激活小胶质细胞和星形胶质细胞,分泌大量的炎症因子。
- 还没有人留言评论。精彩留言会获得点赞!