基于磁控的微球阵列芯片、检测组件和检测系统、方法
1.本发明属于生物芯片技术领域,尤其涉及一种基于磁控的微球阵列芯片、检测组件和检测系统、方法。
背景技术:
2.蛋白质或核酸的定量检测是生物化学、食品安全、生命科学以及医学临床诊断重要分析领域之一。在蛋白质或核酸定量检测中,对样品中待测蛋白质或核酸的浓度进行灵敏度高、准确可靠、方便高效的检测是一项重要的工作。
3.在现有蛋白质定量检测的方法中,如考马斯亮蓝法,存在灵敏度和准确性较低等不足。同时,一些利用蛋白质分子间特异性结合的原理所构建的生物芯片技术也被用于蛋白的定量检测,如蛋白微阵列法,但是这些定量检测方式不仅灵敏度较低,而且芯片无法重复使用,导致检测成本较高。
4.另外,数字酶联免疫吸附实验(enzyme-linked immunosorbnent assay,elisa)技术快速发展,通过将目标物单分散并逐一计数,实现目标分子的数字化分析。现有技术中,基于微孔阵列和基于微滴阵列技术的elisa技术芯片加工成本较高,无法重复使用。刘等[chem. sci, 2018, 9, 6605]已经建立了多种高灵敏的基于单微球阵列的免疫分析方法,但这些技术检测过程繁琐、自动化程度不高。因此发展自动化、低成本的数字化免疫分析方法很重要。
技术实现要素:
[0005]
为了解决上述问题,有必要提供一种基于磁控的微球阵列芯片、检测组件和检测系统、方法。
[0006]
本发明第一方面提供一种基于磁控的微球阵列芯片,包括芯片基板;所述芯片基板内部开设有第一微流道、第二微流道和反应腔,所述芯片基板顶面设置有进样口和出样口;所述反应腔一侧通过所述第一微流道与所述进样口相连通,所述反应腔另一侧通过所述第二微流道与所述出样口相连通;所述芯片基板内位于所述反应腔下方嵌设有微磁锥阵列。
[0007]
本发明第二方面提供一种基于磁控的微球阵列检测组件,包括:所述的基于磁控的微球阵列芯片;以及设置于所述基于磁控的微球阵列芯片下方,并可调整与所述微磁锥阵列的间距的第二磁体。
[0008]
本发明第三方面提供一种基于所述基于磁控的微球阵列检测组件的检测系统,包括与所述进样口连通,并用于存储待检测液的储液器;进口与所述出样口连通,并用于存储废液的废液池;与所述废液池的出口连通的负压泵;以及用于照射微球阵列,以能够通过荧光抗原法定量检测出待检测液中微球数量的光
源。
[0009]
本发明第四方面提供一种检测方法,包括以下步骤:步骤1,调整所述磁体与所述微磁锥阵列的间距至预定距离;步骤2,打开所述负压泵,并调节所述分液器加入功能化磁性微球液,使各个功能化磁性微球分别被所述微磁锥阵列中的各个微磁锥形成的微磁场分别捕获;步骤3,调节所述分液器加入检测试剂;步骤4,关闭所述负压泵,用激发光照射微球阵列;步骤5,观察微球阵列中产生绿色荧光信号的微球个数,产生荧光的微球记为1,反之记为0;统计为1的个数,即可定量检测出待检测液中微球数量;步骤6,撤去所述磁体,以释放磁性微球;打开所述负压泵,并调节所述分液器加入洗脱液,以清洁微球阵列芯片。
[0010]
本发明有益效果:1、实现了目标生物标志物高灵敏、自动化、快速高效检测,而且通过数字化分析,显著提高了检测的准确度;2、通过设计微磁控阵列开关,芯片可重复使用,有效降低了检测成本。
[0011]
本发明的附加方面和优点将在下面的描述部分中变得明显,或通过本发明的实践了解到。
附图说明
[0012]
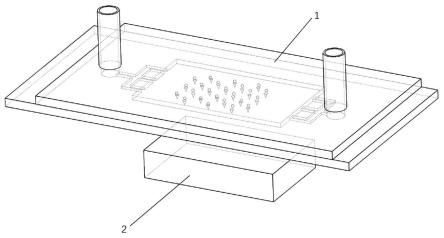
本发明的上述和/或附加的方面和优点从结合下面附图对实施例的描述中将变得明显和容易理解,其中:图1是本发明中基于磁控的微球阵列检测组件的组装结构图。
[0013]
图2是本发明中基于磁控的微球阵列检测组件的爆炸结构示意图。
[0014]
图3是本发明中磁体和微磁锥的磁场图。
[0015]
图4是本发明中检测系统的具体实施图。
具体实施方式
[0016]
为了能够更清楚地理解本发明的上述目的、特征和优点,下面结合附图和具体实施方式对本发明进行进一步的详细描述。需要说明的是,在不冲突的情况下,本技术的实施例及实施例中的特征可以相互组合。
[0017]
在下面的描述中阐述了很多具体细节以便于充分理解本发明,但是,本发明还可以采用其他不同于在此描述的其他方式来实施,因此,本发明的保护范围并不受下面公开的具体实施例的限制。
[0018]
实施例1如图1、图2和图3所示,本实施例提出一种基于磁控的微球阵列芯片,包括芯片基板1;所述芯片基板1内部开设有第一微流道7、第二微流道8和反应腔9,所述芯片基板1顶面设置有进样口5和出样口6;所述反应腔9一侧通过所述第一微流道7与所述进样口5相连通,所述反应腔9另一侧通过所述第二微流道8与所述出样口6相连通;
所述芯片基板1内位于所述反应腔9下方嵌设有微磁锥阵列10;所述微磁锥阵列10中的单个微磁锥为团聚成锥体的磁纳米颗粒,其中,锥体的尖端可以指向所述反应腔9,也可以背向所述反应腔9。
[0019]
特别的,微球的半径小于所述微磁锥底面直径,微球的直径大于所述微磁锥底面直径,其中,微球的直径最大是第一微流道7的三分之一。
[0020]
需要说明的是,所述磁纳米颗粒优选为四氧化三铁磁纳米颗粒,在其它实施例中,也可以采用其它材质的磁纳米颗粒。
[0021]
本实施例中微磁锥的工作原理为:磁性材料里面分成很多微小的区域,每一个微小区域就叫一个磁畴,每一个磁畴都有自己的磁矩。磁化前,各个磁畴的磁矩方向不同,磁场互相抵消,所以整个材料对外就不显磁性。当磁性材料被放进另一外部磁场中时,磁性材料中磁畴的磁矩方向变得一致,从而被磁化且对外显磁性。外部磁场越强,这些磁矩方向越趋于一致,磁化产生的磁场越强,反之亦然。
[0022]
当外部磁场的场强由近及远愈发衰弱,通过增大(减小)永磁体与微磁锥的距离使外部场强变小(变大),进而弱化(强化)微磁锥内磁矩方向一致的趋势,从而削弱(增强)局域性微磁场场强。因此控制磁体与微磁锥的距离可以调节局域性微磁场的磁场强度。将磁体放置距微磁锥理论距离处,从而产生理论磁场强度的局域性微磁场。通过调整微磁锥体积的尺度大小可以确保该局域性微磁场捕获单个微球后不影响其他微球流出芯片。将磁体撤去后,微磁锥不再受外部磁场磁化影响,内部磁畴的磁矩方向恢复各向性相互抵消,局域性微磁场消失,微球被释放。
[0023]
实施例2本实施例与实施例1的区别在于:提供了一种具体的芯片基板结构和微磁锥阵列的制作方法,其中,所述芯片基板1包括键合为一体的上基板3和下基板4;所述第一微流道7、所述第二微流道8和所述反应腔9开设在所述上基板3上,且底壁敞开设置;所述微磁锥阵列10嵌设在所述下基板4内;所述微磁锥阵列10的面积小于所述反应腔9的底面面积。
[0024]
所述微磁锥阵列的制作方法包括:s1,制作作为制作下基板4的模具的模板;s2,将磁纳米颗粒溶液滴加在所述模板上;s3,在所述模板下方放置一块第一磁体,对磁纳米颗粒溶液施加磁场,磁纳米颗粒溶液在磁场的作用下分散成阵列化排列的微磁锥;s4,将光固化溶液倾倒于所述模板上,施加光照固化光固化溶液为膜;s5,剥离固化后的膜作为所述下基板。
[0025]
需要说明的是,步骤s3的操作决定了微磁锥的大小及排布方式,对于本实施例来说,主要与磁体施加的磁场强度有关,通过控制磁场强度即可控制磁纳米颗粒形成的微磁锥的直径,以及呈阵列化排列的各微磁锥的间隔。
[0026]
特别的,还包括步骤s6,键合所述上基板和所述下基板,从而完成芯片基板的制作。
[0027]
所述第一磁体可以为永磁体也可以为电磁铁。
[0028]
实施例3本实施例提供一种基于磁控的微球阵列检测组件,包括:如实施例2所述的基于磁控的微球阵列芯片;以及设置于所述基于磁控的微球阵列芯片下方,并可调整与所述微磁锥阵列10的间距的第二磁体2。
[0029]
具体的,所述第二磁体2为永磁体或电磁铁。
[0030]
本实施例中,将磁体2置于微球阵列芯片的下方,磁体2施加外部磁场,微磁锥阵列10中每个微磁锥在外部磁场的诱导下产生垂直于反应腔向上的微磁场,微磁锥阵列10产生磁性且每个微磁锥都可以捕获单个磁性微球。使用时,最先进入反应腔9的磁性微球会优先被临近微磁场所捕获,后面的磁性微球绕过被捕获的磁性微球继续被经过的微磁场捕获,直到所有磁性微球都被捕获从而形成磁性微球阵列11。检测结束后撤去磁体,局域性微磁场消失,失去捕获磁性微球阵列11的能力释放磁性微球。
[0031]
需要说明的是,要实现单个磁性微球的捕获,微磁锥的底面直径大小(以50 μm为例)与要捕获的磁性微球直径(以50 μm为例)有关,一般使它们大小相当即可。磁体的间距的作用是使其所在位置产生的磁化磁场(即各微磁锥附近区域的磁场)为5500 gauss~7000 gauss的场强以磁化微磁锥。其中,微流道的宽度也是与要捕获的磁性微球直径有关的,区间范围以(3d,4d]为佳(d表示磁性微球直径)。
[0032]
实施例4本实施例提供一种基于实施例3所述基于磁控的微球阵列检测组件的检测系统,如图4所示,包括与所述进样口5连通,并用于存储待检测液的储液器;进口与所述出样口6连通,并用于存储废液的废液池16;与所述废液池16的出口连通的负压泵17;以及用于照射微球阵列11,以能够通过荧光抗原法定量检测出待检测液中微球数量的光源。
[0033]
具体的,所述储液器包括分液器12,用于存储功能化磁性微球液的第一储液池13,用于存储检测试剂的第二储液池14,以及用于存储洗脱液的第三储液池15;所述分液器12的多个入口同时与所述第一储液池13、所述第二储液池14和所述第三储液池15连通;所述分液器12的出口与所述进样口5连通。
[0034]
本实施例检测系统的检测方法,包括以下步骤:步骤1,调整所述磁体2与所述微磁锥阵列10的间距至预定距离,以生成5500gauss~7000gauss的原磁场以磁化微磁锥形成微磁场;步骤2,打开所述负压泵17,调节所述分液器12加入功能化磁性微球液,并使功能化磁性微球液以10ml/min~30ml/min的流速通过所述反应腔9,使各个功能化磁性微球分别被所述微磁锥阵列10中的各个微磁锥形成的微磁场分别捕获;步骤3,调节所述分液器12加入检测试剂;步骤4,关闭所述负压泵17,用激发光照射微球阵列11;步骤5,观察是否产生绿色荧光信号,产生荧光记为1,反之记为0;统计为1的个数,即可定量检测出待检测液中微球数量;步骤6,撤去所述磁体2,以释放磁性微球;打开所述负压泵17,并调节所述分液器
12加入洗脱液,以清洁微球阵列芯片,清洗后的微球阵列芯片即可以重复使用。
[0035]
本实施例的前提是:认为功能化的磁性微球足够小,每个磁性微球表面只能结合一个抗原。因此,微球数量反应了抗原数量,通过定量检测待检测液中微球数量,即可实现待检测液中抗原数量的定量检测。
[0036]
实施例5本实施例提供一种以甲胎蛋白(alpha fetoprotein,afp)为例的具体的微球阵列检测组件的检测系统及其检测方法。
[0037]
微球阵列检测组件中,第二磁体采用永磁体2;微球阵列芯片中,上基板3为尺寸70mm
×
60mm
×
6mm的pdms聚合物板,下基板4为80mm
×
60mm
×
6mm的pdms聚合物板,反应腔9的尺寸为20mm
×
17mm
×
100μm,所述第一微流道7、第二微流道8的宽度为150μm。
[0038]
进样口5与分液器12出口连通,分液器12多个入口同时与第一储液池13、第二储液池14和第三储液池15连通;出样口6与废液池14入口连通,废液池14出口与负压泵17连通。第一储液池13中含有浓度为5ng/ml直径为40μm的功能化磁性微球液,第二储液池14中含有5ng/ml的荧光基团fitc修饰的afp抗体溶液,第三储液池15含有洗脱液。
[0039]
具体检测方法:(1)永磁体2正对微磁锥阵列10放置于下基板4下方3cm处,生成5500gauss的原磁场以磁化微磁锥形成微磁场;(2)打开所述负压泵17,调节所述分液器12加入功能化磁性微球液,并使功能化磁性微球液以20ml/min的流速通过所述反应腔9,使各个功能化磁性微球分别被所述微磁锥阵列10中的各个微磁锥形成的微磁场分别捕获;(3)调节所述分液器12加入检测试剂;(4)关闭负压泵17,用488 nm激发光照射微球阵列11;(5)观察是否产生绿色荧光信号,产生荧光记为1,反之记为0;统计为1的个数,定量检测出待检测液中微球数量,从而获得待检测液中afp抗原数量;(6)撤去永磁体2,以释放磁性微球;打开所述负压泵17,并调节所述分液器12加入洗脱液,以清洁微球阵列芯片。
[0040]
以上所述,仅为本发明的具体实施方式,但本发明的保护范围并不局限于此,任何熟悉本技术领域的技术人员在本发明揭露的技术范围内,可轻易想到变化或替换,都应涵盖在本发明的保护范围之内。因此,本发明的保护范围应以所述权利要求的保护范围为准。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1