多模态影像组学的分析方法、装置及终端与流程
本发明属于生物医学工程技术领域,尤其涉及一种多模态影像组学的分析方法、装置及终端。
背景技术:
传统医学影像分析一般只关注肿瘤在单一模态中的体现。而影像组学可以将传统的医学影像转化为可挖掘的数据信息。在影像组学研究中,现有技术主要是获取四种解剖影像的静态信息,而没有考虑影像中包含的动态信息,无法多方面地提取图像特征,从而导致所提取出的特征数和样本病例有限,不能最大限度地挖掘医学影像信息。
技术实现要素:
鉴于此,本发明实施例提供了一种多模态影像组学的分析方法、装置及终端,以解决现有技术在影像组学研究中无法多方面提取图像特征的问题,以实现最大限度地挖掘医学影像信息。
第一方面,提供了一种多模态影像组学的分析方法,所述方法包括:
获取多种模态影像,并对所述多种模态影像进行预处理;
对预处理之后的模态影像进行区域分割,获取每一种模态影像对应的感兴趣区域;
对每一种模态影像的每一个感兴趣区域进行高通量特征提取,获取每一个感兴趣区域对应的特征;
以所述多种模态影像的每一个感兴趣区域对应的特征组成源特征,采用预设的聚类算法对所述源特征进行特征聚类;
根据特征聚类的结果构建影像组学标志物。
进一步地,所述多种模态影像包括四种MR解剖成像以及弥散张量成像、弥散加权成像、动态对比增强成像;
所述四种MR解剖成像包括T1加权成像、T1对比增强成像、T2加权成像、T2流动衰减反转恢复序列成像。
进一步地,所述获取多种模态影像,并对所述多种模态影像进行预处理包括:
获取多种模态影像;
对所述多种模态影像进行图像配准、平滑处理和插值处理。
进一步地,对所述多种模态影像进行图像配准包括:
选取四种MR解剖成像中的T1对比增强成像作为基准图像模态;
通过相似性度量获取空间坐标变换参数;
根据所述空间坐标变换参数,将所述多种模态影像中的其余模态影像与所述T1对比增强成像进行配准。
进一步地,所述感兴趣区域对应的特征中包括形态特征、灰度特征以及纹理特征。
第二方面,提供了一种多模态影像组学的分析装置,所述装置包括:
预处理模块,用于获取多种模态影像,并对所述多种模态影像进行预处理;
分割模块,用于对预处理之后的模态影像进行区域分割,获取每一种模态影像对应的感兴趣区域;
特征提取模块,用于对每一种模态影像的每一个感兴趣区域进行高通量特征提取,获取每一个感兴趣区域对应的特征;
特征聚类模块,用于以所述多种模态影像的每一个感兴趣区域对应的特征组成源特征,采用预设的聚类算法对所述源特征进行特征聚类;
构建模块,用于根据特征聚类的结果构建影像组学标志物。
进一步地,所述多种模态影像包括四种MR解剖成像以及弥散张量成像、弥散加权成像、动态对比增强成像;
所述四种MR解剖成像包括T1加权成像、T1对比增强成像、T2加权成像、T2流动衰减反转恢复序列成像。
进一步地,所述预处理模块包括:
获取单元,用于获取多种模态影像;
处理单元,用于对所述多种模态影像进行图像配准、平滑处理和插值处理。
进一步地,所述处理单元具体用于:
选取四种MR解剖成像中的T1对比增强成像作为基准图像模态;
通过相似性度量获取空间坐标变换参数;
根据所述空间坐标变换参数,将所述多种模态影像中的其余模态影像与所述T1对比增强成像进行配准。
进一步地,所述感兴趣区域对应的特征中包括形态特征、灰度特征以及纹理特征。
第三方面,提供了一种终端,所述终端包括处理器,所述处理器用于执行存在存储器的以下程序模块:
预处理模块,用于获取多种模态影像,并对所述多种模态影像进行预处理;
分割模块,用于对预处理之后的模态影像进行区域分割,获取每一种模态影像对应的感兴趣区域;
特征提取模块,用于对每一种模态影像的每一个感兴趣区域进行高通量特征提取,获取每一个感兴趣区域对应的特征;
特征聚类模块,用于以所述多种模态影像的每一个感兴趣区域对应的特征组成源特征,采用预设的聚类算法对所述源特征进行特征聚类;
构建模块,用于根据特征聚类的结果构建影像组学标志物。
与现有技术相比,本发明实施例通过获取多种模态影像,并对所述多种模态影像进行预处理;然后对预处理之后的模态影像进行区域分割,获取每一种模态影像对应的感兴趣区域;对每一种模态影像的每一个感兴趣区域进行高通量特征提取,获取每一个感兴趣区域对应的特征;最后以所述多种模态影像的每一个感兴趣区域对应的特征组成源特征,采用预设的聚类算法对所述源特征进行特征聚类,并根据特征聚类的结果构建影像组学标志物;从而解决了现有技术在影像组学研究中无法多方面提取图像特征的问题,极大地丰富了用于特征聚类的源特征数量以及特征聚类后的代表性特征种类,实现了最大限度地挖掘医学影像信息。
附图说明
为了更清楚地说明本发明实施例或现有技术中的技术方案,下面将对实施例或现有技术描述中所需要使用的附图作简单地介绍,显而易见地,下面描述中的附图仅仅是本发明的一些实施例,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据这些附图获得其他附图。
图1是本发明实施例提供的多模态影像组学的分析方法的实现流程图;
图2是本发明实施例提供的多模态影像组学的分析方法中步骤S101的具体实现流程;
图3是本发明实施例提供的通过K均值聚类算法对脑胶质瘤进行聚类分析的实现流程示意图;
图4是本发明实施例提供的多模态影像组学的分析装置的组成结构图。
具体实施方式
为了使本发明的目的、技术方案及优点更加清楚明白,以下结合附图及实施例,对本发明进行进一步详细说明。应当理解,此处所描述的具体实施例仅仅用以解释本发明,并不用于限定本发明。
本发明实施例通过获取多种模态影像,并对所述多种模态影像进行预处理;然后对预处理之后的模态影像进行区域分割,获取每一种模态影像对应的感兴趣区域;对每一种模态影像的每一个感兴趣区域进行高通量特征提取,获取每一个感兴趣区域对应的特征;最后以所述多种模态影像的每一个感兴趣区域对应的特征组成源特征,采用预设的聚类算法对所述源特征进行特征聚类,并根据特征聚类的结果构建影像组学标志物;从而解决了现有技术在影像组学研究中无法多方面提取图像特征的问题,极大地丰富了用于特征聚类的源特征数量以及特征聚类后的代表性特征种类,实现了最大限度地挖掘医学影像信息。本发明实施例还提供了相应的装置,以下分别进行详细的说明。
图1示出了本发明实施例提供的多模态影像组学的分析方法的实现流程。
在本发明实施例中,所述多模态影像组学的分析方法应用于计算机、服务器等设备。
参阅图1,所述多模态影像组学的分析方法包括:
在步骤S101中,获取多种模态影像,并对所述多种模态影像进行预处理。
在这里,本发明实施例在原有影像组学研究中所采用的四种MR解剖成像模态的基础上引入了弥散张量成像、弥散加权成像、动态对比增强成像。因此,本发明实施例中所述的多种模态影像包括四种MR解剖成像以及弥散张量成像、弥散加权成像、动态对比增强成像。其中,所述四种MR解剖成像包括T1加权成像、T1对比增强成像、T2加权成像、T2流动衰减反转恢复序列成像。所述弥散张量成像和弥散加权成像均为根据水分子运动特征来显示脑补特征的成像方式。所述动态对比增强成像则可以反映肿瘤内部的血流动态变化和灌注状况。
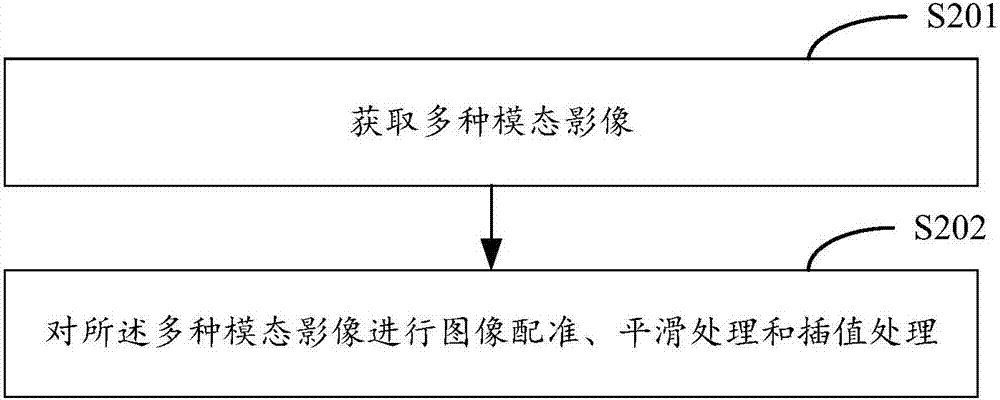
在本发明实施例中,不同模态影像通过不同的设备采用不同的成像方式得到。由于图像获取的参数不同,需要先对所述四种MR解剖成像以及弥散张量成像、弥散加权成像、动态对比增强成像进行预处理。示例性地,图2示出了本发明实施例提供的多模态影像组学的分析方法中步骤S101的具体实现流程。
参阅图2,所述步骤S101包括:
在步骤S201中,获取多种模态影像。
所述多种模态影像即上述的四种MR解剖成像以及弥散张量成像、弥散加权成像、动态对比增强成像,每一种模态影像包括相同数目的图像,优选为20至40张。
在步骤S202中,对所述多种模态影像进行图像配准、平滑处理和插值处理。
在本发明实施例中,所述预处理包括图像配准、图像平滑以及插值处理。在这里,图像配准是指对一张图像求取一种或者一系列的空间变换,使其与另一张图像上的对应像素达到空间上的一致。其中,图像配准的方式包括相对配准和绝对配准。相对配准是指选择多图像中的一张图像作为参考图像,将其他的相关图像与之配准,其中配准的坐标关系是任意的;绝对配准是指预先定义一个控制网格,将所有的图像相对于这个网格进行配准,即通过分别对各图像进行几何校正来使各个图像的对应像素在空间上是一致的。
作为本发明的一个优选示例,可以选取所述四种MR解剖成像中的T1对比增强成像作为基准图像模态;然后通过相似性度量获取空间坐标变换参数;根据所述空间坐标变换参数,将所述多种模态影像中的其余模态影像分别与所述T1对比增强成像进行配准。具体地,在选取T1对比增强成像作为基准图像模态之后,T1对比增强成像中包括的若干张图像均作为基准图像,将其余六种模态影像中的每一张图像与所述T1对比增强成像中的对应图像进行统一的坐标系转换。
作为本发明的一个优选实例,所述平滑处理包括均值滤波器、中值滤波器等,优选采用中值滤波器对每一种模态影像进行图像平滑处理。本发明实施例通过平滑处理,将在数据获取、形态学处理的过程中人为引入的不平滑的毛刺、锋利的边缘等情况进行滤除,进一步保证预处理之后的模态影像的纯净度。
需要说明的是,本发明实施例所述的图像配准、图像平滑处理和插值处理的先后顺序根据实际的需求安排;可以对所述模态影像先进行图像配准、再进行平滑处理和插值处理;或者,对所述模态影像先进行平滑处理和插值处理,然后再进行图像配准。具体的先后顺序根据所提取的特征种类而定。比如,当提取灰度特征、形状特征以及大部分纹理特征时,优选先进行图像配准、再进行平滑处理和插值处理;当提取少量指定的纹理特征时,优选先进行平滑处理和插值处理,然后进行图像配准,以提高特征提取的效果。
在步骤S102中,对预处理之后的模态影像进行区域分割,获取每一种模态影像对应的感兴趣区域。
在这里,经过区域分割,每一种模态影像对应一个或者多个感兴趣区域。示例性地,以脑胶质瘤的影响分析为例,对T2流动衰减反转恢复图像分割肿瘤水肿区域,即整个肿瘤区域;对T1对比增强成像分割肿瘤增强区、坏死区;对弥散张量成像、弥散加权成像以及动态对比增强成像则分别分割肿瘤增强区,以提取血流信息和物质分布等动态信息;所述T1加权成像、T2加权成像则用于肿瘤分割结果的对照。
在步骤S103中,对每一种模态影像的每一个感兴趣区域进行高通量特征提取,获取每一个感兴趣区域对应的特征。
本发明实施例通过区域分割,得到每一种模态影像对应的一个或者多个感兴趣区域,然后采用高通量特征提取对应的一组特征。其中,所提取的特征包括形态特征、灰度特征以及纹理特征。所述形态特征用于描述肿瘤的三维特征。所述灰度特征用于描述每一个感兴趣区域中的所有像素对应的灰度值。所述纹理特征用于量化肿瘤内部的异质性。示例性地,表1给出了本发明实施例提供的所提取的每一个感兴趣区域对应的一组特征的组成示例。在表1中,所述特征集包括28个形态特征、12个灰度特征以及52个纹理特征。
表1
本发明实施例对四种MR解剖成像、弥散张量成像、弥散加权成像、动态对比增强成像中的每一种模态影像的每一个感兴趣区域,提取其对应的一组形态特征、灰度特征以及纹理特征,增加了图像动态信息和功能变化信息,比如血流流动情况、物质分布情况,从而实现了最大限度地挖掘不同模态影像中的信息,极大地丰富了用于特征聚类的源特征数量。
在步骤S104中,以所述多种模态影像的每一个感兴趣区域对应的特征组成源特征,采用预设的聚类算法对所述源特征进行特征聚类。
在这里,所述预设的聚类算法包括层次化聚类算法、基于密度和网格的聚类算法、K均值聚类算法等。
示例性地,以下以前面所述的脑胶质瘤的影响分析为例来对聚类进行说明。为了实现特征降维,这里采用划分式聚类算法中的典型方法K均值算法来进行特征聚类。其中,K均值聚类算法的目的是使每一个源特征和聚类中心之间的差的平方和最小化。图3示出了本发明实施例提供的通过K均值聚类算法对脑胶质瘤进行聚类分析的实现流程,包括:
在步骤S301中,随机选取k个聚类中心。
在步骤S302中,以所述多种模态影像的每一个感兴趣区域对应的特征组成源特征,计算每一个源特征与每一个聚类中心之间的距离值,将所述源特征分配至距离值最小的聚类中心所标明的类中。
在步骤S303中,在分配完后,计算偏差值,所述偏差值为每一个源特征与所述k个聚类中心之间的距离平方和。
在步骤S304中,判断所述偏差值是否收敛。
若是时,执行步骤S305;否则,返回执行步骤S301,重新选取k个聚类中心,进行下一轮特征聚类运算。
在步骤S305中,结束本次聚类运算。
在这里,假设通过步骤S301中所选取的聚类中心为C1,…,Ck,所述偏差值的计算公式为:
在上式中,xi表示第i个源特征,d2(xi,Cr)表示第i个源特征与第r个聚类中心之间的差的平方,即距离的平方,D表示偏差值,用于衡量K均值算法的效果,偏差值D越小效果越好。
经实验得到,通过本发明实施例得到的用于特征聚类的源特征数量可达1564个,聚类后的代表性特征种类可达10大类,远远超过了现有的文献和专利,因此,通过本发明实施例,可以大大地丰富特征聚类前的源特征数量以及特征聚类后的代表性特征种类。
在步骤S105中,根据特征聚类的结果构建影像组学标志物。
在本发明实施例中,所述构建影像组学标志物是采用计算机自动识别和分类方法对临床疾病进行预测及分析。具体地,基于已经完成特征提取的所有患者的所有特征与患者的临床病理、生存期等需要预测和分析的参数进行对比,将不同的模态影像的特征进行“训练数据集”和“验证数据集”的分类。对训练数据集中不同类别的病变数据分别采用计算机自动识别方法进行模型训练,并将一个完备的训练模型用于验证数据集实现未知病类的分析和预测,得到患者的病理、临床分期、基因信息和生存期的定性以及定量的分析结果。
综上所述,本发明实施例通过获取多种模态影像,并对所述多种模态影像进行预处理;然后对预处理之后的模态影像进行区域分割,获取每一种模态影像对应的感兴趣区域;对每一种模态影像的每一个感兴趣区域进行高通量特征提取,获取每一个感兴趣区域对应的特征;最后以所述多种模态影像的每一个感兴趣区域对应的特征组成源特征,采用预设的聚类算法对所述源特征进行特征聚类,并根据特征聚类的结果构建影像组学标志物;从而解决了现有技术在影像组学研究中无法多方面提取图像特征的问题,丰富了用于特征聚类的源特征数量以及特征聚类后的代表性特征种类,实现了最大限度地挖掘医学影像信息。
图4示出了本发明实施例提供的多模态影像组学的分析装置的组成结构,为了便于说明,仅示出了与本发明实施例相关的部分。
在本发明实施例中,所述装置用于实现上述图1至图3实施例中所述的多模态影像组学的分析方法,可以是内置于计算机、服务器内的软件单元、硬件单元或者软硬件结合的单元。
参阅图4,所述装置包括:
预处理模块41,用于获取多种模态影像,并对所述多种模态影像进行预处理;
分割模块42,用于对预处理之后的模态影像进行区域分割,获取每一种模态影像对应的感兴趣区域;
特征提取模块43,用于对每一种模态影像的每一个感兴趣区域进行高通量特征提取,获取每一个感兴趣区域对应的特征;
特征聚类模块44,用于以所述多种模态影像的每一个感兴趣区域对应的特征组成源特征,采用预设的聚类算法对所述源特征进行特征聚类;
构建模块45,用于根据特征聚类的结果构建影像组学标志物。
在本发明实施例中,所述多种模态影像包括四种MR解剖成像以及弥散张量成像、弥散加权成像、动态对比增强成像;所述四种MR解剖成像包括T1加权成像、T1对比增强成像、T2加权成像、T2流动衰减反转恢复序列成像。所述弥散张量成像和弥散加权成像均为根据水分子运动特征来显示脑补特征的成像方式。所述动态对比增强成像则可以反映肿瘤内部的血流动态变化和灌注状况。每一种模态影像包括相同数目的图像,优选为20至40张。
由于图像获取的参数不同,为了保证图像的一致性,需要对所述四种MR解剖成像以及弥散张量成像、弥散加权成像、动态对比增强成像进行预处理。在本发明实施例中,所述预处理模块41包括:
获取单元411,用于获取多种模态影像;
处理单元412,用于对所述多种模态影像进行图像配准、平滑处理和插值处理。
在这里,图像配准是指对一张图像求取一种或者一系列的空间变换,使其与另一张图像上的对应像素达到空间上的一致。其中,图像配准的方式包括相对配准和绝对配准。相对配准是指选择多图像中的一张图像作为参考图像,将其他的相关图像与之配准,其中配准的坐标关系是任意的;绝对配准是指预先定义一个控制网格,将所有的图像相对于这个网格进行配准,即通过分别对各图像进行几何校正来使各个图像的对应像素在空间上是一致的。
作为本发明的一个优选示例,可以基于T1对比增强成像来进行图像配准,此时,所述处理单元412还可以用于:
选取四种MR解剖成像中的T1对比增强成像作为基准图像模态;
通过相似性度量获取空间坐标变换参数;
根据所述空间坐标变换参数,将所述多种模态影像中的其余模态影像与所述T1对比增强成像进行配准。
具体地,在选取T1对比增强成像作为基准图像模态之后,T1对比增强成像中包括的若干张图像均作为基准图像,所述处理单元412将其余六种模态影像中的每一张图像与所述T1对比增强成像中的对应图像进行统一的坐标系转换。
作为本发明的一个优选实例,所述处理单元412可以采用均值滤波器、中值滤波器进行平滑处理,优选采用中值滤波器对每一种模态影像进行图像平滑处理。本发明实施例通过平滑处理,将在数据获取、形态学处理的过程中人为引入的不平滑的毛刺、锋利的边缘等情况进行滤出,进一步保证了预处理之后的模态影像的纯净度。
需要说明的是,本发明实施例所述的图像配准、图像平滑处理和插值处理的先后顺序根据实际的需求安排;所述预处理单元412可以对所述模态影像先进行图像配准、再进行平滑处理和插值处理;或者,所述预处理单元412可以先对所述模态影像进行平滑处理和插值处理,然后再进行图像配准。具体的先后顺序根据所提取的特征种类而定。比如,当提取灰度特征、形状特征以及大部分纹理特征时,优选先进行图像配准、再进行平滑处理和插值处理;当提取少量指定的纹理特征时,优选先进行平滑处理和插值处理,然后进行图像配准,以提高特征提取的效果。
进一步地,本发明实施例通过所述分割模块42对每一种模态影像进行区域分割,得到每一种模态影像对应的一个或者多个感兴趣区域,然后通过特征提取模块43进行高通量特征提取。其中,所提取的特征包括形态特征、灰度特征以及纹理特征。所述形态特征用于描述肿瘤的三维特征。所述灰度特征用于描述每一个感兴趣区域中的所有像素对应的灰度值。所述纹理特征用于量化肿瘤内部的异质性。表1给出了本发明实施例提供的所提取的特征的组成示例。在表1中,所述特征包括28个形态特征、12个灰度特征以及52个纹理特征。
本发明实施例通过对四种MR解剖成像、弥散张量成像、弥散加权成像、动态对比增强成像中的每一种模态影像的每一个感兴趣区域,提取其对应的一组形态特征、灰度特征以及纹理特征,相对于现有技术所提取的特征增加了图像动态信息和功能变化信息,比如血流流动情况、物质分布情况,从而极大地丰富了用于特征聚类的源特征数量。
进一步地,所述特征聚类模块44所使用的述预设的聚类算法包括层次化聚类算法、基于密度和网格的聚类算法、K均值聚类算法等。
示例性地,以下以脑胶质瘤的影响分析为例来对聚类进行说明。为了实现特征降维,这里通过所述特征提取模块43采用划分式聚类算法中的典型方法K均值算法来进行特征聚类。其中,K均值聚类算法的目的是使每一个特征和聚类中心之间的差的平方和最小化。所述特征提取模块43具体用于。
随机选取k个聚类中心;
以所述多种模态影像的每一个感兴趣区域对应的特征组成源特征,计算每一个源特征与每一个聚类中心之间的距离值,将所述源特征分配至距离值最小的聚类中心所标明的类中;
在分配完后,计算偏差值,所述偏差值为每一个源特征与所述k个聚类中心之间的距离平方和;
判断所述偏差值是否收敛;
若是时,结束本次聚类运算。否则,重新选取k个聚类中心,进行下一轮特征聚类运算。
在这里,假设所选取的聚类中心为C1,…,Ck,所述偏差值的计算公式为:
在上式中,xi表示第i个源特征,d2(xi,Cr)表示第i个源特征与第r个聚类中心之间的差的平方,即距离的平方,D表示偏差值,用于衡量K均值算法的效果,偏差值D越小效果越好。
经实验得到,通过本发明实施例得到的用于特征聚类的源特征数量可达1564个,聚类后的代表性特征种类可达10大类,远远超过了现有的文献和专利,因此,通过本发明实施例,可以大大地丰富特征聚类前的源特征数量以及特征聚类后的代表性特征种类。
需要说明的是,本发明实施例中的装置可以用于实现上述方法实施例中的全部技术方案,其各个功能模块的功能可以根据上述方法实施例中的方法具体实现,其具体实现过程可参照上述实例中的相关描述,此处不再赘述。
本发明还提供了一种终端,所述终端用于实现多模态影像组学的分析方法。在本实施例中,终端包括:处理器,其中所述处理器用于执行存在存储器的以下程序模块:
预处理模块,用于获取多种模态影像,并对所述多种模态影像进行预处理;
分割模块,用于对预处理之后的模态影像进行区域分割,获取每一种模态影像对应的感兴趣区域;
特征提取模块,用于对每一种模态影像的每一个感兴趣区域进行高通量特征提取,获取每一个感兴趣区域对应的特征;
特征聚类模块,用于以所述多种模态影像的每一个感兴趣区域对应的特征组成源特征,采用预设的聚类算法对所述源特征进行特征聚类;
构建模块,用于根据特征聚类的结果构建影像组学标志物。
其中,所述多种模态影像包括四种MR解剖成像以及弥散张量成像、弥散加权成像、动态对比增强成像;所述四种MR解剖成像包括T1加权成像、T1对比增强成像、T2加权成像、T2流动衰减反转恢复序列成像。
进一步地,所述预处理模块包括:
获取单元,用于获取多种模态影像;
处理单元,用于对所述多种模态影像进行图像配准、平滑处理和插值处理。
进一步地,所述处理单元具体用于:
选取四种MR解剖成像中的T1对比增强成像作为基准图像模态;
通过相似性度量获取空间坐标变换参数;
根据所述空间坐标变换参数,将所述多种模态影像中的其余模态影像与所述T1对比增强成像进行配准。
其中,所述感兴趣区域对应的特征中包括形态特征、灰度特征以及纹理特征。
应当理解,在本发明实施例中,所称处理器可以是中央处理单元(Central Processing Unit,CPU)和/或图形处理器(Graphic Processing Unit,GPU),也可以在此基础上结合其他通用处理器、数字信号处理器(Digital Signal Processor,DSP)、专用集成电路(Application Specific Integrated Circuit,ASIC)、现成可编程门阵列(Field-Programmable Gate Array,FPGA)或者其他可编程逻辑器件、分立门或者晶体管逻辑器件、分立硬件组件等。
可选地,所述终端还可以包括一个或多个输入设备、一个或多个输出设备、。上述处理器、输入设备、输出设备、存储器通过总线连接。
所述输入设备可以包括触控板、指纹采传感器(用于采集用户的指纹信息和指纹的方向信息)、麦克风、通信模块(比如Wi-Fi模块、2G/3G/4G网络模块)、物理按键等。
输出设备可以包括显示器(LCD等)、扬声器等。其中,显示器可用于显示由用户输入的信息或提供给用户的信息等。显示器可包括显示面板,可选的,可以采用液晶显示器(Liquid Crystal Display,LCD)、有机发光二极管(Organic Light-Emitting Diode,OLED)等形式来配置显示面板。进一步的,上述触摸屏可覆盖在显示器上,当触摸屏检测到在其上或附近的触摸操作后,传送给处理器以确定触摸事件的类型,随后处理器根据触摸事件的类型在显示器上提供相应的视觉输出。
具体实现中,本发明实施例中所描述的处理器、输入设备、输出设备、存储器可执行本发明实施例提供的多模态影像组学的分析方法的实施例中所描述的实现方式,在此不再赘述。
综上所述,本发明实施例通过获取多种模态影像,并对所述多种模态影像进行预处理;然后对预处理之后的模态影像进行区域分割,获取每一种模态影像对应的感兴趣区域;对每一种模态影像的每一个感兴趣区域进行高通量特征提取,获取每一个感兴趣区域对应的特征;最后以所述多种模态影像的每一个感兴趣区域对应的特征组成源特征,采用预设的聚类算法对所述源特征进行特征聚类,并根据特征聚类的结果构建影像组学标志物;从而解决了现有技术在影像组学研究中无法多方面提取图像特征的问题,丰富了用于特征聚类的源特征数量以及特征聚类后的代表性特征种类,实现了最大限度地挖掘医学影像信息。
本领域普通技术人员可以意识到,结合本文中所公开的实施例描述的各示例的单元及算法步骤,能够以电子硬件、或者计算机软件和电子硬件的结合来实现。这些功能究竟以硬件还是软件方式来执行,取决于技术方案的特定应用和设计约束条件。专业技术人员可以对每个特定的应用来使用不同方法来实现所描述的功能,但是这种实现不应认为超出本发明的范围。
所属领域的技术人员可以清楚地了解到,为描述的方便和简洁,上述描述的装置和单元的具体工作过程,可以参考前述方法实施例中的对应过程,在此不再赘述。
在本申请所提供的几个实施例中,应该理解到,所揭露的方法、装置及终端,可以通过其它的方式实现。例如,以上所描述的装置实施例仅仅是示意性的,例如,所述模块、单元的划分,仅仅为一种逻辑功能划分,实际实现时可以有另外的划分方式,例如多个单元或组件可以结合或者可以集成到另一个系统,或一些特征可以忽略,或不执行。另一点,所显示或讨论的相互之间的耦合或直接耦合或通信连接可以是通过一些接口,装置或单元的间接耦合或通信连接,可以是电性,机械或其它的形式。
所述作为分离部件说明的单元可以是或者也可以不是物理上分开的,作为单元显示的部件可以是或者也可以不是物理单元,即可以位于一个地方,或者也可以分布到多个网络单元上。可以根据实际的需要选择其中的部分或者全部单元来实现本实施例方案的目的。
另外,在本发明各个实施例中的各功能单元、模块可以集成在一个处理单元中,也可以是各个单元、模块单独物理存在,也可以两个或两个以上单元、模块集成在一个单元中。
所述功能如果以软件功能单元的形式实现并作为独立的产品销售或使用时,可以存储在一个计算机可读取存储介质中。基于这样的理解,本发明的技术方案本质上或者说对现有技术做出贡献的部分或者该技术方案的部分可以以软件产品的形式体现出来,该计算机软件产品存储在一个存储介质中,包括若干指令用以使得一台计算机设备(可以是个人计算机,服务器,或者网络设备等)执行本发明各个实施例所述方法的全部或部分步骤。而前述的存储介质包括:U盘、移动硬盘、只读存储器(ROM,Read-Only Memory)、随机存取存储器(RAM,Random Access Memory)、磁碟或者光盘等各种可以存储程序代码的介质。
以上所述,仅为本发明的具体实施方式,但本发明的保护范围并不局限于此,任何熟悉本技术领域的技术人员在本发明揭露的技术范围内,可轻易想到变化或替换,都应涵盖在本发明的保护范围之内。因此,本发明的保护范围应所述以权利要求的保护范围为准。
- 还没有人留言评论。精彩留言会获得点赞!