基于多标签与多解码器的全心脏ct分割方法及装置
1.本发明属于医学图像处理和计算机视觉技术领域,具体涉及一种基于多标签与多解码器的全心脏ct分割方法。
背景技术:
2.心血管疾病已成为全球人类死亡的首要因素,根据《中国心血管健康与疾病报告2019》统计,目前心血管病死亡占城乡居民总死亡原因的首位,农村为45.91%,城市为43.56%。心血管病给人类健康带了巨大的威胁,使医疗系统负担日益加重。随着计算机技术和医学影像设备的发展,医疗影像已经被广泛用于心血管疾病的诊断。临床上,从胸腔ct中,利用计算机识别和分割出心脏的各个解剖结构有着很大的临床需求,对计算机辅助诊断、介入治疗有着重要的意义。
3.全心脏分割的目的是在医学影像中分割出重要的心脏解剖结构,包括左右心室、左右心房、心肌和主要的大血管(如升主动脉,肺动脉等),近年来,深度学习技术越来越多地应用于图像分割领域,并展现出了相当的分割效果,逐渐成为图像分割领域的研究热点。然而,在医学图像分割领域,心脏分割方法主要存在两点问题:
4.其一,现有心脏分割方法主要集中于对心脏某一个或部分几个解剖结构进行分割,如左心房和左心室,较少涉及到全心脏的分割。全心脏分割任务通常具有更多的类别,通常涵盖了心脏的各个主要解剖结构,如左心房、左心室、右心房、右心室、主动脉、肺动脉等;
5.其二,现有心脏分割方法主要是单标签分割的方式,忽略了不同解剖结构之间的关系。临床上,ct血管造影能够增强心脏各解剖结构的区分性,是检查心脏病变的重要手段。受心脏结构特点的影响,连通的血腔(如左心房、室)造影剂浓度接近,在ct影像中,其灰度差异较小;然而,心脏左右血腔(如左心房和右心房)不直接连通,受到人体血液循环的影响,造影剂浓度差异相对较大,体现在ct影像上,其灰度差异较大。这种灰度差异性造成了不同解剖结构的类间距离的不一致性,比如左心房和左心室在灰度上有着更高的相似度,左心房和右心房的相似性较小。
技术实现要素:
6.本发明旨在至少在一定程度上解决相关技术中的技术问题之一。
7.为此,本发明的第一个目的在于提出一种基于多标签与多解码器的全心脏ct分割方法,用于实现对全心脏进行不同粒度的语义分割。
8.本发明的第二个目的在于提出一种基于多标签与多解码器的全心脏ct分割装置。
9.为达上述目的,本发明第一方面实施例提出了一种基于多标签与多解码器的全心脏ct分割方法,包括:获取训练ct图像,训练ct图像包括多个待分割目标对象以及所述多个待分割目标对象对应的第一标签信息;将多个待分割目标对象的第一标签信息按照预设规则进行融合,得到多个第二标签信息,其中,第一标签信息的粒度小于第二标签信息的粒
度;对ct图像进行预处理,并将预处理后的ct图像剪裁为多个预设大小的图像块;构建u-net网络,所述u-net网络包括第一解码器和第二解码器,第一解码器用于分割细粒度标签,第二解码器用于分割粗粒度标签;根据图像块,以及第一标签信息和所述第二标签信息,对u-net网络进行训练,生成分割模型。
10.本发明实施例提出的基于多标签与多解码器的全心脏ct分割方法,基于多标签与多解码器的全心脏ct分割方法,合理地利用类间距离的不一致性信息,引导分割模型更好地学习到心脏解剖结构的特点,从而提升分割效果。将结构上连通的类别,进行标签融合,作为粗粒度的分割标签。在细粒度和粗粒度标签上,分别对全心脏进行不同粒度的分割,即把全心脏分割视作多标签的分割任务,其中每个体素有粗粒度的类别和细粒度的类别。通过这种多语义标签的分割方式,旨在充分利用各个类别的类间不一致性信息,使得模型更容易学习和优化。最终,提出利用多解码器的3d u-net网络模型,每个解码器分别预测不同粒度的标签。采用多任务学习机制,对每个解码器进行联合优化,实现对全心脏进行不同粒度的语义分割,从而实现利用类间距离不一致性信息辅助分割模型的学习。
11.另外,根据本发明上述实施例的基于多标签与多解码器的全心脏ct分割方法还可以具有以下附加的技术特征:
12.进一步地,在本发明的一个实施例中,在生成分割模型之后,还包括:
13.获取待分割的ct图像;
14.对所述待分割的ct图像进行预处理并切分成多个图像块,将所述多个图像块分别输入至所述分割模型,得到各个图像块的分割结果;
15.对所述分割结果进行拼接,生成所述待分割的ct图像的目标分割结果。
16.进一步地,在本发明的一个实施例中,对ct图像进行预处理,包括:
17.各向同性采样、线性窗灰度截断、统一化ct影像坐标系统。
18.进一步地,在本发明的一个实施例中,采集训练ct图像,其中包括全心脏结构,对图像进行手工分割与标注,获得第一标签信息,其中分割的类别包括左心房、左心室、主动脉、右心房、右心室、肺动脉、左心肌。
19.进一步地,在本发明的一个实施例中,预设规则,包括:根据心脏的解剖结构先验和不同解剖结构的类间的相似性差异,对第一标签信息进行融合得到第二标签信息,其中类别包括:左血腔、右血腔、左心肌。
20.进一步地,在本发明的一个实施例中,各向同性采样,包括:
21.将空间分辨率统一为m毫米,其中,m根据数据的特点和任务需求进行选取,采样后,每个体素与它的上下左右相邻的体素的空间间隔为m毫米。
22.进一步地,在本发明的一个实施例中,线性窗灰度截断,包括:
23.根据心脏的灰度范围,选择对数据集中的ct图像进行加线性窗,将灰度裁切到-1000~800之间,再对每幅ct图像进行最大最小归一化。
24.进一步地,在本发明的一个实施例中,统一化ct影像坐标系统,包括:
25.将所有ct的坐标系进行统一到las坐标系统,选择left,anterior,superior三个方向,作为ct的3个维度的正方向。
26.进一步地,在本发明的一个实施例中,3d u-net网络架构包括一个编码器和两个非共享参数的解码器,所述编码器和两个解码器之间分别存在跳层连接;其中,第一解码器
对所述第一标签信息进行分割,第二解码器对所述第二标签信息进行分割,两个解码器采用加权的交叉熵作为粗细粒度分割任务的损失函数,并采用联合训练的方式,对所述分割模型进行优化。
27.为达上述目的,本发明第二方面实施例提出了一种基于多标签与多解码器的全心脏ct分割装置,包括:获取模块,用于获取训练ct图像,所述训练ct图像包括多个待分割目标对象以及所述多个待分割目标对象对应的第一标签信息;融合模块,用于将所述多个待分割目标对象的第一标签信息按照预设规则进行融合,得到多个第二标签信息,其中,所述第一标签信息的粒度小于所述第二标签信息的粒度;预处理模块,用于对所述ct图像进行预处理,并将预处理后的所述ct图像剪裁为多个预设大小的图像块;构建模块,用于构建u-net网络,所述u-net网络包括第一解码器和第二解码器,所述第一解码器用于分割细粒度标签,所述第二解码器用于分割粗粒度标签;训练模块,用于根据所述图像块,以及所述第一标签信息和所述第二标签信息,通过最小化损失函数,对所述u-net网络进行训练,生成分割模型。
附图说明
28.本发明上述的和/或附加的方面和优点从下面结合附图对实施例的描述中将变得明显和容易理解,其中:
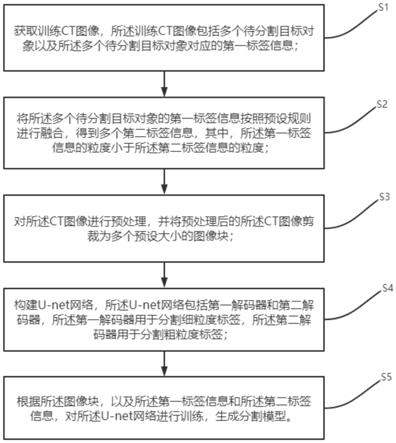
29.图1为本发明实施例所提供的一种基于多标签与多解码器的全心脏ct分割方法的流程示意图。
30.图2为本发明实施例所提供的一种基于多标签与多解码器的全心脏ct分割装置的流程示意图。
31.图3为本发明实施例所提供的基于多标签与多解码器的全心脏ct分割方法总体流程示意图。
32.图4为本发明实施例所提供的心脏的解剖结构先验和不同解剖结构的类间的相似性差异示意图。
33.图5为本发明实施例所提供的细粒度类别标签示意图。
34.图6为本发明实施例所提供的粗粒度类别标签示意图。
35.图7为本发明实施例所提供的3d u-net架构示意图。
36.图8、9、10为本发明实施例所提供的分割结果示意图。
具体实施方式
37.下面详细描述本发明的实施例,所述实施例的示例在附图中示出,其中自始至终相同或类似的标号表示相同或类似的元件或具有相同或类似功能的元件。下面通过参考附图描述的实施例是示例性的,旨在用于解释本发明,而不能理解为对本发明的限制。
38.下面参考附图描述本发明实施例的基于多标签与多解码器的全心脏ct分割方法和装置。
39.图1为本发明实施例所提供的一种基于多标签与多解码器的全心脏ct分割方法的流程示意图。
40.如图1所示,该基于多标签与多解码器的全心脏ct分割方法包括以下步骤:
41.s1:获取训练ct图像,训练ct图像包括多个待分割目标对象以及所述多个待分割目标对象对应的第一标签信息;
42.s2:将多个待分割目标对象的第一标签信息按照预设规则进行融合,得到多个第二标签信息,其中,第一标签信息的粒度小于第二标签信息的粒度;
43.s3:对ct图像进行预处理,并将预处理后的ct图像剪裁为多个预设大小的图像块;
44.s4:构建u-net网络,所述u-net网络包括第一解码器和第二解码器,第一解码器用于分割细粒度标签,第二解码器用于分割粗粒度标签;
45.s5:根据图像块,以及第一标签信息和所述第二标签信息,对u-net网络进行训练,生成分割模型。
46.进一步地,在本发明的一个实施例中,在生成分割模型之后,还包括:
47.获取待分割的ct图像;
48.对所述待分割的ct图像进行预处理并切分成多个图像块,将所述多个图像块分别输入至所述分割模型,得到各个图像块的分割结果;
49.对所述分割结果进行拼接,生成所述待分割的ct图像的目标分割结果。
50.进一步地,在本发明的一个实施例中,采集训练ct图像,其中包括全心脏结构,对图像进行手工分割与标注,获得第一标签信息,其中分割的类别包括左心房、左心室、主动脉、右心房、右心室、肺动脉、左心肌。
51.进一步地,在本发明的一个实施例中,预设规则,包括:根据心脏的解剖结构先验和不同解剖结构的类间的相似性差异,对第一标签信息进行融合得到第二标签信息,其中类别包括:左血腔、右血腔、左心肌。
52.优选的,所述步骤s2中,根据心脏的解剖结构先验和不同解剖结构的类间的相似性差异,对步骤s1中标注的细粒度标签,即左心房、左心室、主动脉、右心房、右心室、肺动脉、左心肌,进行标签融合,生成粗粒度类别标签,即左血腔、右血腔、左心肌,其中,粗粒度类别中左血腔类由细粒度类别左心房、左心室、主动脉组成,右血腔由右心房、右心室、肺动脉组成。
53.通过这种标签融合的方式,充分表征粗细粒度的信息,同时把全心脏分割视作多标签的分割任务,其中每个体素有粗粒度的类别和细粒度的类别,通过这种多语义标签的分割方式,旨在充分利用各个类别的类间不一致性信息,使得模型更容易学习和优化。
54.进一步地,在本发明的一个实施例中,对ct图像进行预处理,包括:
55.各向同性采样、线性窗灰度截断、统一化ct影像坐标系统。
56.进一步地,在本发明的一个实施例中,各向同性采样,包括:
57.将空间分辨率统一为m毫米,其中,m根据数据的特点和任务需求进行选取,采样后,每个体素与它的上下左右相邻的体素的空间间隔为m毫米。
58.进一步地,在本发明的一个实施例中,线性窗灰度截断,包括:
59.根据心脏的灰度范围,选择对数据集中的ct图像进行加线性窗,将灰度裁切到-1000~800之间,再对每幅ct图像进行最大最小归一化。
60.进一步地,在本发明的一个实施例中,统一化ct影像坐标系统,包括:
61.将所有ct的坐标系进行统一到las坐标系统,选择left,anterior,superior三个方向,作为ct的3个维度的正方向。
62.优选的,所述步骤s3中,预处理操作包括各向同性采样、线性窗灰度截断、统一化ct影像坐标系统。
63.优选的,所述各向同性采样操作为:由于检查目的和采集设备的不同,不同的ct影像通常具有不同的空间分辨率,同一幅ct影像沿着不同的方向通常也具有不同的空间分辨率,比如沿着z轴的空间分辨率通常小于沿着x和y轴方向的分辨率,即空间分辨率的各向异性问题,在同一分辨率的数据训练的模型在分割不同分辨率的图像时,往往会造成性能的退化现象,因此,针对ct图像的空间分辨率的各向异性问题,采用了网格采样(grid sampling)的方法,将空间分辨率统一为m毫米(m可以根据数据的特点和任务需求进行选取),采样后,每个体素与它的上下左右相邻的体素的空间间隔为m毫米,通过实现空间分辨率的各向同性,能够使后续cnn分割模型中的相同尺寸的卷积核覆盖的区域为相同的体积,解决因ct图像空间分辨率的各向异性造成的分割精度的退化。
64.优选的,所述线性窗灰度截断操作为:ct图像中的每一个体素的灰度反映了对应组织结构对x射线的吸收系数,通常用hu值来表达,hu值的范围通常在-1000~1000范围内,以水的hu值等于0为基准,-1000通常是空气的hu值,具有致密结构的骨组织的hu值通常大于400,由于胸腔中器官和组织较多,不同组织之间密度差异较大,如肺部的密度较小,脊柱和肋骨的密度较大,使得胸腔ct的灰度有着较高的动态范围,增大了心脏的分割难度,因此,根据检查时的心脏区域的灰度范围,对ct图像进行加线性窗,将灰度裁切到-1000~800之间,最后再对每幅ct图像进行最大最小归一化。
65.优选的,所述统一化ct影像坐标系统操作为:由于不同ct图像采集设备的不同和病人拍摄角度的不同,使得采集的图像具有较大的角度差异,这种角度的差异严重影响分割精度,我们实现了把所有ct的坐标系进行统一到las坐标系统,即选择left,anterior,superior三个方向,作为ct的3个维度的正方向,后续的训练和推理,皆采用las坐标系统,解决了模型对不同坐标系统的ct图像分割泛化能力差的问题。
66.进一步地,在本发明的一个实施例中,3d u-net网络架构包括一个编码器和两个非共享参数的解码器,所述编码器和两个解码器之间分别存在跳层连接;其中,第一解码器对所述第一标签信息进行分割,第二解码器对所述第二标签信息进行分割,两个解码器采用加权的交叉熵作为粗细粒度分割任务的损失函数,并采用联合训练的方式,对所述分割模型进行优化。
67.优选的,所述步骤s4、s5中,搭建的双解码器的3d u-net架构是一种全卷积网络,基础的卷积操作采用3d cnn,双解码器的3d u-net架构具有一个共享参数的编码器,两个非共享参数的解码器,编码器和两个解码器之间分别存在跳层连接,其中,第一解码器对细粒度标签进行分割,第二解码器对粗粒度标签进行分割,两个解码器都采用加权的交叉熵作为粗细粒度分割任务的损失函数,并采用联合训练的方式,对模型进行优化,实现粗细粒度的多标签分割。网络的基本单元包括3d卷积层、池化层、上采样层、batch norm层,其中,3d卷积层的卷积核尺寸为3*3*3,用于提取ct图像特征;池化层的步长为2,用于对特征图进行下采样,增强高层语义的表征的同时减小计算量;上采样层的作用是对特征图进行上采样,恢复图像的分辨率;batch norm层的作用是对数据进行归一化,在训练阶段加快收敛速度。
68.本发明实施例提出的基于多标签与多解码器的全心脏ct分割方法,具备以下有益
效果:
69.第一,本发明合理地利用类间距离的不一致性信息,引导分割模型更好地学习到心脏解剖结构的特点,从而提升分割效果。对于细粒度标签,将结构上连通的类别,进行标签融合,生成粗粒度的分割标签。在细粒度和粗粒度标签上,分别对全心脏进行不同粒度的分割,即把全心脏分割视作多标签的分割任务,其中每个体素有粗粒度的类别和细粒度的类别,通过这种多语义标签的分割方式,旨在充分利用各个类别的类间不一致性信息,使得模型更容易学习和优化。最终,提出利用多解码器的3d u-net网络模型,每个解码器分别预测不同粒度的标签。采用多任务学习机制,对每个解码器进行联合优化,实现对全心脏进行不同粒度的语义分割,从而实现利用类间距离不一致性信息辅助分割模型的学习。
70.第二,本发明采用了网格采样的方法,将空间分辨率统一为m毫米(m可以根据数据的特点和任务需求进行选取),采样后,每个体素与它的上下左右相邻的体素的空间间隔为m毫米,通过实现空间分辨率的各向同性,能够使后续cnn分割模型中的相同尺寸的卷积核覆盖的区域为相同的体积,解决因ct图像空间分辨率的各向异性造成的分割精度退化的问题。
71.第三,本发明通过把ct的坐标系进行统一到las坐标系统,即选择left,anterior,superior三个方向,作为ct的3个维度的正方向,解决了模型对不同坐标系统的ct图像分割泛化能力差的问题。
72.本实施例采用公开全心脏分割数据集mm-whs中的ct图像,总体流程如图3所示,包括训练阶段和推理阶段,来展示本发明的详细操作步骤。
73.训练阶段:
74.步骤1.1:从mm-whs数据集中读取ct训练图像和对应标签;
75.步骤1.2:将标签中的7个类别,按照心脏各个结构的连通情况进行标签融合,得到具有3个类别的粗粒度标签,具体来说,把原标签中的左心房、左心室、主动脉标签融合成同一类,记为左血腔类;同样地,把右心房、右心室、肺动脉标签融合成同一类,记为右血腔类;得到融合后的粗粒度标签有3个粗粒度类别,即左血腔、右血腔、左心肌;
76.步骤1.3:对输入的胸腔ct图像进行预处理,包括各向同性采样、线性窗灰度截断、统一化ct影像坐标系统,接着,从中随机裁剪出长宽高为96*96*96的图像块,把相对应的细粒度标签和粗粒度标签也裁剪出来;
77.步骤1.4:搭建具有两个解码器的u-net网络,第一个解码器用于分割细粒度标签,第二个解码器用于分割粗粒度标签;损失函数采用带权重的交叉熵损失;
78.步骤1.5:利用采样的图像块和粗细粒度标签对多解码的u-net进行训练;
79.步骤1.6:训练完成后,保存模型权重;
80.进一步地,步骤1.2中,如图4所示,根据心脏的解剖结构先验和不同解剖结构的类间的相似性差异,对步骤1.1中标注的细粒度标签(如图5所示),即左心房、左心室、主动脉、右心房、右心室、肺动脉、左心肌,进行标签融合,生成粗粒度类别标签(如图6所示),即左血腔、右血腔、左心肌,其中,粗粒度类别中左血腔类由细粒度类别左心房、左心室、主动脉组成,右血腔由右心房、右心室、肺动脉组成。通过这种标签融合的方式,充分表征粗细粒度的信息,同时把全心脏分割视作多标签的分割任务,其中每个体素有粗粒度的类别和细粒度的类别,通过这种多语义标签的分割方式,旨在充分利用各个类别的类间不一致性信息,使
得模型更容易学习和优化。
81.进一步地,步骤1.3和步骤2.3中,预处理操作包括各向同性采样、线性窗灰度截断、统一化ct影像坐标系统,详细操作如下:
82.1)各向同性采样
83.针对ct图像的空间分辨率的各向异性问题,采用网格采样(grid sampling)的方法,将空间分辨率统一为m毫米,在本实施例中,m取1,即将空间分辨率统一为1毫米。采样后,每个体素与它的上下左右相邻的体素(如果存在)的空间间隔为1毫米。通过实现空间分辨率的各向同性,能够使后续cnn分割模型中的相同尺寸的卷积核覆盖的区域为相同的体积,解决因ct图像空间分辨率的各向异性造成的分割精度的退化。
84.2)线性窗灰度截断
85.ct图像中的每一个体素的灰度反映了对应组织结构对x射线的吸收系数,通常用hu值来表达。hu值的范围通常在-1000~1000范围内,以水的hu值等于0为基准,-1000通常是空气的hu值,具有致密结构的骨组织的hu值通常大于400。通过对mm-whs数据集中的ct图像的灰度进行统计,发现大多数的ct图像的灰度值的分布在约-3000~2000的范围不等。因此,根据心脏的灰度范围,选择对数据集中的ct图像进行加线性窗,将灰度裁切到-1000~800之间,最后再对每幅ct图像进行最大最小归一化:
86.3)统一化ct影像坐标系统
87.不同设备或病人检查姿势可能会造成ct图像的坐标系的正方向的不同。实验发现,这种坐标系的差异严重影响分割精度。我们实现了把所有ct的坐标系进行统一到las坐标系统,即选择left,anterior,superior三个方向,作为ct的3个维度的正方向。后续的训练和推理,皆采用las坐标系统,解决了模型对不同坐标系统的ct图像分割泛化能力差的问题。步骤1.4中,如图7所示,搭建的双解码器的3d u-net架构是一种全卷积网络,基础的卷积操作采用3d cnn。双解码器的3d u-net架构具有一个共享参数的编码器,两个非共享参数的解码器,编码器和解码器之间存在跳层连接。其中,一个解码器对细粒度标签进行分割,另一个解码器对粗粒度标签进行分割,编码器和解码器的具体网络参数可见表格1和表格2。两个解码器都采用加权的交叉熵作为粗细粒度分割任务的损失函数,并采用联合训练的方式,对模型进行优化,实现粗细粒度的多标签分割。网络的基本单元包括3d卷积层、池化层、上采样层、batch norm层,其中,3d卷积层的卷积核尺寸为3*3*3,用于提取ct图像特征;池化层的步长为2,用于对特征图进行下采样,增强高层语义的表征的同时减小计算量;上采样层的作用是对特征图进行上采样,恢复图像的分辨率;batch norm层的作用是对数据进行归一化,在训练阶段加快收敛速度。加权的交叉熵损失公式形如:其中,p
ic
为第i个像素预测为类别c的概率;y
ic
是该像素的真实标签,即当像素i属于第c类时,y
ic
为1,否则为0;c为总类别数量,n是一幅图像中的像素数量;nc是图像中类别c的像素数量。
88.在表格2中,class_num是分割的类别数量,对应于图7中的细粒度分割解码器,class_num为8,表示有8个类,分别为背景类、左心房、左心室、主动脉、右心房、右心室、肺动
脉、左心肌;对应于图7中的粗粒度分割解码器,class_num为4,表示有4个类,分别为背景类、左血腔、右血腔、左心肌。
89.层类型卷积核输入尺寸输出尺寸卷积层3
×3×
3,1696
×
96
×
96
×
196
×
96
×
96
×
16bn+relu+池化层-96
×
96
×
96
×
1648
×
48
×
48
×
16卷积层3
×3×
3,3248
×
48
×
48
×
1648
×
48
×
48
×
32bn+relu+池化层-48
×
48
×
48
×
3224
×
24
×
24
×
32卷积层3
×3×
3,6424
×
24
×
24
×
3224
×
24
×
24
×
64bn+relu-24
×
24
×
24
×
6424
×
24
×
24
×
64卷积层3
×3×
3,6424
×
24
×
24
×
6424
×
24
×
24
×
64bn+relu+池化层-24
×
24
×
24
×
6412
×
12
×
12
×
64卷积层3
×3×
3,12812
×
12
×
12
×
6412
×
12
×
12
×
128bn+relu-12
×
12
×
12
×
12812
×
12
×
12
×
128卷积层3
×3×
3,12812
×
12
×
12
×
12812
×
12
×
12
×
128bn+relu+池化层-12
×
12
×
12
×
1286
×6×6×
128卷积层3
×3×
3,1286
×6×6×
1286
×6×6×
128bn+relu-6
×6×6×
1286
×6×6×
128卷积层3
×3×
3,1286
×6×6×
1286
×6×6×
128bn+relu-6
×6×6×
1286
×6×6×
128
90.表格1编码器参数
[0091][0092]
表格2解码器参数
[0093]
最后,按照如下推理阶段的步骤,实现对ct图像的分割,分割结果如图8、9、10所示。
[0094]
推理阶段:
[0095]
步骤2.1:加载步骤1.6中保存的模型;
[0096]
步骤2.2:输入待分割的ct图像;
[0097]
步骤2.3:对ct图像进行预处理,包括各向同性采样、线性窗灰度截断、统一化ct影
像坐标系统。接着,把图像裁剪成k个有重叠区域的图像块,每个图像块的尺寸为96*96*96;
[0098]
步骤2.4:用模型对k个图像块分别进行分割,得到k个分割结果;
[0099]
步骤2.5:把分割好的k个分割结果进行拼接,得到最终的分割结果。
[0100]
为了实现上述实施例,本发明还提出一种基于多标签与多解码器的全心脏ct分割装置。
[0101]
图2为本发明实施例提供的一种基于多标签与多解码器的全心脏ct分割装置的结构示意图。
[0102]
如图2所示,该基于多标签与多解码器的全心脏ct分割装置包括:获取模块10,融合模块20,预处理模块30,构建模块40,训练模块50;其中,获取模块用于获取训练ct图像,所述训练ct图像包括多个待分割目标对象以及所述多个待分割目标对象对应的第一标签信息;融合模块用于将所述多个待分割目标对象的第一标签信息按照预设规则进行融合,得到多个第二标签信息,其中,所述第一标签信息的粒度小于所述第二标签信息的粒度;预处理模块用于对所述ct图像进行预处理,并将预处理后的所述ct图像剪裁为多个预设大小的图像块;构建模块用于构建u-net网络,所述u-net网络包括第一解码器和第二解码器,所述第一解码器用于分割细粒度标签,所述第二解码器用于分割粗粒度标签;训练模块用于根据所述图像块,以及所述第一标签信息和所述第二标签信息,对所述u-net网络进行训练,生成分割模型。
[0103]
在本说明书的描述中,参考术语“一个实施例”、“一些实施例”、“示例”、“具体示例”、或“一些示例”等的描述意指结合该实施例或示例描述的具体特征、结构、材料或者特点包含于本发明的至少一个实施例或示例中。在本说明书中,对上述术语的示意性表述不必须针对的是相同的实施例或示例。而且,描述的具体特征、结构、材料或者特点可以在任一个或多个实施例或示例中以合适的方式结合。此外,在不相互矛盾的情况下,本领域的技术人员可以将本说明书中描述的不同实施例或示例以及不同实施例或示例的特征进行结合和组合。
[0104]
此外,术语“第一”、“第二”仅用于描述目的,而不能理解为指示或暗示相对重要性或者隐含指明所指示的技术特征的数量。由此,限定有“第一”、“第二”的特征可以明示或者隐含地包括至少一个该特征。在本发明的描述中,“多个”的含义是至少两个,例如两个,三个等,除非另有明确具体的限定。
[0105]
尽管上面已经示出和描述了本发明的实施例,可以理解的是,上述实施例是示例性的,不能理解为对本发明的限制,本领域的普通技术人员在本发明的范围内可以对上述实施例进行变化、修改、替换和变型。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1