基于细胞分析的异常预测方法、装置、设备及介质与流程
1.本发明涉及一种基于细胞分析的异常预测方法、装置、设备及介质,属于智能医疗技术领域。
背景技术:
2.细胞形态变化与疾病往往是息息相关的,通过对细胞形态的分析可以辅助进行疾病的诊断,比如,骨髓细胞形态检查就是通过抽取病人的骨髓制成载玻片,然后经过染色,在显微镜底下观察各种细胞的形态,从而对临床疾病的诊断提供有用的信息。通过细胞形态学检查,发现骨髓中含有大量的未成熟的幼稚细胞、或者各种血细胞数量都出现明显减少的情况、或者发现大量破碎的红细胞碎片,通常都指示异常,通过对细胞形态学分析结果能充分反映受检者细胞的具体情况,现有的技术方案主要是通过人工对细胞进行分析,依赖于人的专业度,导致分析的速度不仅慢而且没有准确度也不高。
技术实现要素:
3.针对上述提到的目前细胞分析的速度慢且准确度不高的问题,本发明的目的在于提供一种基于细胞分析的异常预测的方法、装置、设备及介质,通过识别到细胞的细胞图,并转换为特征向量,以确定出异常特征向量,进而根据第一异常筛选模型确定患者的异常类型,无需人工操作,并且具有一个统一的标准,可以实现对检测样本的异常类型进行快速,准确的分析,可以节省大量的医疗资源。
4.根据本发明的实施方案,提供第一个方案为:一种基于细胞分析的异常预测方法包括以下步骤:
5.获取到待检测样本的载玻片;
6.通过细胞扫片机对所述载玻片进行拍摄,得到细胞图;
7.通过预设的图片识别方式,获取所述细胞图中各个细胞的细胞特征,所述细胞特征至少包括细胞的大小、细胞的结构、细胞的密度以及细胞的颜色中的至少两种特征;
8.将各个细胞的细胞特征按照预设的转换方法转换为特征向量;
9.将所述特征向量与正常细胞的目标向量进行比较;
10.根据比较结果确定所述特征向量中的异常特征向量,得到第一异常特征向量集;
11.将所述第一异常特征向量集输入至预设的第一异常筛选模型中,得到待检测样本的异常类型,其中,所述第一异常筛选模型为神经网络模型,通过不同异常类型的第一异常特征向量集训练而成。
12.进一步地,作为本发明一种更为优选地实施方案,所述根据比较结果确定所述特征向量中的异常特征向量,得到第一异常特征向量集的步骤之后,还包括:
13.将所述异常特征向量输入至预设的第二异常筛选模型中,得到待检测样本的暂时异常类型;
14.基于所述暂时异常类型设置比较参数,根据所述比较参数重新确定所述特征向量
中的异常特征向量,以得到第二异常特征向量集;
15.将所述第二异常特征向量集输入至预设的第一异常筛选模型中,得到待检测样本的异常类型。
16.进一步地,作为本发明一种更为优选地实施方案,所述通过预设的图片识别方式,获取所述细胞图中各个细胞的细胞特征的步骤,包括:
17.通过canny算子确定所述细胞图的一个轮廓点作为初始轮廓点,并对所述初始轮廓点进行坐标标记;
18.按照初始方向搜索所述初始轮廓点的八邻域像素,将与所述初始轮廓点像素相同的邻域像素确定为下一个轮廓点并进行坐标标记,根据下一个轮廓点依次搜索所述目标图片的其余轮廓点,直至搜索的轮廓点为所述初始轮廓点,从而得到对应所述初始轮廓点的细胞轮廓;其中所述初始方向为顺时针方向或逆时针方向;
19.重新确定初始轮廓点,从而得到所述细胞图中各个细胞的细胞轮廓;
20.根据所述细胞轮廓及其所在的位置以及细胞轮廓中的颜色确定各个细胞的细胞特征。
21.进一步地,作为本发明一种更为优选地实施方案,所述将所述第一异常特征向量集输入至预设的第一异常筛选模型中,得到待检测样本的异常类型的步骤之前,还包括:
22.获取训练数据,并将所述训练数据中的各个样本数据进行分类处理;
23.将各类别的所述样本数据依次输入至未训练的第一异常筛选模型中进行训练,训练完毕后得到所述第一异常筛选模型。
24.进一步地,作为本发明一种更为优选地实施方案,所述将所述特征向量与正常细胞的目标向量进行比较的步骤,包括:
25.获取所述正常细胞的目标向量,并基于所述目标向量设置范围值;
26.当所述特征向量超出了所述范围值时,认定为异常特征向量,当所述特征向量在所述范围值之内时,认定为正常向量。
27.进一步地,作为本发明一种更为优选地实施方案,所述将所述第二异常特征向量集输入至预设的第一异常筛选模型中,得到待检测样本的异常类型的步骤之后,还包括:
28.根据所述异常类型获取对应所述异常类型的目标异常类型标准;
29.根据所述目标异常类型标准和所述各个细胞的细胞特征以确定待检测样本是否属于所述异常类型。
30.进一步地,作为本发明一种更为优选地实施方案,所述将所述第二异常特征向量集输入至预设的第一异常筛选模型中,得到待检测样本的异常类型的步骤之后,还包括:
31.将所述细胞图按照所述异常类型所对应的特征提取网络进行特征提取,得到特征图像,其中,所述特征图像包括多个通道;
32.使用公式对所述特征图像进行一维特征描述,得到一维特征图;其中,z
l
表示所述特征图像的第l个通道的子图像,x
l
(i,j)表示第l个通道的子图像的像素值,w和h分别表示第l个通道的子图像的宽和高;
33.根据公式m1=σ(w2δ(w1z))以及公式m2=σ(w4δ(w3z))计算得到第一向量和第二向量;其中,m1表示第一向量,m2表示第二向量,w2、w1、w3、w4表示预设的参数,且w2=w4以及w1=
w3中至少有一个不成立,σ表示relu的激活函数,σ表示sigmoid激活函数;
34.通过所述第一向量和所述第二向量分别对所述特征图像进行加权,得到第一目标特征图m1和第二目标特征图m2;
35.根据公式m=max(m
1∩
m2)计算得到判别性区域特征,并基于所述判别性区域特征对所述细胞图的异常类型进行检测,其中,max(m
1∩
m2)表示相同的像素点位置处m1和m2取最大像素值。
36.根据本发明的实施方案,提供第二个方案为:
37.一种基于细胞分析的异常预测装置,包括以下模块:
38.获取模块,用于获取到待检测样本的载玻片;
39.拍摄模块,用于通过细胞扫片机对所述载玻片进行拍摄,得到细胞图;
40.识别模块,用于通过预设的图片识别方式,获取所述细胞图中各个细胞的细胞特征,所述细胞特征至少包括细胞的大小、细胞的结构、细胞的密度以及细胞的颜色中的至少两种特征;
41.转换模块,用于将各个细胞的细胞特征按照预设的转换方法转换为特征向量;
42.比较模块,用于将所述特征向量与正常细胞的目标向量进行比较;
43.确定模块,用于根据比较结果确定所述特征向量中的异常特征向量,得到第一异常特征向量集;
44.输入模块,用于将所述第一异常特征向量集输入至预设的第一异常筛选模型中,得到待检测样本的异常类型,其中,所述第一异常筛选模型为神经网络模型,通过不同异常类型的第一异常特征向量集训练而成。
45.进一步地,作为本发明一种更为优选地实施方案,所述基于细胞分析的异常预测装置,还包括:
46.异常特征向量输入模块,用于将所述异常特征向量输入至预设的第二异常筛选模型中,得到待检测样本的暂时异常类型;
47.参数设置模块,用于基于所述暂时异常类型设置比较参数,根据所述比较参数重新确定所述特征向量中的异常特征向量,以得到第二异常特征向量集;
48.第二异常特征向量集输入模块,用于将所述第二异常特征向量集输入至预设的第一异常筛选模型中,得到待检测样本的异常类型。
49.进一步地,作为本发明一种更为优选地实施方案,所述识别模块,包括:
50.初始轮廓点确定子模块,用于通过canny算子确定所述细胞图的一个轮廓点作为初始轮廓点,并对所述初始轮廓点进行坐标标记;
51.八邻域像素搜索子模块,用于按照初始方向搜索所述初始轮廓点的八邻域像素,将与所述初始轮廓点像素相同的邻域像素确定为下一个轮廓点并进行坐标标记,根据下一个轮廓点依次搜索所述目标图片的其余轮廓点,直至搜索的轮廓点为所述初始轮廓点,从而得到对应所述初始轮廓点的细胞轮廓;其中所述初始方向为顺时针方向或逆时针方向;
52.初始轮廓点重新确定子模块,用于重新确定初始轮廓点,从而得到所述细胞图中各个细胞的细胞轮廓;
53.细胞特征确定子模块,用于根据所述细胞轮廓及其所在的位置以及细胞轮廓中的颜色确定各个细胞的细胞特征。
54.进一步地,作为本发明一种更为优选地实施方案,所述基于细胞分析的异常预测装置,还包括:
55.训练数据获取模块,用于获取训练数据,并将所述训练数据中的各个样本数据进行分类处理;
56.训练模块,用于将各类别的所述样本数据依次输入至未训练的第一异常筛选模型中进行训练,训练完毕后得到所述第一异常筛选模型。
57.进一步地,作为本发明一种更为优选地实施方案,所述比较模块,包括:
58.目标向量获取模块,用于获取所述正常细胞的目标向量,并基于所述目标向量设置范围值;
59.异常特征向量认定模块,用于当所述特征向量超出了所述范围值时,认定为异常特征向量,当所述特征向量在所述范围值之内时,认定为正常向量。
60.一种计算机设备,包括存储器和处理器,其特征在于,所述存储器存储有计算机程序,所述计算机程序被所述处理器执行时,使得所述处理器执行以下步骤:
61.获取到待检测样本的载玻片;
62.通过细胞扫片机对所述载玻片进行拍摄,得到细胞图;
63.通过预设的图片识别方式,获取所述细胞图中各个细胞的细胞特征,所述细胞特征至少包括细胞的大小、细胞的结构、细胞的密度以及细胞的颜色中的至少两种特征;
64.将各个细胞的细胞特征按照预设的转换方法转换为特征向量;
65.将所述特征向量与正常细胞的目标向量进行比较;
66.根据比较结果确定所述特征向量中的异常特征向量,得到第一异常特征向量集;
67.将所述第一异常特征向量集输入至预设的第一异常筛选模型中,得到待检测样本的异常类型,其中,所述第一异常筛选模型为神经网络模型,通过不同异常类型的第一异常特征向量集训练而成。
68.一种计算机可读存储介质,包括:存储有计算机程序,所述计算机程序被处理器执行时,使得所述处理器执行以下步骤:
69.获取到待检测样本的载玻片;
70.通过细胞扫片机对所述载玻片进行拍摄,得到细胞图;
71.通过预设的图片识别方式,获取所述细胞图中各个细胞的细胞特征,所述细胞特征至少包括细胞的大小、细胞的结构、细胞的密度以及细胞的颜色中的至少两种特征;
72.将各个细胞的细胞特征按照预设的转换方法转换为特征向量;
73.将所述特征向量与正常细胞的目标向量进行比较;
74.根据比较结果确定所述特征向量中的异常特征向量,得到第一异常特征向量集;
75.将所述第一异常特征向量集输入至预设的第一异常筛选模型中,得到待检测样本的异常类型,其中,所述第一异常筛选模型为神经网络模型,通过不同异常类型的第一异常特征向量集训练而成。
76.与现有技术相比,本技术提供的技术方案主要利用细胞扫片机对所述载玻片进行拍摄,得到细胞图,再通过将各个细胞的细胞特征转化为特征向量进行识别,以得到异常特征向量。从而将得到的异常特征向量集输入至模型中得到待检测样本的异常类型。本技术的技术方案无需人工操作,并且具有一个统一的标准,可以实现对患者的异常类型进行快
速,准确的分析,可以节省大量的医疗资源。
附图说明
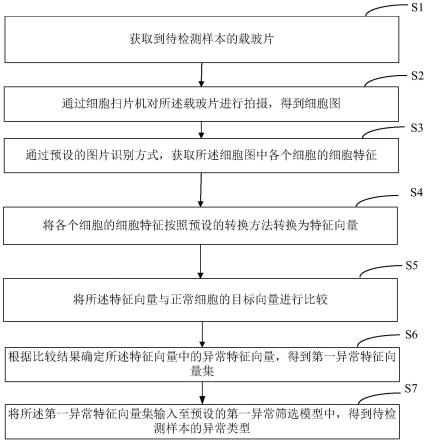
77.图1为本发明基于细胞分析的异常预测方法的流程示意图;
78.图2为本发明基于细胞分析的异常预测装置的结构示意框图;
79.图3为一个实施例中计算机设备的内部结构示意图。
具体实施方式
80.为了使本领域的技术人员更好地理解本技术中的技术方案,下面将结合本技术实施例中的附图对本技术实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例仅仅是本技术的一部分实施例,而不是全部的实施例。基于本技术中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都属于本技术保护的范围。
81.需要说明的是,当元件被称为“固定于”或“设置于”另一个部件上,它可以直接在另一个部件上或者间接设置在另一个部件上;当一个部件被称为是“连接于”另一个部件,它可以是直接连接到另一个部件或间接连接至另一个部件上。
82.需要理解的是,术语“长度”、“宽度”、“上”、“下”、“前”、“后”、“左”、“右”、“竖直”、“水平”、“顶”、“底”“内”、“外”等指示的方位或位置关系为基于附图所示的方位或位置关系,仅是为了便于描述本技术和简化描述,而不是指示或暗示所指的装置或部件必须具有特定的方位、以特定的方位构造和操作,因此不能理解为对本技术的限制。
83.此外,术语“第一”、“第二”仅用于描述目的,而不能理解为指示或暗示相对重要性或者隐含指明所指示的技术特征的数量。由此,限定有“第一”、“第二”的特征可以明示或者隐含地包括一个或者更多个该特征。在本技术的描述中,“多个”、“若干个”的含义是两个或两个以上,除非另有明确具体的限定。
84.须知,本说明书附图所绘示的结构、比例、大小等,均仅用以配合说明书所揭示的内容,以供熟悉此技术的人士了解与阅读,并非用以限定本技术可实施的限定条件,故不具技术上的实质意义,任何结构的修饰、比例关系的改变或大小的调整,在不影响本技术所能产生的功效及所能达成的目的下,均应仍落在本技术所揭示的技术内容得能涵盖的范围内。
85.参照图1,根据本发明的实施方案,提供第一个方案为:
86.一种基于细胞分析的异常预测方法,包括以下步骤:
87.s1:获取到待检测样本的载玻片;
88.s2:通过细胞扫片机对所述载玻片进行拍摄,得到细胞图;
89.s3:通过预设的图片识别方式,获取所述细胞图中各个细胞的细胞特征,所述细胞特征至少包括细胞的大小、细胞的结构、细胞的密度以及细胞的颜色中的至少两种特征;
90.s4:将各个细胞的细胞特征按照预设的转换方法转换为特征向量;
91.s5:将所述特征向量与正常细胞的目标向量进行比较;
92.s6:根据比较结果确定所述特征向量中的异常特征向量,得到第一异常特征向量集;
93.s7:将所述第一异常特征向量集输入至预设的第一异常筛选模型中,得到待检测样本的异常类型,其中,所述第一异常筛选模型为神经网络模型,通过不同异常类型的第一异常特征向量集训练而成。不同的异常类型对应不同的疾病,有利于根据异常类型的预测对患者可能的疾病进行预测,有利于辅助医生进行诊断。
94.其中,待检测样本可以是骨髓细胞样本,也可以是血液细胞样本,还可以是其他细胞样本,这里不做限定。
95.在一个实施例中,步骤s1中,获取的载玻片为从患者身上抽取的骨髓细胞制作成的载玻片,步骤s2中,细胞扫片机具体为是蔡司显微镜,其可以对细胞进行拍摄,从而得到细胞图,步骤s3中,预设的图片识别方式可以是是通过findcontours()函数对于细胞的轮廓进行获取,进而得到细胞的大小,结构,根据识别到的细胞确定细胞的密度,以及根据细胞轮廓内的颜色确定细胞的颜色,从而得到对应的细胞特征。步骤s4中,将各个细胞的细胞特征按照预设的转换方法转换为特征向量,具体地,可以将各个细胞特征进行数值的转换,例如,细胞的大小,一般指细胞的最大直径,然后将该最大直径转换为具体的数值,由于细胞特征至少包括了两种特征,因此,不同的特征可以组成不同的列,以得到细胞的细胞特征所对应的特征向量。步骤s5中,将所述特征向量与正常细胞的目标向量进行比较,比较的方式具体为,比较特征向量中每个特征的值是否超出了预设范围,该预设范围可以预先根据正常的细胞进行设置,当然,也可以是综合所有的特征进行比较,本技术对此不作限定。步骤s6中,根据比较结果,即超出了预设范围的特征向量记为异常特征向量,进而得到第一异常特征向量集,需要说明的是,该第一异常特征向量集包括了识别到的所有异常特征向量,即包括了一个或者多个异常特征向量;步骤s7中,根据第一异常特征向量集来得到待检测样本的异常类型,其中,所述第一异常筛选模型为神经网络模型,通过不同异常类型的第一异常特征向量集训练而成,具体地训练方式后续有详细说明,此处不再赘述。从而实现了无需人工操作,并且具有一个统一的标准,可以实现对患者的异常类型进行快速,准确的分析,可以节省大量的医疗资源。
96.具体地进行阐述,所述根据比较结果确定所述特征向量中的异常特征向量,得到第一异常特征向量集的步骤s6之后,还包括:
97.s701:将所述异常特征向量输入至预设的第二异常筛选模型中,得到待检测样本的暂时异常类型;
98.s702:基于所述暂时异常类型设置比较参数,根据所述比较参数重新确定所述特征向量中的异常特征向量,以得到第二异常特征向量集;
99.s703:将所述第二异常特征向量集输入至预设的第一异常筛选模型中,得到待检测样本的异常类型。
100.需要说明的是,第二异常筛选模型也可以是第一异常筛选模型,其训练方式与第一异常筛选模型相同,此处不再赘述,此处设置了第二异常筛选模型是为了便于后续设置比较参数,例如是细胞的颜色发生了变化,那么需要在颜色方面进行更进一步的设置参数,以便于筛选这一类型的异常细胞,即异常特征向量,从而得到这种异常类型更加精确的第二异常特征向量集,然后进行精确的分析,从而实现对异常类型的进一步确定,提高了异常类型预测的精度。
101.具体地进行阐述,所述通过预设的图片识别方式,获取所述细胞图中各个细胞的
细胞特征的步骤s3,包括:
102.s301:通过canny算子确定所述细胞图的一个轮廓点作为初始轮廓点,并对所述初始轮廓点进行坐标标记;
103.s302:按照初始方向搜索所述初始轮廓点的八邻域像素,将与所述初始轮廓点像素相同的邻域像素确定为下一个轮廓点并进行坐标标记,根据下一个轮廓点依次搜索所述目标图片的其余轮廓点,直至搜索的轮廓点为所述初始轮廓点,从而得到对应所述初始轮廓点的细胞轮廓;其中所述初始方向为顺时针方向或逆时针方向;
104.s303:重新确定初始轮廓点,从而得到所述细胞图中各个细胞的细胞轮廓;
105.s304:根据所述细胞轮廓及其所在的位置以及细胞轮廓中的颜色确定各个细胞的细胞特征。
106.需要补充说明的是,通过canny算子确定初始轮廓点,即从形状的轮廓上选取一点作为初始轮廓点,然后通过坐标对初始轮廓点进行标记,例如,可以将该初始轮廓点作为坐标原点,以便于后续计算,当然,也可以用其他坐标点来进行标记,通过标记可以迅速定位到这个点即可。从顺时针方向或者逆时针方向,搜索初始轮廓点的八邻域像素点,搜索八邻域像素时,初始轮廓点将搜索到的第一个符合要求的像素点作为下一个轮廓点,然后将搜索到的下一个轮廓点作为当前轮廓点,并按照上述选定的方向继续搜索下一个轮廓点,依次搜索直至搜索到的轮廓点为初始轮廓点,在搜索过程中通过坐标为每个轮廓点进行标记,由此可以得知每个轮廓点的坐标,最终得到各个细胞的细胞轮廓,根据所述细胞轮廓及其所在的位置以及细胞轮廓中的颜色确定各个细胞的细胞特征。
107.具体地进行阐述,所述将所述第一异常特征向量集输入至预设的第一异常筛选模型中,得到待检测样本的异常类型的步骤s7之前,还包括:
108.s601:获取训练数据,并将所述训练数据中的各个样本数据进行分类处理;
109.s602:将各类别的所述样本数据依次输入至未训练的第一异常筛选模型中进行训练,训练完毕后得到所述第一异常筛选模型。
110.需要说明的是,实现了对第一异常筛选模型的训练。为了更好的训练第一异常筛选模型,使训练后的第一异常筛选模型预测各种异常类型更加精确,可以将训练数据进行分类处理,分类的方法可以通过余弦相似度算法进行计算,然后将各类别的样本数据依次输入第一异常筛选模型中进行训练,得到训练后的第一异常筛选模型。
111.具体地进行阐述,所述将所述特征向量与正常细胞的目标向量进行比较的步骤s5,包括:
112.s501:获取所述正常细胞的目标向量,并基于所述目标向量设置范围值;
113.s502:当所述特征向量超出了所述范围值时,认定为异常特征向量,当所述特征向量在所述范围值之内时,认定为正常向量。
114.需要说明的是,通过获取到正常细胞的目标向量,设置对应的范围值,由于该正常细胞的目标向量可以预先获取,因此,设置范围值的方式可以是人工进行设置,当所述特征向量超出了所述范围值时,认定为异常特征向量,当所述特征向量在所述范围值之内时,认定为正常向量。
115.具体地进行阐述,所述将所述第二异常特征向量集输入至预设的第一异常筛选模型中,得到待检测样本的异常类型的步骤s7之后,还包括:
116.s801:根据所述异常类型获取对应所述异常类型的目标异常类型标准;
117.s802:根据所述目标异常类型标准和所述各个细胞的细胞特征以判断所述细胞是否患有目标异常类型。
118.需要说明的是,由于细胞的细胞特征已知,只需要将其与目标异常类型的标准进行比较,从而可以确定是否患有目标异常类型,具体地,各种目标异常类型具有不同的指标,因此,只需要对比指标与细胞特征,就可以得到是否患有目标异常类型,该指标可以预先针对各种不同的目标异常类型进行设置,此处只需要进行比较即可。
119.具体地进行阐述,所述将所述第二异常特征向量集输入至预设的第一异常筛选模型中,得到待检测样本的异常类型的步骤s7之后,还包括:
120.s801:将所述细胞图按照所述异常类型所对应的特征提取网络进行特征提取,得到特征图像,其中,所述特征图像包括多个通道;
121.s802:使用公式对所述特征图像进行一维特征描述,得到一维特征图;其中,z
l
表示所述特征图像的第l个通道的子图像,x
l
(i,j)表示第l个通道的子图像的像素值,w和h分别表示第l个通道的子图像的宽和高;
122.s803:根据公式m1=σ(w2δ(w1z))以及公式m2=σ(w4δ(w3z))计算得到第一向量和第二向量;其中,m1表示第一向量,m2表示第二向量,w2、w1、w3、w4表示预设的参数,且w2=w4以及w1=w3中至少有一个不成立,σ表示relu的激活函数,σ表示sigmoid激活函数;
123.s804:通过所述第一向量和所述第二向量分别对所述特征图像进行加权,得到第一目标特征图m1和第二目标特征图m2;
124.s805:根据公式m=max(m
1∩
m2)计算得到判别性区域特征,并基于所述判别性区域特征对所述细胞图的异常类型进行检测,其中,max(m
1∩
m2)表示相同的像素点位置处m1和m2取最大像素值。
125.需要说明的是,根据公式m1=σ(w2δ(w1z))以及公式m2=σ(w4δ(w3z))计算得到第一注意力向量和第二注意力向量;其中,m1表示第一注意力向量,m2表示第二注意力向量,w2、w1、w3、w4表示预设的参数,且w2=w4以及w1=w3中至少有一个不成立,σ表示relu的激活函数,σ表示sigmoid激活函数,过所述第一注意力向量和所述第二注意力向量分别对所述特征向量进行加权,得到第一目标特征图和第二目标特征图。其中,参数w2、w1、w3、w4,可以为每个特征生成不同的权重,从而建模了生成特征的通道之间的相关性,此处的通道是指输出不同特征的通道,在一个具体的实施例中,为了提高模型提取特征的精确性,对于匹配度更高的特征应当赋予更高的权重,即通过对应的注意力向量对其进行加权,得到对应的第一目标特征图和第二目标特征图。本技术可以得到两个不同的注意力机制所得到的两个目标特征图,这两个目标特征图可以集中在相同的判别性区域,因此为了选择出可以求出其交集作为最终的细胞特征,进而提高了细胞特征的识别能力,使具有目标异常类型所对应的特征能够更加凸显出来,便于识别。
126.参照图2,根据本发明的实施方案,提供第二个方案为:
127.一种基于细胞分析的异常预测装置,包括以下模块:
128.获取模块10,用于获取到待检测样本的载玻片;
129.拍摄模块20,用于通过细胞扫片机对所述载玻片进行拍摄,得到细胞图;
130.识别模块30,用于通过预设的图片识别方式,获取所述细胞图中各个细胞的细胞特征,所述细胞特征至少包括细胞的大小、细胞的结构、细胞的密度以及细胞的颜色中的至少两种特征;
131.转换模块40,用于将各个细胞的细胞特征按照预设的转换方法转换为特征向量;
132.比较模块50,用于将所述特征向量与正常细胞的目标向量进行比较;
133.确定模块60,用于根据比较结果确定所述特征向量中的异常特征向量,得到第一异常特征向量集;
134.输入模块70,用于将所述第一异常特征向量集输入至预设的第一异常筛选模型中,得到待检测样本的异常类型,其中,所述第一异常筛选模型为神经网络模型,通过不同异常类型的第一异常特征向量集训练而成。
135.具体地进行阐述,所述基于细胞分析的异常预测装置,还包括:
136.异常特征向量输入模块,用于将所述异常特征向量输入至预设的第二异常筛选模型中,得到待检测样本的暂时异常类型;
137.参数设置模块,用于基于所述暂时异常类型设置比较参数,根据所述比较参数重新确定所述特征向量中的异常特征向量,以得到第二异常特征向量集;
138.第二异常特征向量集输入模块,用于将所述第二异常特征向量集输入至预设的第一异常筛选模型中,得到待检测样本的异常类型。
139.具体地进行阐述,所述识别模块30,包括:
140.初始轮廓点确定子模块,用于通过canny算子确定所述细胞图的一个轮廓点作为初始轮廓点,并对所述初始轮廓点进行坐标标记;
141.八邻域像素搜索子模块,用于按照初始方向搜索所述初始轮廓点的八邻域像素,将与所述初始轮廓点像素相同的邻域像素确定为下一个轮廓点并进行坐标标记,根据下一个轮廓点依次搜索所述目标图片的其余轮廓点,直至搜索的轮廓点为所述初始轮廓点,从而得到对应所述初始轮廓点的细胞轮廓;其中所述初始方向为顺时针方向或逆时针方向;
142.初始轮廓点重新确定子模块,用于重新确定初始轮廓点,从而得到所述细胞图中各个细胞的细胞轮廓;
143.细胞特征确定子模块,用于根据所述细胞轮廓及其所在的位置以及细胞轮廓中的颜色确定各个细胞的细胞特征。
144.具体地进行阐述,所述基于细胞分析的异常预测装置,还包括:
145.训练数据获取模块,用于获取训练数据,并将所述训练数据中的各个样本数据进行分类处理;
146.训练模块,用于将各类别的所述样本数据依次输入至未训练的第一异常筛选模型中进行训练,训练完毕后得到所述第一异常筛选模型。
147.具体地进行阐述,所述比较模块50,包括:
148.目标向量获取模块,用于获取所述正常细胞的目标向量,并基于所述目标向量设置范围值;
149.异常特征向量认定模块,用于当所述特征向量超出了所述范围值时,认定为异常特征向量,当所述特征向量在所述范围值之内时,认定为正常向量。
150.在该技术方案中,需要说明的是,该基于细胞分析的异常预测装置实现的方式与
基于细胞分析的异常预测方法的原理相同,此处不再赘述。
151.图3示出了一个实施例中计算机设备的内部结构图。该计算机设备具体可以是终端,也可以是服务器。如图3所示,该计算机设备包括通过系统总线连接的处理器、存储器和网络接口。其中,存储器包括非易失性存储介质和内存储器。该计算机设备的非易失性存储介质有存储操作系统,还可有存储计算机程序,该计算机程序被处理器执行时,可使得处理器实现上述的基于细胞分析的异常预测方法。该内存储器中也可储存有计算机程序,该计算机程序被处理器执行时,可使得处理器执行上述的基于细胞分析的异常预测方法。本领域技术人员可以理解,图3中示出的结构,仅仅是与本技术方案相关的部分结构的框图,并不构成对本技术方案所应用于其上的设备的限定,具体的设备可以包括比图中所示更多或更少的部件,或者组合某些部件,或者具有不同的部件布置。
152.在一个实施例中,提供了一种计算机设备,包括存储器和处理器,所述存储器有存储计算机程序,所述计算机程序被所述处理器执行时,使得所述处理器执行上述基于细胞分析的异常预测方法的步骤。
153.在一个实施例中,提出了一种计算机可读存储介质,有存储计算机程序,计算机程序被处理器执行时,使得处理器执行上述基于细胞分析的异常预测方法的步骤。
154.可以理解的是,上述基于基于细胞分析的异常预测方法、装置、计算机设备以及计算机可读存储介质属于一个总的发明构思,实施例可相互适用。
155.本领域普通技术人员可以理解实现上述实施例方法中的全部或部分流程,是可以通过计算机程序来指令相关的硬件来完成,所述的程序可存储于一非易失性计算机可读取存储介质中,该程序在执行时,可包括如上述各方法的实施例的流程。其中,本技术所提供的各实施例中所使用的对存储器、存储、数据库或其它介质的任何引用,均可包括非易失性和/或易失性存储器。非易失性存储器可包括只读存储器(rom)、可编程rom(prom)、电可编程rom(eprom)、电可擦除可编程rom(eeprom)或闪存。易失性存储器可包括随机存取存储器(ram)或者外部高速缓冲存储器。作为说明而非局限,ram以多种形式可得,诸如静态ram(sram)、动态ram(dram)、同步dram(sdram)、双数据率sdram(ddrsdram)、增强型sdram(esdram)、同步链路(synchlink)dram(sldram)、存储器总线(rambus)直接ram(rdram)、直接存储器总线动态ram(drdram)、以及存储器总线动态ram(rdram)等。
156.对所公开的实施例的上述说明,使本领域专业技术人员能够实现或使用本发明。对这些实施例的多种修改对本领域的专业技术人员来说将是显而易见的,本文中所定义的一般原理可以在不脱离本发明的精神或范围的情况下,在其他实施例中实现。因此,本发明将不会被限制于本文所示的这些实施例,而是要符合与本文所公开的原理和新颖特点相一致的最宽的范围。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1