确定血管中心线真伪以及截断位置的方法与装置与流程
确定血管中心线真伪以及截断位置的方法与装置
1.本案为基于于2021年04月30日提交的中国专利局、申请号为2021104842117、申请名称“确定血管中心线真伪以及截断位置的方法与装置”的案件提出的分案申请。
技术领域
2.本技术涉及医疗影像领域,具体而言,涉及一种确定血管中心线真伪以及截断位置的方法、装置、计算机可读存储介质与处理器。
背景技术:
3.从医疗影像(ct造影/核磁共振/超声影像等)中分割冠脉血管具有非常重要的临床意义。在临床中,对于冠脉血管结构分析是理解冠脉血管病变描述冠脉血管疾病的必要环节。医学影像中冠脉血管的分割对于图像理解、图像分析、中心线提取、图像分割、模型重构有很高的研究价值与技术挑战。传统的血管分割算法大都未能同时兼顾复杂影像中血管分割的准确性与效率,且分割结果容易受到图像质量的影响。
4.血管中心线的提取需要用到相关的图像分割算法,图像语义分割算法是一种将图像中的每一个像素按照类别进行分类的算法。基于神经网络的语义分割算法2014年被首次提出,经过几年的快速发展,图像语义分割算法在图像分割的结果和速度上均取得了显著的提高。与图像分类算法不同,图像语义分割需要对图像每个像素点进行精确分割,图像语义分割是像素级别的。但是由于卷积神经网络在进行卷积和池化过程中丢失了图像细节,即特征图像逐渐变小,很难做到每一个像素点都能够精确的分割。图像语义分割算法的结果很大程度上取决于图像的特征提取方面,图像的特征提取的越充分,语义分割像素的正确率就会越高,目前主流的效果显著的图像语义分割算法的采样方式有3种。u-net网络模型采用将特征在通道维度拼接在一起,以更好的利用浅层特性图的信息。deeplab系列网络模型采用了空洞卷积来提取图像特征,空洞卷积的使用增大了过滤器的感受野,使对特征的提取更加全面。特征金字塔模型通过将深层特征信息与浅层信息结合以提高图像信息的提取效率。但以上3种图像特征的采样方式都不能解决边界像素分类难的问题。由于医疗图像中血管分支多且杂乱,边界像素分类的准确性直接影响着整体图像的分割效果,而且对于贴近骨骼,组织,病变等的血管,由于像素流明接近,这些血管的边界特征不是特别明显,也加大了血管分割的难度。
5.即采用现有技术中的图像分割算法未能精确提取血管的中心线,无法准确推荐血管截断位置。
技术实现要素:
6.本技术的主要目的在于提供一种确定血管中心线真伪以及截断位置的方法、装置、计算机可读存储介质与处理器,以解决现有技术中图像分割算法未能精确提取血管的中心线,无法准确推荐血管截断位置的问题。
7.为了实现上述目的,根据本技术的一个方面,提供了一种确定血管中心线真伪以
及截断位置的方法,包括:采用深度学习算法构建目标血管的3d血管模型;获取所述目标血管的原始中心线;根据所述原始中心线构建空间树模型;根据所述3d血管模型和所述空间树模型,确定真实中心线和血管截断位置;根据所述3d血管模型和所述空间树模型,确定真实中心线,包括:将所述3d血管模型和所述空间树模型融合;确定所述3d血管模型中的血管分支与所述空间树模型中的树枝的重合度;在所述重合度大于阈值的情况下,确定所述树枝对应的所述原始中心线为预定中心线,所述预定中心线的部分或者全部为所述真实中心线。
8.进一步地,采用深度学习算法构建目标血管的3d血管模型,包括:获取所述目标血管的原始3d影像;对所述原始3d影像进行切分得到多个2d影像;采用所述深度学习算法构建分割模型;采用所述分割模型对所述2d影像进行运算,得到2d分割图像;将多个所述2d分割图像拼接,得到所述3d血管模型。
9.进一步地,在采用所述深度学习算法构建分割模型的过程中,所述方法还包括:配置所述2d影像的采样点数;配置所述2d影像的大小。
10.进一步地,在采用所述深度学习算法构建分割模型的过程中,所述方法还包括:配置第一分类参数,所述第一分类参数为前景像素的分类参数;配置第二分类参数,所述第二分类参数为背景像素的分类参数,所述第一分类参数是所述第二分类参数的预定倍。
11.进一步地,采用所述深度学习算法构建分割模型,包括:在gpu加速下,采用所述深度学习算法构建所述分割模型。
12.进一步地,确定所述3d血管模型中的血管分支与所述空间树模型中的树枝的重合度,包括:获取所述3d血管模型中的血管分支上各点的第一坐标;获取所述空间树模型中的树枝上各点的第二坐标;根据所述第一坐标和所述第二坐标相等的对数,确定所述重合度。
13.进一步地,根据所述原始中心线构建空间树模型,包括:从所述原始中心线的末端倒推获取所述原始中心线上各点的空间位置;将各所述点的空间位置转化为3d图像的索引信息;根据多个所述3d图像的索引信息构建所述空间树模型。
14.根据本技术的另一个方面,提供了一种确定血管中心线真伪以及截断位置推荐的装置,包括:第一构建单元,用于采用深度学习算法构建目标血管的3d血管模型;获取单元,用于获取所述目标血管的原始中心线;第二构建单元,用于根据所述原始中心线构建空间树模型;确定单元,用于根据所述3d血管模型和所述空间树模型,确定真实中心线和血管截断位置;
15.进一步地,所述确定单元包括:第一融合模块,用于将所述3d血管模型和所述空间树模型融合;第二确定模块,用于确定所述3d血管模型中的血管分支与所述空间树模型中的树枝的重合度;第三确定模块,用于在所述重合度大于阈值的情况下,确定所述树枝对应的所述原始中心线为预定中心线,所述预定中心线的部分或者全部为所述真实中心线。
16.根据本技术的又一个方面,提供了一种计算机可读存储介质,所述计算机可读存储介质包括存储的程序,其中,在所述程序运行时控制所述计算机可读存储介质所在设备执行任意一种所述的确定血管中心线真伪以及截断位置的方法。
17.根据本技术的再一个方面,提供了一种处理器,所述处理器用于运行程序,其中,所述程序运行时执行任意一种所述的确定血管中心线真伪以及截断位置的方法。
18.应用本技术的技术方案,通过采用深度学习算法构建目标血管的3d血管模型,可
以构建出精确的3d血管模型,再获取目标血管的原始中心线,再将所有的原始中心线组合成空间树模型,进而将精确的3d血管模型和空间树模型融合,根据融合的结果,可以实现对真实中心线和血管的截断位置的精确确定。结合空间树模型和深度学习算法能够大幅提高血管真伪判别以及截断位置推荐的准确性,极大的提高了医疗影像中血管判定以及截断位置选择的效率。
附图说明
19.构成本技术的一部分的说明书附图用来提供对本技术的进一步理解,本技术的示意性实施例及其说明用于解释本技术,并不构成对本技术的不当限定。在附图中:
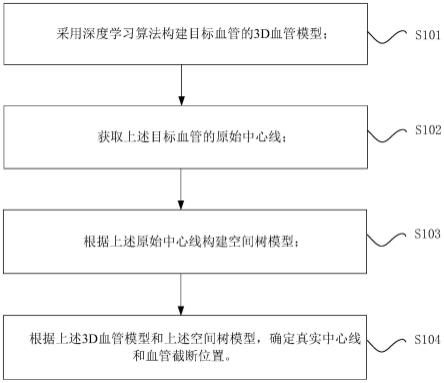
20.图1示出了根据本技术的实施例的确定血管中心线真伪以及截断位置的方法流程图;
21.图2示出了根据本技术的实施例的冠脉血管真伪判别以及截断位置推荐结果图;
22.图3示出了根据本技术的实施例的构建目标血管的3d血管模型过程图;
23.图4示出了根据本技术的实施例的确定血管中心线真伪以及截断位置的装置示意图。
具体实施方式
24.需要说明的是,在不冲突的情况下,本技术中的实施例及实施例中的特征可以相互组合。下面将参考附图并结合实施例来详细说明本技术。
25.为了使本技术领域的人员更好地理解本技术方案,下面将结合本技术实施例中的附图,对本技术实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例仅仅是本技术一部分的实施例,而不是全部的实施例。基于本技术中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都应当属于本技术保护的范围。
26.需要说明的是,本技术的说明书和权利要求书及上述附图中的术语“第一”、“第二”等是用于区别类似的对象,而不必用于描述特定的顺序或先后次序。应该理解这样使用的数据在适当情况下可以互换,以便这里描述的本技术的实施例。此外,术语“包括”和“具有”以及他们的任何变形,意图在于覆盖不排他的包含,例如,包含了一系列步骤或单元的过程、方法、系统、产品或设备不必限于清楚地列出的那些步骤或单元,而是可包括没有清楚地列出的或对于这些过程、方法、产品或设备固有的其它步骤或单元。
27.应该理解的是,当元件(诸如层、膜、区域、或衬底)描述为在另一元件“上”时,该元件可直接在该另一元件上,或者也可存在中间元件。而且,在说明书以及权利要求书中,当描述有元件“连接”至另一元件时,该元件可“直接连接”至该另一元件,或者通过第三元件“连接”至该另一元件。
28.为了便于描述,以下对本技术实施例涉及的部分名词或术语进行说明:
29.点采样(pointrend):是一种特殊的图像语义分割算法,该算法引入了对图像中每一个点的监督来提高图像整体的分割结果。相比传统的图像分割算法模型,点采样(pointrend)算法模型在自然场景和道路场景图像分割的结果取得了显著的提升。
30.正如背景技术中所介绍的,现有技术中的图像分割算法未能精确提取血管的中心
线,无法准确推荐血管截断位置,为解决图像分割算法未能精确提取血管的中心线,无法准确推荐血管截断位置的问题。本技术的实施例提供了一种确定血管中心线真伪以及截断位置的方法、装置、计算机可读存储介质与处理器。
31.根据本技术的实施例,提供了一种确定血管中心线真伪以及截断位置的方法。
32.图1是根据本技术实施例的确定血管中心线真伪以及截断位置的方法的流程图。如图1所示,该方法包括以下步骤:
33.步骤s101,采用深度学习算法构建目标血管的3d血管模型;
34.步骤s102,获取上述目标血管的原始中心线;
35.步骤s103,根据上述原始中心线构建空间树模型;
36.步骤s104,根据上述3d血管模型和上述空间树模型,确定真实中心线和血管截断位置。
37.具体地,采用最短路径算法得到原始中心线,具体的实现方式是根据给定的起始位置和终止位置,计算两者之间的最短路径从而获得中心线。
38.具体地,采用深度学习算法确定的3d血管模型较为准确。
39.具体地,根据上述原始中心线构建空间树模型的实现方式是将所有的原始中心线组合起来得到空间树模型。具体地,从原始中心线的末端倒推获取原始中心线上点的空间位置,并将各点的空间位置转化为3d图像的索引信息(各点在3d图像中的坐标)来构建中心线的空间模型。
40.具体地,如图2所示,图2中的纯黑色的部分表示3d血管模型(是一种冠脉血管的3d血管模型),有一部分原始中心线被3d血管模型包裹,有一部分原始中心线未被3d血管模型包裹,可以初步确定被3d血管模型包裹的原始中心线为真实的中心线,未被3d血管模型包裹原始中心线可能是真实的中心线也可能是虚假的中心线。
41.具体地,如图2所示,将3d血管模型和上述空间树模型融合在一起,使得原始中心线与3d血管模型的对应位置融合在一起,根据融合的结果,确定真实中心线和血管的截断位置。
42.具体地,将原始中心线与3d血管模型融合的具体的方式是:将两者统一至同一套坐标系统下达到融合的效果。
43.具体地,上述血管可以为冠脉血管、腹部器官等。上述目标血管的原始医疗影像可以为cta影像,mri影像等。
44.传统的冠脉血管的建模都是根据预分割的模型,人工的去除预分割模型中非冠脉血管的部分,比如静脉血管等,建模难度大,效果差,效率低。本技术的方案无需人工处理,且大大提高了血管真伪判别以及截断位置推荐的准确性。
45.上述方案中,通过采用深度学习算法构建目标血管的3d血管模型,可以构建出精确的3d血管模型,再获取目标血管的原始中心线,再将所有的原始中心线组合成空间树模型,进而将精确的3d血管模型和空间树模型融合,根据融合的结果,可以实现对真实中心线和血管的截断位置的精确确定。结合空间树模型和深度学习算法能够大幅提高血管真伪判别以及截断位置推荐的准确性,极大的提高了医疗影像中血管判定以及截断位置选择的效率。
46.需要说明的是,在附图的流程图示出的步骤可以在诸如一组计算机可执行指令的
计算机系统中执行,并且,虽然在流程图中示出了逻辑顺序,但是在某些情况下,可以以不同于此处的顺序执行所示出或描述的步骤。
47.本技术的一种实施例中,根据上述3d血管模型和上述空间树模型,确定真实中心线和血管截断位置,包括:将上述3d血管模型和上述空间树模型融合;从上述空间树模型的树枝的树梢(末端)开始查询,上述树枝与上述3d血管模型开始重叠的位置(第一次重叠的位置)为上述血管截断位置(如图2所示);确定从上述树梢至上述血管截断位置对应的上述原始中心线为虚假中心线;去掉上述虚假中心线后,剩余的部分为上述真实中心线。由图2可以看出,真实的中心线可能是被3d血管模型包裹,也可能不被3d血管模型包裹。即第一次重叠的位置之后的中心线无论是否被包裹,均视为真实的中心线。
48.本技术的一种实施例中,根据上述3d血管模型和上述空间树模型,确定真实中心线,包括:将上述3d血管模型和上述空间树模型融合;确定上述3d血管模型中的血管分支与上述空间树模型中的树枝的重合度;在上述重合度大于阈值的情况下,确定上述树枝对应的上述原始中心线为预定中心线,上述预定中心线的部分或者全部为上述真实中心线。即重合度越大是真实中心线的可能性越大。在上述重合度小于或者等于阈值的情况下,确定树枝对应的上述原始中心线为虚假中心线。
49.具体地,确定3d血管模型中的血管分支与上述空间树模型中的树枝的重合度,包括:获取3d血管模型中的血管分支上各点的第一坐标;获取空间树模型中的树枝上各点的第二坐标;根据上述第一坐标和上述第二坐标相等的对数,确定重合度,对数越大,则重合度越高,对数越小,则重合度越低。
50.本技术的一种实施例中,采用深度学习算法构建目标血管的3d血管模型,包括:获取上述目标血管的原始3d影像;对上述原始3d影像进行切分得到多个2d影像;采用上述深度学习算法构建分割模型;采用上述分割模型对上述2d影像进行运算,得到2d分割图像;将多个上述2d分割图像拼接,得到上述3d血管模型。具体地,本实施例中的深度学习算法可以采用pointrend图像分割算法。图3a为cta影像(原始3d影像),图3b为cta影像的切片(2d影像),图3c为cta影像的切片归一化处理后的结果,图3d为切片中冠脉血管分割结果(2d分割图像),图3e为将切片分割结果拼接起来的cta中冠脉血管的分割结果(3d血管模型)。采用分割模型对归一化处理后的2d影像进行运算,得到2d分割图像,以得到更为准确的2d分割图像。
51.本技术的一种实施例中,在采用上述深度学习算法构建分割模型的过程中,上述方法还包括:配置上述2d影像的采样点数;配置上述2d影像的大小。即根据血管图像的特性,适应性地设置2d影像上的采样点数,以及适用性地配置2d影像的大小,以保证分割模型的构建速度和构建精度。具体地,针对采集到的大小为512*512的cta影像,可以将训练过程中采样点数设置为1024,将预测过程中的采样点数设置为4096,由于训练过程中采样的点的位置是随机的,所以在预测的时候可以选择不超过原图像像素个数的任意多个点进行预测即可,在实验过程中,预测过程中的点数设置为4096,模型的表现最佳。在模型训练过程中将输入数据的大小(2d影像的大小)随机设置为(256,384,512,640,768,896,1024);采用不同的采样点数和2d影像的大小对分割模型记性训练,得到训练结果,得到最优的训练结果对应的“采样点数”和“2d影像的大小”,将此“采样点数”和“2d影像的大小”作为后续的输入参数。使得模型的泛化效果达到最佳指标。具体地,本实施例中的深度学习算法可以采用
pointrend图像分割算法。
52.本技术的一种具体的实施例中,深度学习算法采用pointrend图像分割算法,由于pointrend图像分割算法有较好的边界识别效果,使得识别出的2d分割图像更为准确,解决边界像素分类难的问题,对于一些贴近骨骼,组织,病变等的血管,也可以达到较好的分割效果。利用pointrend模型的分割结果结合空间树模型大幅提高血管真伪判别以及截断位置推荐的准确性,极大的提高了医疗影像中血管判定以及截断位置选择的效率。
53.本技术的一种实施例中,在采用上述深度学习算法构建分割模型的过程中,上述方法还包括:配置第一分类参数,上述第一分类参数为前景像素的分类参数;配置第二分类参数,上述第二分类参数为背景像素的分类参数,上述第一分类参数是上述第二分类参数的预定倍。其中,第一分类参数是指“将前景像素误分为背景像素时造成的损失”,第二分类参数是指“将背景像素误分为前景像素时造成的损失”,从2d影像中分割出2d分割图像(即目标血管部分)其实是将背景图像与前景图像分割开,一般而言,前景图像(即目标血管部分)小于背景图像(即除目标血管之外的背景的部分),所以将前景像素误分为背景像素造成的影响相较于将背景图像误分为前景图像造成的影响较大,所以设置第一分类参数是上述第二分类参数的预定倍。例如,第一分类参数是第二分类参数的两倍。具体地,本实施例中的深度学习算法可以采用pointrend图像分割算法。通过设置第一分类参数和第二分类参数,有助于得到精确的2d分割图像。使得模型的泛化效果达到最佳指标。
54.本技术的一种实施例中,采用上述深度学习算法构建分割模型,包括:在gpu加速下,采用上述深度学习算法构建上述分割模型。利用gpu加速,能够大幅加快目标血管图像的分割速度,同时降低了其他分支血管和组织等对目标血管的干扰,并且减少了对初始医疗影像预处理的要求,对医疗影像中冠脉血管的分割具有很好的鲁棒性。
55.本技术实施例还提供了一种确定血管中心线真伪以及截断位置的装置,需要说明的是,本技术实施例的确定血管中心线真伪以及截断位置的装置可以用于执行本技术实施例所提供的用于确定血管中心线真伪以及截断位置的方法。以下对本技术实施例提供的确定血管中心线真伪以及截断位置的装置进行介绍。
56.图4是根据本技术实施例的确定血管中心线真伪以及截断位置的装置的示意图。如图4所示,该装置包括:
57.第一构建单元10,用于采用深度学习算法构建目标血管的3d血管模型;
58.获取单元20,用于获取上述目标血管的原始中心线;
59.第二构建单元30,用于根据上述原始中心线构建空间树模型;
60.确定单元40,用于根据上述3d血管模型和上述空间树模型,确定真实中心线和血管截断位置。
61.上述方案中,第一构建单元采用深度学习算法构建目标血管的3d血管模型,可以构建出精确的3d血管模型,获取单元获取目标血管的原始中心线,第二构建单元将所有的原始中心线组合成空间树模型,确定单元将精确的3d血管模型和空间树模型融合,根据融合的结果,可以实现对真实中心线和血管的截断位置的精确确定。结合空间树模型和深度学习算法能够大幅提高血管真伪判别以及截断位置推荐的准确性,极大的提高了医疗影像中血管判定以及截断位置选择的效率。
62.本技术的一种实施例中,确定单元包括第一融合模块、查询模块、第一确定模块和
处理模块,第一融合模块用于将上述3d血管模型和上述空间树模型融合;查询模块用于从上述空间树模型的树枝的树梢(末端)开始查询,上述树枝与上述3d血管模型开始重叠的位置(第一次重叠的位置)为上述血管截断位置(如图2所示);第一确定模块用于确定从上述树梢至上述血管截断位置对应的上述原始中心线为虚假中心线;处理模块用于去掉上述虚假中心线后,剩余的部分为上述真实中心线。由图2可以看出,真实的中心线可能是被3d血管模型包裹,也可能不被3d血管模型包裹。即第一次重叠的位置之后的中心线无论是否被包裹,均视为真实的中心线。
63.本技术的一种实施例中,确定单元包括第一融合模块、第二确定模块和第三确定模块,第一融合模块用于将上述3d血管模型和上述空间树模型融合;第二确定模块用于确定上述3d血管模型中的血管分支与上述空间树模型中的树枝的重合度;第三确定模块用于在上述重合度大于阈值的情况下,确定上述树枝对应的上述原始中心线为预定中心线,上述预定中心线的部分或者全部为上述真实中心线。即重合度越大是真实中心线的可能性越大。在上述重合度小于或者等于阈值的情况下,确定树枝对应的上述原始中心线为虚假中心线。
64.本技术的一种实施例中,第一构建单元包括获取模块、切分模块、构建模块、运算模块和拼接模块,获取模块用于获取上述目标血管的原始3d影像;切分模块用于对上述原始3d影像进行切分得到多个2d影像;构建模块用于采用上述深度学习算法构建分割模型;运算模块用于采用上述分割模型对上述2d影像进行运算,得到2d分割图像;拼接模块用于将多个上述2d分割图像拼接,得到上述3d血管模型。具体地,本实施例中的深度学习算法可以采用pointrend图像分割算法。图3a为cta影像(原始3d影像),图3b为cta影像的切片(2d影像),图3c为cta影像的切片归一化处理后的结果,图3d为切片中冠脉血管分割结果(2d分割图像),图3e为将切片分割结果拼接起来的cta中冠脉血管的分割结果(3d血管模型)。采用分割模型对归一化处理后的2d影像进行运算,得到2d分割图像,以得到更为准确的2d分割图像。
65.本技术的一种实施例中,上述装置还包括第一配置单元和第二配置单元,第一配置单元用于在采用上述深度学习算法构建分割模型的过程中,配置上述2d影像的采样点数;第二配置单元用于在采用上述深度学习算法构建分割模型的过程中,配置上述2d影像的大小。具体地,针对采集到的大小为512*512的cta影像,可以将训练过程中采样点数设置为1024,将预测过程中的采样点数设置为4096,由于训练过程中采样的点的位置是随机的,所以在预测的时候可以选择不超过原图像像素个数的任意多个点进行预测即可,在实验过程中,预测过程中的点数设置为4096,模型的表现最佳。在模型训练过程中将输入数据的大小(2d影像的大小)随机设置为(256,384,512,640,768,896,1024);采用不同的采样点数和2d影像的大小对分割模型记性训练,得到训练结果,得到最优的训练结果对应的“采样点数”和“2d影像的大小”,将此“采样点数”和“2d影像的大小”作为后续的输入参数。使得模型的泛化效果达到最佳指标。具体地,本实施例中的深度学习算法可以采用pointrend图像分割算法。
66.本技术的一种实施例中,上述装置还包括第三配置单元和第四配置单元,第三配置单元用于在采用上述深度学习算法构建分割模型的过程中,配置第一分类参数,上述第一分类参数为前景像素的分类参数;第四配置单元用于在采用上述深度学习算法构建分割
模型的过程中,配置第二分类参数,上述第二分类参数为背景像素的分类参数,上述第一分类参数是上述第二分类参数的预定倍。其中,第一分类参数是指“将前景像素误分为背景像素时造成的损失”,第二分类参数是指“将背景像素误分为前景像素时造成的损失”,从2d影像中分割出2d分割图像(即目标血管部分)其实是将背景图像与前景图像分割开,一般而言,前景图像(即目标血管部分)小于背景图像(即除目标血管之外的背景的部分),所以将前景像素误分为背景像素造成的影响相较于将背景图像误分为前景图像造成的影响较大,所以设置第一分类参数是上述第二分类参数的预定倍。例如,第一分类参数是第二分类参数的两倍。具体地,本实施例中的深度学习算法可以采用pointrend图像分割算法。通过设置第一分类参数和第二分类参数,有助于得到精确的2d分割图像。使得模型的泛化效果达到最佳指标。
67.本技术的一种实施例中,构建模块还用于在gpu加速下,采用上述深度学习算法构建上述分割模型。利用gpu加速,能够大幅加快目标血管图像的分割速度,同时降低了其他分支血管和组织等对目标血管的干扰,并且减少了对初始医疗影像预处理的要求,对医疗影像中冠脉血管的分割具有很好的鲁棒性。
68.所述确定血管中心线真伪以及截断位置的装置包括处理器和存储器,上述第一构建单元、获取单元、第二构建单元和确定单元等均作为程序单元存储在存储器中,由处理器执行存储在存储器中的上述程序单元来实现相应的功能。
69.处理器中包含内核,由内核去存储器中调取相应的程序单元。内核可以设置一个或以上,通过调整内核参数来实现对血管中心线真伪以及截断位置的确定。
70.存储器可能包括计算机可读介质中的非永久性存储器,随机存取存储器(ram)和/或非易失性内存等形式,如只读存储器(rom)或闪存(flash ram),存储器包括至少一个存储芯片。
71.本发明实施例提供了一种计算机可读存储介质,所述计算机可读存储介质包括存储的程序,其中,在所述程序运行时控制所述计算机可读存储介质所在设备执行所述确定血管中心线真伪以及截断位置的方法。
72.本发明实施例提供了一种处理器,所述处理器用于运行程序,其中,所述程序运行时执行所述确定血管中心线真伪以及截断位置的方法。
73.本发明实施例提供了一种设备,设备包括处理器、存储器及存储在存储器上并可在处理器上运行的程序,处理器执行程序时实现至少以下步骤:
74.步骤s101,采用深度学习算法构建目标血管的3d血管模型;
75.步骤s102,获取上述目标血管的原始中心线;
76.步骤s103,根据上述原始中心线构建空间树模型;
77.步骤s104,根据上述3d血管模型和上述空间树模型,确定真实中心线和血管截断位置。
78.本文中的设备可以是服务器、pc、pad、手机等。
79.本技术还提供了一种计算机程序产品,当在数据处理设备上执行时,适于执行初始化有至少如下方法步骤的程序:
80.步骤s101,采用深度学习算法构建目标血管的3d血管模型;
81.步骤s102,获取上述目标血管的原始中心线;
82.步骤s103,根据上述原始中心线构建空间树模型;
83.步骤s104,根据上述3d血管模型和上述空间树模型,确定真实中心线和血管截断位置。
84.本领域内的技术人员应明白,本技术的实施例可提供为方法、系统、或计算机程序产品。因此,本技术可采用完全硬件实施例、完全软件实施例、或结合软件和硬件方面的实施例的形式。而且,本技术可采用在一个或多个其中包含有计算机可用程序代码的计算机可用存储介质(包括但不限于磁盘存储器、cd-rom、光学存储器等)上实施的计算机程序产品的形式。
85.本技术是参照根据本技术实施例的方法、设备(系统)、和计算机程序产品的流程图和/或方框图来描述的。应理解可由计算机程序指令实现流程图和/或方框图中的每一流程和/或方框、以及流程图和/或方框图中的流程和/或方框的结合。可提供这些计算机程序指令到通用计算机、专用计算机、嵌入式处理机或其他可编程数据处理设备的处理器以产生一个机器,使得通过计算机或其他可编程数据处理设备的处理器执行的指令产生用于实现在流程图一个流程或多个流程和/或方框图一个方框或多个方框中指定的功能的装置。
86.这些计算机程序指令也可存储在能引导计算机或其他可编程数据处理设备以特定方式工作的计算机可读存储器中,使得存储在该计算机可读存储器中的指令产生包括指令装置的制造品,该指令装置实现在流程图一个流程或多个流程和/或方框图一个方框或多个方框中指定的功能。
87.这些计算机程序指令也可装载到计算机或其他可编程数据处理设备上,使得在计算机或其他可编程设备上执行一系列操作步骤以产生计算机实现的处理,从而在计算机或其他可编程设备上执行的指令提供用于实现在流程图一个流程或多个流程和/或方框图一个方框或多个方框中指定的功能的步骤。
88.在一个典型的配置中,计算设备包括一个或多个处理器(cpu)、输入/输出接口、网络接口和内存。
89.存储器可能包括计算机可读介质中的非永久性存储器,随机存取存储器(ram)和/或非易失性内存等形式,如只读存储器(rom)或闪存(flash ram)。存储器是计算机可读介质的示例。
90.计算机可读介质包括永久性和非永久性、可移动和非可移动媒体可以由任何方法或技术来实现信息存储。信息可以是计算机可读指令、数据结构、程序的模块或其他数据。计算机的存储介质的例子包括,但不限于相变内存(pram)、静态随机存取存储器(sram)、动态随机存取存储器(dram)、其他类型的随机存取存储器(ram)、只读存储器(rom)、电可擦除可编程只读存储器(eeprom)、快闪记忆体或其他内存技术、只读光盘只读存储器(cd-rom)、数字多功能光盘(dvd)或其他光学存储、磁盒式磁带,磁带磁磁盘存储或其他磁性存储设备或任何其他非传输介质,可用于存储可以被计算设备访问的信息。按照本文中的界定,计算机可读介质不包括暂存电脑可读媒体(transitory media),如调制的数据信号和载波。
91.还需要说明的是,术语“包括”、“包含”或者其任何其他变体意在涵盖非排他性的包含,从而使得包括一系列要素的过程、方法、商品或者设备不仅包括那些要素,而且还包括没有明确列出的其他要素,或者是还包括为这种过程、方法、商品或者设备所固有的要素。在没有更多限制的情况下,由语句“包括一个
……”
限定的要素,并不排除在包括要素的
过程、方法、商品或者设备中还存在另外的相同要素。
92.从以上的描述中,可以看出,本技术上述的实施例实现了如下技术效果:
93.1)、本技术的确定血管中心线真伪以及截断位置的方法,通过采用深度学习算法构建目标血管的3d血管模型,可以构建出精确的3d血管模型,再获取目标血管的原始中心线,再将所有的原始中心线组合成空间树模型,进而将精确的3d血管模型和空间树模型融合,根据融合的结果,可以实现对真实中心线和血管的截断位置的精确确定。结合空间树模型和深度学习算法能够大幅提高血管真伪判别以及截断位置推荐的准确性,极大的提高了医疗影像中血管判定以及截断位置选择的效率。
94.2)、本技术的确定血管中心线真伪以及截断位置的装置,第一构建单元采用深度学习算法构建目标血管的3d血管模型,可以构建出精确的3d血管模型,获取单元获取目标血管的原始中心线,第二构建单元将所有的原始中心线组合成空间树模型,确定单元将精确的3d血管模型和空间树模型融合,根据融合的结果,可以实现对真实中心线和血管的截断位置的精确确定。结合空间树模型和深度学习算法能够大幅提高血管真伪判别以及截断位置推荐的准确性,极大的提高了医疗影像中血管判定以及截断位置选择的效率。
95.以上所述仅为本技术的优选实施例而已,并不用于限制本技术,对于本领域的技术人员来说,本技术可以有各种更改和变化。凡在本技术的精神和原则之内,所作的任何修改、等同替换、改进等,均应包含在本技术的保护范围之内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1