在季铵碱协同作用下合成石榴石结构的锂镧锆氧系固体电解质材料的固相合成方法与流程
本发明属于无机材料合成领域,具体涉及一种在季铵碱协同作用下合成石榴石结构的锂镧锆氧系(Li-La-Zr-O,LLZO)固体电解质材料的固相合成方法。
背景技术:
目前已有多种固态电解质材料获得了国内外科研工作者的广泛关注与研究,包括非晶态的LiPON,氧化物体系的Li3xLa2/3-xTiO3(LLTO)、Li1+xAlxTi2-x(PO4)3 (LATP)、Li1+xAlxGe2-x(PO4)3(LAGP)、Li7La3Zr2O12(LLZO),硫化物体系的 xLi2S-(1-x)P2S5、Li10GeP2S12(LGPS),聚合物体系的聚氧化乙烯(PEO)等。其中,具有石榴石结构的氧化物型锂离子导体LLZO,因其较高的室温锂离子电导率、较宽的电化学窗口以及对金属锂和环境空气良好的稳定性等优势而备受青睐。
Weppner教授课题组在非专利文献Angew.Chem.Int.Ed.,2007,46, 7778-7781中首次报道了通过固相反应法合成的具有石榴石结构的锂离子导体 Li7La3Zr2O12(LLZO),其于25℃时的锂离子电导率高达~3.0×10-4S/cm,且于 18~300℃范围内的电导活化能为~0.30eV。并且,在申请号为200880023221.3 的中国发明专利“具有石榴石结构的离子导体”中,Weppner教授正式公开了 LLZO等具有石榴石型结构的化学稳定固体离子导体材料的相关物理特性及其制备方法,并提出其在电池、蓄电池、电致变色装置和其他电化学电池中的用途。之后,众多科研工作者对LLZO体系材料开展了大量的研究工作。
目前,用于LLZO系固体电解质材料的制备方法多种多样,包括固相反应法、 Pechini法、甘氨酸法、EDTA法、沉淀法等。其中,高温固相反应法所需的工艺设备比较简单,制备条件容易控制,易于实现大批量合成,因而最具工业化应用价值。进行固相反应时,所用的锂源化合物可以是氧化锂(Li2O)、无水氢氧化锂(LiOH)、一水合氢氧化锂(LiOH·H2O)、碳酸锂(Li2CO3)、硝酸(LiNO3)、硫酸锂(Li2SO4)、草酸锂(Li2C2O4)、醋酸锂(CH3COOLi)等中的一种或几种的混合物。不过,出于成本、环保等因素的考虑,更宜像镍钴锰酸锂(LiCoO2)、磷酸铁锂(LiFePO4)、钛酸锂(Li4Ti5O12)等正、负极材料一样,使用一水合氢氧化锂或碳酸锂作为工业化生产中的锂源进行合成(其他锂源化合物包括无水氢氧化锂在内,要么成本会高出许多,要么在参与高温固相反应时会释放出污染性气体,故而只适宜于实验室内小规模实验,却并非理想的工业合成原料)。相较而言,一水合氢氧化锂的熔点较低(~462℃,无水氢氧化锂为~471℃),活性更高,在与其他原料进行高温固相反应时能够起到有效的助烧结作用,使得在相对较低的反应温度下即可制得理想的目标产物;而碳酸锂的熔点则相对较高(~723℃),导致其参与高温固相反应时的反应活性相对较差,往往需要在更高温度或是经历更长时间的处理方能得到理想的目标产物。不过,一水合氢氧化锂的碱性和腐蚀性都是极强的,并且在批量加工时极易形成粉尘,会对人体造成灼伤和损害;此外,一水合氢氧化锂也易吸收空气中的二氧化碳而变质,需要妥善储存。相比之下,碳酸锂的稳定性和安全性则要更好一些。
对于LLZO系固体电解质材料的合成,根据大量非专利文献如Angew.Chem. Int.Ed.,2007,46,7778-7781、Inorg.Chem.,2011,50,1089-1097等中的描述,如使用碳酸锂作为锂源,需将碳酸锂粉体与其他原料包括镧源化合物、锆源化合物、掺杂元素化合物等充分混合均匀,并预压成块体后再做高温共烧方可得到立方相的LLZO系固体电解质材料,否则若将混合后的粉体直接高温共烧则会生成绝缘性的锆酸镧相;而如果使用一水合氢氧化锂(或无水氢氧化锂) 作为锂源,则只需将其与其他原料充分混匀后,直接在高温共烧便可制得立方相的LLZO系固体电解质材料。
对于工业化的大规模合成而言,先将混合均匀的各种原料预压成块体进行高温固相反应,而后再将烧结后的块体(通常硬度极高)研磨成粉体的作业方式,无疑会是非常复杂且成本高昂的,因而碳酸锂并不适宜于直接作为LLZO系固体电解质材料合成的工业化原料;而如果使用一水合氢氧化锂作为锂源进行 LLZO系固体电解质材料的工业化生产,基于其强碱性、强腐蚀性和不稳定性方面的考虑,必须谨慎对待一系列的加工和储存事宜,以防对作业人员造成伤害或发生变质。
季铵碱是一种有机强碱,其碱性与KOH、NaOH相当,在工业科研领域有着极为广泛的用途,可以作为有机硅合成方面的催化剂,作为沸石、分子筛合成的模板剂,作为气相色谱前处理剂,化学反应的相转移催化剂,有机酸的滴定剂,作为印刷电路板的蚀刻剂以及微电子芯片制造中的清洗剂等,目前国内外对季按碱的研究多限于短链季铵碱,对长链季铵碱的研究鲜有报道,而长链季铵碱不仅保持了传统短链季铵碱的强碱性,而且具有表面活性,因此可同时作为有机强碱和表面活性剂来使用,其应用领域比传统短链季按碱更为广泛。本发明人员首次尝试将季铵碱应用于LLZO系固体电解质材料的合成。
技术实现要素:
针对LLZO系固体电解质材料的工业化合成中,单纯使用一水合氢氧化锂 (LiOH·H2O)或碳酸锂(Li2CO3)作为锂源均存在一些弊端的现状,本发明提供了一种将季铵碱与锂源按一定比例复合搭配使用用于实现LLZO系固体电解质材料工业化制备的固相合成方法,该方法既可以满足无需将充分混合后的原料预压成块体便可直接高温共烧制得纯相的LLZO系固体电解质材料的基本需求,兼顾工业化合成中的高效性、环保性与安全性原则。
本发明所提供的在季铵碱协同作用下合成石榴石结构的LLZO系固体电解质材料的固相合成方法,合成中所采用的锂源为主要为碳酸锂,按一定比例复合搭配季铵碱,其中季铵碱与碳酸锂的摩尔比为:0.05:1~1:1。季铵碱的分子结构式如下:
其中,R1、R2、R3、R4分别独立的选自氢、烷基、烯基、炔基、苯基或芳基;或R1、R2、R3、R4分别独立的选自含有硼、硅、氮、磷、氧、硫、氟、氯、溴及碘中至少一种元素的基团;R1、R2、R3、R4均为独立取代基团,或其中两个相邻基团联合成环。
作为优选,所述季铵碱的分子结构式中R1、R2、R3、R4均为独立取代基团,且R1、R2、R3、R4分别为氢或者碳原子数为1~18的烷基。
季铵碱是一种有机强碱,其碱性与KOH、NaOH相当,与碳酸锂复合,可以发挥类似氢氧化锂的活性;特别是长链季铵碱不仅保持了传统短链季铵碱的强碱性,而且具有表面活性,因此可同时作为有机强碱和表面活性剂来使用。季铵碱与碳酸锂的摩尔比为:0.05:1~1:1,优选0.1:1~0.9:1。季铵碱比例过高,成本上升;季铵碱比例过低,协调作用不明显。
作为优选,所述LLZO系固体电解质材料具体为立方相石榴石结构的 Li7La3Zr2O12及对其进行各种掺杂和改性的衍生物Li7-δCzLa3-yByZr2-zAxO12(其中,A 为Ta、Nb、Sb、W、Y、V、Sc、Bi、Si、Ti、Te、Hf、Ge、Zn、Sn等元素中的一种或几种,B为Mg、Ca、Sr、Ba、Ce、Pr、Nd、Sm、Pm、Eu等元素中的一种或几种,C为Al、Ga、B、In、Tl等元素中的一种或几种,x、y、z符合0≤x ≤1,0≤y≤1,0≤z≤0.5,且x+y+z>0),包括但不限于Li6.5La3Zr1.5Ta0.5O12、 Li6.28Al0.24La3Zr2O12、Li6.15Al0.2La3Zr1.75Nb0.25O12、Li6.8La2.95Ca0.05Zr1.75Nb0.25O12、 Li6.6La3Zr1.6Sb0.4O12、Li6.75La3Zr1.75Nb0.25O12、Li6.25Ga0.25La3Zr2O12等氧化物。
作为优选,所述的固相合成方法按如下步骤进行:
(1)将所述锂源和季铵碱复合物与镧源化合物、锆源化合物及其他掺杂元素的对应原料化合物按目标产物LLZO系固体电解质材料分子式中的摩尔比进行称量并混合(其中所述混合锂源需过量2~15wt%以补偿在后续高温处理过程中的挥发性损失),同时加入适量的混料溶剂,球磨6~24小时。在季铵碱的作用下,尤其是长碳链季铵碱的作用下,可以使锂源和季铵碱的复合物与镧源化合物、锆源化合物及其他掺杂元素的对应原料化合物充分混合,从而促进高温下固相反应进行完全。
(2)借助一定技术手段将充分混磨好的原料混合物粉体与所述混料溶剂分离,从而获得充分干燥的固相反应原料混合物粉体。
(3)将所述充分干燥的固相反应原料混合物粉体装入坩埚或匣钵中,于高温反应6~24小时,得到所述目标产物LLZO系固体电解质材料。
作为优选,所述镧源化合物为氧化镧、氢氧化镧、碳酸镧、乙酸镧、草酸镧、硝酸镧、硫酸镧等中的一种或几种的混合物,优选为氧化镧,并在使用前将氧化镧于800~950℃焙烧1~24小时;所述锆源化合物为氧化锆、氢氧化锆、硝酸氧锆、乙酸锆、硝酸锆、碳酸锆、硫酸锆等中的一种或几种的混合物,优选为氧化锆,并在使用前将氧化锆于120~600℃焙烧1~24小时;所述其他掺杂元素的对应原料化合物为该掺杂元素的氧化物、氢氧化物、碳酸盐、硝酸盐等中的一种或几种的混合物,优选该掺杂元素的氧化物,如氧化钽、氧化铝、氧化铌、氧化锑、氧化钨等,并在使用前将所述掺杂元素的氧化物于120~600℃焙烧1~24小时。
作为优选,所述混料溶剂为无水乙醇、工业酒精、异丙醇、丙酮、去离子水中的一种。
作为优选,所述将充分混磨好的原料混合物粉体与所述混料溶剂分离的技术手段为喷雾干燥、离心分离、蒸馏、抽滤、冷冻干燥等技术中的一种。
作为优选,所述高温反应过程是在850~1000℃的高温进行的,优选在 900~950℃进行;所述高温反应的气氛既可以是环境空气,也可以是流动的空气或氧气气氛;所述高温反应之前的升温速率为1~10℃/min,反应结束后的降温速率为1~5℃/min。
作为优选,所述高温反应完成并降温后,可进一步通过球磨、砂磨等手段将所述目标产物LLZO系固体电解质材料的粒度控制到后续应用时所需水平。
本发明的有益效果:
作为优选,通过将所述季铵碱与锂源复合物用于所述LLZO系固体电解质材料的制备过程中,相比于单一使用碳酸锂作为锂源时的情况,可从根本上避免必须将充分混合的原料混合物粉体预压成块体后再于高温固相反应,而后又将烧结后的硬度极高的块体再度研磨成粉体的繁琐作业方式,同时相比于单一使用一水合氢氧化锂作为锂源时的情况,也可充分降低因一水合氢氧化锂的强碱性、强腐蚀性和不稳定性等弊端所带来的的安全和品质隐患。
作为优选,除强调采用季铵碱作为协同剂,其余制备工序与传统固相合成方法并无明显区别,因而制备工艺简单,操作条件温和,易于实现工业化推广。
附图说明
图1是本发明各实施例和对比例中所合成的LLZO系固体电解质材料的X射线衍射图。
图2是本发明部分实施例和对比例中所合成的LLZO系固体电解质材料在烧结为致密块体后的断面扫描电镜照片:a)实施例1;b)实施例2;c)实施例3; d)实施例4;e)对比例1;f)对比例3。
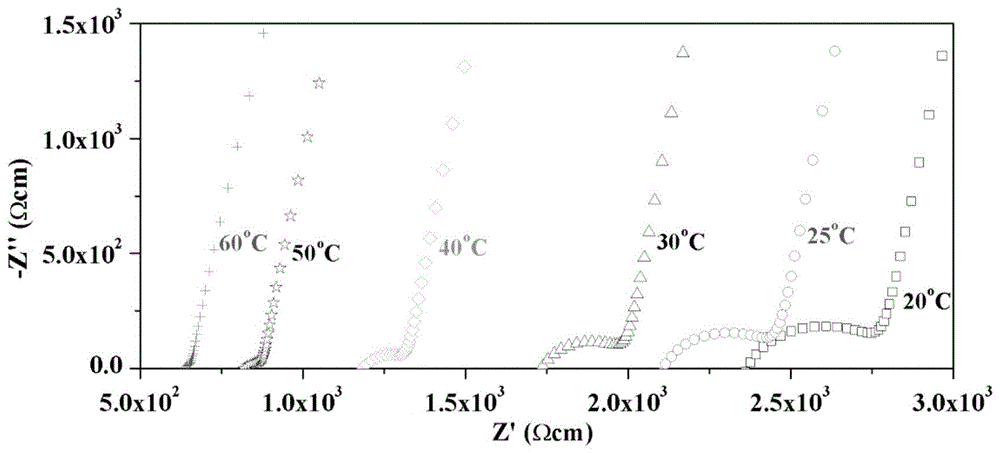
图3是本发明实施例2中所合成的Li6.75La3Zr1.75Nb0.25O12固体电解质材料:a) 与不同温度测得的交流阻抗谱图和b)阿伦尼乌斯曲线。
具体实施方式
以下结合附图和具体实施例对本发明作进一步详细说明,不过这些附图和具体实施例仅用于说明而非限制本发明。
本发明主要提供了一种使用碳酸锂和季铵碱复合物作为锂源制备LLZO系固体电解质材料的固相合成方法,具体流程为:
(1)将碳酸锂、季铵碱按一定比例与镧源化合物(如氧化镧、氢氧化镧等)、锆源化合物(如氧化锆)以及其他掺杂元素的对应原料化合物(如氧化钽、氧化铝、氧化铌等)按目标产物Li7La3Zr2O12或Li7-δCzLa3-yByZr2-zAxO12(其中,A为 Ta、Nb、Sb、W、Y、V、Sc、Bi、Si、Ti、Te、Hf、Ge、Zn、Sn等元素中的一种或几种,B为Mg、Ca、Sr、Ba、Ce、Pr、Nd、Sm、Pm、Eu等元素中的一种或几种,C为Al、Ga、B、In、Tl等元素中的一种或几种,x、y、z符合0≤x≤1,0 ≤y≤1,0≤z≤0.5,且x+y+z>0)中的化学计量比进行混合。为补偿后续高温处理过程中锂的挥发性损失,锂源的用量需酌情过量2~15wt%。随后加入适量的混料溶剂(如无水乙醇、工业酒精、异丙醇、丙酮、去离子水等)和研磨介质 (如氧化锆珠),球磨(行星或辊筒球磨)6~24小时以确保各种原料粉体充分混合均匀。
(2)待各种原料粉体经球磨充分混合均匀后,通过喷雾干燥、离心分离、蒸馏、抽滤或冷冻干燥等技术手段实现混料溶剂与原料混合物粉体的分离。在本发明的各项实施例和对比例中,都是通过喷雾干燥的方式实现混料溶剂与原料混合物粉体的分离过程的。
(3)将与混料溶剂充分分离后的固相反应原料混合物粉体装入坩埚或匣钵中,于850~1000℃高温反应6~24小时,从而制得目标产物LLZO系固体电解质材料。
(4)可进一步通过球磨、砂磨等手段将高温反应制得的LLZO系固体电解质材料磨细至D50为几微米甚至几百纳米的粉体。
通过X衍射衍射仪、激光粒度分析仪、交流阻抗谱等对最终制备的LLZO系固体电解质粉体的基本物性进行测量和分析。为测试LLZO系固体电解质材料的锂离子电导率,需将制得的LLZO系固体电解质粉体于~100Mpa压力下压制成型为直径~15mm、厚度~1mm的LLZO系固体电解质圆片,并于1050~1230℃的高温烧结10~36小时形成致密的块体。高温烧结时,为尽可能的避免锂的挥发所引起的材料物相改变(会生成绝缘性的锆酸镧相),需用母粉将LLZO系固体电解质圆片掩埋起来进行烧结(烧结完成后,掩埋的母粉中一般都会有锆酸镧作为杂相生成,而LLZO系固体电解质块体则会得益于母粉的保护而几乎没有杂相产生)。烧结时所用气氛可以为环境空气,也可以为流动的空气或氧气氛围,烧结前的升温速率一般为1~10℃/min,烧结完成后的降温速率为1~5℃/min。烧结后LLZO系固体电解质块体的致密度可通过扫描电子显微镜进行观测。烧结完成后,对LLZO系固体电解质块体的表面和侧边进行适度打磨以彻底去除边缘可能产生的锆酸镧等杂相,随后测量出片状LLZO系固体电解质块体的直径与厚度,再于其两表面均匀涂上一层金浆,烘干后于800~950℃的高温热处理0.5~2小时,降温后连接上银网和导线进行交流阻抗谱测试,LLZO系固体电解质块体的锂离子电导率σ可由下式(1)求得
式(1)中,t和d分别为片状LLZO系固体电解质块体的厚度和直径,Rg和Rgb分别为其晶粒电阻和晶界电阻,分别对应于测得的阻抗谱的Nyquist曲线中的半圆弧在高频段和低频段于实轴上的截距。
此外,LLZO系固体电解质材料的锂离子电导率σ与绝对温度T的关系符合下式(2)所示的Arrhenius方程
式(2)中,σ0为指前因子,Ea为LLZO系固体电解质材料的锂离子电导活化能,R为理想气体常数。据此,可利用交流阻抗谱测得不同温度下LLZO系固体电解质块体材料的锂离子电导率σ,然后以ln(σT)为纵轴、1000/T为横轴作图,所得直线的斜率即为-Ea/1000R,由此便可计算出LLZO系固体电解质块体材料的锂离子电导活化能Ea。
实施例1
实施例1中所合成的LLZO系固体电解质材料为Li6.28Al0.24La3Zr2O12,所用锂源复合物为季铵碱(四甲基氢氧化铵):Li2CO3=0.8:1(摩尔比)。
Li6.28Al0.24La3Zr2O12材料的合成:(1)预先将La2O3粉体于900℃焙烧12小时,将Al2O3和ZrO2粉体于600℃焙烧5小时;(2)按照分子式分别称取Li2CO3(Li 的过量值为5%)、Al2O3、La2O3、ZrO2以及季铵碱粉体于球磨罐中,加入适量异丙醇和氧化锆珠,在辊筒球磨机上球磨24小时;(3)球磨完成后,使用有机溶剂喷雾干燥设备去除并回收异丙醇,得到干燥的原料混合物粉体;(4)将原料混合物粉体装入匣钵中,以3℃/min的速率升温至900℃,于环境空气条件下焙烧12小时,之后再以3℃/min的速率降温至室温;(5)进一步通过球磨将固相反应后得到的Li6.28Al0.24La3Zr2O12粉体磨至D50为~3微米的细粉,进行相关物性表征。
Li6.28Al0.24La3Zr2O12材料的物性表征:(1)通过X衍射衍射手段对制得的 Li6.28Al0.24La3Zr2O12粉体的物相进行表征,结果如图1中所示,为理想的立方石榴石结构;(2)通过激光粒度分析仪对制得的Li6.28Al0.24La3Zr2O12粉体的粒径和比表面进行测试,结果如表1中所示;(3)将制得的Li6.28Al0.24La3Zr2O12粉体于~100MPa压力下压成直径~15mm、厚度~1mm的圆片并用母粉掩埋后放入刚玉坩埚中,以3℃/min的速率升温至1150℃,于流动空气气氛中烧结10小时,之后再以3℃/min的速率降温至室温,通过扫描电子显微镜对烧结后的 Li6.28Al0.24La3Zr2O12圆片的致密性进行观测,结果如图2a所示,致密度尚可,但仍有少量闭孔存在;(4)在烧结并打磨后的Li6.28Al0.24La3Zr2O12圆片的两面均匀涂上一层金浆,烘干后于900℃热处理2小时,待冷却至室温后进行电导率测试,所测得的室温(25℃)条件下的交流阻抗谱图,进一步结合式(1)所计算出的室温锂离子电导率已被列入表1中。
表1.本发明部分实施例和对比例所合成的LLZO系固体电解质材料的基本物性
实施例2
实施例2中所合成的LLZO系固体电解质材料为Li6.75La3Zr1.75Nb0.25O12,所用锂源复合物为季铵碱(四甲基氢氧化铵):Li2CO3=1:1(摩尔比)。
Li6.75La3Zr1.75Nb0.25O12材料的合成:(1)预先将La2O3粉体于900℃焙烧12小时,将Nb2O5和ZrO2粉体于600℃焙烧5小时;(2)按照分子式分别称取Li2CO3 (Li的过量值为3%)、Al2O3、La2O3、Nb2O5、ZrO2以及季铵碱粉体于球磨罐中,加入适量无水乙醇和氧化锆珠,在辊筒球磨机上球磨24小时;(3)球磨完成后,使用有机溶剂喷雾干燥设备去除并回收无水乙醇,得到干燥的原料混合物粉体;(4)将原料混合物粉体装入匣钵中,以3℃/min的速率升温至900℃,于环境空气条件下焙烧12小时,之后再以3℃/min的速率降温至室温;(5) 进一步通过球磨将固相反应后得到的Li6.75La3Zr1.75Nb0.25O12粉体磨至D50为~3微米的细粉,进行相关物性表征。
Li6.75La3Zr1.75Nb0.25O12材料的物性表征:(1)通过X射线衍射手段对制得的 Li6.75La3Zr1.75Nb0.25O12粉体的物相进行表征,结果如图1中所示,为理想的立方石榴石结构;(2)通过激光粒度分析仪对制得的Li6.75La3Zr1.75Nb0.25O12粉体的粒径和比表面进行测试,结果如表1中所示;(3)将制得的Li6.75La3Zr1.75Nb0.25O12粉体于~100MPa压力下压成直径~15mm、厚度~1mm的圆片并用母粉掩埋后放入刚玉坩埚中,以2℃/min的速率升温至1150℃,于流动氧气气氛中烧结10小时,之后再以3℃/min的速率降温至室温,通过扫描电子显微镜对烧结后的 Li6.75La3Zr1.75Nb0.25O12圆片的致密性进行观测,结果如图2b所示,致密度较好;(4) 在烧结并打磨后的Li6.75La3Zr1.75Nb0.25O12圆片的两面均匀涂上一层金浆,烘干后于 900℃热处理1小时,待冷却至室温后进行电导率测试,所测得的室温(25℃) 条件下的交流阻抗谱图,进一步结合式(1)所计算出的室温锂离子电导率已被列入表1中;(5)进一步在20℃、30℃、40℃、50℃、60℃等温度下测得 Li6.75La3Zr1.75Nb0.25O12圆片的交流阻抗谱图如图3a中所示,进一步结合式子(2),以ln(σT)为纵轴、1000/T为横轴所作Arrhenius曲线如图3b中所示,由此可推算出所制备的Li6.75La3Zr1.75Nb0.25O12材料的锂离子电导活化能为0.348eV。
实施例3
实施例3中所合成的LLZO系固体电解质材料为Li6.5La3Zr1.5Ta0.5O12,所用锂源为LiOH·H2O与Li2CO3,Li2CO3为主要锂盐,占80%(质量百分比),与季铵碱 (四乙基氢氧化铵)复合,季铵碱:Li2CO3=0.3:1(摩尔比)。
Li6.5La3Zr1.5Ta0.5O12材料的合成:(1)预先将La2O3粉体于900℃焙烧12小时,将Ta2O5和ZrO2粉体于600℃焙烧5小时;(2)按照分子式分别称取LiOH·H2O与 Li2CO3(Li的过量值为10%)、La2O3、Ta2O5、ZrO2以及季铵碱粉体于球磨罐中,加入适量异丙醇和氧化锆珠,在辊筒球磨机上球磨18小时;(3)球磨完成后,使用有机溶剂喷雾干燥设备去除并回收异丙醇,得到干燥的原料混合物粉体;(4)将原料混合物粉体装入匣钵中,以4℃/min的速率升温至950℃,于环境空气条件下焙烧10小时,之后再以3℃/min的速率降温至室温;(5)进一步通过球磨将固相反应后得到的Li6.5La3Zr1.5Ta0.5O12粉体磨至D50为~3微米的细粉,进行相关物性表征。
Li6.5La3Zr1.5Ta0.5O12材料的物性表征:(1)通过X衍射衍射手段对制得的 Li6.5La3Zr1.5Ta0.5O12粉体的物相进行表征,结果如图1中所示,为理想的立方石榴石结构;(2)通过激光粒度分析仪对制得的Li6.5La3Zr1.5Ta0.5O12粉体的粒径和比表面进行测试,结果如表1中所示;(3)将制得的Li6.5La3Zr1.5Ta0.5O12粉体于~100MPa压力下压成直径~15mm、厚度~1mm的圆片并用母粉掩埋后放入刚玉坩埚中,以3℃/min的速率升温至1150℃,于流动氧气气氛中烧结12小时,之后再以3℃/min的速率降温至室温,通过扫描电子显微镜对烧结后的 Li6.5La3Zr1.5Ta0.5O12圆片的致密性进行观测,结果如图2c所示,致密度较好;(4) 在烧结并打磨后的Li6.5La3Zr1.5Ta0.5O12圆片的两面均匀涂上一层金浆,烘干后于 900℃热处理2小时,待冷却至室温后进行电导率测试,所测得的室温(25℃) 条件下的交流阻抗谱图,进一步结合式(1)所计算出的室温锂离子电导率已被列入表1中。
实施例4
实施例4中所合成的LLZO系固体电解质材料为Li6.15Al0.2La3Zr1.75Nb0.25O12,所用锂源为LiOH·H2O与Li2CO3,Li2CO3为主要锂盐,占60%(质量百分比),与季铵碱(十六烷基三甲基氢氧化铵)复合,季铵碱:Li2CO3=0.1:1(摩尔比)。
Li6.15Al0.2La3Zr1.75Nb0.25O12材料的合成:(1)预先将La(OH)3粉体于200℃焙烧2小时,将Al2O3、Nb2O5和ZrO2粉体于600℃焙烧5小时;(2)按照分子式分别称取LiOH·H2O、Li2CO3(Li的过量值为8%)、Al2O3、La(OH)3、Nb2O5、ZrO2以及季铵碱,粉体于球磨罐中,加入适量去离子水和氧化锆珠,在辊筒球磨机上球磨24小时;(3)球磨完成后,使用开式喷雾干燥设备去除去离子水,得到干燥的原料混合物粉体;(4)将原料混合物粉体装入匣钵中,以3℃/min的速率升温至900℃,于环境空气条件下焙烧12小时,之后再以3℃/min的速率降温至室温;(5)进一步通过球磨将制得的Li6.15Al0.2La3Zr1.75Nb0.25O12粉体磨至D50为~3微米的细粉,进行相关物性表征。
Li6.15Al0.2La3Zr1.75Nb0.25O12材料的物性表征:(1)通过X衍射衍射手段对制得的Li6.15Al0.2La3Zr1.75Nb0.25O12粉体的物相进行表征,结果如图1中所示,为理想的立方石榴石结构;(2)通过激光粒度分析仪对制得的Li6.15Al0.2La3Zr1.75Nb0.25O12粉体的粒径和比表面进行测试,结果如表1中所示;(3)将制得的Li6.15Al0.2La3Zr1.75Nb0.25O12粉体于~100MPa压力下压成直径~15mm、厚度~1mm的圆片并用母粉掩埋后放入刚玉坩埚中,以3℃/min的速率升温至1150℃,于流动氩气气氛中烧结12小时,之后再以3℃/min的速率降温至室温,通过扫描电子显微镜对烧结后的Li6.15Al0.2La3Zr1.75Nb0.25O12圆片的致密性进行观测,结果如图2d 所示,致密度较好;(4)在烧结并打磨后的Li6.15Al0.2La3Zr1.75Nb0.25O12圆片的两面均匀涂上一层金浆,烘干后于900℃热处理1小时,待冷却至室温后进行电导率测试,所测得的室温(25℃)条件下的交流阻抗谱图,进一步结合式(1)所计算出的室温锂离子电导率已被列入表1中。
实施例5
实施例5中所合成的LLZO系固体电解质材料为Li6.6La3Zr1.6Sb0.4O12,所用锂源为LiOH·H2O与Li2CO3,Li2CO3为主要锂盐,占85%(质量百分比),与季铵碱 (四甲基氢氧化铵)复合,季铵碱:Li2CO3=0.5:1(摩尔比)。
Li6.6La3Zr1.6Sb0.4O12材料的合成与表征:(1)预先将La2O3粉体于900℃焙烧 12小时,将Sb2O3粉体于150℃焙烧2小时,将ZrO2粉体于600℃焙烧5小时; (2)按照分子式分别称取LiOH·H2O、Li2CO3、La2O3、Sb2O3和ZrO2以及季铵碱粉体于球磨罐中,加入适量无水乙醇和氧化锆珠,在行星球磨机上球磨12小时; (3)球磨完成后,使用有机溶剂喷雾干燥设备去除并回收无水乙醇,得到干燥的原料混合物粉体;(4)将原料混合物粉体装入匣钵中,以3℃/min的速率升温至950℃,于环境空气条件下焙烧10小时,之后再以3℃/min的速率降温至室温;(5)通过X衍射衍射手段对制得的Li6.6La3Zr1.6Sb0.4O12粉体的物相进行表征,结果如图1中所示,为理想的立方石榴石结构。
实施例6
实施例6中所合成的LLZO系固体电解质材料为Li6.8La2.95Ca0.05Zr1.75Nb0.25O12,所用锂源为LiOH·H2O与Li2CO3,Li2CO3为主要锂盐,占90%(质量百分比),与季铵碱(四甲基氢氧化铵)复合,季铵碱:Li2CO3=0.8:1(摩尔比)。
Li6.8La2.95Ca0.05Zr1.75Nb0.25O12材料的合成与表征:(1)预先将La(OH)3粉体于 200℃焙烧2小时,将Ca(OH)2粉体于150℃焙烧2小时,将Nb2O5和ZrO2粉体于600℃焙烧5小时;(2)按照分子式分别称取LiOH·H2O、Li2CO3、La(OH)3、Ca(OH)2、 Nb2O5、ZrO2以及季铵碱粉体于球磨罐中,加入适量异丙醇和氧化锆珠,在行星球磨机上球磨18小时;(3)球磨完成后,使用有机溶剂喷雾干燥设备去除并回收异丙醇,得到干燥的原料混合物粉体;(4)将原料混合物粉体装入匣钵中,以2.5℃/min的速率升温至900℃,于环境空气条件下焙烧12小时,之后再以 3℃/min的速率降温至室温;(5)通过X衍射衍射手段对制得的 Li6.8La2.95Ca0.05Zr1.75Nb0.25O12粉体的物相进行表征,结果如图1中所示,为理想的立方石榴石结构。
对比例1
对比例1中所合成的LLZO系固体电解质材料为Li6.75La3Zr1.75Nb0.25O12,所用锂源为LiOH·H2O,Li的过量值为3%。
Li6.75La3Zr1.75Nb0.25O12材料的合成:(1)预先将La2O3粉体于900℃焙烧12小时,将Nb2O5和ZrO2粉体于600℃焙烧5小时;(2)分别称取291.75克LiOH·H2O、488.71克La2O3、33.23克Nb2O5和215.64克ZrO2粉体于球磨罐中,加入适量无水乙醇和氧化锆珠,在辊筒球磨机上球磨24小时;(3)球磨完成后,使用有机溶剂喷雾干燥设备去除并回收无水乙醇,得到干燥的原料混合物粉体;(4) 将原料混合物粉体装入匣钵中,以3℃/min的速率升温至900℃,于环境空气条件下焙烧12小时,之后再以3℃/min的速率降温至室温;(5)进一步通过球磨将固相反应后得到的Li6.75La3Zr1.75Nb0.25O12粉体磨至D50为~3微米的细粉,进行相关物性表征。
Li6.75La3Zr1.75Nb0.25O12材料的物性表征:(1)通过X衍射衍射手段对制得的 Li6.75La3Zr1.75Nb0.25O12粉体的物相进行表征,结果如图1中所示,为理想的立方石榴石结构;(2)通过激光粒度分析仪对制得的Li6.75La3Zr1.75Nb0.25O12粉体的粒径和比表面进行测试,结果如表1中所示;(3)将制得的Li6.75La3Zr1.75Nb0.25O12粉体于~100MPa压力下压成直径~15mm、厚度~1mm的圆片并用母粉掩埋后放入刚玉坩埚中,以2℃/min的速率升温至1150℃,于流动氧气气氛中烧结10小时,之后再以3℃/min的速率降温至室温,通过扫描电子显微镜对烧结后的 Li6.75La3Zr1.75Nb0.25O12圆片的致密性进行观测,结果如图2e所示,致密度较好;(4) 在烧结并打磨后的Li6.75La3Zr1.75Nb0.25O12圆片的两面均匀涂上一层金浆,烘干后于 900℃热处理1小时,待冷却至室温后进行电导率测试,所测得的室温(25℃) 条件下的交流阻抗谱图,进一步结合式(1)所计算出的室温锂离子电导率已被列入表1中。
对比例1中的合成方案与实施例2中的方案除所用锂源复合物不同之外,其余合成与测试条件均是相同的,从表1、图1、图2和图3中相关结果的对比来看,两种方案所合成的Li6.75La3Zr1.75Nb0.25O12的基本物性是非常接近的。由此可见,本发明所述的使用碳酸锂/季铵碱复合物制备LLZO系固体电解质材料的固相合成方法可以获得与使用一水合氢氧化锂作为锂源时相当的合成效果,但却可充分降低因一水合氢氧化锂的强碱性、强腐蚀性和不稳定性等弊端所带来的的安全和品质隐患。
对比例2
对比例2中所合成的LLZO系固体电解质材料为Li6.75La3Zr1.75Nb0.25O12,所用锂源为Li2CO3,Li的过量值为3%。
Li6.75La3Zr1.75Nb0.25O12材料的合成与表征:(1)预先将La2O3粉体于900℃焙烧 12小时,将Nb2O5和ZrO2粉体于600℃焙烧5小时;(2)分别称取25.68克Li2CO3、 48.87克La2O3、3.32克Nb2O5和21.56克ZrO2粉体于球磨罐中,加入适量无水乙醇和氧化锆珠,在行星球磨机上球磨24小时;(3)球磨完成后,使用有机溶剂喷雾干燥设备去除并回收无水乙醇,得到干燥的原料混合物粉体;(4)将原料混合物粉体装入匣钵中,以3℃/min的速率升温至900℃,于环境空气条件下焙烧12 小时,之后再以3℃/min的速率降温至室温;(5)通过X衍射衍射手段对制得的 Li6.75La3Zr1.75Nb0.25O12粉体的物相进行表征,结果如图1中所示,可以看出并未得到立方相石榴石结构的Li6.75La3Zr1.75Nb0.25O12,产物中只有锆酸镧等杂相存在。
对比例3
对比例3中所合成的LLZO系固体电解质材料为Li6.75La3Zr1.75Nb0.25O12,所用锂源为Li2CO3,Li的过量值为3%。
Li6.75La3Zr1.75Nb0.25O12材料的合成:(1)预先将La2O3粉体于900℃焙烧12小时,将Nb2O5和ZrO2粉体于600℃焙烧5小时;(2)分别称取25.68克Li2CO3、48.87克La2O3、 3.32克Nb2O5和21.56克ZrO2粉体于球磨罐中,加入适量无水乙醇和氧化锆珠,在行星球磨机上球磨24小时;(3)球磨完成后,使用有机溶剂喷雾干燥设备去除并回收无水乙醇,得到干燥的原料混合物粉体;(4)将原料混合物粉体于~100MPa 压力下压成直径~22mm、厚度~3mm的圆片,装入坩埚中,以3℃/min的速率升温至900℃,于环境空气条件下焙烧12小时,之后再以3℃/min的速率降温至室温; (5)待降温后再将焙烧后的圆片块体放入玛瑙研钵中磨成粉末,随后进一步通过球磨将其磨至D50为~3微米的细粉,进行相关物性表征。
Li6.75La3Zr1.75Nb0.25O12材料的物性表征:(1)通过X衍射衍射手段对制得的 Li6.75La3Zr1.75Nb0.25O12粉体的物相进行表征,结果如图1中所示,为理想的立方石榴石结构,并无锆酸镧等杂相存在;(2)通过激光粒度分析仪对制得的 Li6.75La3Zr1.75Nb0.25O12粉体的粒径和比表面进行测试,结果如表1中所示;(3)将制得的Li6.75La3Zr1.75Nb0.25O12粉体于~100MPa压力下压成直径~15mm、厚度~1mm的圆片并用母粉掩埋后放入刚玉坩埚中,以2℃/min的速率升温至1150℃,于流动氧气气氛中烧结10小时,之后再以3℃/min的速率降温至室温,通过扫描电子显微镜对烧结后的Li6.75La3Zr1.75Nb0.25O12圆片的致密性进行观测,结果如图2f所示,致密度较好;(4)在烧结并打磨后的Li6.75La3Zr1.75Nb0.25O12圆片的两面均匀涂上一层金浆,烘干后于900℃热处理1小时,待冷却至室温后进行电导率测试,所测得的室温(25℃)条件下的交流阻抗谱图,进一步结合式(1)所计算出的室温锂离子电导率已被列入表1中。
对比例3与对比例2中Li6.75La3Zr1.75Nb0.25O12粉体的合成条件基本相同,只是对比例3中是对混磨后的原料混合物粉体进行了预压后再进行高温焙烧处理,最终便成功制得纯的立方相石榴石结构的Li6.75La3Zr1.75Nb0.25O12材料,而未做此预压处理的对比例2则只是合成了锆酸镧等杂相,由此可见当使用碳酸锂作为锂源进行 LLZO系固体电解质材料的合成时,是必须在高温固相反应前对原料混合物粉体做预压处理的。而在本发明的实施例中,当加入使用合适比例的季铵碱时,以几乎相同的合成条件制备固体电解质材料时,则无需做次预压处理便能顺利制得性能优异粉体,从而充分证明了本发明所提出的方案应用于LLZO系固体电解质材料的固相合成方案的优越性。
以上显示和描述了本发明的基本原理、主要特征和本发明的优点。本行业的技术人员应该了解,本发明不受上述实施例的限制,上述实施例和说明书中描述的只是说明本发明的原理,在不脱离本发明精神和范围的前提下,本发明还会有各种变化和改进,这些变化和改进都落入要求保护的本发明范围内。
- 还没有人留言评论。精彩留言会获得点赞!