非水电解液及其制备方法、以及锂离子电池与流程
1.本发明涉及电池技术领域,尤其涉及一种非水电解液及其制备方法、以及锂离子电池。
背景技术:
2.锂离子电池的电解液对于电池性质具有重要影响。对于非水电解液而言,若不能充分除去非水电解液中的水,则残留的水会与非水电解液中的锂盐反应生成具有腐蚀性的强酸,对非水电解液的锂盐和锂离子电池造成一定破坏。
3.相关技术中通过向电解液中添加酸酐类物质、含硅氧键化合物或含硅氮键化合物等作为除酸除水的添加剂。虽然这些添加剂能够在一定程度上降低电解液中的水含量与酸含量,但是其效果有限,对于水和酸的去除并不彻底,或者仍会生成新的具有反应活性的物质,继续对锂离子电池的相关材料造成破坏,导致锂离子电池性能的难以提升。
技术实现要素:
4.本技术公开一种非水电解液及其制备方法、以及锂离子电池,以解决现有非水电解液因对水和酸的去除效果有限,导致锂离子电池性能难以提升的问题。
5.第一个方面,本技术提供一种非水电解液,所述非水电解液包括:
6.非水溶剂;
7.锂盐;
8.第一添加剂,所述第一添加剂的结构通式如下:
[0009][0010]
其中,r1为-h、-cf3、-c(ch3)3、-so2cf3或-cooc(ch3)3中的一种;r2、r3、r4、r5各自独立的选自吸电子基团。
[0011]
可选地,在所述第一添加剂中,所述r2、r3各自独立的选自-h、-cf3、-c(ch3)3、-cooc(ch3)3、-ch3、-coch3或-c6h5cf3;r4、r5各自独立的选自-h、-cf3、-c(ch3)3、-cooc(ch3)3、-ch3、-coch3或-c6h5cf3。
[0012]
优选地,在所述第一添加剂中,r1、r2、r3、r4均为-h,r5为-c6h5cf3;
[0013]
或者,r1、r3、r4均为-h,r2、r5均为-cooc(ch3)3;
[0014]
或者,r1为-c(ch3)3,r2、r3、r4、r5均为-ch3;
[0015]
或者,r1为-so2cf3,r3、r4均为h,r2、r5均为-cooc(ch3)3。
[0016]
进一步地,所述第一添加剂在所述非水电解液中的质量百分比为0.5%~5%。
[0017]
可选地,所述非水溶剂包括碳酸二甲酯、碳酸二乙酯、碳酸甲乙酯、碳酸乙烯酯、碳酸丙烯酯中的一种或多种的组合。
[0018]
可选地,所述锂盐括六氟磷酸锂、双(三氟甲基磺酰)亚胺锂、双氟磺酰亚胺锂、四氟硼酸锂、双草酸硼酸锂、二氟草酸硼酸锂或高氯酸锂中的一种或多种的组合。
[0019]
进一步地,在所述非水电解液中,所述锂盐的浓度为0.8mol/l~1.5mol/l。
[0020]
进一步地,所述非水电解液还包括第二添加剂,所述第二添加剂包括氟代碳酸乙烯酯、碳酸亚乙烯酯、1,3-丙磺酸内酯、硫酸乙烯酯、三(三甲基硅烷)硼酸酯、三乙基磷酸酯中的一种或多种的组合。
[0021]
第二个方面,本技术提供一种如第一个方面所述的非水电解液的制备方法,所述制备方法包括以下步骤:在水分含量小于或者等于1ppm的惰性气体氛围中,向所述非水溶剂中加入干燥的所述锂盐,待所述锂盐溶解后,加入所述第一添加剂。
[0022]
第三个方面,本技术提供一种锂离子电池,所述锂离子电池包括如第一个方面所述的非水电解液。
[0023]
与现有技术相比,本发明具备以下有益效果:
[0024]
本技术发明人在经过大量实验测试后发现,通过在非水电解液中添加上述第一添加剂作为除水除酸的添加剂,能够较彻底的去除非水电解液中的水和酸,解决相关技术中添加剂不能较彻底有效的去除水和酸的问题。本技术实施例的上述第一添加剂为胍基化合物或胍基化合物的衍生物,其是具有一个碳氮双键和两个碳氮单键的特殊结构,具有较强的碱性且容易与水作用发生水解反应,生成有机胺类化合物,而有机胺能够继续与非水电解液中的游离酸发生反应生成中性的无机盐,从而达到更有效的除水和除酸效果。由于第一添加剂能够先除水、后除酸,且除水除酸后生成的物质不再具有反应活性,从而起到减少非水电解液的副反应、保护锂离子电池的正极材料的作用,利于提高整个锂离子电池体系额的稳定性,有助于提高锂离子电池的循环性能。
具体实施方式
[0025]
下面将对本发明实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例仅是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
[0026]
在本发明中,术语“上”、“下”、“左”、“右”、“前”、“后”、“顶”、“底”、“内”、“外”、“中”、“竖直”、“水平”、“横向”、“纵向”等指示的方位或位置关系,这些术语主要是为了更好地描述本发明及其实施例,并非用于限定所指示的装置、元件或组成部分必须具有特定方位,或以特定方位进行构造和操作。
[0027]
并且,上述部分术语除了可以用于表示方位或位置关系以外,还可能用于表示其他含义,例如术语“上”在某些情况下也可能用于表示某种依附关系或连接关系。对于本领域普通技术人员而言,可以根据具体情况理解这些术语在本发明中的具体含义。
[0028]
此外,术语“安装”、“设置”、“设有”、“连接”、“相连”应做广义理解。例如,可以是固定连接,可拆卸连接,或整体式构造;可以是机械连接,或电连接;可以是直接相连,或者是通过中间媒介间接相连,又或者是两个装置、元件或组成部分之间内部的连通。对于本领域普通技术人员而言,可以根据具体情况理解上述术语在本发明中的具体含义。
[0029]
此外,术语“第一”、“第二”等主要是用于区分不同的装置、元件或组成部分(具体
的种类和构造可能相同也可能不同),并非用于表明或暗示所指示装置、元件或组成部分的相对重要性和数量。除非另有说明,“多个”的含义为两个或两个以上。
[0030]
此外,本技术实施例使用锂盐、非水溶剂、第一添加剂和第二添加剂等试剂均可以通过商业购买获得。
[0031]
下面将结合具体实施例对本技术的技术方案作进一步的说明。
[0032]
在锂离子电池所使用的非水电解液中,由于锂盐对于水极为敏感,容易与水反应生成酸,而酸会对锂离子电池的正极材料等造成破坏,故可以通过向非水电解液中加入添加剂来严格控制水的含量。
[0033]
相关技术中使用酸酐类物质、含硅氧键化合物或含硅氮键化合物等作为除酸除水的添加剂。虽然上述添加剂能够去除非水电解液中的大部分水,但是申请人在实际开发和改进锂离子电池性能的过程中发现,使用上述添加剂的非水电解液,较难帮助锂离子电池的性能得到进一步提升。经过申请人的反复实验测试和分析,申请人发现,酸酐类物质、含硅氧键化合物或含硅氮键化合物在去除水和酸的能力方面存在明显的局限,即上述这些添加剂在除水后还是导致酸的形成或者仍然会生成新的官能团破坏锂离子电池的相关材料。
[0034]
申请人发现,酸酐类物质虽然可通过水解生成有机酸来减少非水电解液中的水含量,但是水解生成的有机酸在非水电解液的有机溶剂中仍具有一定解离度,会生成少量游离的h
+
离子,故酸酐类物质并不能较彻底的控制去除非水电解液中的水和酸。而含硅氧键化合物和含硅氮键化合物主要利用硅氧键、硅氮键易与水发生反应的特点,来降低电解液中的水含量与酸含量。但是这些化合物与水反应后会生成含有羟基的硅醇类物质,虽然其反应活性比水会低一些,但仍然具有反应活性,会继续与一些锂盐发生反应,对锂离子电池的整个体系造成破坏,不利于锂离子电池性能的综合提升。
[0035]
为更好地解决非水电解液中的除酸和除水问题,使非水电解液中的水和酸能够被更加彻底、更加有效的去除,以使锂离子电池的综合性能得到提升,本技术实施例提供一种非水电解液及其制备方法、以及锂离子电池来解决上述问题。
[0036]
第一个方面,本技术实施例提供一种非水电解液,包括非水溶剂、锂盐和第一添加剂,其中第一添加剂的结构通式如下:
[0037][0038]
其中,r1为-h、-cf3、-c(ch3)3、-so2cf3或-cooc(ch3)3中的一种;r2、r3、r4、r5各自独立的选自吸电子基团。
[0039]
本技术发明人在经过大量实验测试后发现,通过在非水电解液中添加上述第一添加剂作为除水除酸的添加剂,能够较彻底的去除非水电解液中的水和酸,解决相关技术中添加剂不能较彻底有效的去除水和酸的问题。本技术实施例的上述第一添加剂为胍基化合物或胍基化合物的衍生物,其是具有一个碳氮双键和两个碳氮单键的特殊结构,具有较强的碱性且容易与水作用发生水解反应,生成有机胺类化合物,而有机胺能够继续与非水电解液中的游离酸发生反应生成中性的无机盐,从而达到更有效的除水和除酸效果。由于第一添加剂能够先除水、后除酸,且除水除酸后生成的物质不再具有反应活性,从而起到减少
非水电解液的副反应、保护锂离子电池的正极材料的作用,利于提高整个锂离子电池体系的稳定性,有助于提高锂离子电池的循环性能。
[0040]
以r1、r3、r4、r5均为h,r2为吸电子基团为例,当第一添加剂与水发生反应时,其反应方程式为:
[0041][0042]
在上述反应中,胍基化合物与水发生反应生成带有氨基的化合物和酰胺类化合物,其中的氨基和酰胺继续与非水电解液中的酸发生反应,生成中性的有机盐。由于该反应中不会生成有机酸,故不会出现因有机酸的解离而持续破坏锂离子电池的相关结构(如正极材料、sei膜、cei膜等)的情况出现。又由于氨基和酰胺能够与酸发生反应,故即便非水电解液中存在游离的h
+
,也能够被反应掉,从而以先除水、再除酸的作用方式将水和酸有效去除。
[0043]
可选地,在第一添加剂中,r2、r3各自独立的选自-h、-cf3、-c(ch3)3、-cooc(ch3)3、-ch3、-coch3或-c6h5cf3;r4、r5各自独立的选自-h、-cf3、-c(ch3)3、-cooc(ch3)3、-ch3、-coch3或-c6h5cf3。当r2、r3、r4、r5这些连接在碳氮单键侧面的基团采用上述吸电子基团时,有利于碳氮单键的断裂,提高第一添加剂的活性,使其更容易与水发生水解反应,进而提高第一添加剂的除水能力。
[0044]
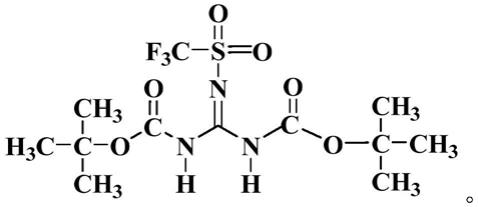
优选地,在第一添加剂中,r1、r2、r3、r4均为-h,r5为-c6h5cf3;或者,r1、r3、r4均为-h,r2、r5均为-cooc(ch3)3;或者,r1为-c(ch3)3,r2、r3、r4、r5均为-ch3;或者,r1为-so2cf3,r3、r4均为h,r2、r5均为-cooc(ch3)3。使用这些优选的第一添加剂时,本实施例非水电解液的除水和除酸效果更好。
[0045]
进一步地,第一添加剂在非水电解液中的质量百分比为0.5%~5%。
[0046]
其中,第一添加剂在非水电解液中的质量百分比为0.5%~5%包括该数值范围内的任一点值,例如第一添加剂在非水电解液中的质量百分比为0.5%、0.8%、1.0%、1.5%、2.0%、2.5%、3.0%、3.5%、4.0%、4.5%或5.0%。当第一添加剂在非水电解液的添加量为0.5%~5%质量百分比时,非水电解液的除水和除酸效果最佳,且不易引发其他副反应。
[0047]
可选地,非水溶剂包括碳酸二甲酯、碳酸二乙酯、碳酸甲乙酯、碳酸乙烯酯、碳酸丙烯酯中的一种或多种的组合。锂盐和第一添加剂在上述非水溶剂中具有良好的溶解性,有助于第一添加剂更好地分散在其中,起到相应的除水和除酸作用。
[0048]
可选地,锂盐括六氟磷酸锂、双(三氟甲基磺酰)亚胺锂、双氟磺酰亚胺锂、四氟硼酸锂、双草酸硼酸锂、二氟草酸硼酸锂或高氯酸锂中的一种或多种的组合。
[0049]
优选地,锂盐为六氟磷酸锂。虽然六氟磷酸锂是常用的锂盐电解质,但是六氟磷酸锂对水极为敏感,易与水反应生成hf,且游离的酸会与锂离子电池中的其他碱性物质发生反应重新生成水,这样会对锂盐造成持续性的破坏。不仅如此,hf还会对锂离子电池的正极材料、sei膜和cei膜造成破坏,甚至催化有机溶剂的分解,最终导致锂离子电池的性能变差。因此,对于采用六氟磷酸锂作为锂盐的锂离子电池来说,更加充分、更加有效的除水和除酸,就十分重要。在本技术实施例的非水电解液中,第一添加剂会先与水反应实现除水的作用,而后可通过水解反应生成的物质继续与酸反应实现除酸的作用,且除水和除酸后所生成的是中性的盐,而非仍具有一定解离能力的酸或者仍具有反应活性的羟基,不会对六
氟磷酸锂造成破坏而产生新的问题,由此可满足六氟磷酸锂对于除水除酸的高要求,进而利于提高锂离子电池的性能。
[0050]
进一步地,在非水电解液中,锂盐的浓度为0.8mol/l~1.5mol/l。其中,锂盐的浓度为0.8mol/l~1.5mol/l包括该浓度范围内的任一点值,例如锂盐的浓度为0.8mol/l、1.0mol/l、1.2mol/l或1.5mol/l。
[0051]
进一步地,非水电解液还包括第二添加剂,第二添加剂包括氟代碳酸乙烯酯、碳酸亚乙烯酯、1,3-丙磺酸内酯、硫酸乙烯酯、三(三甲基硅烷)硼酸酯、三乙基磷酸酯中的一种或多种的组合。在本技术实施例中,将第一添加剂与第二添加剂联合使用,二者可起到协同作用,使锂离子电池形成更加稳定的sei膜。
[0052]
第二个方面,本技术实施例提供一种如第一个方面的非水电解液的制备方法,包括以下步骤:在水分含量小于或者等于1ppm的惰性气体氛围中,向非水溶剂中加入干燥的锂盐,待锂盐溶解后,加入第一添加剂。
[0053]
本技术实施例的制备方法使用水分含量非常小的惰性气体为非水解电解液的制备提供干燥气氛,且使用干燥锂盐进行配制,由此在原料控制和制备过程控制非水电解液中的水含量,并进一步利用第一添加剂的除水出酸作用,使制备好的第一添加剂应用于锂离子电池时,具有极低的水含量和酸含量。
[0054]
第三个方面,本技术实施例提供一种锂离子电池,特别是锂离子二次电池,该锂离子电池包括第一个方面所述的非水电解液。由于该非水电解液采用的第一添加剂能够充分地去除水和去除酸,不会对锂离子电池的正极材料或sei膜、cei膜等造成持续性破坏,利于提高锂离子电池的综合性能。
[0055]
为了对本技术的技术方案及技术效果做更详细的说明,下面将通过更具体的实施例、应用例和性能测试结果等对本技术进行进一步说明。
[0056]
实施例一
[0057]
本实施例提供一种非水电解液,包括非水溶剂、锂盐、第一添加剂和第二添加剂,其中第一添加剂的结构式为:
[0058][0059]
其中,非水溶剂为碳酸乙烯酯碳酸二甲酯和碳酸甲乙酯的混合溶剂,锂盐为六氟磷酸锂,第二添加剂为碳酸亚乙烯酯。
[0060]
上述非水电解液的制备方法包括以下步骤:在水分含量≤1ppm的氩气气氛中,将30g的碳酸乙烯酯、30g的碳酸二甲酯和40g的碳酸甲乙酯进行混合得到混合溶剂,向混合溶剂中加入13.9g干燥的六氟磷酸锂固体,待六氟磷酸锂完全溶解后,再加入0.58g上述第一添加剂1-(3-(三氟甲基)苯基)胍、以及1.15g碳酸亚乙烯酯,混合均匀后得到非水电解液。
[0061]
在该非水电解液中,非水溶剂的组成为碳酸乙烯酯:碳酸二甲酯:碳酸甲乙酯=3:3:4(质量比),锂盐浓度为1mol/l,第一添加剂的含量为非水电解液总质量的0.5%,第二添加剂的含量为电解液总质量的1%。
[0062]
实施例二
[0063]
本实施例与实施例一的区别仅在于,本实施例中未加入第二添加剂。
[0064]
实施例三
[0065]
本实施例与实施例二的区别仅在于,本实施例的第一添加剂的结构式为:
[0066][0067]
实施例四
[0068]
本实施例与实施例二的区别仅在于,本实施例的第一添加剂的结构式为:
[0069][0070]
实施例五
[0071]
本实施例与实施例二的区别仅在于,本实施例的第一添加剂的结构式为:
[0072][0073]
实施例六
[0074]
本实施例与实施例二的区别仅在于,本实施例中第一添加剂在非水电解液中的质量比为2%。
[0075]
实施例七
[0076]
本实施例与实施例二的区别仅在于,本实施例中第一添加剂在非水电解液中的质量比为5%。
[0077]
实施例八
[0078]
本实施例与实施例一的区别仅在于,本实施例中的第二添加剂为氟代碳酸乙烯酯添加剂。
[0079]
对比例一
[0080]
本对比例与实施例一的区别在于,不使用第一添加剂和第二添加剂,非水电解液中非水溶剂的组成为碳酸乙烯酯:碳酸甲乙酯=3:7(质量比)。
[0081]
对比例二
[0082]
本对比例与实施例一的区别仅在于,不使用第一添加剂。
[0083]
对比例三
[0084]
本对比例与实施例六的区别仅在于,本对比例使用三(三甲基硅烷)磷酸酯这一含
硅氧键化合物作为除水的添加剂。
[0085]
对比例四
[0086]
本对比例与实施例六的区别仅在于,本对比例使用n,n-二乙氨基三甲基硅烷这一含硅氮键化合物作为除水的添加剂。
[0087]
本技术还对上述实施例和对比例进行了一系列性能测试。
[0088]
除水除酸能力测试
[0089]
将上述实施例和对比例的非水电解液放置三天后进行水分含量和酸度测试(按hf计),其中水分含量用卡尔费休水分仪进行测试,酸度用三乙胺溶液进行滴定测试。结果如下表1所示:
[0090] 水分/ppm酸度/ppm实施例一8.418.7实施例二5.111.4实施例三16.517.1实施例四11.216.3实施例五8.112.5实施例六3.25.4实施例七2.43.9实施例八8.217.8对比例一5645.2对比例二6847.6对比例三9.622.3对比例四8.524.7
[0091]
表1:非水电解液的除水除酸性能测试结果
[0092]
锂离子电池的循环稳定性测试
[0093]
电池采用购买所得未注液的软包装电池,向其中注入上述实施例和对比例电解液得到待测试循环稳定性的锂离子电池。其中,电池的正极材料为ncm811材料,电池的负极材料为改性天然石墨材料,电池设计的容量为1ah,电池的电解液注液量为4.0g。将上述锂离子电池在充放电仪上进行充放电循环测试,测试温度为25℃,循环倍率为1c,充电电压为3.0v~4.3v。计算循环后的容量保持率,计算公式为:第n次循环后的容量保持率=(第n次循环后的放电容量/首次循环放电容量)*100%。测试结果如下表2所示:
[0094] 300次循环容量保持率(%)实施例一98.2实施例二96.5实施例三94.2实施例四91.6实施例五95.9实施例六98.6实施例七89.1实施例八97.7
对比例一71.2对比例二90.2对比例三96.0对比例四95.4
[0095]
表2:使用非水电解液的锂离子电池的循环稳定性测试结果
[0096]
根据上述水分、酸度、循环稳定性的测试结果可以得出以下结论:
[0097]
(1)通过比较实施例一、实施例二、对比例一和对比例二的除水除酸结果可知,当非水电解液中使用第一添加剂时,非水电解液中的水分和酸度可以控制在较低水平;当非水电解液中不使用第一添加剂时,非水电解液中的水分和酸度明显升高很多。可见第一添加剂的加入确实能够将非水电解液中的水含量和酸含量控制在较低水平。
[0098]
通过比较实施例二、对比例三、对比例四的除水除酸结果可知,使用含硅氧键化合物或含硅氮键化合物作为除水的添加剂时,虽然其能够除水,但是酸的含量仍然超过20ppm。而对非水电解液进行除水的目的不仅是要除水,更是要控制酸的含量,这是因为游离的酸是对正极材料、sei膜等造成破坏的主要原因。而含硅氧键化合物或含硅氮键化合物仅具备一定除水能力,其生成的含羟基化合物导致其仍具有一定活性,无法有效控制酸的含量。
[0099]
(2)通过比较实施例二、实施例三、实施例四、实施例五的除水除酸结果和循环稳定性结果可知,虽然这些第一添加剂都能有效控制水和酸的含量,但是第一添加剂采用时,无论是对水和酸的含量控制,还是最终锂离子电池的循环稳定性都具有更佳的结果。可见,第一添加剂本身的官能团结构对其反应活性、控制水和酸的能力也具有一定影响。具体是,当第一添加剂的侧面所连的基团(即r2~r5)为吸电子基团时,有利于碳氮单键的断裂,有助于增强胍基化合物的活性,相比侧面所连接的为斥电子基团的胍基化合物,更容易与水反应发生水解,能提高胍基化合物的除水能力。而当r1为强吸电子基团时,则更不易发生水解,这是因为碳氮双键容易与相连的原子形成类似共轭键的结构,增强化合物的稳定性。
[0100]
(3)通过比较实施例二、实施例六、实施例七的测试结果可知,随着第一添加剂添加量的增多,非水电解液的除水除酸效果也逐步增强,当第一添加剂的添加量占非水电解液总质量的2%时,其除水除酸效果最佳,且此时的循环稳定性也最高。但当继续增加第一添加剂的添加量时,虽然水分含量和酸度仍有下降,但是锂离子电池的循环稳定性已开始下降。因此本技术实施例的第一添加剂的添加量占非水电解液的2%时,其综合效果最佳。
[0101]
(4)通过比较实施例一、实施例二、实施例八的测试结果可知,当本技术实施例的非水电解液中除了第一添加剂之外,还添加有第二添加剂时,锂离子电池的循环稳定性更高,可以达到98%左右,且同时兼具良好的除水除酸能力。这是由于第一添加剂能够有效地先除水、后除酸,保证锂离子电池体系形成的sei膜不会因非水电解液中存在的活性氢(即水和酸)而受到破坏,再结合第二添加剂有助于sei膜的形成,从而通过第一添加剂和第二添加剂的协同作用,进一步保证了sei膜的稳定性,使锂离子电池的循环稳定性得以提高。而在对比例一和对比例二中,锂离子电池的循环容量保持率明显下降较多,不如第一添加
剂与第二添加剂联用时的稳定性高。
[0102]
以上对本发明实施例公开的一种非水电解液及其制备方法、以及锂离子电池进行了详细介绍,本文中应用了具体个例对本发明的原理及实施方式进行了阐述,以上实施例的说明只是用于帮助理解本发明的技术方案及其核心思想;同时,对于本领域的一般技术人员,依据本发明的思想,在具体实施方式及应用范围上均会有改变之处,综上,本说明书内容不应理解为对本发明的限制。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1