油酸改性介孔氧化硅负载抗真菌药的复合材料及其制备方法与流程
本发明涉及一种油酸改性介孔氧化硅负载抗真菌药的复合材料,以及该复合材料的制备方法,属于抗菌材料技术领域。
背景技术:
据发明人所知,目前,二氧化硅材料以其良好的生物相容性而闻名。随着有序介孔氧化硅材料的出现,介孔氧化硅材料成为理想的药物递送载体,目前已有研究将sba-15作为药物控释的载体。
有研究人员通过溶剂法在二氯甲烷溶液中将抗真菌药伊曲康唑负载到sba-15上,以形成介孔氧化硅sba-15/伊曲康唑复合材料,使伊曲康唑分子在sba-15二氧化硅材料中分散存在,进而增强疏水性药物伊曲康唑在有序介孔氧化硅材料sba-15中的释放。然而,该复合材料在大量使用时易产生耐药菌株,从而威胁人类健康;该复合材料的药物伊曲康唑溶出仍然较快,且不能达到持续高效的抗真菌效果。亟待研制出能克服以上缺陷的复合材料。
技术实现要素:
本发明的目的在于:针对上述现有技术存在的问题,提出一种油酸改性介孔氧化硅负载抗真菌药复合材料的制备方法,所得材料具有长效抗真菌性能,对烟曲霉和白色念珠菌均有较强的杀伤作用,并且对白色念珠菌生物膜的形成具有明显的抑制作用,从而延缓耐药菌的产生。同时,还提出由该制备方法制得的复合材料,以及该复合材料的用途。
本发明解决其技术问题的技术方案如下:
一种油酸改性介孔氧化硅负载抗真菌药复合材料的制备方法,其特征是,包括以下步骤:
第一步、将介孔氧化硅分散于3-氨丙基三乙氧基硅烷与甲苯的混合溶液中,于反应条件下反应;反应后,收集固形物;将固形物洗涤、干燥后,得氨基化介孔氧化硅;
第二步、将氨基化介孔氧化硅分散于含有油酸和活化剂的二氯甲烷溶液中,于反应条件下反应;反应后,收集固形物;将固形物洗涤、干燥后,得oa修饰介孔氧化硅;
第三步、将oa修饰介孔氧化硅分散于正己烷中,作为第一液体;将十六烷基三甲基溴化铵溶于纯化水中,以氨水调节ph至7.0-10.0,加入第一液体,于反应条件下反应;反应后,收集固形物;将固形物洗涤、干燥后,得oa-ctab修饰介孔氧化硅;
第四步、将oa-ctab修饰介孔氧化硅分散于二氯甲烷中,加入含抗真菌药的二氯甲烷溶液,于反应温度下搅拌至溶剂挥干,干燥后即得油酸改性介孔氧化硅负载抗真菌药复合材料成品。
该制备方法在制得氨基化介孔氧化硅后,先以油酸修饰,继而以ctab修饰,最后负载抗真菌药以制得复合材料成品。该复合材料具有长效抗真菌性能,对烟曲霉和白色念珠菌均有较强的杀伤作用,并且对白色念珠菌生物膜的形成具有明显的抑制作用,从而延缓耐药菌的产生。
本发明进一步完善的技术方案如下:
优选地,第一步中,所述3-氨丙基三乙氧基硅烷与甲苯的体积比为0.1±0.005:1;所述介孔氧化硅与甲苯的质量体积比为0.2±0.005g:20±5ml;第一步中,先将介孔氧化硅于100℃±10℃干燥至少4小时,再将介孔氧化硅分散于3-氨丙基三乙氧基硅烷与甲苯的混合溶液中;第一步的反应条件为:反应温度78℃±5℃,反应时间至少12小时,反应过程中持续回流搅拌;采用过滤或离心的方式收集固形物;洗涤条件为:采用无水乙醇、去离子水分别洗涤至少3次;干燥温度为60℃±5℃。
采用该优选方案,可进一步优化第一步中的各物料比例、及各具体条件。其中,3-氨丙基三乙氧基硅烷即aptes。
优选地,第二步中,所述油酸与活化剂的摩尔比为1:1.2±0.1;所述油酸与二氯甲烷的比例为0.95±0.1mmol:20±5ml;所述氨基化介孔氧化硅与二氯甲烷溶液的质量体积比为40±1mg:4±1ml;所述活化剂为碳二亚胺;
第二步的反应条件为:反应温度为室温,反应时间至少12小时,反应过程中持续搅拌,室温指26℃±10℃;采用过滤或离心的方式收集固形物;洗涤条件为:采用无水乙醇洗涤至少3次;干燥温度为60℃±5℃。
采用该优选方案,可进一步优化第二步中的各物料比例、及各具体条件。其中,油酸即oa,碳二亚胺即edc。
优选地,第三步中,所述oa修饰介孔氧化硅与正己烷的比例为100±5mg:5±1ml;所述十六烷基三甲基溴化铵在纯化水中的浓度为10±1mmol/l:所述oa修饰介孔氧化硅与十六烷基三甲基溴化铵浓度的比例为10±0.5mg:1±0.1mmol/l。
采用该优选方案,可进一步优化第三步中的各物料比例。其中,十六烷基三甲基溴化铵即ctab。
优选地,第三步中,将十六烷基三甲基溴化铵溶于纯化水后,先将其加热至反应温度并保持,再以氨水调节ph;第三步的反应条件为:反应温度为40℃±5℃,反应时间至少1小时,反应过程中持续搅拌;采用过滤或离心的方式收集固形物;洗涤条件为:采用去离子水洗涤至少3次;干燥温度为60℃±5℃。
采用该优选方案,可进一步优化第三步中的各具体条件。
优选地,第四步中,所述抗真菌药为伊曲康唑;所述oa-ctab修饰介孔氧化硅与其二氯甲烷的比例为80±1mg:4±0.5ml;所述伊曲康唑与其二氯甲烷的比例为20±1mg:4±0.5ml;所得油酸改性介孔氧化硅负载抗真菌药复合材料中伊曲康唑的负载量为10-20wt%;第四步的反应温度为室温,室温指26℃±10℃;干燥采用40℃±5℃下真空干燥。
采用该优选方案,可进一步第四步中的各物料比例、各具体条件。其中,伊曲康唑即itz。
优选地,第一步中,所述介孔氧化硅为sba-15,且其制备过程为:
s1.将p123加至去离子水中,搅拌至澄清;加入盐酸溶液,加入氯化钠,搅拌混匀;逐滴加入正硅酸乙酯并搅拌反应;
s2.将所得混合物移至聚四氟乙烯高温反应釜中进行反应,之后于烘箱中老化;收集固形物,并将所得固形物洗涤、干燥;
s3.将固形物研磨成粉,煅烧后研磨即得sba-15。
采用该优选方案,可进一步明确介孔氧化硅及其具体制备过程。
本发明还提出:
采用前文所述制备方法制得的油酸改性介孔氧化硅负载抗真菌药复合材料。
该复合材料具有长效抗真菌性能,对烟曲霉和白色念珠菌均有较强的杀伤作用,并且对白色念珠菌生物膜的形成具有明显的抑制作用,从而延缓耐药菌的产生。
本发明还提出:
前文所述油酸改性介孔氧化硅负载抗真菌药复合材料的用途,其特征是,所述用途为用于制备抗真菌剂。
该用途为前文所述复合材料适用的抗真菌功能。
优选地,所述抗真菌剂针对的真菌包括烟曲霉、白色念珠菌。
采用该优选方案,可进一步明确针对的微生物种类。
与现有技术相比,本发明的有益效果如下:
本发明制备方法在制得氨基化介孔氧化硅后,先以油酸修饰,继而以ctab修饰,最后负载抗真菌药以制得复合材料成品。本发明复合材料具有长效抗真菌性能,对烟曲霉和白色念珠菌均有较强的杀伤作用,并且对白色念珠菌生物膜的形成具有明显的抑制作用,从而延缓耐药菌的产生。
附图说明
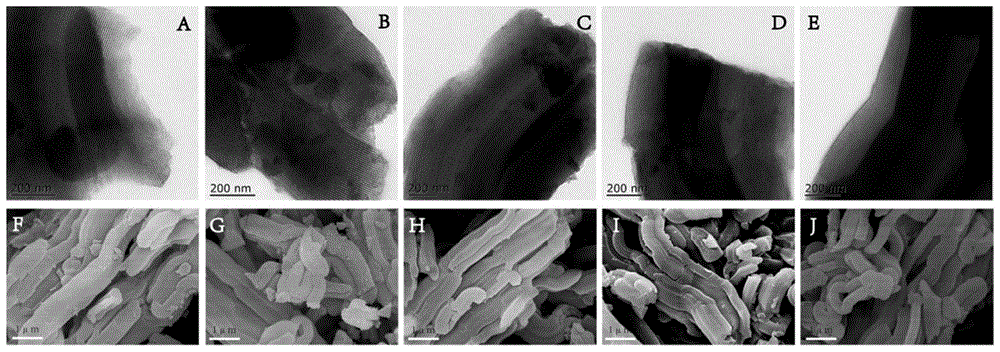
图1为本发明实施例4的透射电镜图(a~e)和扫描电镜(f~i),从左至右依次为sba-15、sba-15-nh2、sba-15-oa、sba-15-oa-ctab、sba-15-oa-ctab/itz。
图2为本发明实施例4中sba-15-oa-ctab/itz的能量色散光谱图。
图3为本发明实施例4的傅里叶红外光谱图,由上至下依次为sba-15、sba-15-nh2、sba-15-oa、sba-15-oa-ctab、sba-15-oa-ctab/itz。
图4为本发明实施例4的小角xrd图谱,由上至下依次为sba-15、sba-15-nh2、sba-15-oa、sba-15-oa-ctab/itz。
图5为本发明实施例4的氮气吸脱附图。
图6为本发明实施例4的热重分析图,按曲线右侧末端由上至下依次为sba-15、sba-15-nh2、sba-15-oa、sba-15-oa-ctab、sba-15-oa-ctab/itz。
图7本发明实施例4的itz体外释放曲线图。
图8为本发明实施例5中对烟曲霉(共培养72小时)的生长效果评价结果图。
图9为本发明实施例5中对白色念珠菌(共培养72小时)的生长效果评价结果图。
图10为本发明实施例6中对白色念珠菌(共培养24小时)的生物膜形成抑制效果的评价结果图。
图11为本发明实施例6中荧光分光光度计检测样本与烟曲霉孢子孵育过程中产生的活性氧的结果图。
图12为本发明实施例6中荧光显微镜检测sba-15-oa-ctab/itz与烟曲霉孢子孵育过程中产生的活性氧结果图(上:明场图像;下:荧光图像)。
具体实施方式
下面参照附图并结合实施例对本发明作进一步详细描述。但是本发明不限于所给出的例子。
实施例1
本实施例为制备介孔氧化硅sba-15。
本实施例的基本制备过程包括:
s1.将p123加至去离子水中,搅拌至澄清;加入盐酸溶液,加入氯化钠,搅拌混匀;逐滴加入正硅酸乙酯并搅拌反应;
s2.将所得混合物移至聚四氟乙烯高温反应釜中进行反应,之后于烘箱中老化;收集固形物,并将所得固形物洗涤、干燥;
s3.将固形物研磨成粉,煅烧后研磨即得sba-15。
以下是作为示例的具体制备过程:
称取4.0gp123,加80ml去离子水搅拌溶解至澄清。量取70ml3.4mhcl溶液加入到上述澄清溶液中,加入4.0gnacl,于40℃搅拌1h。在搅拌状态下,逐滴加入9.1ml正硅酸乙酯teos,于40℃下搅拌24h。将上述反应液转移至聚四氟乙烯高温反应釜中继续反应,之后置于烘箱中100℃老化24h。得到的产物离心去除上清,收集固形物,分别用乙醇、去离子水各洗涤三次,烘箱中干燥后研磨。将所得粉末转移至坩埚中,550℃焙烧6h,研磨备用,即为介孔氧化硅sba-15。保存备用于后续实施例。
实施例2
本实施例为制备oa修饰介孔氧化硅。
本实施例的基本制备过程包括:
第一步、将介孔氧化硅分散于3-氨丙基三乙氧基硅烷与甲苯的混合溶液中,于反应条件下反应;反应后,收集固形物;将固形物洗涤、干燥后,得氨基化介孔氧化硅;记作sba-15-nh2。
其中,3-氨丙基三乙氧基硅烷与甲苯的体积比为0.1±0.005:1;介孔氧化硅与甲苯的质量体积比为0.2±0.005g:20±5ml。具体而言,先将介孔氧化硅于100℃±10℃干燥至少4小时,再将介孔氧化硅分散于3-氨丙基三乙氧基硅烷aptes与甲苯的混合溶液中;反应条件为:反应温度78℃±5℃,反应时间至少12小时,反应过程中持续回流搅拌;采用过滤或离心的方式收集固形物;洗涤条件为:采用无水乙醇、去离子水分别洗涤至少3次;干燥温度为60℃±5℃。
第二步、将氨基化介孔氧化硅分散于含有油酸oa和活化剂edc的二氯甲烷溶液中,于反应条件下反应;反应后,收集固形物;将固形物洗涤、干燥后,得oa修饰介孔氧化硅;记作sba-15-oa。
其中,油酸与活化剂的摩尔比为1:1.2±0.1;油酸与二氯甲烷的比例为0.95±0.1mmol:20±5ml;氨基化介孔氧化硅与二氯甲烷溶液的质量体积比为40±1mg:4±1ml;活化剂为碳二亚胺。具体而言,反应条件为:反应温度为室温,反应时间至少12小时,反应过程中持续搅拌,室温指26℃±10℃;采用过滤或离心的方式收集固形物;洗涤条件为:采用无水乙醇洗涤至少3次;干燥温度为60℃±5℃。
以下是作为示例的具体制备过程:
第一步、先将实施例1的sba-15于烘箱中100℃干燥4h;再从中称取200mgsba-15分散于2mlaptes和20ml的甲苯混合溶液中,78℃回流搅拌12h。反应后,过滤收集固形物,将固形物以无水乙醇、去离子水洗涤三次,烘箱中60℃干燥过夜,得氨基化介孔氧化硅;记作sba-15-nh2。
第二步、称取100mgsba-15-nh2分散到10ml的含有0.48mmol油酸oa和0.58mmol活化剂edc的二氯甲烷dcm溶液中,室温搅拌过夜;反应后,离心收集固形物,将固形物以无水乙醇洗涤,烘干,得oa修饰介孔氧化硅;记作sba-15-oa。
实施例3
本实施例为制备油酸改性介孔氧化硅负载抗真菌药复合材料。
本实施例的基本制备过程包括:
第一步、将实施例2的oa修饰介孔氧化硅分散于正己烷中,作为第一液体;将十六烷基三甲基溴化铵ctab溶于纯化水中,以氨水调节ph至7.0-10.0,加入第一液体,于反应条件下反应;反应后,收集固形物;将固形物洗涤、干燥后,得oa-ctab修饰介孔氧化硅;记作sba-15-oa-ctab。
其中,oa修饰介孔氧化硅与正己烷的比例为100±5mg:5±1ml;十六烷基三甲基溴化铵在纯化水中的浓度为10±1mmol/l:oa修饰介孔氧化硅与十六烷基三甲基溴化铵浓度的比例为10±0.5mg:1±0.1mmol/l。具体而言,将十六烷基三甲基溴化铵溶于纯化水后,先将其加热至反应温度并保持,再以氨水调节ph;反应条件为:反应温度为40℃±5℃,反应时间至少1小时,反应过程中持续搅拌;采用过滤或离心的方式收集固形物;洗涤条件为:采用去离子水洗涤至少3次;干燥温度为60℃±5℃。此步通过酰胺反应接枝油酸分子。
第二步、将oa-ctab修饰介孔氧化硅分散于二氯甲烷中,加入含抗真菌药伊曲康唑itz的二氯甲烷溶液,于反应温度下搅拌至溶剂挥干,干燥后即得油酸改性介孔氧化硅负载抗真菌药复合材料成品;记作sba-15-oa-ctab/itz。
其中,oa-ctab修饰介孔氧化硅与其二氯甲烷的比例为80±1mg:4±0.5ml;伊曲康唑与其二氯甲烷的比例为20±1mg:4±0.5ml;所得油酸改性介孔氧化硅负载抗真菌药复合材料中伊曲康唑的负载量为10-20wt%;反应温度为室温,室温指26℃±10℃;干燥采用40℃±5℃下真空干燥。
以下是作为示例的具体制备过程:
第一步、称取100mg实施例2的sba-15-oa超声分散于5ml正己烷中,作为第一液体;称取91mgctab溶于25ml水中,水浴加热至40℃,nh3·h2o调ph至7.0-10.0;将第一液体加到ctab溶液中,40℃搅拌1h。反应后,离心收集固形物;将固形物水洗,烘干。即得sba-15-oa-ctab。
第二步、称取80mg上述sba-15-oa-ctab分散于4ml二氯甲烷中,加入4ml含20mg的itz的二氯甲烷溶液,室温搅拌至溶剂挥干,40℃真空干燥,获得负载量处于10-20wt%之间的复合材料成品,记作sba-15-oa-ctab/itz。
实施例4
对实施例3制得的sba-15-oa-ctab/itz进行特性鉴定,其结果包括:透射电镜(tem)图、扫描电镜(sem)图、能量色散光谱图、傅里叶红外光谱图、小角xrd图谱、氮气吸脱附图、热重分析图、体外释放曲线。鉴定时采用的对照组选自sba-15、sba-15-nh2、sba-15-oa、sba-15-oa-ctab、sba-15-oa-ctab/itz。
以下为实施例3示例制得的sba-15-oa-ctab/itz的各项特性鉴定结果(且各对照组:sba-15由实施例1示例制得,sba-15-nh2、sba-15-oa分别由实施例2示例制得,sba-15-oa-ctab由实施例3示例制得):
图1为合成过程中一系列介孔硅材料(sba-15、sba-15-nh2、sba-15-oa、sba-15-oa-ctab、sba-15-oa-ctab/itz)的透射电镜(tem)和扫描电镜(sem)图,从图中可以看出,sba-15形貌规整,呈短棒状,经改性及负载伊曲康唑药物后,短棒状规整结构没有明显改变,说明该复合材料制备过程中不会改变sba-15的形貌特征。
图2为sba-15-oa-ctab/itz的能量色散光谱图,图中可见复合材料含有c、o、si、br、cl等元素并且元素分布均匀一致,证明修饰物和药物分子成功负载在载体上。
图3为sba-15-oa-ctab/itz及各对照组(sba-15、sba-15-nh2、sba-15-oa、sba-15-oa-ctab)的傅里叶红外光谱图,在2928和2852波数处出现的c-h特征峰,这来源于修饰物上含有的亚甲基;sba-15-oa-ctab/itz在1694波数处出现新的c=o特征峰,这归因于负载的药物的三氮唑环上的羰基特征峰。
图4为sba-15-oa-ctab/itz及各对照组(sba-15、sba-15-nh2、sba-15-oa)的小角xrd图谱,图中可见sba-15-oa-ctab/itz的特征衍射峰对应sba-15的(100),(110)和(200)晶面,进一步证实其六方介观结构。
图5为sba-15-oa-ctab/itz及各对照组(sba-15、sba-15-nh2、sba-15-oa、sba-15-oa-ctab)的氮气吸脱附图,典型的iv型吸附等温线进一步说明复合材料的介观结构,随着氨基、油酸和ctab的逐步嫁接以及伊曲康唑的负载,孔径的逐步减小表明sab-15成功修饰和负载药物。
图6为sba-15-oa-ctab/itz及各对照组(sba-15、sba-15-nh2、sba-15-oa、sba-15-oa-ctab)的热重分析图,通过各分子分解温度和重量热损失速率的差异可见,复合材料的重量热损失模式不同,说明sab-15的成功修饰。
图7为sba-15-oa-ctab/itz及itz的体外释放曲线,从图中可以看出该复合材料中药物伊曲康唑itz的释放相较于游离的药物呈现出缓慢释放的趋势,说明该复合材料在体外具有良好的缓释功能。
此外,其它由实施例3制得的sba-15-oa-ctab/itz的各项特性鉴定结果与以上结果相同或基本相同,且由各项特性鉴定结果得出的结论与以上结论相同。
实施例5
本实施例针对多个介孔硅材料进行抗菌实验。这些介孔硅材料包括:实施例3制得的sba-15-oa-ctab和sba-15-oa-ctab/itz,实施例2制得的sba-15-oa,以及作为对比例的sba-15/itz、sba-15-oa/itz。此外,还采用伊曲康唑的市售抗菌药剂sporanox作为对比例。
在对比例中,sba-15/itz为采用实施例1所得sba-15代替sba-15-oa-ctab,并按照实施例3第二步的相同条件制得;sba-15-oa/itz为采用实施例2所得sba-15-oa代替sba-15-oa-ctab,并按照实施例3第二步的相同条件制得。
以下为具体结果,其中,sba-15-oa-ctab和sba-15-oa-ctab/itz由实施例3示例制得;sba-15-oa由实施例2示例制得;sba-15/itz为采用实施例1示例所得sba-15代替sba-15-oa-ctab,并按照实施例3示例第二步的相同条件制得;sba-15-oa/itz为采用实施例2示例所得sba-15-oa代替sba-15-oa-ctab,并按照实施例3示例第二步的相同条件制得。
用表面涂布法将烟曲霉孢子或白色念珠菌分别接种于yag培养基或沙氏琼脂培养基上,将上述测试样本分别制成悬浊液,均匀涂布于固体培养基上,在37℃培养箱中共培养,实验结果如图8和图9所示。
由图8可见,sba-15-oa、sba-15-oa-ctab均未显示出明显的抗菌性能;在含有相同含量的伊曲康唑的sporanox、sba-15/itz、sba-15-oa/itz中,对烟曲霉的生长均表现出一定程度的抑制作用,但随着时间增长培养基上均有明显的菌落生长;仅有涂布含有相同含量的伊曲康唑的sba-15-oa-ctab/itz的培养基可维持72小时无烟曲霉生长。
由图9可见,sba-15-oa、sba-15-oa-ctab均未显示出明显的抗菌性能;在含有相同含量的伊曲康唑的sporanox、sba-15/itz、sba-15-oa-ctab/itz都表现出对白色念珠菌明显的抗菌活性,可长期抑制菌落的生长。
此外,其它由实施例3制得的sba-15-oa-ctab/itz的各项实验结果与以上结果相同或基本相同,且由各项实验结果得出的结论与以上结论相同。
以上各项结果表明,sba-15-oa-ctab/itz具有广谱长效的抗真菌作用。
实施例6
本实施例针对多个介孔硅材料进行抗菌实验。这些介孔硅材料包括:实施例3制得的sba-15-oa-ctab/itz,以及作为对比例的sba-15/itz。此外,还采用伊曲康唑的市售抗菌药剂sporanox作为对比例。
sba-15/itz为采用实施例1所得sba-15代替sba-15-oa-ctab,并按照实施例3第二步的相同条件制得。
以下为具体结果,其中,sba-15-oa-ctab/itz由实施例3示例制得;sba-15/itz为采用实施例1示例所得sba-15代替sba-15-oa-ctab,并按照实施例3示例第二步的相同条件制得。
将上述测试样本分别制成悬浊液,梯度稀释加入到白色念珠菌悬液中,37℃共孵育24小时后,弃去培养液,固定生物膜,显微镜观察白色念珠菌生物膜的形成状态,实验结果如图10所示。
在对照组sporanox、sba-15/itz中可见成熟的生物膜形成,由孢子、菌丝和假菌丝组成致密的网状系统,黏附在基底表面。在sba-15-oa-ctab/itz处理组可见,在较低的浓度时,可见到浮游细胞,明显地抑制了菌丝的生长,抑制生物膜的形成。
进一步验证sba-15-oa-ctab/itz的抗真菌机制是否与活性氧的产生有关。将上述测试样本分别制成悬浊液,加入到烟曲霉孢子悬液中,37℃共孵育2小时后,加入终浓度10微摩尔的dcfh-da荧光探针,37℃共孵育30分钟后,dcfh-da荧光探针进入细胞后生成dcfh,进一步与胞内活性氧作用生成绿色荧光物质,分别用荧光分光光度计检测;进而以荧光显微镜检测。以此来检测sba-15-oa-ctab/itz抗菌过程中是否产生活性氧。
图11的荧光分光光度计检测结果中,与sba-15/itz、itz(单独的伊曲康唑原料药)、h2o2处理组相比,sba-15-oa-ctab/itz处理组于ex=425nm,em=530nm处荧光强度明显更高,且比sporanox处理组略高,说明在抗菌过程中有活性氧的产生。
图12为荧光显微镜结果,可见sba-15-oa-ctab/itz有明显的绿色荧光,即为dcf+细胞,进一步证实了抗菌过程中活性氧累积。
此外,其它由实施例3制得的sba-15-oa-ctab/itz的实验结果与以上结果相同或基本相同,且由实验结果得出的结论与以上结论相同。
以上结果表明,sba-15-oa-ctab/itz在抗菌的同时能对白色念珠菌生物膜的形成具有明显的抑制作用,从而延缓耐药菌的产生;而且sba-15-oa-ctab/itz的抗真菌机制与活性氧的产生有关。
除上述实施例外,本发明还可以有其他实施方式。凡采用等同替换或等效变换形成的技术方案,均落在本发明要求的保护范围。
- 还没有人留言评论。精彩留言会获得点赞!