一种用于高等级生物安全实验室的物表消毒液及其制备方法与流程
[0001]
本发明涉及生物技术领域,具体为一种用于高等级生物安全实验室的物表消毒液及其制备方法。
背景技术:
[0002]
自然界存在各种微生物,其中有些微生物可导致人类或动物发生疾病,这类微生物称为病原微生物,根据病原微生物对人和动物的传染性和致病性不同,将其分为不同的类别,其中能够导致人类或动物严重疾病的病原微生物叫高致病性病原微生物,比如埃博拉病毒、sars冠状病毒、新型冠状病毒和艾滋病病毒等。为了研究这些高致病性病原微生物就需要相应的高防护水平的生物安全实验室,即高等级生物安全实验室。
[0003]
在研究高致病性病原微生物过程中,既要采取各种措施确保实验人员不能受到感染,又要保证高致病性病原微生物不能由实验室内逃逸到外部环境中去。因此,高等级生物安全实验室的建设与其他实验室存在显著差别,实验室建设既需要有各种生物安全防护设施设备防止病原微生物逃逸,又要使用消毒剂对高致病性病原微生物进行杀灭。由于生物安全防护设施设备包括围护结构、气密门、化学淋浴、双扉灭菌器、活毒废水处理系统、高效空气过滤器、实验室通风系统等都大量使用不锈钢等金属材料,并利用焊接工艺连接成型,并且在使用消毒剂时需要将消毒剂喷洒到上述设施设备表面,因此高等级生物安全实验室在选择消毒剂时,既要确保消毒剂对高致病性病原微生物具有杀灭作用,同时还要对不锈钢等金属构件没有腐蚀作用或者腐蚀作用很小。但在现有消毒剂中,对不锈钢等金属腐蚀性低的消毒剂消毒效果差,因不能完全杀灭高致病性病原微生物而不能在高等级生物安全实验室使用,而对高致病性病原微生物具有杀灭作用的消毒剂对不锈钢等金属均有不同程度的腐蚀作用,长期使用会导致不锈钢等金属构件发生锈蚀,从而降低上述设施设备的生物安全防护作用,不仅缩短其使用寿命造成经济损失,甚至导致高致病性病原微生物逃逸到实验室外部环境中,进而造成人民生命财产损失并带来严重的社会问题。因此,研发一种既能够有效杀灭高致病性病原微生物、又对不锈钢等金属没有腐蚀性或者腐蚀性很低的消毒剂十分必要,针对以上问题,本发明提供了一种用于高等级生物安全实验室的物表消毒液及其制备方法。
技术实现要素:
[0004]
(一)解决的技术问题
[0005]
针对现有技术的不足,本发明提供了一种用于高等级生物安全实验室的物表消毒液及其制备方法。既解决了对高致病性病原微生物的高效杀灭效果,又解决了现有消毒剂对金属尤其是对不锈钢材料腐蚀性较强、降低高等级生物安全实验室设施设备的完整性而发生高致病性病原微生物泄漏引起生物安全事故的问题。
[0006]
(二)技术方案
[0007]
为实现以上目的,本发明通过以下技术方案予以实现:该消毒液由氯化季铵盐、多
酶溶液、水溶性硅油、乳化剂、防腐剂、纳米镁、螯合稳定剂和着色剂等组成。
[0008]
通过将纳米镁加入到消毒液中而降低消毒液对金属尤其是不锈钢材料的腐蚀作用,但是进一步研究发现,随着消毒液储存时间的延长纳米镁会发生聚集而粒径变大,使纳米镁不能均匀分布在溶液中从而降低防腐蚀作用。因此,研究者创造性应用磁化技术,对消毒液进行磁化,使溶液中的纳米镁带有磁性而产生相互排斥作用,进而降低其聚集而形成稳定的分散体系,消毒液的稳定性显著提升,使消毒液长期保持对金属的防腐蚀作用,同时在消毒液使用过程中,因为纳米镁带有磁性,首先附着在不锈钢等金属表面,能够更好地发挥防腐蚀作用。
[0009]
应用上述技术方案生产的消毒液,具有良好的杀灭病毒和细菌的功效,尤其能有效杀灭烈性传染病病毒,同时对金属的腐蚀性显著降低,用于高等级生物安全实验室时,可有效保护实验室设施设备的完整性,确保其生物安全防护性能而避免高致病性病原微生物泄漏到实验室外部环境中发生生物安全事故,同时,该消毒液对人和动物实际无毒,使用方便,去除无残留,环境友好,清理方便,在确保产品功效的前提下,技术实现需求的成本不高,在用于高等级生物安全实验室时,可杀灭不限于埃博拉病毒、sars冠状病毒、2019新型冠状病毒、艾滋病毒、基孔肯尼亚病毒等高致病性病原微生物。该消毒液在满足高等级生物安全实验室的特殊需求外,还可以用于医院、车站、宾馆等公共场所的消毒需求,在公共场所可杀灭常见致病菌,包括但不限于铜绿假单胞菌、白色念珠菌、金黄色葡萄球菌和大肠杆菌等。
[0010]
消毒液中的乳化剂是能使两种或两种以上互不相溶的组分的混合液体形成稳定的乳状液的一类化合物,其作用原理是在乳化过程中,分散相以微滴(微米级)的形式分散在连续相中,乳化剂降低了混合体系中各组分的界面张力,并在微滴表面形成较坚固的薄膜或由于乳化剂给出的电荷而在微滴表面形成双电层,阻止微滴彼此聚集,而保持均匀的乳状液,优选的乳化剂为壬基酚聚氧乙烯醚(np-10)、辛基酚聚氧乙烯醚、单式双甘油酯、卵磷脂、脂肪酸脂和聚磷酸盐其中的一种或多种组合。
[0011]
消毒液中的氯化季铵盐具有对高致病性病原微生物杀灭作用,所述氯化季铵盐为十二烷基二甲基氯化铵、十二烷基二甲基苄基氯化铵、c12-c14烷基苄基二甲基氯化铵、c12-c16烷基苄基二甲基氯化铵、c12-c14烷基[(苯乙基)甲基]二甲基氯化铵、二甲基乙基苄基氯化铵和c8-c10二烷基二甲基氯化铵其中的一种或多种组合。
[0012]
消毒液中创造性的加入纳米镁,能够显著降低消毒液对金属尤其是对不锈钢的腐蚀作用,优选的纳米镁在消毒液中的质量百分浓度为0.015%-0.05%,粒径为1-25nm。同时使用磁化器将溶液中的纳米镁磁化,形成稳定的磁性体系,避免纳米镁聚集以保持其防腐蚀性能。
[0013]
消毒液中的多酶溶液能有效去除附着在金属表面的生物膜,尤其是一些设施设备的关节或关节腔,单独依靠洗刷无法去除血液和组织液残留的生物膜,生物膜的存在往往会造成消毒液杀灭病原微生物效果不佳。多酶溶液可以有效的溶解生物膜,确保消毒液可以直接作用于器械,达到良好的消毒作用。优选的多酶溶液为液体淀粉酶、液体碱性蛋白酶、脂肪酶和纤维素酶组成的复合溶液。
[0014]
消毒液中加入水溶性的硅油能有效润滑金属器械,设备和设施的关节或关节腔,优选的水溶性硅油为道康宁dc-193。
[0015]
防腐剂是能抑制微生物活动,防止产品腐败变质的一类添加剂,要使产品有一定的保藏期,就必须采用一定的措施来防止微生物的感染和繁殖。实践证明,采用防腐剂是达到上述目的最经济、最有效和最简捷的办法之一,消毒液优选的防腐剂为尼泊金甲酯、尼泊金乙酯、氯化苯甲烃铵、氯化十六烷基吡啶、溴化十六烷铵、度米芬其中的一种或多种组合。
[0016]
螯合稳定剂为丙三醇、丁二醇、丙二醇、聚乙二醇、已二醇、三乙醇胺、吐温-80、硫酸钠、乙二胺四乙酸二钠、乙二胺四乙酸四钠其中的一种或多种组合。
[0017]
着色剂为赤藓红、胭脂红、甜菜红、苋菜红、亚甲蓝、靛蓝、柠檬黄其中的一种或多种组合。
[0018]
本发明还公开了高等级生物安全实验室物表消毒液的制备方法,具体包括但不限于以下步骤:
[0019]
1、物料的溶解与混合:取适量的纯化水将螯合稳定剂以及水溶性硅油混合均匀;
[0020]
2、稳定体系的形成:将多酶溶液加入其中溶解,加入乳化剂后低温下使用均质机均质乳化后,陈化8小时消泡,形成螯合稳定剂均匀包裹多酶物质组成的稳定体系,又被乳化剂形成的乳化微球包裹住;
[0021]
3、消毒液的最终制成:在搅拌下分别缓慢将着色剂和氯化季铵盐加入到溶液中,均匀搅拌混合后,再加入适量的纳米镁,搅拌均匀,使用磁化器将溶液中的纳米镁快速磁化,形成稳定的磁性体系,最后再静置消泡、灌装和包装即得最终的消毒液。
[0022]
(三)有益效果
[0023]
本发明提供了一种高等级生物安全实验室物表消毒液及其制备方法。具备以下有益效果:该消毒液对埃博拉病毒、sars冠状病毒、2019新型冠状病毒、艾滋病毒、基孔肯尼亚病毒等高致病性病原微生物具有显著杀灭效果;同时通过在消毒液中加入适量的纳米镁可明显降低消毒液对金属尤其是对不锈钢材料的腐蚀性,从而保护高等级生物安全实验室设施设备的完整性以避免高致病性病原微生物的泄漏进而发生生物安全事故,另外在消毒液制备过程中使用磁化器对消毒液中的纳米镁进行磁化,防止消毒液在储存中纳米镁聚集而丧失防金属腐蚀作用。
[0024]
该消毒液不仅能够用于高等级生物安全实验室对高致病性病原微生物杀灭,而且还可以用于医院、车站、宾馆等公共场所对铜绿假单胞菌、白色念珠菌、金黄色葡萄球菌和大肠杆菌等常见致病菌的杀灭。
[0025]
同时该消毒液对人体和动物无毒副作用,使用方便,去除无残留,环境友好,清理方便,在确保产品功效的前提下,技术实现需求的成本不高。
附图说明
[0026]
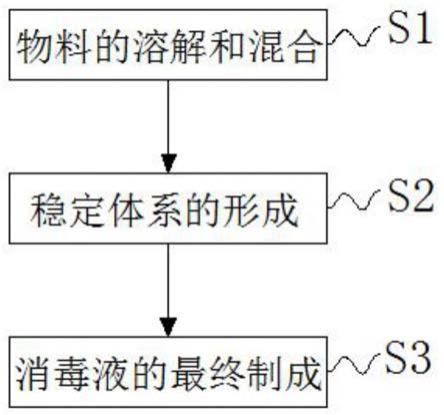
图1为本发明的流程图;
[0027]
图2为本发明对比实验的统计表图;
[0028]
图3为本发明不同浓度的消毒液对新型冠状病毒的杀灭效果示意图。
具体实施方式
[0029]
下面将结合本发明实施例中的附图,对本发明实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例仅仅是本发明一部分实施例,而不是全部的实施例。基于
本发明中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
[0030]
请参阅图1-3,本发明实施例提供四种技术方案:高等级生物安全实验室物表消毒液的制备方法,具体包括以下实施例:
[0031]
实施例1
[0032]
s1、物料的溶解与混合:取60g的纯化水溶解8g硫酸钠和2g碳酸钠后,加入5g丙二醇和5g水溶性硅油混合均匀;
[0033]
s2、稳定体系的形成:将0.2g液体淀粉酶、0.1g脂肪酶和0.05g液体碱性蛋白酶加入其中溶解,加入8gnp-10后低温下使用均质机均质乳化后,陈化8小时消泡,形成5g丙二醇均匀包裹多酶物质组成的稳定体系,又被8gnp-10形成的乳化微球包裹住;
[0034]
s3、消毒液的最终制成:在搅拌下分别缓慢将0.01g柠檬黄、0.5g吐温-80、2.5g二甲基苄基氯化铵、2.25g二甲基乙基苄基氯化铵、0.5gc12-c16烷基苄基二甲基氯化铵和0.1g度米芬加入到溶液中,均匀搅拌混合后,加入0.027g纳米镁,补足水量定重后,搅拌均匀。使用磁化器将溶液中的纳米镁快速磁化,形成稳定的磁性体系,最后再静置消泡、灌装和包装即得最终的消毒液。
[0035]
实施例2
[0036]
s1、物料的溶解与混合:取60g的纯化水溶解6g丁二醇和4g碳酸钠后,加入4g丙三醇和6g水溶性硅油混合均匀;
[0037]
s2、稳定体系的形成:将0.2g纤维素酶、0.1g脂肪酶和0.05g液体碱性蛋白酶加入其中溶解,加入8gnp-10后低温下使用均质机均质乳化后,陈化8小时消泡,形成4g丙三醇均匀包裹多酶物质组成的稳定体系,又被8gnp-10形成的乳化微球包裹住;
[0038]
s3、消毒液的最终制成:在搅拌下分别缓慢将0.01g柠檬黄、0.5g已二醇、2.5g二甲基苄基氯化铵、2.25gc8-c10二烷基二甲基氯化铵、0.5gc12-c16烷基苄基二甲基氯化铵和0.1g度米芬加入到溶液中,均匀搅拌混合后,加入0.015g纳米镁,补足水量定重后,搅拌均匀。使用磁化器将溶液中的纳米镁快速磁化,形成稳定的磁性体系,最后再静置消泡、灌装和包装即得最终的消毒液。
[0039]
实施例3
[0040]
s1、物料的溶解与混合:取60g的纯化水溶解8g聚乙二醇和2g碳酸钠后,加入5g丁二醇和5g水溶性硅油混合均匀;
[0041]
s2、稳定体系的形成:将0.2g液体淀粉酶、0.1g纤维素酶和0.05g液体碱性蛋白酶加入其中溶解,加入8gnp-10后低温下使用均质机均质乳化后,陈化8小时消泡,形成5g丁二醇均匀包裹多酶物质组成的稳定体系,又被8gnp-10形成的乳化微球包裹住;
[0042]
s3、消毒液的最终制成:在搅拌下分别缓慢将0.01g柠檬黄、0.5g乙二胺四乙酸四钠、2.5g二甲基苄基氯化铵、2.25g二甲基乙基苄基氯化铵、0.5gc12-c16烷基苄基二甲基氯化铵和0.1g度米芬加入到溶液中,均匀搅拌混合后,加入0.035g纳米镁,补足水量定重后,搅拌均匀。使用磁化器将溶液中的纳米镁快速磁化,形成稳定的磁性体系,最后再静置消泡、灌装和包装即得最终的消毒液。
[0043]
实施例4
[0044]
s1、物料的溶解与混合:取60g的纯化水溶解5g聚乙二醇和5g碳酸钠后,加入2g丁
二醇和8g水溶性硅油混合均匀;
[0045]
s2、稳定体系的形成:将0.1g液体淀粉酶、0.2g纤维素酶和0.05g液体碱性蛋白酶加入其中溶解,加入8gnp-10后低温下使用均质机均质乳化后,陈化8小时消泡,形成2g丁二醇均匀包裹多酶物质组成的稳定体系,又被8gnp-10形成的乳化微球包裹住;
[0046]
s3、消毒液的最终制成:在搅拌下分别缓慢将0.1g柠檬黄、0.41g乙二胺四乙酸四钠、2.4g二甲基苄基氯化铵、2.35g二甲基乙基苄基氯化铵、0.5gc12-c16烷基苄基二甲基氯化铵和0.1g度米芬加入到溶液中,均匀搅拌混合后,加入0.05g纳米镁,补足水量定重后,搅拌均匀。使用磁化器将溶液中的纳米镁快速磁化,形成稳定的磁性体系,最后再静置消泡、灌装和包装即得最终的消毒液。
[0047]
对比实验
[0048]
某消毒液检测中心对由实施例1、实施例2、实施例3以及实施例4分别制成的消毒液进行检测,检测内容为:消毒液中不同含量的纳米镁对金属的腐蚀效果以及对病毒、细菌的杀灭作用,同时在检测的过程中统计数据并制作统计表图。
[0049]
对比试验结果
[0050]
通过查看附图2可知,某消毒液检测中心采用本发明实施例1-4分别制得四组消毒液,并根据最终实验数据得出通过实施例1制备而成的消毒液效果最佳,其各组分含量如表1所示。通过在该消毒液中加入纳米镁,从而降低消毒液对金属尤其是对不锈钢材料的腐蚀作用,另外对消毒液中的镁离子进行磁化,使其带有磁性,有助于纳米镁附着在不锈钢等金属表面,起到良好的防腐蚀作用。加入纳米镁配制的消毒液,不仅杀菌效果好且防金属腐蚀性能强,具有良好的杀灭病毒和细菌的功效,尤其能有效杀灭烈性传染病病毒,对人体无毒无副作用,使用方便,去除无残留,环境友好,清理方便,在确保产品功效的前提下,技术实现需求的成本不高,不仅可以满足实验所需,更可以满足广大民众的需求,并且利用了新的防金属腐蚀技术来确保生物实验室的安全。
[0051]
表1实施例1中各组分含量数据表
[0052][0053]
一、物表消毒液对高致病性病原微生物杀灭测试结果:
[0054]
1、对新型冠状病毒的杀灭效果:由附图3可见(注:cpe:细胞病变效应;“+”有cpe;
“-”
无cpe;1/2/3表示3次重复),将实施例1所制成的消毒液进行稀释,当浓度大于1.6%时,15秒即可完全杀灭2
╳
104tcid
50
病毒;消毒液的浓度为0.56%时,30秒可以完全杀灭2
╳
104tcid
50
病毒;消毒液的浓度为0.19%时,2分钟可以完全杀灭2
╳
104tcid
50
病毒。
[0055]
2、对埃博拉病毒的杀灭效果:将实施例1所制成的消毒液稀释为1%时,与埃博拉病毒作用1min即可杀灭99.999%的病毒。
[0056]
3、在19-21℃条件下,将实施例1所制成的消毒液稀释为5%时,作用5min对大肠杆菌、金黄色葡萄球菌、铜绿假单胞菌的杀灭对数值均大于5,对白色念珠菌的杀灭对数值大于4。
[0057]
4、在19-21℃条件下,将实施例1所制成的消毒液稀释为5%时作用5min对木质物表面上的自然菌的杀灭对数值大于1,对污染于棉布片上的大肠杆菌各次试验的杀灭对数值均大于3。
[0058]
二、抗腐蚀实验数据:
[0059]
对实施例1原液的实验数据如下:
[0060]
1、产品酸碱度测试为:ph=11.6。
[0061]
2、金属腐蚀性试验表明,消毒液对不锈钢腐蚀速率为0.00011mm/a,基本无腐蚀,对碳钢腐蚀速率为0.00244mm/a,基本无腐蚀。
[0062]
3、粒径分布。
[0063]
通过查看表2消毒剂稳定性粒径分布可知,对纳米镁进行磁强化是确保消毒液中纳米镁稳定的重要手段,未磁化的纳米镁在消毒液中存放3个月后就开始发生镁聚集的情况,纳米镁的粒径开始逐渐变大,而磁强化后的纳米镁在消毒液中即使存放12个月粒径未发生较大变化,发生聚集的情况非常小,因此消毒液中加入纳米镁后为确保其状态稳定,磁强化技术是非常重要的技术手段。
[0064]
表2消毒剂稳定性粒径分布
[0065]
[0066][0067]
三、毒性试验数据:
[0068]
经过对实施例1所制成的消毒液进行检测,结果如下:
[0069]
1、消毒液原液对新西兰兔的一次完整皮肤刺激强度试验属无刺激性。
[0070]
2、消毒液原液对雌雄小鼠急性经口毒性试验属实际无毒。
[0071]
3、消毒液原液对小鼠骨髓细胞染色体未呈现致微核作用。
[0072]
需要说明的是,在本文中,诸如第一和第二等之类的关系术语仅仅用来将一个实体或者操作与另一个实体或操作区分开来,而不一定要求或者暗示这些实体或操作之间存在任何这种实际的关系或者顺序。而且,术语“包括”、“包含”或者其任何其他变体意在涵盖非排他性的包含,从而使得包括一系列要素的过程、方法、物品或者设备不仅包括那些要素,而且还包括没有明确列出的其他要素,或者是还包括为这种过程、方法、物品或者设备所固有的要素。
[0073]
尽管已经示出和描述了本发明的实施例,对于本领域的普通技术人员而言,可以理解在不脱离本发明的原理和精神的情况下可以对这些实施例进行多种变化、修改、替换
和变型,本发明的范围由所附权利要求及其等同物限定。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1