用于预防和治疗动物病症的益生菌和发酵代谢物的制作方法
相关申请的交叉引用本申请基于并要求于2017年12月14日提交的序列号为62/598,730的美国临时申请的优先权,其全部内容通过引用并入本申请中。本申请涉及益生菌微生物和由其制备的发酵代谢物。值得特别注意的是,本申请涉及可用于治疗或预防动物疾病或病症的益生菌和发酵代谢物。
背景技术:
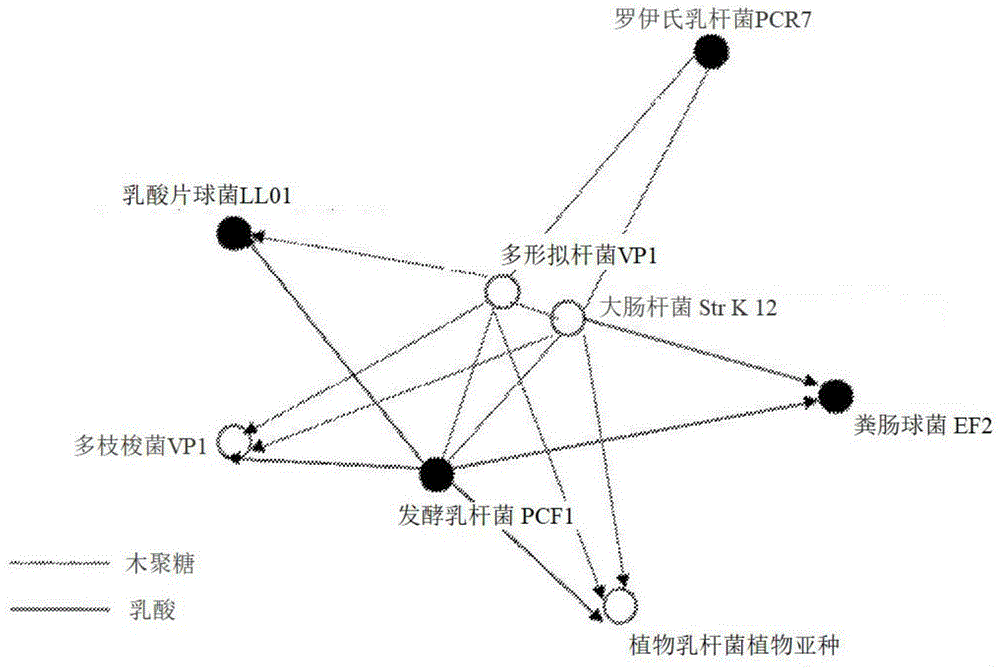
:自从1940年代初发现抗生素以来,抗生素就作为性能增强添加剂在动物食品生产行业中发挥了不可或缺的作用(mckenna,2017)。在大多数农场中,抗生素被用于治疗临床感染,控制和预防疾病的传播,并主要用于促进动物的生长(americanmeatinstitute,2013)。临床研究表明,当抗生素被用作生长促进剂时,可通过稳定肠道微生物菌群,改善总体性能,并预防肠道疾病来促进羊群健康(hassan,2010年)。例如,研究已表明,长期使用亚治疗剂量的四环素和泰乐菌素可提高家禽、猪和牛的饲料转化率(landers,2012)。这些益处推动了整个行业朝着以抗生素为中心的生产实践。当前,在美国,在牲畜生命周期中的不同时期可能用到的十二类抗生素大多是人用抗生素的类似物(landers,2012)。2012年,动物用抗生素售出超过3000万磅,是人用抗生素售出量的四倍多,体现了抗生素在食品行业中的重要作用(taillant,2015)。然而,随着在食品生产中抗生素使用的增长,由抗生素引发的大量问题也随之出现。值得注意的是,抗生素的广泛使用可能导致致病菌产生耐药性。技术实现要素:本申请的一个方面涉及一种混合物,其包括至少两种微生物、以及最好是由所述至少两种微生物共同生长时产生的代谢物。在某些实施方案中,混合物包括选自以下的至少两种微生物:罗伊氏乳杆菌、乳酸片球菌、粪肠球菌、戊糖片球菌、嗜酸乳杆菌、发酵乳杆菌和植物乳杆菌,以及最好是由所述至少两种微生物共同生长时产生的代谢物。本申请的另一方面涉及一种治疗或预防所需动物疾病或病症的方法。该方法包括向动物饲喂包括至少两种微生物以及最好由所述至少两种微生物共同生长时产生的代谢物组成的混合物。在某些实施方案中,该混合物包括选自罗伊氏乳杆菌、乳酸片球菌、粪肠球菌、戊糖片球菌、嗜酸乳杆菌、发酵乳杆菌和植物乳杆菌中的至少两种微生物,以及最好由所述至少两种微生物共同生长时产生的代谢物。本申请的其他方面和特征将在下文中在某种程度上变得显而易见,且在某种程度上被指出。附图说明图1是交叉喂养模型示例图。图2是进化树示例图。图3是示例性混合物生产相关部分实验结果汇总表。图4是示例性实验结果汇总图,主要是激酶组图谱的热图和聚类。来自多肽阵列的原始激酶组信号被输入到定制软件包piika2中。piika2整合了每组实验和组织的生物学重复,对数据进行归一化,并生成具有代表性的激酶组图谱。激酶组图谱可比较相对相似性,热图显示阵列上每种多肽的相对磷酸化程度。图5是示例性实验结果汇总图,主要是主要是相对于对照组激酶组图谱的实验组激酶组谱的biosub热图和聚类。来自多肽阵列的原始激酶组信号被输入到定制软件包piika2中。piika2整合了每组实验和组织的生物学重复,对数据进行归一化,并生成具有代表性的激酶组图谱。将每个实验组的图谱与对照组的激酶组图谱进行比较,然后所得的激酶组图谱可比较相对相似性,热图显示给定实验组相对于对照组在阵列上每种肽的相对磷酸化程度。图6是按月的活菌计数图。图7示出90℃稳定性测试的数据。图8示出为期六个月的稳定性测试结果。图9示出混合物及其组成菌株的有机酸图谱比较。图10示出分批发酵的有机酸指纹图谱。图11示出两种混合物及其组成菌株的分批发酵的有机酸指纹图谱比较。优选的具体实施方式本文提供了用于治疗和预防动物疾病或病症的方法和混合物。该混合物包括益生菌,主要是至少两种微生物的混合物。在某些实施方案中,这些微生物选自罗伊氏乳杆菌(lactobacillusreuteri)、乳酸片球菌(pediococcusacidilactici)和粪肠球菌(enterococcusfaecium)。在某些实施方案中,该混合物还包括戊糖片球菌(pediococcuspentosaceus)、嗜酸乳杆菌(lactobacillusacidophilus)、发酵乳杆菌(lactobacillusfermentum)和植物乳杆菌(lactobacillusplantarum)中的一种或多种微生物。在某些实施方案中,本发明中的混合物不仅包括微生物,还包括当微生物共同生长时的发酵产物,例如,生物后代谢物(post-bioticmetabolite),主要是短链脂肪酸。本发明的其他方面涉及使用本发明的混合物来治疗或预防动物疾病或病症。已经发现,本发明的微生物多菌株复合同时发酵与单菌株独立多次发酵时产生的代谢物不同和/或产生的代谢物比例不同与。进一步发现,本发明的微生物的不同组合,以及它们独特的发酵代谢混合物,特别是短链脂肪酸,对动物健康具有益处。其对动物健康有益的原因之一是由于饲喂给生产动物的饲料不能被本发明中的微生物最有效地转化为短链脂肪酸供动物使用。通过将混合物中的可靠且定量的短链脂肪酸代谢物直接递送给动物,短链脂肪酸可以间接地被用于生成丙酮酸和乙酰辅酶a(acetyl-coa)。这些是克雷布斯能量循环(krebsenergycycle)的重要中间体。此外,本发明中的混合物包括不同的短链脂肪酸比例,且可以以对动物健康有益的浓度递送。相反,短链脂肪酸的直接口服给药会限制吸收,原因是所给剂量可能会超过动物胃肠道系统惯于接收的量。更加有益的是,将本发明中的混合物施用于动物可以减少或甚至消除对抗生素的需求。进一步发现,本申请中的混合物和发酵代谢物(例如短链脂肪酸)具热稳定性,可以耐受生产动物饲料在运输、储存和造粒期间常见的高温环境。因此,产生热稳定的有益脂肪酸是本发明在农业和其他工业中的一个益处。一、混合物一方面,本申请中的混合物包括选自罗伊氏乳杆菌、乳酸片球菌、粪肠球菌、戊糖片球菌、嗜酸乳杆菌、发酵乳杆菌和植物乳杆菌中的至少两种微生物,以及最好是由所述至少两种微生物共同生长时所产生的代谢物。在某些方面,所述至少两种微生物选自罗伊氏乳杆菌、乳酸片球菌和粪肠球菌,且最好与由所述至少两种微生物共同生长时所产生的益生菌发酵物(特别是短链脂肪酸)一起使用。在某些实施方案中,此混合物还额外包括选自戊糖片球菌、嗜酸乳杆菌、发酵乳杆菌和植物乳杆菌中的一种或多种微生物。在某些实施方案中,本发明中的混合物包括选自罗伊氏乳杆菌、乳酸片球菌和粪肠球菌中的至少一种微生物和选自戊糖片球菌、嗜酸性乳杆菌、发酵乳杆菌和植物乳杆菌中的至少一种微生物,且最好与由所选微生物共同生长时所产生的益生菌发酵物(特别是短链脂肪酸)一起使用。在某些实施方案中,该混合物包括罗伊氏乳杆菌、乳酸片球菌和粪肠球菌;罗伊氏乳杆菌、乳酸片球菌、粪肠球菌和戊糖片球菌;罗伊氏乳杆菌、乳酸片球菌、粪肠球菌、戊糖片球菌和发酵乳杆菌;罗伊氏乳杆菌、乳酸片球菌和嗜酸乳杆菌;或包括罗伊氏乳杆菌、乳酸片球菌、粪肠球菌和嗜酸乳杆菌;在每种情况下,最好与由所选微生物共同生长时所产生的益生菌发酵物(特别是短链脂肪酸)一起使用。在某些实施方案中,该混合物包括选自罗伊氏乳杆菌、乳酸片球菌、粪肠球菌、戊糖片球菌、嗜酸乳杆菌、发酵乳杆菌和植物乳杆菌中的至少两种微生物,且最好与由所选微生物共同生长时所产生的代谢物(特别是短链脂肪酸)一起使用。本发明的示例性混合物包括,但不限于以下列举的例子:罗伊氏乳杆菌和乳酸片球菌;罗伊氏乳杆菌和粪肠球菌;罗伊氏乳杆菌和戊糖片球菌;乳酸片球菌和粪肠球菌;乳酸片球菌和戊糖片球菌;粪肠球菌和戊糖片球菌;罗伊氏乳杆菌、乳酸片球菌和粪肠球菌;罗伊氏乳杆菌、乳酸片球菌和戊糖片球菌;乳酸片球菌、粪肠球菌和戊糖片球菌;罗伊氏乳杆菌和嗜酸乳杆菌;乳酸片球菌和嗜酸乳杆菌;粪便球菌和嗜酸乳杆菌;罗伊氏乳杆菌、乳酸片球菌和嗜酸乳杆菌;乳酸片球菌、粪肠球菌和嗜酸乳杆菌;罗伊氏乳杆菌和嗜酸乳杆菌;罗伊氏乳杆菌和罗伊氏乳杆菌;罗伊氏乳杆菌和植物乳杆菌;粪肠球菌和嗜酸乳杆菌;粪肠球菌和发酵乳杆菌;粪肠球菌和植物乳杆菌;戊糖片球菌和嗜酸乳杆菌;戊糖片球菌和发酵乳杆菌;戊糖片球菌和植物乳杆菌;乳酸片球菌和嗜酸乳杆菌;乳酸片球菌和发酵乳杆菌;乳酸片球菌和植物乳杆菌;嗜酸乳杆菌和发酵乳杆菌;嗜酸乳杆菌和植物乳杆菌;或发酵乳杆菌和植物乳杆菌;在每种情形下,该混合物可单独使用,或可进一步添加以下一种或多种微生物,包括罗伊氏乳杆菌、乳酸片球菌、粪肠球菌、戊糖片球菌、嗜酸乳杆菌、发酵乳杆菌和植物乳杆菌;在每种情形下,最好与由所选微生物共同生长时所产生的益生菌发酵物(特别是短链脂肪酸)一起使用。在以上列举的每个实施方案中,可以使用以下一种或多种菌株:罗伊氏乳杆菌pcr7、乳酸片球菌pcll01、粪肠球菌pcef02、戊糖片球菌pcpp01、发酵乳杆菌pcf01和市售的嗜酸乳杆菌pcla18。本发明的某些实施方案包括罗伊氏乳杆菌pcr7、乳酸片球菌pcll01、粪肠球菌pcef02和戊糖片球菌pcpp01;或包括罗伊氏乳杆菌pcr7、乳酸片球菌pcll01、粪肠球菌pcef02、戊糖片球菌pcpp01和发酵乳杆菌pcf01的组合;且最好与由所选微生物共同生长时所产生的益生菌发酵物一起使用。粪肠球菌(例如pcef02)优选低毒性菌株,对于预期用途是可以接受的。已经发现,本发明中的微生物的混合物在单独发酵时生成不同的发酵产物。另外,由于发酵过程中微生物之间的竞争,某些微生物在发酵后数量可能减少。如实施例14中详述,一个包含罗伊氏乳杆菌、乳酸片球菌、粪肠球菌和戊糖片球菌的混合物所产生的发酵代谢物与单菌株发酵时产生的代谢物不同。下表列出了产生不同发酵产物的其他微生物组合。表1.发酵产物在一个实施方案中,该混合物可以进一步包括选自片球菌属,乳杆菌属,乳球菌属,双歧杆菌属,明串珠菌属,链球菌属和芽孢杆菌属中的一个或多个种的微生物。在另一个实施方案中,该混合物可进一步包含一种或多种下述微生物:戊糖片球菌,嗜酸乳杆菌,植物乳杆菌,鼠李糖乳杆菌,发酵乳杆菌,双歧乳杆菌,短乳杆菌,保加利亚乳杆菌,干酪乳杆菌,德氏乳杆菌,鼠李糖乳杆菌,瑞士乳杆菌,约氏乳杆菌,乳酸乳杆菌(lactobacilluslactis),乳酸乳杆菌乳脂亚种,乳酸乳杆菌乳酸亚种,副干酪乳杆菌,乳脂乳球菌,乳酸乳球菌,乳酸乳球菌乳脂亚种,婴儿双岐杆菌,乳酸双歧杆菌,动物双歧杆菌,双叉双歧杆菌,长双歧杆菌,短双歧杆菌,肠膜明串珠菌肠膜亚种,肠膜明串珠菌乳脂亚种,牛链球菌,唾液链球菌,唾液链球菌嗜热亚种,凝结芽孢杆菌,解淀粉芽孢杆菌,地衣芽孢杆菌,枯草芽孢杆菌,以及迟缓芽孢杆菌。在以上列举的每个实施方案中,可以使用一种或多种以下菌株:罗伊氏乳杆菌pcr7、乳酸片球菌pcll01、粪肠球菌pcef02、戊糖片球菌pcpp01、发酵乳杆菌pcf01和市售的嗜酸乳杆菌pcla18。本申请中的混合物中所包括的微生物可以从微生物菌种保藏种子中心(例如,美国典型微生物菌种保藏中心)获得,或从微生物或益生菌菌株的商业供应商处购得。据此,然后在合适的条件下在发酵培养基中培养微生物,供其生长。如下表所示,某些专有微生物已被保存到农业研究服务菌株菌种保藏中心(agriculturalresearchserviceculturecollectionnrrl)——伊利诺伊州北方研究服务菌种保藏研究皮奥里亚实验室(northernresearchserviceculturecollectionresearchlaboratoryperoria)。表2.nrrl编号#nrrl#菌株编号属/种1b-67717pcll01乳酸片球菌2b-67718pcr7罗伊氏乳杆菌3b-67719pcpp01戊糖片球菌4b-67720pcef02粪肠球菌5b-67701pcla18嗜酸乳杆菌a.发酵过程市场上的许多益生菌产品仅提供了一种或多种微生物。然而,在本发明中的某些实施方案中,该混合物的制备是通过首先在合适的培养基中发酵微生物的组合以产生包含在混合物中的代谢物或“后生物”(postbiotics)。在一个实施方案中,例如,一种混合物包括选自罗伊氏乳杆菌、乳酸片球菌和粪肠球菌中的至少两种微生物,并可包括选自戊糖片球菌、嗜酸乳杆菌、发酵乳杆菌和植物乳杆菌中的一种或多种微生物,该混合物也可以是前面更详细描述过的任何一种混合物,均可以被添加到发酵培养基中并进行培养。此外,所述至少两种微生物可以产生包含在混合物中的代谢物。合适的发酵培养基可以包括含有以下组分的培养基,例如糖蜜,诸如基于甜菜汁、甘蔗汁、蔗糖、右旋糖、葡萄糖、玉米浆固体,或玉米浆的糖蜜。在一个实施方案中,发酵培养基中的糖蜜量可以为约1%v/v至约10%v/v。在一些实施方案中,发酵培养基中的糖蜜量可以为约1%v/v、约2%v/v、约3%v/v、约4%v/v、约5%v/v、约6%v/v、约7%v/v、约8%v/v、约9%v/v,或约10%v/v。在一些实施方案中,发酵培养基可以包含更高含量的糖蜜。在一些实施方案中,发酵培养基中糖蜜:水比例可以达到约20:80v/v至约35:65v/v。在其他实施方案中,发酵培养基中糖蜜:水比例可以为约20:80v/v、约25:75v/v、约30:70v/v或约35:65v/v。发酵培养基还可以包含其他配方组分,例如一种或多种外源益生元,例如低聚果糖(fos)、低聚半乳糖、低聚木糖、低聚异麦芽糖、菊粉低聚糖、低聚葡萄糖、大豆低聚糖、低聚乳果糖、异麦芽酮糖、赤藓糖醇、或甘露寡糖,以制备例如5%的液态或固态配方。发酵培养基还可以包含甘油,例如甘油在发酵培养基中比例约为0.5%至3%。在某些实施方案中,所公开的发明包括一种混合物,该混合物包含选自罗伊氏乳杆菌、乳酸片球菌和粪肠球菌中的至少两种微生物,并可包含选自戊糖片球菌、嗜酸乳杆菌、发酵乳杆菌和植物乳杆菌中的一种或多种微生物,该混合物也可以是前面更详细描述过的任何一种混合物。该混合物被添加到含有糖蜜并可能含有甘油的发酵培养基中生长以产生代谢物。糖蜜和甘油在培养基中的浓度可以是上述的任何浓度。在某些实施方案中,一个混合物包括罗伊氏乳杆菌和乳酸片球菌;罗伊氏乳杆菌、乳酸片球菌和嗜酸乳杆菌;罗伊氏乳杆菌、乳酸片球菌和粪肠球菌;罗伊氏乳杆菌、乳酸片球菌、粪肠球菌和戊糖片球菌;罗伊氏乳杆菌、乳酸片球菌、粪肠球菌、戊糖片球菌和发酵乳杆菌;或包括罗伊氏乳杆菌、乳酸片球菌、粪肠球菌和嗜酸乳杆菌。该混合物被添加到含有上述任何浓度的糖蜜并可能同时含有甘油、菊粉和/或低聚果糖的发酵培养基中生长以产生代谢物。在某些实施方案中,含有低浓度糖蜜并可能同时含有甘油的弱培养基被用于生产含有足以治疗或预防疾病或病症的微生物和代谢物的混合物。在某些实施方案中,可使用以下菌株中的一株或多株:罗伊氏乳杆菌pcr7、乳酸片球菌pcll01、粪肠球菌pcef02、戊糖片球菌pcpp01、发酵乳杆菌pcf01和市售菌株嗜酸乳杆菌pcla18。发酵培养基还可以包含一个氮源、蛋白质源、微量元素、维生素、缓冲剂,或其他组分。在一个实施方案中,发酵培养基可以包含一种氮源。合适的氮源包括但不限于酵母提取物、丙氨酸、精氨酸、天冬酰胺、天冬氨酸、谷氨酰胺、异亮氨酸、柠檬酸铵、丝氨酸、缬氨酸和硫酸铵、铵盐、乳清提取物、脱脂奶粉、玉米浆或固体、大豆粉、蚕豆蛋白胨、玉米蛋白胨、豌豆蛋白胨、小麦蛋白胨、马铃薯蛋白胨、酪蛋白水解物、羽扇豆蛋白胨、麦芽提取物、肉蛋白胨和大米蛋白胨。在某些实施方案中,氮源可以占发酵培养基配方的1%至15%。在一个实施方案中,发酵过程可以包括使用一些试剂,例如氢氧化铵、氢氧化钠、碳酸钠和碳酸钙,作为ph控制剂。在一个实施方案中,发酵培养基可以包含一种蛋白质源。合适的蛋白质源包括但不限于大豆提取物、酵母提取物、豌豆提取物、蚕豆提取物、玉米提取物、马铃薯提取物、乳制品提取物、脱脂奶粉、木薯提取物、麦芽提取物、肉提取物、麦芽提取物和大米提取物。在某些实施方案中,蛋白质源可以占发酵培养基配方的1%至15%。在一个实施方案中,发酵培养基可以包含一种微量元素。合适的微量元素包括但不限于铁、锌、铜、锰、镁、钼和钴。下表列出了微量元素的典型范围。表3.微量元素成份范围(g/l)kh2po41.0–4.0mgso4.7h2o0.25–3.0kcl0.5–12.0caco31.5–17.0feso40.01–0.1znso40.1–1.0mnso40.01–0.1cuso0.003–0.01namoo4.2h2o0.01–0.1该表转载自《发酵技术原理》(principlesoffermentationtechnologyp.f.stanbury,a.whitakerands.j.hallsecondeditionp.103)。在一个实施方案中,发酵培养基可以包含一种缓冲剂。合适的缓冲剂包括但不限于二磷酸钾、磷酸钾、碳酸钠、碳酸氢钠、碳酸钾和碳酸氢钾。下表列出了缓冲剂的典型范围。表4.缓冲剂成分范围(g/l)磷酸氢二钾1-5柠檬酸0.5-2.5柠檬酸一钠0.5-10柠檬酸二钠0.5-10柠檬酸三钠0.5-10碳酸钠0.5-5碳酸钙0.5-5氢氧化钠用于将ph滴定至碱性更强的范围氢氧化铵用于将ph滴定至碱性更强的范围在一些实施方案中,发酵培养基包含蛋白胨、牛肉提取物、酵母提取物、葡萄糖、乙酸钠、聚山梨酯80、磷酸氢二钾、乙酸铵、硫酸镁和硫酸锰。在一些实施方案中,发酵培养基包含约0.5%至约2.5%的酪蛋白、约0.5%至约3.5%的牛肉提取物、约0.1%至约3.5%的酵母提取物、约1.0%至约5.0%的葡萄糖、约0.1%至约5.0%的乙酸钠、约0.05%至约0.5%的聚山梨酸酯80、约0.05%至约0.5%的磷酸氢二钾、约0.05%至约0.5%的乙酸铵、约0.005%至0.5%约0.1%的硫酸镁、以及约0.0005至约0.01%的硫酸锰。在一些实施方案中,可以改良发酵培养基,包括例如用豌豆蛋白胨、大豆蛋白胨、马铃薯蛋白胨、玉米蛋白胨、蚕豆蛋白胨或肉蛋白胨替换酪蛋白胨。在一些实施方案中,在微生物开始生长之前的发酵培养基中可以包含氨基酸赖氨酸。如不受理论的限制,赖氨酸可以提高短链脂肪酸丁酸盐的生成。在某些实施方案中,本发明包括一种混合物,其包括选自罗伊氏乳杆菌、乳酸片球菌和粪肠球菌中的至少两种微生物,同时可以包含选自戊糖片球菌、嗜酸乳杆菌、发酵乳杆菌和植物乳杆菌中的一种或多种微生物,该混合物也可以是前面更详细描述过的任何一种混合物。该混合物被添加到含有以上被提到的任何浓度的糖蜜同时可能含有甘油的发酵培养基中。合适的发酵条件包括一个从约25℃至约42℃的温度范围。在一些实施方案中,发酵温度可以为约25℃、约26℃、约27℃、约28℃、约29℃、约30℃、约3℃、约32℃、约33℃、约34℃、约35℃、约36℃、约37℃、约38℃、约39℃、约40℃、约4℃,或约42℃。典型的发酵时长为18至50个小时。目标发酵时长取决于ph值、od读数、和溶液的总酸度和碱度。将微生物生长的容器保持在厌氧或有氧条件下。b.配方在一些实施方案中,在微生物生长结束后,可以将培养基和细菌配制成含有益生菌微生物和由微生物产生的发酵代谢物的制剂。其中发酵代谢物可以包括短链脂肪酸、糖、寡糖,或细菌素中的一种或多种。在某些实施方案中,该制剂包含二级和/或三级代谢物。另外,由于发酵过程中微生物之间的竞争,某些微生物在发酵产物中的数量可能会减少。该制剂可以是液体或固体形式。在一个实施方案中,代谢物可以包含一种短链脂肪酸。合适的短链脂肪酸包括但不限于乙酸、甲酸、丙酸、丁酸、异丁酸、戊酸、琥珀酸和异戊酸。微生物在繁殖期间在发酵培养基中产生大量的短链脂肪酸,例如在约0.5mg/ml至约30.0mg/ml的范围内。在一些实施方案中,在发酵培养基中生成的短链脂肪酸的量可以为约0.5mg/ml、约1.0mg/ml、约1.5mg/ml、约2.0mg/ml、约2.5mg/ml、约3.0mg/ml、约3.5mg/ml、约4.0mg/ml、约4.5mg/ml、约5.0mg/ml、约5.5mg/ml、约6.0mg/ml、约6.5mg/ml、约7.0mg/mlml、约7.5mg/ml、约8.0mg/ml、约8.5mg/ml、约9.0mg/ml、约9.5mg/ml、约10.0mg/ml、约10.5mg/ml、约11.0mg/ml、约11.5mg/ml、约12.0mg/ml、约12.5mg/ml、约13.0mg/ml、约13.5mg/ml、约14.0mg/ml、约14.5mg/ml、约15.0mg/ml、约15.5mg/ml、约16.0mg/ml、约16.5mg/ml、约17.0mg/ml、约17.5mg/ml、约18.0mg/ml、约18.5mg/ml、约19.0mg/ml、约19.5mg/ml、约20.0mg/ml、约20.5mg/ml、约21.0mg/ml、约21.5mg/ml、约22.0mg/ml、约22.5mg/ml、约23.0mg/ml、约23.5mg/ml、约24.0mg/ml、约24.5mg/ml、约25.0mg/mlml、约25.5mg/ml、约26.0mg/ml、约26.5mg/ml、约27.0mg/ml、约27.5mg/ml、约28.0mg/ml、约28.5mg/ml、约29.0mg/ml、约29.5mg/ml,或约30.0mg/ml。在另一个实施方案中,代谢物可以包含一种糖。合适的糖包括但不限于四碳糖、五碳糖和六碳糖。合适的四碳糖包括但不限于赤藓糖和苏糖。合适的五碳糖包括但不限于核糖、阿拉伯糖、木糖和来苏糖。合适的六碳糖包括但不限于葡萄糖、半乳糖、甘露糖、阿洛糖、麦芽糖、古洛糖、艾杜糖和塔洛糖。这些代谢物通常是中间代谢物,在发酵过程中被微生物消耗,进而生成本发明中混合物中所包含的最终代谢物。在另一个实施方案中,代谢物可以包含一种寡糖。合适的寡糖包括但不限于低聚果糖、低聚半乳糖、低聚木糖、赤藓糖醇、异麦芽酮糖、异麦芽低聚糖和甘露寡糖。某些寡糖“益生元”在发酵过程中被细菌消耗。细菌在发酵过程中会生成一些新的“益生元”。在另一个实施方案中,代谢物可以包含一种细菌素。合适的细菌素包括但不限于嗜酸杆菌素、嗜酸乳菌素或罗伊氏菌素。可以生成的其他发酵代谢物,包括多肽、功能蛋白、酶、氨基酸、硫化氢、过氧化氢、酒精、二氧化碳、二氧化硫、多酚、甘露醇和维生素。在一些实施方案中,在微生物生长结束时,所获得的混合物(例如包含益生菌微生物和发酵代谢物的生长培养基)可以被直接用于预防或治疗动物的疾病或病症。在一些实施方案中,在微生物生长结束时,培养基和细菌可以被用于制备含有混合物的液体或固体制剂。因此,例如,该混合物可以被直接添加到动物的供水中。在一个实施方案中,本文中公开的混合物,其组分包含选自罗伊氏乳杆菌、乳酸片球菌和粪肠球菌中的至少两种微生物,同时可以包含选自戊糖片球菌、嗜酸乳杆菌、发酵乳杆菌和植物乳杆菌中的一种或多种微生物,且该混合物也包括上文中更详细描述过的任何混合物,其组分还包含由所包含的至少两种微生物共同生长时所产生的代谢物。该混合物可以被配制成液体或固体形式。本发明中的某些实施方案包含本文中公开的混合物,其包括选自罗伊氏乳杆菌、乳酸片球菌和粪肠球菌中的至少两种微生物,同时可以包含选自戊糖片球菌、嗜酸乳杆菌、发酵乳杆菌和植物乳杆菌中的一种或多种微生物,且该混合物也包含上文中更详细描述过的任何混合物,其组分还包含由上述的至少两种微生物在含有糖蜜和可能含有上述的甘油、菊粉和/或低聚果糖的培养基中共同生长时产生的代谢物。在某些实施方案中,一种混合物含有罗伊氏乳杆菌和乳酸片球菌;罗伊氏乳杆菌、乳酸片球菌和粪肠球菌;罗伊氏乳杆菌、乳酸片球菌、粪肠球菌和戊糖片球菌;或罗伊氏乳杆菌、乳酸片球菌、粪肠球菌和嗜酸乳杆菌;且含有由所选微生物在含有上述任何浓度的糖蜜和可能含有甘油、菊粉和/或低聚果糖的培养基中共同生长时所产生的代谢物。已经发现,本发明中的微生物组合以及它们的独特的发酵代谢物混合物(特别是短链脂肪酸代谢物),对动物健康有益处。详细信息见实施例12-14。液体或固体制剂形式可通过本领域中已知的技术实现。制备固体制剂的此类技术包括喷雾干燥、蒸发、离心、切向流过滤,和微滤。可以使用的干燥设备包括但不限于喷雾干燥器、对流烘箱、微波干燥器、布弗洛瓦克(buflovak)干燥器、冷冻干燥器,或旋转鼓式干燥器。制备粉末制剂时可包含一种填充剂,例如麦芽糊精、玉米淀粉、木薯淀粉、木薯葡萄糖、微晶纤维素、米粉、大米淀粉、一种益生元,例如菊粉和低聚果糖。在一些实施方案中,可以将液体混合物浓缩以制备更浓缩的液体混合物。可以使用本领域中通常已知的技术来浓缩液体混合物。在一些实施方案中,可以通过离心、超滤和蒸发来制备更浓缩的液体混合物。在一些实施方案中,固体混合物可以被粉末化或造粒。可以使用本领域通常已知的技术将固体混合物粉末化或造粒。在一些实施方案中,可以制备制剂以获得特定的微生物计数。在一些实施方案中,所述制剂可包含至少约1.0×105cfu/g或cfu/ml的乳酸菌数。在其他实施方案中,所述制剂可包含至少1.0×107cfu/g或cfu/ml的乳酸菌数。乳酸菌的典型计数范围为1.0×105至1.0×1010cfu/g或cfu/ml。二、方法一方面,本申请的方法包含治疗或预防有需要的动物中的疾病或病症,该方法包含向该动物饲喂一种混合物,该混合物包含选自罗伊氏乳杆菌混合物、乳酸片球菌和粪肠球菌中的至少两种微生物,同时可以含有选自戊糖片球菌、嗜酸乳杆菌、发酵乳杆菌和植物乳杆菌中的一种或多种微生物,且该混合物包括上文中更详细描述过的任何微生物混合物,其组分还包含由上述所选至少两种微生物在上述任何一种培养基配方中共同生长时所产生的代谢物。在某些实施方案中,本申请的方法包含治疗或预防有需要的动物中的疾病或病症的方法,该方法包括向所述动物饲喂一种混合物,该混合物包含:罗伊氏乳杆菌和乳酸片球菌;罗伊氏乳杆菌、乳酸片球菌和粪肠球菌;罗伊氏乳杆菌、乳酸片球菌、粪肠球菌和戊糖片球菌;或罗伊氏乳杆菌、乳酸片球菌、粪肠球菌和嗜酸乳杆菌,以及包含由所选微生物在上述任何一种培养基中共同生长时所产生的代谢物。在一个实施方案中,所述疾病或病症可能是一种胃肠道疾病。在另一个实施方案中,所述疾病或病症可能累及胃肠道的一部分。在一个实施方案中,所述疾病或病症可能累及胃肠道的十二指肠部分。在另一个实施方案中,所述疾病或病症可能累及胃肠道的空肠部分。在一个实施方案中,该疾病或病症可能是坏死性肠炎、沙门氏菌性肠炎、球虫病、乳腺炎、禽流感、鸡痘、传染性支气管炎、鹌鹑支气管炎、喉气管炎、新城疫、霉菌毒素中毒、猪疥癣、胸膜肺炎、胃溃疡、肠扭转、猪副嗜血杆菌病、猪细小病毒病、呕吐和消瘦病、猪流行性腹泻、牛呼吸道疾病综合症、梭菌病、牛呼吸道合胞体病、牛病毒性腹泻、睡眠嗜血杆菌病、传染性牛鼻气管炎、3型副流感、溶血性巴氏杆菌病或多杀性巴氏杆菌病。在另一个实施方案中,所述疾病或病症可能是坏死性肠炎、沙门氏菌性肠炎,球虫病,或乳腺炎。在一个实施方案中,所述疾病或病症可能是一种繁殖性疾病或病症。例如,饲喂本发明中的制剂给动物可能增加家禽的产卵频率,可能降低哺乳生产动物中死胎或木乃伊胎的发生率和/或可能提高哺乳生产动物中活胎的数量。在一个实施方案中,所述疾病或病症可能是由一种传染性微生物引起的。在一些实施方案中,该传染性微生物可能是来自梭菌属。该梭菌属可能是但不限于不和谐梭菌(clostridiumabsonum)、醋酸梭菌(c.aceticum)、醋酸还原梭菌(c.acetireducens)、丙酮丁醇梭菌(c.acetobutylicum)、酸性梭菌(c.acidisoli),耐酸性梭菌(c.aciditolerans),尿酸梭菌(c.acidurici)、耐氧梭菌(c.aerotolerans)、埃氏梭菌(c.aestuarii)、阿卡吉梭菌(c.akagii)、奥德氏梭菌(c.aldenense)、阿氏梭菌(c.aldrichii)、奥吉氏梭菌(c.algidicarnis)、解木聚糖梭菌(c.algidixylanolyticum)、海藻梭菌(c.algidicarni)、嗜寒冷梭菌(c.algoriphilum)、碱性纤维梭菌(c.alkalicellulosi)、亚马逊梭菌(c.amazonense)、嗜氨基梭菌(c.aminophilum)、氨基戊酸梭菌(c.aminovalericum)、苦杏仁苷梭菌(c.amygdalinum)、解淀粉梭菌(c.amylolyticum)、灌木梭菌(c.arbusti)、北极梭菌(c.arcticum)、阿根廷梭菌(c.argentinense)、天冬梭菌(c.asparagiforme)、金黄丁酸梭菌(c.aurantibutyricum)、自产乙醇梭菌(c.autoethanogenum)、巴氏梭菌(c.baratii)、巴勒特梭菌(c.bartlettii)、拜氏梭菌(c.beijerinckii)、双酶梭菌(c.bifermentans)、博尼氏梭菌(c.bornimense)、肉毒梭菌(c.botulinum)、鲍曼梭菌(c.bowmanii)、布氏梭菌(c.bryantii)、丁酸梭菌(c.butyricum)、尸毒梭菌(c.cadaveris)、克安尼梭菌(c.caenicola)、卡氏梭菌(c.caminithermale)、食一氧化碳梭菌(c.carboxidivorans)、肉梭菌(camis)、卡文迪什梭菌(c.cavendishii)、隐藏梭菌(c.celatum)、速生梭菌(c.celerecrescens)、产纤维二糖梭菌(c.cellobioparum)、纤维素酶梭菌、解纤维素梭菌、纤维素梭菌(c.cellulosi)、噬纤维梭菌(c.cellulovorans)、瘤胃梭菌(c.chartatabidum)、鸣疽梭菌(c.chauvoei)、铬还原梭菌(c.chromiireducens)、柠檬酸梭菌(c.citroniae)、克拉黄酮梭菌(c.clariflavum)、梭状样梭菌(c.clostridioforme)、球形梭菌(c.coccoides)、匙形梭菌(c.cochlearium)、克利坦梭菌(c.colletant)、耳蜗形梭菌(c.cocleatum)、狗肠梭菌(c.colicanis)、鹧鸪梭菌(c.colinum)、食胶原梭菌(c.collagenovorans)、柱形芽胞梭菌(c.cylindrosporum)、艰难梭菌(c.difficile)、二醇梭菌(c.diolis)、双孢梭菌(c.disporicum)、德雷克氏梭菌(c.drakei)、坚韧梭菌(c.durum)、酯梭菌(c.esterteticum)、酯化梭菌酯化亚种(c.estertheticumestertheticum)、酯化梭菌拉勒米亚种(c.estertheticumlaramiense)、谲诈梭菌(c.fallax)、费地浸麻梭菌(c.felsineum)、热梭菌(c.fervidum)、菲氏梭菌(c.fimetarium)、乙酸甲酰梭菌(c.formicaceticum)、严寒梭菌(c.frigidicarnis)、恶寒梭菌(c.frigoris)、冈氏梭菌(c.ganghwense)、产气梭菌(c.gasigenes)、戈氏梭菌(c.ghonii)、乙二醇梭菌(c.glycolicum)、甘草梭菌(c.glycyrrhizinilyticum)、格氏梭菌(c.grantii)、溶血梭菌(c.haemolyticum)、嗜盐梭菌(c.halophilum)、矛形梭菌(c.hastiforme)、海瑟薇梭菌(c.hathewayi)、食草梭菌(c.herbivorans)、希拉诺梭菌(c.hiranonis)、溶组织梭菌(c.histolyticum)、单丙酸梭菌(c.homopropionicum)、华癸梭菌(c.huakuii)、亨氏梭菌(c.hungatei)、产氢梭菌(c.hydrogeniformans)、羟基苯甲酸梭菌(c.hydroxybenzoicum)、海利氏梭菌(c.hylemonae)、(c.jeddahense)、空肠梭菌(c.jejuense)、吲哚梭菌(c.indolis)、无害梭菌(c.innocuum)、肠梭菌(c.intestinale)、不规则梭菌(c.irregulare)、板蓝根梭菌(c.isatidis)、约氏梭菌(c.josui)、克鲁佛梭菌(c.kluyveri)、乳酸发酵梭菌(c.lactatifermentans)、拉库氏梭菌(c.lacusfryxellense)、拉勒米梭菌(c.laramiense)、拉瓦氏梭菌(c.lavalense)、缓纤维梭菌(c.lentocellum)、缓腐梭菌(c.lentoputrescens)、柔嫩梭菌(c.leptum)、泥渣梭菌(c.limosum)、海滨梭菌(c.litorale)、液态梭菌(c.liquoris)、象牙海岸梭菌(c.lituseburense)、扬氏梭菌(c.ljungdahlii)、洛氏梭菌(c.lortetii)、伦登梭菌(c.lundense)、窑泥梭菌(c.luticellarii)、大梭菌(c.magnum)、恶名梭菌(c.malenominatum)、芒氏梭菌(c.mangenotii)、马犹姆贝梭菌(c.mayombei)、最大梭菌(c.maximum)、食甲氧基苯甲酸梭菌(c.methoxybenzovorans)、甲基戊糖梭菌(c.methylpentosum)、念珠状梭菌(c.moniliforme)、新丙酸梭菌(c.neopropionicum)、系结梭菌(c.nexile)、硝基酚梭菌(c.nitrophenolicum)、诺维梭伊菌(c.novyi)、海洋梭菌(c.oceanicum)、环形梭菌(c.orbiscindens)、乳清酸梭菌(c.oroticum)、米曲霉梭菌(c.oryzae)、草酸梭菌(c.oxalicum)、溶纸梭菌(c.papyrosolvens)、奇异梭菌(c.paradoxum)、副产气荚膜梭菌(c.paraperfringens)(又名魏氏梭菌)、副腐化梭菌(c.paraputrificum)、牧场梭菌(c.pascui)、巴斯德氏梭菌(c.pasteurianum)、食缩氨酸梭菌(c.peptidivorans)、多年生梭菌(c.perenne)、产气荚膜梭菌(c.perfringens)、芬氏梭菌(c.pfennigii)、植物发酵梭菌(c.phytofermentans)、毛发状梭(c.piliforme)、解多糖梭菌(c.polysaccharolyticum)、多内源孢子梭菌(c.polyendosporum)、包氏梭菌(c.populeti)、丙酸梭菌(c.propionicum)、蛋白溶解梭菌(c.proteoclasticum)、解朊梭菌(c.proteolyticum)、嗜冷梭菌(c.psychrophilum)、略紫色梭菌(c.puniceum)、(c.punense)、解嘌呤环梭菌(c.purinilyticum)、腐化梭菌(c.putrefaciens)、腐败梭菌(c.putrificum)、橡树梭菌(c.quercicolum)、奎宁梭菌(c.quinii)、多枝梭菌(c.ramosum)、直肠梭菌(c.rectum)、玫瑰色梭菌(c.roseum)、糖化丁酸梭菌(c.saccharobutylicum)、糖化梭菌(c.saccharogumia)、解糖梭菌(c.saccharolyticum)、糖化过丁酸丙酮梭菌(c.saccharoperbutylacetonicum)、撒丁岛梭菌(c.sardiniense)、平底锅形梭菌(c.sartagoforme)、苏氏梭菌(c.saudiense)、塞内加尔梭菌(c.senegalense)、粪味梭菌(c.scatologenes)、西尔玛赫梭菌(c.schirmacherense)、斯金登梭菌(c.scindens)、败血梭菌(c.septicum)、索氏梭菌(c.sordellii)、楔样梭菌(c.sphenoides)、螺状梭菌(c.spiroforme)、产芽胞梭菌(c.sporogenes)、球孢梭菌(c.sporosphaeroides)、粪堆梭菌(c.stercorarium)、(c.stercorariumleptospartum)、粪堆梭菌粪堆亚种(c.stercorariumstercorarium)、堆梭菌热乳亚种(c.stercorariumthermolacticum)、斯蒂克兰德梭菌(c.sticklandii)、斯托敏氏梭菌(c.straminisolvens)、偏端梭菌(c.subterminale)、苏弗雷梭菌(c.sufflavum)、产硫梭菌(c.sulfidigenes)、水井坊梭菌(c.swellfunianum)、共生梭菌(c.symbiosum)、泰格鲁梭菌(c.tagluense)、旋舞梭菌(c.tarantellae)、大洋温层梭菌(c.tepidiprofundi)、白蚁梭菌(c.termitidis)、第三梭菌(c.tertium)、破伤风梭菌(c.tetani)、破伤风形梭菌(c.tetanomorphum)、热乙酸梭菌(c.thermaceticum)、热自养梭菌(c.thermautotrophicum)、嗜热碱梭菌(c.thermoalcaliphilum)、嗜热丁酸梭菌(c.thermobutyricum)、热纤梭菌(c.thermocellum)、高温堆肥梭菌(c.thermocopriae)、嗜热硫化氢梭菌(c.thermohydrosulfuricum)、热乳梭菌(c.thermolacticum)、耐热梭菌(c.thermopalmarium)、热溶纸梭菌(c.thermopapyrolyticum)、嗜热化糖梭菌(c.thermosaccharolyticum)、热产琥珀酸梭菌(c.thermosuccinogenes)、热产硫磺梭菌(c.thermosulfurigenes)、减硫代硫酸盐梭菌(c.thiosulfatireducens)、酪丁酸梭菌(c.tyrobutyricum)、尿梭菌(c.uliginosum)、超大型梭菌(c.ultunense)、胃梭菌(c.ventriculi)、绒毛梭菌(c.villosum)、文氏梭菌(c.vincentii)、绿色梭菌(c.viride)、秃鹰梭菌(c.vulturis)、解木聚糖梭菌(c.xylanolyticum)、或食木聚糖梭菌(c.xylanovorans)。在另一个实施方案中,该梭菌可以是产气荚膜梭菌。在一个实施方案中,所述混合物可以降低动物粪便中病原体的含量。在一个实施方案中,所述混合物可以降低动物粪便中氨的含量。在一个实施方案中,所述混合物可以降低动物通过呼吸作用或以消化气体的形式制造并释放到环境中甲烷的量。在一个实施方案中,所述混合物可以提高饲料转化率。在一个实施方案中,所述混合物可以降低动物死亡率。在一个实施方案中,所述混合物可以提高动物平均每日体重增加量。在一个实施方案中,所述混合物可以提高蛋壳的质量和蛋的重量。在一个实施方案中,所述混合物可以调节动物的胃肠道微生物组。在另一个实施方案中,所述混合物可以调节动物的胃肠道免疫应答反应。在其他实施方案中,所述混合物可以调节动物胃肠道蛋白的磷酸化反应。在一些实施方案中,固态混合物可以被添加到动物的饲料中或作为补充剂提供给动物。在一个实施方案中,该混合物可以以固体形式提供并添加到动物饲料配额中。在一些实施方案中,可以以约0.1kg/吨至约2.0kg/吨饲料的量将固体混合物添加到动物饲料配额中。在其他实施方案中,该固态混合物在动物饲料配额中的量为约0.1kg/吨、约0.25kg/吨、约0.5kg/吨、约0.75kg/吨、约1.0kg/吨、约1.0kg/吨、约1.25kg/吨、约1.5kg/吨、约1.75kg/吨,或约2.0kg/吨。在一些实施方案中,可以将液体混合物添加到动物的饮用水供应中。在一个实施方案中,该混合物可以以液体形式提供并添加到动物的饮用水中。在一些实施方案中,可以以约0.1ml/天/动物至约10ml/天/动物的量将液体混合物添加到动物的饮用水中。在其他实施方案中,该液态混合物在每只动物的引用水中的量可以为约0.1ml/天、约0.25ml/天、约0.5ml/天、约1.0ml/天、约1.25ml/天、约0.1ml/天、约1.5ml/天、约1.75ml/天、约2.0ml/天、约2.25ml/天、约2.5ml/天、约2.75ml/天、约3.0ml/天、约3.25ml/天、约3.5ml/天、约3.75ml/天、约4.0ml/天、约4.25ml/天、约4.5ml/天、约4.75ml/天、约5.0ml/天、约6.25ml/天、约6.5ml/天、约6.75ml/天、约7.0ml/天、约7.25ml/天、约7.5ml/天、约7.75ml/天、约8.0ml/天、约8.25ml/天、约8.5ml/天、约8.75ml/天、约9.0ml/天、约9.25ml/天、约9.5ml/天、约9.75ml/天、或约10.0ml/天。在一个实施方案中,所述混合物可以以液体形式提供并添加到鸡的饮用水中。在一些实施方案中,该液体混合物可以以约0.1ml/天至约2ml/天/动物的量添加到鸡的饮用水中。在其他实施方案中,可以以约0.1ml/天/动物、约0.25ml/天/动物、约0.5ml/天/动物、约1.0ml/天/动物、约1.25ml/天/动物、约1.5ml/天/动物、约1.75ml/天/动物、或约2.0ml/天/动物的量将液态混合物添加到鸡的饮用水中。在一个实施方案中,所述混合物可以以液体形式提供并添加到猪的饮用水中。在一些实施方案中,可以将该液态混合物以约0.5ml/天/动物至约10ml/天/动物的量添加到猪的饮用水中。在其他实施方案中,可以将该液态混合物以约0.5ml/天/动物、约0.75ml/天/动物、约1.0ml/天/动物、约1.25ml/天/动物、约1.5ml/天/动物、约1.75ml/天/动物、约2.0ml/天/动物、约2.25ml/天/动物、约2.5ml/天/动物、约2.75ml/天/动物、约3.0ml/天/动物、约3.25ml/天/动物、约3.5ml/天/动物、约3.75ml/天/动物、约4.0ml/天/动物、约4.25ml/天/动物、约4.5ml/天/动物、约4.75ml/天/动物、约5.0ml/天/动物、约5.25ml/天/动物、约5.5ml/天/动物、约5.75ml/天/动物、约6.0ml/天/动物、约6.25ml/天/动物、约6.5ml/天/动物、约6.75ml/天/动物、约7.0ml/天/动物、约7.25ml/天/动物、约7.5ml/天/动物、约7.75ml/天/动物、约8.0ml/天/动物、约8.25毫升/天/动物、约8.5ml/天/动物、约8.75ml/天/动物、约9.0ml/天/动物、约9.25ml/天/动物、约9.50ml/天/动物、约9.75ml/天/动物、或约10.0ml/天/动物的量添加到猪的饮用水中。对于本领域的技术人员而言,根据本发明的教导,在不脱离本发明的精神和范围的情况下,对所公开的特定实施方式进行改变、修改和变型仍可获得相似或类似的结果。定义与林奈氏生物学分类系统一致,本文中细菌种属名用拉丁名称表示。因此,可以参考某些属、种、亚种和菌株名称来区别微生物。本文中所使用的术语“微生物组(microbiome)”是指存在于动物胃肠道系统中的全部微生物物种的群落。本文中所使用的术语“益生菌(probiotic)”和“益生菌微生物(probioticmicroorganism)”是指一种或多种微生物的混合物,当口服后对动物健康有益处。本文中所使用的术语“益生元(prebiotic)”是指一种非微生物成分,可以选择性添加到益生菌制剂中,其能够诱导胃肠道系统中益生菌微生物的生长或活性。本文中所使用的术语“后生素(postbiotic)”是指一种灭活细菌产物或是来自益生菌的代谢副产物,其在宿主体内具有生物学活性。本文中可互换使用的术语“短链脂肪酸(shortchainfattyacid)”或“scfa”包括乙酸、甲酸、丙酸、丁酸、异丁酸、戊酸、琥珀酸和异戊酸。本文中所使用的术语“动物(animal)”是指但不限于人、家畜、伴侣动物、实验动物和动物园动物。在另一个实施方案中,该动物可以是家畜。在一个实施方案中,该动物可以是牛、猪或家禽。在其他实施方案中,该动物可以是牛、猪或鸡。合适的家畜包括但不限于猪、牛、马、山羊、绵羊、美洲驼和羊驼。在另一个实施方案中,该动物可以是一种伴侣动物。伴侣动物包括但不限于狗、猫、兔子和鸟。在另一个实施方案中,该动物可以是动物园动物。在另一个实施方案中,该动物可以是人。实施例以下实施例将被用于阐述本申请中的各种实施方案。本领域中的技术人员应该理解,以下实施例中公开的技术遵循由发明者发现的在本发明的实践中稳定起作用的具有代表性的技术,因此该技术可以被认为是构成其实施的优选方式。然而,对于本领域的技术人员而言,根据本发明的教导,在不脱离本发明的精神和范围的情况下,对所公开的特定实施方式进行改变、修改和变型仍可获得相似或类似的结果。实施例1采购用于发酵混合物制剂的微生物的方法所使用的菌株是单菌株生物培养物,其存储在含15%至25%甘油的培养基中。这些特定种的菌株是由发明人从purecultures,inc.公司获得,或者是通过生物勘探从市售的食品添加剂中获得,或者从usda/nrrl菌种保藏中心获得。实施例2样品采集和从粪便种分离细菌的方法从美国科罗拉多州的健康犬收集新鲜的粪便样品,并立即在大约-18℃下冷冻。将粪便添加到蛋白胨水中(10%wt/vol)并涡旋以完全匀质化样品。然后将粪便匀浆的梯度稀释液划线到mrs琼脂平板上进行分离。挑选单个菌落,通过mrs琼脂平板分离进一步纯化,一旦获得纯菌落,随后在mrs肉汤培养基中扩大培养。然后用30%的甘油水溶液稀释细菌扩大培养液。然后将1ml等分试样放入2ml体积的冷冻管中,并在-80℃下保存。实施例3样品收集和从市售食品添加剂中分离细菌的方法将购买的益生菌产品接种到非动物性mrs培养基中,并在37℃下培养约15个小时。将一个无菌接种环浸入到细菌培养液中,并划线接种到非动物性mrs琼脂平板上。将该琼脂板过夜培养约18个小时。挑选单个菌落并接种高压灭菌后的非动物性培养基,并在37℃下孵育。然后用50%甘油水溶液对细菌扩大培养液进行1:1稀释。然后将1ml等分试样放入2ml体积的冷冻管中,并在-80℃下保存。实施例4用于鉴别菌株的16srrna测序方法菌株被送到特拉华州纽瓦克市19713的midi实验室(midilaboratoriesnewark,de19713)。测序片段大小约为500个碱基对,并将片段与d16m3libraryrevision3.01进行比对。实施例5菌株的全基因组测序方法根据atcc-ctm建立的标准操作规程(sop)对每株菌进行处理。首先用qiampdnaminikit(qiagen目录编号51304)试剂盒从每个菌株中提取全基因组dna,然后用qubit2.0荧光计按照制造商的说明(thermofisherscientific)对其进行荧光定量。全基因组测序是按照illumina公司推荐的工作流程进行的。首先使用nexteraxtdna文库制备试剂盒(illumina目录编号fc-131-1096)按照制造商的说明进行文库制备。然后用illuminamiseq技术配套miseqreagentkitv3(600-cycle)试剂盒配套(illumina目录号ms-102-3003)对经过质量控制检测的dna文库进行测序。接着使用来自英国剑桥巴布拉汉姆研究所(babrahaminstitute)巴布拉汉姆生物信息学组<https://www.bioinformatics.babraham.ac.uk/projects/fastqc/>)的应用软件fastqc对所得序列的读取质量和准确性进行评估。(最后,将经过质量控制检测并筛选出的序列组装成重叠群,并使用atcc-ctm专有的高级微生物基因组学(advancedmicrobialgenomics,amg)平台对其进行注释。实施例6短链脂肪酸(scfas)检测方法一个使用agilent1100系列hplc单元的hplc检测方法。使用bio-rad有机酸分析柱aminexhpx-87h离子排斥柱为0.2n的h2so4。加热至60℃。如图1所示,基于食物的交叉喂养机制是哺乳动物、鸟类和爬行动物的肠道微生物组的一个关键特征。为了理解交叉喂养机制,用四株菌进行了进一步的建模,并与相同四株菌的全基因组代谢模型进行了比较。此模型进一步与基于scfas生产的几个关键菌株(肠道微生物组参考菌株)建立的模型进行了比较。连同我们的四个全基因组代谢模型,最终的交叉喂养模型的建立使用了多形拟杆菌(bacteroidesthetaiotaomicron)、大肠杆菌k-l2(escherichiacolik-l2)、多枝梭菌(clostridiumramosumvpi)、和植物乳杆菌。交叉喂养模型的运行是基于产生scfa(例如丁酸盐)的两种关键代谢物,即乳酸(次级代谢物)和木聚糖(初级代谢物)。有趣的是,所有四株菌均表现出与其他参考菌株显著的交叉喂养相互作用。该结果突出了以下事实:这些菌株具有利用生产scfas的初级(木聚糖)和次级(乳酸)代谢前体来有效生产scfas的遗传/代谢潜力。实施例7评估病原体抑制的方法使用tsb琼脂板通过孔扩散法测定乳酸菌(lab)的抗菌活性。首先接种已知的病原体标准品到tsb培养基中,并在37℃下培养24±4小时。然后在tsb琼脂平板上平铺100μl细菌培养液。接着在琼脂上打孔,并在每孔中接种25μl过夜发酵液,然后在37℃下培养过夜。测量抑制圈(inhibitionhalo)大小并以mm为单位。下表列出了某些菌株的抑菌结果。表5.菌株在不同培养基中生长对大肠杆菌的抑制作用实施例8针对已知数据库比对序列数据的方法如图3所示,使用prokka管道(<https://github.com/tseemann/prokka>)对基因组草图在通路和酶水平进行注释(。使用400个标记基因数据集对每个基因组进行生物学分类,并最后将其与参考基因组进行比较。用所有四个基因组草图及与其最靠近的前50个系统发育邻居构建最大似然树(bootstrap=1000)。基于全基因组的系统发育分析(如上所述)清楚地确定了每个基因组在物种水平的身份。通过配对全基因组平均核苷酸同源性(ani)分析来分析每个基因组在菌株水平的身份,已确定的菌株水平平均核苷酸同源性阈值为99.9%。配对ani计算结果清楚地突出显示了所有四个菌株,即罗伊氏乳杆菌pcr7、嗜酸乳杆菌pcll01、粪肠球菌pcef02和发酵乳杆菌pcf1,与其菌种水平最接近的基因型相比是新型菌株。用etsing软件模拟微生物组数据(来自表达scfa的基因组的定制基因组数据集)。用irep工具(<https://github.com/christophertbrown/irep>)预测了每个基因组的原位复制速率。对原位复制速率进行的下游分析清楚地表明了每个菌株可以在肠道环境中快速原位生长(使用了>500个培养的参考菌种基因组进行模拟)。用biopieces软件提取了与肠细胞黏附有关的粘液结合因子和纤连蛋白结合因子的近乎完整的蛋白质编码基因序列。有趣的是,发酵乳杆菌pcf1和罗伊氏乳杆菌pcr7对粘蛋白和纤连蛋白结合蛋白均显示出阳性命中率(blastx,e值=10-e5)。通过etsingabricate(<https://github.com/tseemann/abricate>)通道对基因组草图中转座子和/或整合子附近可能存在的任何抗药基因(arg)进行了筛查。正如对益生菌菌株所期望的那样,四个基因组草图中没有一个在转座子和/或整合子附近有任何抗药基因。这些结果清楚地表明了所述菌株能发生基因水平漂移的可能性极低。通过在rast结果输出的子系统功能计数(subsystemfeaturecount)中搜索毒力因子、致病因子和防御子系统因子来注释毒力因子。通过对bactibase数据库(<http://bactibase.hammamilab.org/main.php>)的全面搜索来确定组装序列中细菌素的存在。bactibase包含230种细菌素的经计算或预测的理化性质,其中206种细菌素由革兰氏阳性菌产生,19种细菌素由(革兰氏阴性菌产生。这个数据库中的信息可以允许预测这些多肽的靶标生物,还可以允许快速预测结构/功能关系,从而可以更好地开发利用它们在医学和食品领域中的生物活性。每个全基因组序列组装分别被用作查询条件用于结果搜索。实施例9采用气相色谱法(gc)和火焰离子检测器(fid)来检测scfa的方法样品提取物在配有火焰离子检测器的agilent6890系列的气相色谱仪(gc-fid;安捷伦公司,加利福尼亚州圣克拉拉市)上进行分析。进样速度为10:1的分流比,入口温度为22℃,传输线温度保持在230℃。样品在一根30米长的tg-wax-a色谱柱(thermoscientific,0.25mmid,0.25μm膜厚)上实现分离,条件如下:先在100℃保持1分钟,再以8℃/min的速度升温至180℃,接着在180℃保持1分钟,再以20℃/min的速度升温至200℃,最后在200℃保持5分钟。氦气的载流量被保持在1.2ml/min。使用市售标准品(sigma,美国密苏里州圣路易斯市)的5点标准曲线对短链脂肪酸进行定量,并归一化为内标信号。如图4所示,乙酸的保留时间为5.4和5.5分钟。丙酸的保留时间为6.5分钟。丁酸的保留时间为7.7分钟。乳酸的保留时间为13.2和14.78分钟,而抗坏血酸的保留时间为14.04和15.09分钟。实施例10使用prokka通道评估基因组组装的方法首先,使用idba组装器(一种用于单细胞和宏基因组测序的novo组装器)将原始基因组序列组装成重叠群。然后,使用uniprot数据库对重叠群进行注释。接着,使用biopythongenbank对注释结果进行解析。使用定制的bash和python脚本,将注释文件解析成酶和通路水平的功能矩阵,如下表所示。表6.热稳定蛋白表格列出了基因组中存在的基因拷贝数。实施例11益生菌制剂获得并合并以下菌株:嗜酸乳杆菌pcla18、罗伊氏乳杆菌pcr7、乳酸片球菌pcll01和粪肠球菌pcef02。菌株混合物在含约5%糖蜜、5%菊粉和2.5%v/v甘油的液体培养基中生长。生长完成后,收获培养基和细菌。该收获的混合物可用作益生菌。实施例12益生菌制剂对十二指肠和空肠蛋白的磷酸化如实施例11所述制备益生菌制剂并将其用于鸡的饲喂试验,并检测了鸡的消化道十二指肠和空肠部分的激酶组(manning等,2002)。鸡的饲喂试验分组:空白对照组(i),益生菌制剂饲喂组(ii),产气荚膜梭菌(攻击组(iii),产气荚膜梭菌攻毒并用益生菌制剂治疗组(iv),球虫病疫苗和益生菌制剂联合治疗组(v),以及产气荚膜梭菌攻毒并用球虫病疫苗和益生菌制剂联合治疗组(vi)。将来自每组5只鸡的生物学重复样品合并以生成具有代表性的激酶组图谱。在对数据做组合和归一化处理之后,使用定制软件包piika2(trostetal.,2013)对所得的12组激酶组图谱[(空肠和十二指肠组织各一个,2)×试验分组(i到vi,6)]进行聚类分析。图4是一个聚类分析图,其展示了基于单个蛋白质磷酸化的12组图谱之间的相对相似性。图5是另一个聚类分析图,其展示了相对于每个对应组织的对照激酶组图谱的治疗/组织组合的激酶组图谱。益生菌制剂的作用可见于图4。从经过益生菌制剂饲喂过的鸡处获得的空肠组织倾向于聚集在一起。然而,十二指肠组织样品似乎没有形成特定的聚集模式。从未曾饲喂过益生菌制剂的鸡处获得的空肠组织样品也形成聚集。这些结果提示饲喂益生菌制剂对空肠组织有明显的作用,其独立于产气荚膜梭菌攻击的作用。参照图5,取自不同试验组的十二指肠组织样品再次几乎没有显示出任何区别。空肠组织样品似乎再次基于饲喂的代谢物而聚集,其中饲喂非益生菌制剂组的样品保持独立。从代谢物聚集中去除最多的是经产气荚膜梭菌诱导致坏死性肠炎后经益生菌制剂治疗组的样品,这些结果提示与饲喂其他代谢物的试验组相比,该组相对于空白对照而言发生的变化最大。实施例13用益生菌制剂治疗后空肠生物学过程和信号通路的鉴别用实施例12中不同试验组(i到iv)的鸡获得多肽阵列,试验发现其中空肠组织样品中的单个多肽表现出相对于空白对照组(i)的差异磷酸化模式。然后对这些单个多肽进行蛋白质string分析(szklarczykdetal.,2015;<https://string-db.org>)以揭示其相关的生物学过程(go),并进行kegg分析(kanesham,gotos,2000);<https://www.genome.jp/kegg/pathway.html>)以揭示其相关的信号传导通路。表7和表8示出了益生菌制剂饲喂组鸡(ii)的string和kegg结果。表9和表10示出了产气荚膜梭菌攻毒组鸡(iii)的string和kegg结果。表11和12示出了先经产气荚膜梭菌攻毒后经益生菌制剂治疗组鸡(iv)的string和kegg结果。需要注意的是,某些生物过程在表与表之间可能会发生重叠,而生物过程的成员必须是唯一的才能被用于分析。因此,相同的术语可能在不同组间出现,但是在不同组间以不同的方式被富集。这表明,被富集的各种生物过程在不同试验组间表现不同。表7和表9中突出显示的是与免疫信号传导相关的术语。益生菌制剂饲喂组(表7)中突出显示的所有生物学过程也都出现在产气荚膜梭菌攻毒组(表9)中,但是需要注意的是,用于生成每个组的表格的列表都是不同且唯一的。因此,尽管在不同试验组间出现了相同的术语,但它们代表的是在同一个生物学过程中的变化。有趣的是,益生菌+产气荚膜梭菌攻毒组(表11)在string分析中的前20条通路中并没有出现相同的免疫相关的生物学通路的富集。这表明,重叠使用益生菌制剂和产气荚膜梭菌时,它们各自可能会在空肠组织中发挥其独特的作用,但是当将它们放在一起时,不会富集出新的免疫相关的生物学过程。关于表8、表10和表12,需要注意的是不同表格之间的kegg通路可能会重叠,且通路成员必须是唯一的才能被用于分析。因此,相同的术语可能会出现在不同组间,但是其在不同组间以不同的方式被富集。这表明,在不同试验组间被富集的各种kegg通路表现不同。表7.与未经治疗的鸡相比,唯独在益生菌制剂饲喂组鸡的空肠组织中富集的前20个生物过程(go)生物学过程蛋白质数量错误发现率对化学刺激的细胞反应368.62e-12对有机物的细胞反应323.00e-11磷酸化259.43e-11跨膜受体蛋白酪氨酸激酶信号通路211.13e-10酶联受体蛋白信号通路232.10e-10蛋白质磷酸化211.03e-09信号调节347.35e-09对刺激反应的调节366.90e-08对免疫反应的调节196.90e-08磷代谢过程277.12e-08对有机物质的反应317.12e-08对细胞通讯的调节339.58e-08对免疫系统过程的调节231.57e-07含磷酸盐的化合物代谢过程261.94e-07细胞表面受体信号通路276.22e-07对信号传导的调控296.58e-07对化学物质的反应369.23e-07对免疫系统过程的正向调控172.70e-06先天免疫反应182.70e-06单细胞代谢过程374.38e-06表8.与未经治疗的鸡相比,唯独在益生菌制剂饲喂组鸡的空肠组织中富集的前20条kegg通路kegg通路蛋白质数量错误发现率pi3k-akt信号通路146.90e-09fcγr介导的吞噬作用96.90e-09eb病毒感染111.56e-08胰腺癌72.58e-07非酒精性脂肪肝病(nafld)93.08e-07ras信号通路104.99e-07弓形虫病84.99e-07甲型流感95.57e-07破骨细胞分化87.90e-07丙型肝炎89.40e-07麻疹89.40e-07癌症中的通路119.70e-07乙型肝炎81.42e-06vegf信号通路62.15e-06toll样受体信号通路72.40e-06tnf信号通路73.14e-06fcεri信号通路63.49e-06脂肪细胞因子信号通路63.61e-06催乳素信号通路64.08e-06黏附连接64.19e-06表9.与未被攻毒组相比,唯独在产气荚膜梭菌攻毒组鸡的空肠组织中富集的前20个生物过程(go)表10.与未攻毒组相比,唯独在产气荚膜梭菌攻毒组鸡的空肠组织中富集的前20条kegg通路kegg通路肽的数量错误发现率胰岛素信号通路84.18e-06t细胞受体信号通路75.66e-06神经营养因子信号通路71.14e-05自然杀伤细胞介导的细胞毒性71.36e-05局灶性粘连82.00e-05前列腺癌62.00e-05雌激素信号通路62.93e-05癌症中的通路94.47e-05胶质瘤56.17e-05fcεri信号通路58.24e-05破骨细胞分化68.79e-05催乳素信号通路58.79e-05丙型肝炎60.000102erbb信号通路50.000183mapk信号通路70.000416子宫内膜癌40.000436病毒致癌60.000532非小细胞肺癌40.000532foxo信号通路50.000803麻疹50.00108表11.与空白对照组相比,唯独在经产气荚膜梭菌攻毒且经益生菌制剂治疗组鸡的空肠组织中富集的前20个生物过程(go)生物学过程蛋白质数量错误发现率蛋白质自磷酸化119.87e-09酶联受体蛋白信号通路175.74e-08跨膜受体蛋白酪氨酸激酶信号通路151.05e-07细胞蛋白代谢过程的调节211.08e-05细胞内信号转导的调节171.08e-05激酶活性的正调节111.18e-05脂质代谢过程的正调节71.18e-05细胞内信号转导184.55e-05蛋白激酶活性的调节124.55e-05对外部刺激的反应184.88e-05催化活性的正调节164.88e-05多细胞生物过程的调节204.88e-05分子功能的正调节176.06e-05肽基酪氨酸磷酸化76.85e-05蛋白质磷酸化120.000123细胞组分生物生成的调节110.000123蛋白质修饰过程的调节160.000124蛋白质磷酸化的调节140.000128细胞内信号转导的正调节120.000132轴突引导90.000151表12.与空白对照组相比,唯独在经产气荚膜梭菌攻毒且经益生菌制剂治疗组鸡的空肠组织中富集的前20条kegg通路实施例14用益生菌制剂治疗后动物健康参数的评估如实施例11中所述制备益生菌制剂,并将其用于鸡饲喂实验。评价了动物的多种健康参数。试验分组如下:空白对照组(t1),益生菌制剂治疗组(t2),球虫病疫苗治疗组(t3),产气荚膜梭菌攻毒且用球虫病疫苗治疗组(t4),产气荚膜梭菌攻毒组(t5),产气荚膜梭菌攻毒且用益生菌制剂治疗组(t6),球虫病疫苗和益生菌制剂联合治疗组(t7),以及用产气荚膜梭菌攻毒且用球虫病疫苗和益生菌制剂联合治疗组(t8)。用于评估动物健康的参数如下:(a)肠道中产气荚膜梭菌的活菌量,(b)体重增加,(c)产气荚膜梭菌引起的坏死性肠炎病变,和(d)死亡率。实验设计进一步汇总在表13中。表13.实验设计将t8与t4和t5进行比较时,得出以下结果:(a)肠道中产气荚膜梭菌活菌数总量明显降低(分别为t8组1.7×105、t4组6.2×105和t5组14.0×105);(b)体重增加明显更多:分别为t8组增加781g、t4组增加697g、t5组增加695g。作为比较,t1(阴性对照)组的平均体重增加为805g。(c)病变得分显著降低:病变得分分别为t8组0.56、t4组2.3和t5组3.0;(d)死亡率显著降低:死亡率分别为t8组1/50、t4组12/50和t5组21/50。实施例15生产和检测一个用于家禽健康的联合液体混合物中一个特有的有机酸共混物引言。乳酸菌已经被研究了数十年,这些微生物的一个众所周知的能力是能够从五碳和六碳糖源代谢短链有机酸(urdaneta等,1995)。此类酸的实例包括乙酸、丁酸、甲酸、乳酸和丙酸(zalanetal.,2009)。方法。所有操作均在无菌条件下进行。每次发酵试验先从15%-25%甘油/mrs冷冻菌种中选择至多四个乳酸菌单菌株。随后将它们在37℃±2℃下培养1至2天。在此初始繁殖之后,将所有菌株合并到经巴氏灭菌后的培养基和去离子水中,并在30至37℃±2℃下培养5至15天。根据改良的aoac986.13检测方法用hplc分别解析所得样品。样品分析用的是折射率检测器,并通过与有机酸标准品进行对比来鉴别各个峰。结果。小的有机酸是通过乳酸菌的选定组合发酵选定的碳(糖)源的最终产物。如表14和表15所示,选择特定的碳源和微生物组合可能会导致生成三种主要的有机酸。表14.有机酸的生产根据purecultures公司的内部标准操作规程(sop)scfahlc001已对多个批次的发酵物的纯度和短链脂肪酸指纹图谱进行了检测。为德克萨斯州农工大学1号试验生产的,也是生产的第一批编号为17014的产品中含有罗伊氏乳杆菌pcr7、乳酸片球菌pcll01、戊糖片球菌pcpp01和粪肠球菌pcef01。对储存六个月后的该产品进行了检测,此外,还检测了加热到90℃并持续5分钟后的该产品。使用相同的评估sop对第二批编号为18007的产品进行了纯度检测。该产品含有以下菌株:发酵乳杆菌pclf01、罗伊氏乳杆菌pcr7、乳酸片球菌pcll01、戊糖片球菌pcpp01、粪肠球菌pcef02。表15.有机酸的生产讨论。本文所述的技术提供了一种快速、可靠的用于检测和初步描述发酵液中有机酸的方法。同时证明发酵过程的可重复性和生成独有且专有配方的能力。仔细选择碳源和/或微生物可以带来受控的发酵环境,以生产特定的有机酸。如引言中所述,选择特定的有机酸对家禽的体重增加和抵抗病原体都很重要。实施例16活菌计数方法基于美国药典(usp)<202l>食品添加剂微生物计数方法之微生物总数平板计数法。收集的样品加冰袋以确保储存温度低于10℃,并被连夜运送到第三方实验室做检测。培养基制备:按照包装上的说明,制备含0.5g/l半胱氨酸的乳酸菌mrs琼脂平板。先按照无菌操作规范称量10.0g样品,再加90ml无菌蛋白胨缓冲液稀释。接着将样品和缓冲液均质化。取1ml匀质液加99ml蛋白胨缓冲液稀释,并做连续梯度稀释,直到在最终乳酸菌计数的估计值附近获得3个稀释度。在每个含半胱氨酸的mrs琼脂平板上接种0.1ml稀释液,并用无菌涂抹器抹开直到稀释液被完全吸收。把培养基放入无氧温箱中,在37℃下培养48至72小时。接着选择菌落数在30到300之间的平板并计数。结果在图6和表16中示出。表16.各批次产品的乳酸菌计数当产品规格为≥5.0×l07时,产品保质期平均为2.2个月;当产品规格为≥l.0×l07时,产品保质期平均为4.83个月。批次号为18001的产品包含以下菌株:发酵乳杆菌pclf01、罗伊氏乳杆菌pcr7、乳酸片球菌pcll01、戊糖片球菌pcpp01、粪肠球菌pcef01。批次号为18004的产品包含以下菌株:发酵乳杆菌pclf01,罗伊氏乳杆菌pcr7、乳酸片球菌pcll01、戊糖片球菌pcpp01、粪肠球菌pcef01。批次号为18006的产品包含以下菌株:发酵乳杆菌pclf01、罗伊氏乳杆菌pcr7、乳酸片球菌pcll01、戊糖片球菌pcpp01、粪肠球菌pcef01。批次号为18007的产品包含以下菌株:发酵乳杆菌pclf01、罗伊氏乳杆菌pcr7、乳酸片球菌pcll01、戊糖片球菌pcpp01、粪肠球菌pcef01。批次号为181023的产品包含以下菌株:罗伊氏乳杆菌pcr7、乳酸片球菌pcll01、戊糖片球菌pcpp01、粪肠球菌pcef01。实施例1790℃稳定性测试取在糖蜜培养基中且含有罗伊氏乳杆菌pcr7、乳酸片球菌pcll01、戊糖片球菌pppc01和粪肠球菌pcef01的批次号为17014的益生菌制剂约10ml于烧杯中并用铝箔封口,并将样品放入温度为90℃的烤箱中加热。样品达到90℃后开始计时。5分钟后,将样品从烤箱中移出,并放置在冰箱里直到温度降到约为40℃。接着,样品被送往内布拉斯加州奥马哈市的midi实验室,在那里按照改良的aoac986.13检测方法测定有机酸。hplc检测方法使用agilent1100系列的hplc单元和bio-rad有机酸分析柱aminexhpx-87h,该离子排斥柱使用0.2n的h2so4作为。比较一个样品在加热前与90℃加热后其有机酸色谱在峰型、峰量和每个峰面积的相似性。步骤1,确定两个色图谱中均有9个峰。如果两个样品中的任一个样品存在一个新的峰,需要确保其面积不大于所有面积总和的1.5%。步骤2,确保峰3、峰4和峰5的面积比为1:1:1。步骤3,确认两个样品中的乳酸和乙酸浓度为每个样品浓度的±0.5%。结果在图7中示出。实施例18六个月稳定性测试将在糖蜜培养基中且含有罗伊氏乳杆菌pcr7、发酵乳杆菌pclf01、乳酸片球菌pcll01、戊糖片球菌pppc01和粪肠球菌pcef01的批次号为17014的益生菌制剂在约22℃±-2℃的室温下储存。样品在一个8盎司的高密度聚乙烯(hdpe)塑料瓶中储存。储存六个月后,将样品送至内布拉斯加州奥马哈市的midi实验室,在那里按照改良的aoac986.13检测方法测定有机酸。hplc检测方法使用agilent1100系列hplc单元和bio-rad有机酸分析柱aminexhpx-87h,该离子排斥柱使用0.2n的h2so4作为。比较一个样品在生产后5天和在室温下储存6个月后的有机酸色谱在峰型、峰量和每个峰面积的相似性。步骤1,确定两个色图谱中均有9个峰。如果在六个月的样品中出现一个新的峰,需要确保其面积不超过所有面积总和的1.5%。步骤2,确保峰3、峰4和峰5的面积比为1:1:1。步骤3,确认六个月样品中的乳酸和乙酸浓度为原始样品浓度的±0.5%。结果在图8中示出。实施例19干燥稳定性测试将在糖蜜培养基中且含有罗伊氏乳杆菌pcr7、发酵乳杆菌pclf01和粪肠球菌pcef01的批次编号为17003的乳酸菌制剂送至蓝草乳品厂(bluegrassdairy)进行喷雾干燥和滚筒干燥。etsing是干燥领域的标准技术。两种干燥过程都需要添加近85%w/w的麦芽糖糊精。干燥后,样品被送往内布拉斯加州奥马哈市的midi实验室,在那里按照改良的aoac986.13检测方法测定有机酸。hplc检测方法使用agilent1100系列的hplc单元和bio-rad有机酸分析柱aminexhpx-87h,该离子排斥柱使用0.2n的h2so4作为。比较一个样品在起始液体状态和经过喷雾干燥和滚筒干燥后所得干燥粉末的有机酸色谱的峰型/峰量和每个峰面积的相似性。步骤1,确定干燥粉末中乳酸的浓度在理论浓度±25%的范围内。计算方法:用乳酸浓度检测结果乘以99,再除以85(用载体进行稀释的稀释百分比)。如果乙酸在起始液体样品中的含量<0.5%,那么它可能不会存在于干燥样品中,因为乙酸在加热时更容易发生热降解和挥发。实施例20批次和组成菌株的比较使用上文中关于实施例18描述的方法测定某些多菌株批次的有机酸图谱。4种混合物及其组分之间的比较在图10中示出。图11描绘了四种混合物的有机酸“指纹”图谱。图12描绘了某些混合物和组成菌株的对比。产品批次号为et8的产品包含以下菌株:罗伊氏乳杆菌pcr7、乳酸片球菌pcll01、戊糖片球菌pcpp01、粪肠球菌pcef02。产品批次号为et4的产品包含以下菌株:罗伊氏乳杆菌pcr7、乳酸片球菌pcll01、戊糖片球菌pcpp01、粪肠球菌pcef02。参考资料americanmeatinstitute(2013).thefactsaboutantibioticsinlivestock&poultryproduction.americanmeatinstitutewebsite.availablefromlirl:<https://www.meatinstitute.org/index.phpcdc>.(2013).centerfordiseasecontrolandprevention.retrievedfromantibioticresistancethreatsreportandfoodbornegerms:http://www.cdc.gov/narms/resources/threats.html.cdc.(2013).centerfordiseasecontrolandprevention.retrievedfromantibioticresistancethreatsreportandfoodbornegerms:http://www.cdc.gov/narms/resources/threats.html.cheng-hsunchiu,m.p.-l.-h.-h.-j.-s.-y.(2002).theemergenceintaiwanoffluoroquinoloneresistanceinsalmonellaentericaserotypecholeraesuis.nengljmed,413-419.departmentofhealthandhumanservices(ets),foodanddrugadministrationguidancefromindustry:newanimaldrugsandnewanimaldrugcombinationproductsadministeredinoronmedicatedfeedordrinkingwateroffoodproducinganimals:recommendationsfordrugsponsorsforvoluntarilyaligningproductuseconditionswithgfi#209.availablefromeire:<http://www.fda.gov/downloads/animalveterinary/guidancecomplianceenforcement/guidanceforindustry/ucm299624.pdf>.davidg.white,p.s.(2001).theisolationofantibiotic-resistantsalmonellafromretailgroundmeats.nengljmed,1147-1154.fda.(2014,12).withdrawalofenrofloxacinforpoultry.retrievedfromeisdepartmentofhealthandhumanservices:http://www.fda.gov/animalveterinary/safetyhealth/recallswithdrawals/ucm042004.htm.gundogann.,citaks.,yuceln.,devrena.(2005)anoteontheincidenceandantibioticresistanceofstaphylococcusaureusisolatedfrommeatandchickensamples.meatsci2005;69:807-10.hassanh.m.a.,mohamedm.a.,youssefa.w.,hassane.r.(2010).effectofusingorganicacidstosubstituteantibioticgrowthpromotersonperformanceandintestinallanders,timothyf.landers,cohen,bevin,wittum,thomase.,larson,larson1.,(2012).areviewofantibioticuseinfoodanimals:perspective,policy,andpotential.publichealthrep.jan-feb;127(1):4-22.izat,a.,tidwell,n.,thomas,r.,reiber,m.,adams,m.,colberg,m.,&wadroup,p.(1990).effectsofabufferedpropionicacidindietsontheperformanceofbroilerchickensandonthemicrofloraoftheintestineandcarcass.poultryscience,818-826.kanehisam.,gotos.(2000)"kegg:kyotoencyclopediaofgenesandgenomes".nucleicacidsres.28(1):27-30.luckstadt,c.,&theobald,p.(2011).dosedependenteffectsofdiformateonbroilerperformance.inc.luckstadt,standardsofacidifiers-principalsfortheuseoforganicacidsinanimalnutrition(pp.83-87).nottingham:nottinghamuniversitypress.manningg.,whyted.b.,martinezr.,hunter,t.sudarsanams.(2002).theproteinkinasecomplementofthehumangenome.science,298(5600):1912-1934.mckenna,maryn.(2017)bigchicken.washingtondc,nationalgeographicpartners.page31.monikabuczek.(2016).antibioticsinourfood:acomplexproblemthatneedsasolution.americansocietyformicrobiology.availablefromurl:https://www.asm.org/index.php/general-science-blog/item/72-antibiotics-in-our-food-a-complex-problem-that-needs-a-complex-solution.mroz,z.(2005).organicacidsaspotentialalternativestotoantibioticgrowthpromotersforpigs.advancesinporkproduction,169-182.pbsfrontline.(2014).isyourmeatsafe?modernmeat:antibioticdebateoverview.retrievedaugust01,2015,frompbsfrontlinewebsite:http://www.pbs.org/wgbh/pages/firontline/shows/meat/safe/overview.html.phillipst,casewellm.,coxt.,degrootb.,friisc.,jonesr.,etal.(2004).doestheuseofantibioticsinfoodanimalsposearisktohumanhealth?acriticalreviewofpublisheddata.j.antimicrob.chemother.53,28-52.l0.l093/jac/dkg48.raymondm.j.,wohrler.d.,calld.r.(2006).assessmentandpromotionofjudiciousantibioticuseondairyfarmsinwashingtonstate.jdairysci;89:3228-40sanchez,b.,bressollier,p.andurdaci,m.c.(2008).exportedproteinsinprobioticbacteria:adhesiontointestinalsurfaces,hostimmunomodulationandmolecularcross-talkingwiththehost.femsimmunology&medicalmicrobiology,54:1-17.doi:10.111l/j.1574-695x.2008.00454.x.szklarczykd.,franceschinia.,wyders.,forslundk.,hellerd.,huerta-cepasj.,simonovicm.,rotha.,santosa.,tsafouk.p.,kuhnm.,borkp.,jensenl.j.,vonmeringc.(2015)."stringvlo:protein-proteininteractionnetworks,integratedoverthetreeoflife".nucleicacidsres.43(databaseissue):d447-52.teillant,a.a.(2015).economicsofantibioticuseinusswineandpoultryproduction.choicesmagazine.availablefromurlwww.choicesmagazine.org/userfiles/file/cmsarticle_404.pdf.teillant,a.a.(2015).economicsofantibioticuseinusswineandpoultryproduction.choices,pp.1-11.trostb.,kindrachukj.,maattanenp.,nappers.,kusalika.(2013)piika2:anexpanded,web-basedplatformforanalysisofkinomemicroarraydata.plosone8(11):e80837.https://doi.org/l0.l37l/journal.pone.0080837.urdaneta,d.,raffe,d.,ferrer,a.,sulbarandeferrer,b.,cabrera,l.,&perez,m.(1995).short-chainorganicacidsproducedonglucose,lactose,andcitratemediabyenterococcusfaecalis,lactobacilluscasei,andenterobacteraerogenesstrains.bioresourcetechnology,99-103.zalan,z.,hudacek,j.,stetina,j.,chumchalova,j.,&halasz,a.(2009).productionoforganicacidsbylactobacillusstrainsinthreedifferentmedia.europeanfoodresearchandtechnology,395-404.对于本文中引用的所有参考文献,由于其相关的公开内容,在此通过引用明确地并入本申请中。从前述内容可以看出,本发明非常适合于实现上述所有目的和目标,以及本发明的显著和固有的其他优点。由于在不脱离本发明范围的情况下可以对本发明做出许多可能的实施例,因此应当理解,本文阐述的或在附图中示出的所有内容均应解释为说明性的,而不是限制性的。尽管出于例证的目的已经示出并讨论了特定的实施方案,但是当然可以进行各种变化和改良,并且本发明不限于这里描述的形式或部分与步骤的重组,除非这样的限制被包括在权利要求中。此外,将理解,某些特征和子组合是实用的,并且可以在不参考其他特征和子组合的情况下被采用。这是权利要求所预期的并且在权利要求的范围之内。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1