一种治疗癌侵袭引起的镜像痛的药物的制作方法
本发明涉及一种治疗癌侵袭引起的镜像痛的药物。
背景技术:
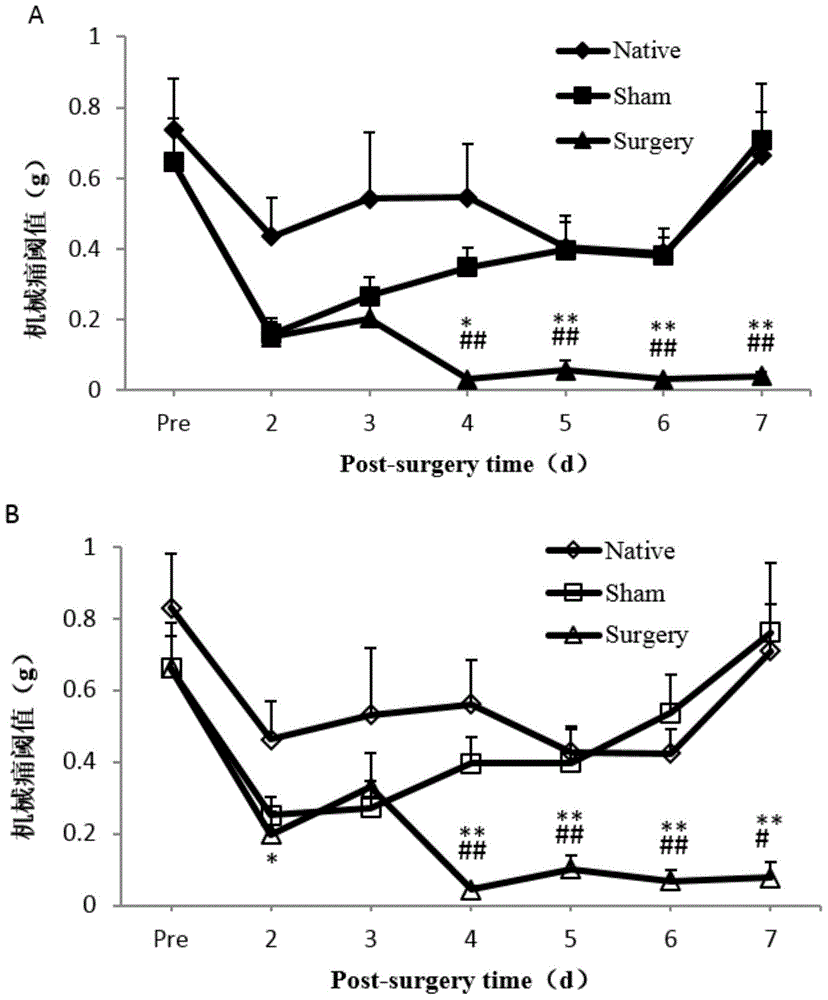
:癌症已经成为严重危害人类健康、导致现代人类死亡的第一大恶疾和顽症。癌痛是癌症患者最常见的临床症状之一,可以出现在癌症的任何阶段。新诊断为恶性肿瘤的患者中约1/4伴有疼痛,治疗过程中约1/3伴有癌痛,进展期约3/4伴有疼痛。癌侵袭痛(CancerInvasionPain,CIP)是由于肿瘤浸润引起的疼痛,癌症患者频发,是难治性癌痛之一。躯体的对称性给人类行动带来便利的同时也带来了不利影响,如躯体一侧损伤出现疼痛或痛敏时,其损伤部位的对侧对称部位(镜像部位)亦出现继发性疼痛和痛敏,即镜像痛(MirrorImagePain,MIP)。该现象最早发现于在美国内战时期,肢体受伤的士兵在受伤对侧的肢体也出现了疼痛感觉。临床上,一些严重的慢性疼痛(如先天性面部关节肌痛、非典型面部痛、慢性偏头痛、紧张型头痛等)、复杂区域疼痛综合征、截肢及中风后遗症均可出现继发性的MIP,给患者生活带来了极大的痛苦。由于MIP发生、发展与维持的机制至今尚不十分清楚,治疗效果也不理想,一般治疗疼痛的药物对MIP的治疗效果是不确定的。技术实现要素:本发明的目的是提供一种治疗癌侵袭引起的镜像痛的药物。本发明提供了一种治疗镜像痛的药物,其活性成分为CQ复方。本发明还提供了第二种治疗镜像痛的药物,其活性成分为所述CQ复方和盐酸金刚烷胺。盐酸金刚烷胺作为CQ复方的增效剂使用,采用人体可接受的剂量范围内的量均可。所述CQ复方和所述盐酸金刚烷胺的质量比为可为3:3-5,具体可为3:4。本发明还提供了一种治疗癌侵袭引起的镜像痛的药物,其活性成分为所述CQ复方。所述癌侵袭具体可为S180瘤株细胞引起的癌侵袭。本发明还提供了第二种治疗癌侵袭引起的镜像痛的药物,其活性成分为所述CQ复方和盐酸金刚烷胺。所述癌侵袭具体可为S180瘤株细胞引起的癌侵袭。盐酸金刚烷胺作为CQ复方的增效剂使用,采用人体可接受的剂量范围内的量均可。所述CQ复方和所述盐酸金刚烷胺的质量比为可为3:3-5,具体可为3:4。本发明还保护所述CQ复方在制备治疗镜像痛的药物中的应用。本发明还保护所述CQ复方和盐酸金刚烷胺在制备治疗镜像痛的药物中的应用。盐酸金刚烷胺作为CQ复方的增效剂使用,采用人体可接受的剂量范围内的量均可。所述CQ复方和所述盐酸金刚烷胺的质量比为可为3:3-5,具体可为3:4。本发明还保护所述CQ复方在制备治疗癌侵袭引起的镜像痛的药物中的应用。所述癌侵袭具体可为S180瘤株细胞引起的癌侵袭。本发明还保护所述CQ复方和盐酸金刚烷胺在制备治疗癌侵袭引起的镜像痛的药物中的应用。所述癌侵袭具体可为S180瘤株细胞引起的癌侵袭。盐酸金刚烷胺作为CQ复方的增效剂使用,采用人体可接受的剂量范围内的量均可。所述CQ复方和所述盐酸金刚烷胺的质量比为可为3:3-5,具体可为3:4。所述CQ复方由组分甲和组分乙组成;所述组分甲为川芎嗪或川芎嗪的盐;所述组分乙为青藤碱或青藤碱的盐;所述组分甲和所述组分乙的质量比为0.5-2.5:1。所述川芎嗪的盐为盐酸川芎嗪或磷酸川芎嗪;所述青藤碱的盐为盐酸青藤碱或磷酸青藤碱。所述组分甲和所述组分乙的质量比为0.8:1。以上任一所述“治疗癌侵袭引起的镜像痛”体现为如下(a)和/或(b)和/或(c)和/或(d)和/或(e):(a)促使机械痛阈值增加;(b)促使脊髓组织内RANTES含量降低;(c)促使脊髓组织内MCP-3含量降低;(d)促使血清内IL-6含量降低;(e)促使血清内MCP-1含量降低。本发明为癌侵袭镜像痛的机制研究和临床治疗提供参考,对于镜像痛的治疗具有重大的应用价值。附图说明图1为各组小鼠癌侵袭侧(图A)和镜像侧(图B)后足机械痛阈值变化(n=13);*P<0.05,**P<0.01,与Native组相比;#P<0.05,##P<0.01,与Sham组相比。图2为盐酸金刚烷胺对CQ复方镇痛作用的影响(图A为癌侵袭侧,图B为镜像侧);*P<0.05,**P<0.01,与CQ组相比。具体实施方式以下的实施例便于更好地理解本发明,但并不限定本发明。下述实施例中的实验方法,如无特殊说明,均为常规方法。下述实施例中所用的试验材料,如无特殊说明,均为自常规生化试剂商店购买得到的。以下实施例中的定量试验,均设置三次重复,结果取平均值。SPF级BALB/c雄性小鼠,体重为18-20g,购于中国食品药品检定研究院,许可证号:SCXK(京)2014-0013。S180瘤株细胞(鼠肉瘤细胞株):参考文献:LeeHJ,LeeJH,LeeEO,etal.SubstancePandbeta-endorphinmediateelectro-acupunctureinducedanalgesiainmousecancerpainmodel[J].AcupunctElectrotherRes,2009,34(1-2):27-40。MuoseCustom8-plexkit:北京旷博生物技术有限公司;货号:T2C081217。MouseGroup116-plexkit:北京旷博生物技术有限公司,货号:C261116。机械痛阈值(缩足阈值)的检测方法:依次用标准化的不同刺激力度(0.008g、0.02g、0.04g、0.07g、0.16g、0.4g、0.6g、1g或2g;从0.008g开始,以每秒一次的频率)的VonFrey纤维丝,垂直刺激小鼠后肢足爪底部中外侧皮肤表面,观察小鼠的缩足反应,连续试验5次,记录出现3次或3次以上缩足反应的最小纤维丝值,作为机械痛阈值。动物行为学数据以均数加减标准误表示,采用SPSS21.0软件进行统计分析。对于重复测量的机械阈值组间差异采用一般线性模型的重复测量资料的方差分析方法检测组间差异,采用多因素方差分析方法分析具体某一时间点的组间差异。细胞因子检测数据以均数加减标准差表示,两组间数据分析采用独立样本t检验,以P<0.05为差异有统计学意义。实施例1和实施例2中涉及连续操作,因此连续计试验天数。盐酸川芎嗪的结构式如下:盐酸青藤碱的结构式如下:川芎嗪可以从川芎中提取得到,也可以通过化学合成的方法获得。常见的提取方法如下:川芎用乙醇超声提取,提取液浓缩干燥,即得。川芎嗪还可被川芎嗪的盐代替,例如盐酸川芎嗪,磷酸川芎嗪等。青藤碱可以从青风藤中提取得到。常见的提取方法如下:1、青藤醇提,酸溶,萃取,水重结晶,即得;2、青藤碱化,苯提,结晶,脱色,水重结晶,即得。由于化学合成技术的发展,青藤碱也可以通过合成的方法获得。青藤碱还可被青藤碱的盐代替,例如盐酸青藤碱,磷酸青藤碱等。盐酸金刚烷胺:东北制药集团沈阳第一制药有限公司,批号:5140102。实施例1、小鼠癌侵袭镜像痛(CancerInvasionInducedMirrorImagePain,CIIMIP)模型的建立试验前连续3天对SPF级BALB/c雄性小鼠进行预刺激(每天一次,每次用定量的VonFrey纤维丝刺激小鼠双侧的后足)。试验第1天将双侧后足机械痛阈值均≥0.4g的小鼠随机分为正常组(Native)、操作对照组(Sham)、手术组(Surgery),Surgery组每只小鼠于右腿股骨大转子(相当于坐骨神经分支部位上方)注射0.2mLS180瘤株细胞液(活细胞浓度为1×107个/mL),Sham组于相同部位注射相同体积相同浓度的灭活S180瘤株细胞液(灭活方法:沸水中煮沸15min,然后台盼蓝染色确定无活细胞),Native组不作任何操作。试验第4天,Surgery组小鼠活动量减少,毛色偏暗,精神状态不佳。试验第4天,Surgery组大部分小鼠瘤株接种部位肿大明显,术侧足趾不能正常伸展,呈保护性外翻体位,且其腿部的肿瘤大小及足趾变形程度随时间而逐渐增加。试验第11天,解剖后发现Surgery组小鼠腿部肿瘤在坐骨神经分支处,肿瘤生长进行性地压迫或侵袭坐骨神经,小鼠腿部组织中分离出肿瘤组织的重量为1.493±0.725g。试验第11天,Sham组小鼠腿部未见肿瘤组织。试验第2-7天连续评价Native组、Sham组及Surgery组小鼠癌侵袭侧的机械痛阈值,发现三组癌侵袭侧机械痛阈值组间有显著差异(P<0.01),见图1A。Surgery组小鼠癌侵袭侧机械痛阈值在试验第2天开始下降,试验第4-7天均稳定维持在(0.031±0.006)g-(0.057±0.029)g,明显低于Sham组和Native组(P<0.05或P<0.01)。Sham组小鼠的癌侵袭侧机械痛阈值在试验第2天亦降低,但随后逐渐回升,试验第5天以后达到Native组水平。在试验第2-7天连续评价Native组、Sham组及Surgery组小鼠镜像侧的机械痛阈值,发现三组小鼠镜像侧机械痛阈值组间亦有显著差异(P<0.01),见图1B。Surgery组小鼠镜像侧机械痛阈值亦在试验第2天下降,试验第4-7天均稳定维持在(0.044±0.012)g-(0.101±0.038)g,明显低于Sham组和Native组(P<0.05或P<0.01)。Surgery组小鼠左前肢和腹部在试验第16天内未见明显的疼痛表现,表明痛敏现象仅发生在癌侵袭侧的镜像部位。试验第5-7天,癌侵袭侧和镜像侧的机械痛阈值均≤0.07g的Surgery组小鼠,即为模型小鼠。实施例2、CQ复方对癌侵袭镜像痛的作用效果一、制备CQ复方CQ复方由盐酸川芎嗪和盐酸青藤碱组成,盐酸川芎嗪和盐酸青藤碱的质量比为0.8:1。取CQ复方,用超纯水溶解,得到40mg/mL的储存液,然后用生理盐水稀释,得到CQ复方溶液。二、分组给药模型组(Model,n=12):对象为实施例1得到的模型小鼠,试验第8天、第9天和第10天各腹腔注射一次生理盐水,单次注射剂量为0.4mL生理盐水/20g小鼠;CQ复方高剂量组(H-CQ,200mg/kg,n=12):对象为实施例1得到的模型小鼠,试验第8天、第9天和第10天各腹腔注射一次CQ复方溶液,单次注射剂量为0.4mLCQ复方溶液/20g小鼠,0.4mLCQ复方溶液中CQ复方的浓度为10mg/mL;CQ复方中剂量组(M-CQ,150mg/kg,n=11):对象为实施例1得到的模型小鼠,试验第8天、第9天和第10天各腹腔注射一次CQ复方溶液,单次注射剂量为0.4mLCQ复方溶液/20g小鼠,0.4mLCQ复方溶液中CQ复方的浓度为7.5mg/mL;CQ复方低剂量组(L-CQ,100mg/kg,n=11):对象为实施例1得到的模型小鼠,试验第8天、第9天和第10天各腹腔注射一次CQ复方溶液,单次注射剂量为0.4mLCQ复方溶液/20g小鼠,0.4mLCQ复方溶液中CQ复方的浓度为5mg/mL;Sham组(Sham,n=11):对象为实施例1中的Sham组小鼠,试验第8天、第9天和第10天各腹腔注射一次生理盐水,单次注射剂量为0.4mL生理盐水/20g小鼠;Native组(Native,n=13):对象为实施例1中的Native组小鼠,试验第8天、第9天和第10天各腹腔注射一次生理盐水,单次注射剂量为0.4mL生理盐水/20g小鼠。三、CQ复方给药后小鼠的机械痛阈值试验第10天,给药前及给药后240min内的小鼠癌侵袭侧机械痛阈值测评结果见表1和表2。表1试验第10天,各组小鼠给药前后癌侵袭侧机械痛阈值给药前给药后30min给药后60min给药后90min给药后120min给药后180min给药后240minNative0.37±0.070.38±0.070.34±0.050.37±0.050.35±0.050.40±0.060.37±0.05Sham0.24±0.050.22±0.050.22±0.050.26±0.050.27±0.040.25±0.040.26±0.04Model0.02±0.00**##0.03±0.01**##0.03±0.01**##0.03±0.01**##0.02±0.01**##0.02±0.01**##0.02±0.01**##L-CQ0.01±0.000.22±0.180.22±0.180.32±0.180.32±0.190.15±0.060.07±0.03M-CQ0.02±0.010.73±0.27△0.72±0.27△0.76±0.27△0.59±0.22△0.33±0.10△0.28±0.13H-CQ0.03±0.011.33±0.25△△1.31±0.22△△1.22±0.21△△0.86±0.17△△0.47±0.15△0.30±0.16**P<0.01,与Native组相比;##P<0.01,与Sham组相比;△P<0.05,△△P<0.01,与Model组相比。表2试验第10天,各组小鼠给药前后镜像侧机械痛阈值给药前给药后30min给药后60min给药后90min给药后120min给药后180min给药后240miNative0.47±0.100.47±0.190.45±0.100.47±0.090.42±0.090.42±0.090.48±0.14Sham0.26±0.050.22±0.060.28±0.050.26±0.050.26±0.050.30±0.060.28±0.05Model0.03±0.01**##0.03±0.02**##0.03±0.01**##0.03±0.01**##0.03±0.01**##0.03±0.01**##0.03±0.01**##L-CQ0.02±0.000.11±0.050.41±0.240.30±0.180.15±0.070.16±0.060.05±0.01M-CQ0.04±0.010.09±0.040.68±0.24△0.84±0.26△0.58±0.20△0.22±0.06△0.21±0.06△H-CQ0.06±0.030.98±0.42△△1.23±0.21△△1.27±0.19△△0.85±0.15△△0.37±0.09△△0.32±0.11△**P<0.01,与Native组相比;##P<0.01,与Sham组相比;△P<0.05,△△P<0.01,与Model组相比。结果表明,应用CQ复方后,模型小鼠原发性的CIP明显减轻,继发性的MIP亦得到明显缓解,均在给药后30min开始发挥明显的镇痛作用,一般在30min或60min时达到药效高峰,240min仍有较好的镇痛效果,且剂量组之间呈明显的量效依赖关系。四、CQ复方给药后小鼠脊髓组织内RANTES和MCP-3的含量RANTES、MCP-3均属于脊髓内趋化因子。试验第11天处死小鼠,取L3-L5段脊髓组织,经匀浆、去蛋白、去微粒得到脊髓匀浆的处理液,采用AimPlex流式高通量多因子检测技术检测小鼠脊髓组织内RANTES和MCP-3的含量。结果见表3。与Sham组相比,Model组内的RANTES、MCP-3含量均显著升高(P<0.01、P<0.05),L-CQ及H-CQ均能显著降低模型小鼠脊髓组织内RANTES、MCP-3的含量(P<0.05)。表3CQ复方给药后脊髓组织内RANTES、MCP-3含量#P<0.05,##P<0.01,与Sham组相比;△P<0.05,与Model组相比。五、CQ复方给药后小鼠血清中炎性因子IL-6及趋化因子MCP-1的含量试验第11天小鼠处死前眼眶取血,收集血清,采用AimPlex流式高通量多因子检测技术检测小鼠血清中炎性因子IL-6及趋化因子MCP-1的含量。结果见表4。与Native组相比,Model组模型小鼠血清中的IL-6、MCP-1含量均显著升高(P<0.05),CQ复方能显著降低模型小鼠血清内IL-6、MCP-1的含量(P<0.01)。表4CQ复方给药后小鼠血清中炎性因子IL-6及趋化因子MCP-1的含量*P<0.05,与Native组相比;△△P<0.01,与Model组相比。实施例3、盐酸金刚烷胺增强CQ复方对于MIP的镇痛作用一、制备模型小鼠试验前连续3天对SPF级BALB/c雄性小鼠进行预刺激(每天一次,每次用定量的VonFrey纤维丝刺激小鼠双侧的后足)。试验第1天取双侧后足机械痛阈值均≥0.4g的小鼠,每只小鼠于右腿股骨大转子(相当于坐骨神经分支部位上方)注射0.2mLS180瘤株细胞液(活细胞浓度为1×107个/ml)。试验第5-7天,癌侵袭侧和镜像侧的机械痛阈值均≤0.07g的Surgery组小鼠,即为模型小鼠。二、制备CQ复方CQ复方由盐酸川芎嗪和盐酸青藤碱组成,盐酸川芎嗪和盐酸青藤碱的质量比为0.8:1。取CQ复方,用超纯水溶解,得到40mg/mL的储存液,然后用生理盐水稀释,得到CQ复方溶液。三、分组给药盐酸金刚烷胺溶液:取盐酸金刚烷胺(Ama),用生理盐水超声溶解,得到10mg/mL的盐酸金刚烷胺溶液。Ama+CQ组(n=12):对象为步骤一得到的模型小鼠,试验第8天,腹腔注射一次CQ复方溶液(150mg/kg,注射剂量为0.4mLCQ复方溶液/20g小鼠,0.4mLCQ复方溶液中CQ复方的浓度为7.5mg/mL),腹腔注射CQ复方溶液30min前灌胃给予10mg/mL的盐酸金刚烷胺溶液(200mg/kg,给药剂量为0.4mL/20g小鼠)。CQ组(n=11):对象为步骤一得到的模型小鼠,试验第8天腹腔注射一次CQ复方溶液(注射剂量为0.4mLCQ复方溶液/20g小鼠,0.4mLCQ复方溶液中CQ复方的浓度为7.5mg/mL);于-30min(给予Ama之前)、0min(腹腔注射CQ复方前)及给予CQ复方后30、60、90、120、180、240min等时间点测评双侧后足的机械痛阈值。在CIIMIP模型小鼠腹腔给予CQ复方30min前,灌胃给予Ama能增强CQ复方对模型小鼠癌侵袭侧和镜像侧机械痛阈值的升高作用。在给药后30-240min内6个时间点均能显著增强CQ复方对于CIP的镇痛作用(P<0.01或P<0.05),见图2A。在给药后30-180min的5个时间均能显著增强CQ复方对于MIP的镇痛作用(P<0.01或P<0.05),见图2B。当前第1页1 2 3
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1